9.5. Произведение растворимости
Подавляющее большинство веществ обладает ограниченной растворимостью в воде и других растворителях. Поэтому на практике часто приходится иметь дело с системами, в которых в состоянии равновесия находятся осадок и насыщенный раствор электролита.
Малорастворимые электролиты при растворении полностью диссоциируют на ионы (в растворе нет нейтральных молекул).
Например, для малорастворимого соединения Ag2CO3 можно записать следующий обратимый процесс:
Ag2CO3(к) 2Ag+(р) + CO32(р) ,
а соответствующая ему константа равновесия будет называться произведением растворимости:
.
Этот процесс является гетерогенным, поэтому константа равновесия определяется только произведением концентраций ионов в растворе и не зависит от концентрации твердого компонента.
Правила записи выражений для произведения растворимости ничем не отличаются от правил записи любых выражений для Кp.Произведение растворимости равно произведению молярных концентраций ионов, участвующих в равновесии, каждая из которых возведена в степень, равную стехиометрическому коэффициенту, при соответствующем ионе в уравнении равновесия.
ПР тесно связано с растворимостью (S моль/л). Так, для электролитов, имеющих катионы и анионы одинакового заряда (AgCl, PbS и др.), очевидно
 ,
а ПР
= S2
,
а ПР
= S2
В общем случае разных зарядов катиона (n+) и аниона (m):
 или
.
или
.
Очевидно,
что ПР, кроме того, можно найти по
термодинамическим данным, так как
ПР = К = 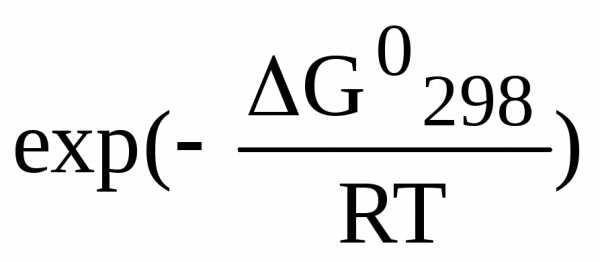
Пример 20. ПР (СаF2) = 3,9.1011. Какова растворимость СаF2 в воде (в граммах на литр и в моль на литр)?
Решение. Равновесие растворения описывается уравнением:
СаF2(Т) Са2+(Р) + 2F(Р) .
Из каждого моля растворившегося СаF2 в растворе появляются 1 моль ионов Са2+ и 2 моль ионов F. Поэтому, обозначая растворимость фторида кальция, выраженную в моль на литр, через х, молярные концентрации Ca2+ и F в растворе можно записать следующим образом: [Ca2+] = х и [F] = 2 x. Выражение для произведения растворимости в данном случае имеет вид
ПР = [Ca2+] [F]2 .
Подставляя в него [Ca2+] = х и [F] = 2 х, находим ПР = х (2 х)2 = 4 х3 = 3,9.1011.
Отсюда х = .
Следовательно, растворимость СаF2, выраженная в моль/л, равна 2,1.104.
Поскольку молярная масса СаF2 равна 78,1 г/моль, то растворимость СаF2, выраженная в г/литр, составит: 2,1.104 моль/л·78,1 г/моль = 1,6·102 г/л.
Пример 21. Какова растворимость (S) Ag2CO3 , если ПР (Ag2CO3) = 8,2.1012 ? Как изменится растворимость при добавлении в 1 литр насыщенного раствора 10,6 г Na2CО3 ? Какое количество Ag2
CO3 выпадет при этом в осадок?Решение. Растворимость найдем по формуле:
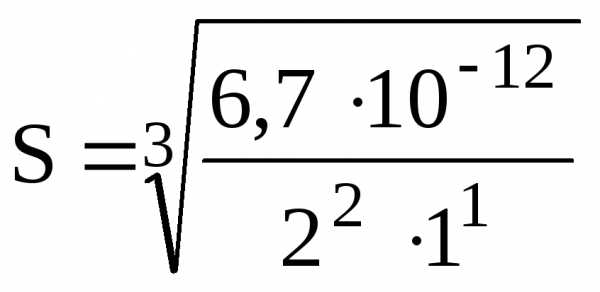 =
1,19.104
моль/л.
=
1,19.104
моль/л.
При растворении 10,6 г Na2CО3 в 1 л раствора добавляется 10,6/106 = 0,1 моль ионов CО32. Если считать, что объем раствора при этом не изменяется, и учесть, что концентрация CО32 до растворения Na2CО3 пренебрежимо мала, то равновесное значение [CО32] = 0,1 моль/л. Отсюда можно найти новую концентрацию Ag+ :
моль/л.
Это соответствует вдвое меньшей концентрации Ag2CO3 , то есть растворимость стала S| = 4,1.106 моль/л, а из 1 л раствора выпало в осадок
моль, или 0,32 г Ag2CO3 .
Полученные результаты показывают, что при добавлении в насыщенный раствор одноименного иона в концентрации, значительно превышающей первоначальную, труднорастворимое вещество практически полностью выпадает в осадок. Этот эффект (выпадение осадка из насыщенного раствора при добавлении одноименного иона) носит название «высаливание» . Он используется для извлечения ценных компонентов из растворов.
Из
выражения для ПР следует, что при
увеличении концентрации одного из ионов
электролита в его насыщенном растворе
(например, путем введения другого
электролита, содержащего тот же ион)
произведение концентраций ионов
электролита становится больше ПР. При
этом равновесие между твердой фазой и
раствором смещается в сторону образования
осадка, так как величина ПР не зависит
от концентрации. Таким образом,
условием образования осадка является
превышение произведения концентраций
ионов малорастворимого электролита
над его произведением растворимости.
Пример 22. Будет ли образовываться осадок при смешении 0,1 л раствора нитрата свинца с концентрацией 3,0·103 М и 0,4 л раствора сульфата натрия с концентрацией 5,0·103 М ? Если да, то сколько граммов?
Решение. Возможными продуктами реакции являются PbSO4 и NaNO3. Соли натрия относятся к хорошо растворимым соединениям, однако PbSO4 имеет ПР = 1,6.108. Чтобы определить, будет ли происходить осаждение PbSO4, следует вычислить произведение концентраций ионов Pb2+ и SO42 и сопоставить полученный результат с ПР.
При смешении двух растворов полный объем становится равным 0,1 + 0,4 = 0,5 л. Число моль Pb2+, содержащихся в 0,1 л раствора Pb(NO3)2 с концентрацией 3,0·103 М, равно
0,1 л·(3,0·103 моль/л) = 3,0·104 моля.
Концентрация Pb2+ в 0,5л смеси растворов должна быть равна [Pb2+]. Число моль SO42— в 0,4 л исходного раствора Na2SO4 равно:
0,4 л·(5,0·103 моль/л) = 2,0·103 моль.
Следовательно, [SO42] в 0,5 л смеси растворов должна быть равна:
.
Находим произведение концентраций ионов:
[Pb2+]·[SO42] = (6,0·104)·(4,0.103) = 2,4·106.
Поскольку произведение концентраций ионов 2,4·106 больше ПР, в смеси растворов должно происходить осаждение PbSO4.
Чтобы определить, какое количество PbSO4 выпадет в осадок, определим концентрацию ионов Pb2+ в растворе: [Pb2+] = 4.104
М.
4.104
М.В 0,5 л содержится в 2 раза меньше 2·104 моль. Следовательно, в осадок выпадет 3·104 2·104 = 1·104 моль или m =n·М = 104·393 4·102 г.
studfiles.net
Произведение растворимости
Определение
Поместим в химический стакан какую-либо
труднорастворимую соль, например, AgCl и добавим к осадку
дистиллированной воды. При этом ионы Ag+ и Cl—,
испытывая притяжение со стороны окружающих диполей воды, постепенно
отрываются от кристаллов и переходят в раствор. Сталкиваясь в растворе,
ионы Ag
1) Переход ионов из осадка в раствор. Скорость этого процесса можно считать постоянной при неизменной температуре: V1 = K1;
2) Осаждение ионов из раствора. Скорость этого процесса V
2 зависит от концентрации ионов Ag+ и Cl—. По закону действия масс:
V2 = k2
Так как данная система находится в состоянии равновесия, то
V1 = V2
k2 = k1
[Ag+]
- [Cl—] = k2 / k1 = const (при T = const)
Таким образом, произведение
концентраций ионов в насыщенном растворе труднорастворимого электролита
при постоянной температуре является постоянной величиной. Эта величина называется произведением растворимости (ПР).
В приведенном примере ПРAgCl = [Ag+] • [Cl—].
В тех случаях, когда электролит содержит два или несколько одинаковых
ионов, концентрация этих ионов, при вычислении произведения
растворимости должна быть возведена в соответствующую степень.
Например, ПРAg
- [S2-]; ПРPbI2 = [Pb2+] [I—]2
В общем случае выражение произведения растворимости для электролита AmBn
ПРAmBn = [A]m [B]n.
Значения произведения растворимости для разных веществ различны.
Например, ПРCaCO3 = 4,8
- 10-9; ПРAgCl = 1,56 10-10.
ПР легко вычислить, зная раcтворимость соединения при данной t°.
Пример 1
Растворимость CaCO3 равна 0,0069 или 6,9
- 10-3 г/л. Найти ПРCaCO3.
Решение
Выразим растворимость в молях:
SCaCO3 = (6,9
· 10-3) / 100,09 = 6,9 • 10-5 моль/л
MCaCO3
Так как каждая молекула CaCO3 дает при растворении по одному иону Ca2+ и CO32-, то
[Ca2+] = [ CO32-] = 6,9
следовательно, ПРCaCO3 = [Ca2+
]
- [CO32-] = 6,9 10-56,9 10-5 = 4,8 10-9
Зная величину ПР, можно в свою очередь вычислить растворимость вещества в моль/л или г/л.
Пример 2
Произведение растворимости ПРPbSO4 = 2,2
Чему равна растворимость PbSO4?
Решение
Обозначим растворимость PbSO4 через X моль/л. Перейдя в раствор, X молей PbSO4 дадут X ионов Pb2+ и X ионов SO42-, т.е.:
[Pb2+] = [SO42-] = X
ПРPbSO4 = [Pb2+] = [SO42-
] = X
X = \e(ПРPbSO4) = \e(2,2
- 10-8) = 1,5 10-4 моль/л.
Чтобы перейти к растворимости, выраженной в г/л, найденную величину умножим на молекулярную массу, после чего получим:
1,5
- 10-4 303,2 = 4,5 10-2 г/л.
Образование осадков
Если
[Ag+]
- [Cl—] < ПРAgCl — ненасыщенный раствор
[Ag+
]
- [Cl—] = ПРAgCl — насыщенный раствор
[Ag+]
- [Cl—] > ПРAgCl — перенасыщенный раствор
Осадок образуется в том
случае, когда произведение концентраций ионов малорастворимого
электролита превысит величину его произведения растворимости при данной
температуре. Когда ионное
произведение станет равным величине ПР, выпадение осадка прекращается.
Зная объем и концентрацию смешиваемых растворов, можно рассчитать,
будет ли выпадать осадок образующейся соли.
Пример 3
Выпадает ли осадок при смешении равных объемов 0,2 M растворов Pb(NO3)2 и NaCl.
ПРPbCl2
= 2,4
Решение
При смешении объем раствора возрастает вдвое и концетрация каждого из веществ уменьшится вдвое, т.е. станет 0,1 M или 1,0
- 10-1 моль/л. Таковы же будут концентрации Pb2+ и Cl—. Следовательно, [Pb2+] [Cl—]2 = 1 10-1 (1 10-1)2 = 1 10-3. Полученная величина превышает ПРPbCl2 (2,4 10-4). Поэтому часть соли PbCl2 выпадает в осадок. Из всего сказанного выше можно сделать вывод о влиянии различных факторов на образование осадков.
Влияние концентрации растворов
Труднорастворимый электролит с достаточно большой величиной ПР нельзя осадить из разбавленных растворов. Например, осадок PbCl2 не будет выпадать при смешении равных объемов 0,1 M растворов Pb(NO3)2 и NaCl. При смешивании равных объемов концентрации каждого из веществ станут 0,1 / 2 = 0,05 M или 5
- 10-2 моль/л. Ионное произведение [Pb2+] [Cl1-]2 = 5 10-2 (5 10-2)2 = 12,5 10-5. Полученная величина меньше ПРPbCl2, следовательно выпадения осадка не произойдет.
Влияние количества осадителя
Для возможно более полного осаждения употребляют избыток осадителя.
Например, осаждаем соль BaCO3: BaCl2 + Na2CO3 ® BaCO3¯ + 2NaCl. После прибавления эквивалентного количества Na2CO3 в растворе остаются ионы Ba2+, концентрация которых обусловлена величиной ПР.
Повышение концентрации ионов CO32-, вызванное прибавлением избытка осадителя (Na2CO3), повлечет за собой соответственное уменьшение концентрации ионов Ba2+ в растворе, т.е. увеличит полноту осаждения этого иона.
Влияние одноименного иона
Растворимость труднорастворимых
электролитов понижается в присутствии других сильных электролитов,
имеющих одноименные ионы. Если к ненасыщенному раствору BaSO4 понемногу прибавлять раствор Na2SO4, то ионное произведение, которое было сначала меньше ПРBaSO4 (1,1
- 10-10), постепенно достигнет ПР и превысит его. Начнется выпадение осадка.
Влияние температуры
ПР является постоянной величиной при
постоянной температуре. С увеличением температуры ПР возрастает,
поэтому осаждение лучше проводить из охлажденных растворов.
Растворение осадков
Правило произведения растворимости
важно для переведения труднорастворимых осадков в раствор. Предположим,
что надо растворить осадок BaСO3. Раствор, соприкасающийся с этим осадком, насыщен относительно BaСO3.
Это означает, что [Ba2+
]
Если добавить в раствор кислоту, то ионы H+ свяжут имеющиеся в растворе ионы CO32- в молекулы непрочной угольной кислоты:
2H+ + CO32- ® H2CO3 ® H2O + CO2
Вследствие этого резко снизится концентрация иона CO32- , ионное произведение станет меньше величины ПРBaCO3. Раствор окажется ненасыщенным относительно BaСO3 и часть осадка BaСO3
перейдет в раствор. При добавлении достаточного количества кислоты
можно весь осадок перевести в раствор. Следовательно, растворение
осадка начинается тогда, когда по какой-либо причине ионное
произведение малорастворимого электролита становится меньше величины
ПР. Для того, чтобы растворить осадок, в раствор вводят такой
электролит, ионы которого могут образовывать малодиссоциированное
соединение с одним из ионов труднорастворимого электролита. Этим
объясняется растворение труднорастворимых гидроксидов в кислотах
Fe(OH)3 + 3HCl ® FeCl3 + 3H2O
Ионы OH— связываются в малодиссоциированные молекулы H2O.
Таблица. Произведение растворимости (ПР) и растворимость при 25°С некоторых малорастворимых веществ
| Формула | Растворимость | ПР моль / л |
| AgBr | 7,94 • 10-7 | 6,3 • 10-13 |
| AgCl | 1,25 • 10-5 | 1,56 • 10-10 |
| AgI | 1,23 • 10-8 | 1,5 • 10-16 |
| Ag2CrO4 | 1,0 • 10-4 | 4,05 • 10-12 |
| BaSO4 | 7,94 • 10-7 | 6,3 • 10-13 |
| CaCO3 | 6,9 • 10-5 | 4,8 • 10-9 |
| PbCl2 | 1,02 • 10-2 | 1,7 • 10-5 |
| PbSO4 | 1,5 • 10-4 | 2,2 • 10-8 |
www.examen.ru
1
Министерство образования Российской Федерации
Владимирский Государственный Университет
Кафедра Химии
Лабораторная работа по общей и неорганической химии №12
«Произведение растворимости»
Выполнил:
Студент группы Х-111
Гынку В. А.
Проверил:
Проф. Орлин Н.А.
Владимир 2011
Основные понятия:
Произведением растворимости (ПР) называют произведение концентрации ионов труднорастворимого электролита в насыщенном растворе.
Если труднорастворимый электролит диссоциирует с образованием нескольких одинаковых ионов, то при вычислении ПР этого электролита концентрации ионов должны быть возведены в степени, равные числу одинаковых ионов в уравнении диссоциации, например:
Pb3(PO4)2 = 3Pb2+ + 2PO43-
ПР (Pb3(PO4)2) = [Pb2+]3[ PO43-]2
Для большинства труднорастворимых электролитов значения их ПР определены и содержатся в соответствующих справочниках. Эти значения ПР используются для решения задач, в частности для определения растворимости и концентрации ионов труднорастворимого соединения в его насыщенном растворе, а также для определения возможности образования осадка труднорастворимого электролита при заданных концентрациях исходных веществ. В этом случае необходимо рассчитать произведение концентрации ионов (ПК) и сравнить его с ПР.
Если ПК ионов в растворе меньше его ПР, то осадок не образуется:
ПК < ПР ( осадок не образуется)
Такой раствор является еще не насыщенным. Если ПК ионов превышает ПР, раствор становится насыщенным, а затем и пересыщенным и это ведет к выпадению осадка:
ПК > ПР ( осадок образуется)
Ненасыщенный раствор каких-либо электролитов, например AgCl, можно сделать насыщенным, если к нему прибавлять электролит с одноименным ионом.
Так, если к ненасыщенному раствору AgCl, у которого ПК < ПРAgCl ( 1,5*10-10), прибавлять понемногу KCl или HCl, то произведение [Ag+][Cl—] постепенно достигает величины ПР, раствор из ненасыщенного становится насыщенным и из раствора выпадает осадок AgCl.
Для растворения осадка нужно, наоборот, уменьшить концентрацию хотя бы одного из ионов в насыщенном растворе, чтобы ПК ионов стало меньше величины ПР.
Этого достигают, как правило, связыванием одного из ионов осадка, находящегося в растворе, с ионом добавляемого реагента в слабодиссоциирующее или летучее соединение.
Растворение труднорастворимого электролита может происходить в случаях образования:
растворимого слабодиссоциирующего соединения;
комплексного соединения;
газообразного вещества;
или в случае ОВР, приводящей к изменению степени окисления ионов труднорастворимого электролита.
Опыт №1.Условия выпадения осадка.
В две пробирки внесли по 3 капли раствора сульфата марганца (II). Затем в одну пробирку добавили 3 капли сероводородной воды, а в другую – столько же раствора сульфида аммония.
Если произведение концентрации ионов превышает произведение растворимости, раствор становится насыщенным, а затем и перенасыщенным и это ведет к выпадению осадка. Сульфат аммония в отличии от сероводородной воды диссоциирует полностью, при этом повышается концентрация ионов серы в растворе (ПК>ПР-выпадает осадок).
Вывод: Осадок выпадает в том случае, когда достигается необходимая концентрация ионов обоих веществ.
Опыт №2.Влияние одноименных ионов на выпадение осадка.
В две пробирки налили по 7-8 капель насыщенного раствора хлората калия. В одну пробирку добавили 4 капли насыщенного раствора хлорида калия, в другую столько же хлорида натрия.
В случае, когда мы добавили KCl мы наблюдали образование на стенках пробирки кристалликов калия.
При этом растворимость хлорида калия уменьшиться, т.к. выпадает осадок.
Вывод: В следствии добавления в раствор одноименных ионов, мы повышаем ПК, что способствует выпадению осадка.
Опыт № 3. Последовательность выпадения осадков малорастворимых солей.
В одной пробирке мы получили осадок PbSO4, путем взаимодействия 3-х капель раствора Na2SO4 с 3-мя каплями раствора Pb(NO3)2. В другой пробирке получили осадок PbCrO4, смешивая 3 капли K2CrO4 с 3-мя каплями раствора Pb(NO3)2. В третью пробирку налили по 3 капли Na2SO4 и K2CrO4, а потом прилили Pb(NO3)2 и по цвету выпавшего осадка мы определили вещество.
Реакции, проводимые в данном опыте:
Как видно из 3-ей реакции выпал осадок PbCrO4 желтого цвета. Это произошло из-за того, что ПР PbCrO4 < ПР PbSO4. Но если мы продолжим добавление в этот раствор Pb(NO3)2, то вскоре закончатся ионы CrO42- и выпадать в осадок будет уже PbSO4.
Вывод: в реакциях идущих с выпадением осадка первым будет выпадать тот, у которого ПР меньше.
В двух пробирках был получен гидроксид магния, осадок белого цвета, путем взаимодействия 2 капель сульфата магния с 2 каплями гидроксида натрия.
В первую пробирку добавлена 1 капля HCl. Осадок растворился.
Во вторую пробирку добавлены 2 капли NH4Cl. Осадок растворился.
Условие растворения осадка по принципу ПР заключается в следующем: осадок растворяется при ПК < ПР.
Вывод: Осадок в первой пробирке растворяется быстрее, так как в этом случае образуется вода – вещество, которое диссоциирует слабее, чем гидроксид аммония, в результате чего в первой реакции химическое равновесие более, чем во второй, смещается в сторону продуктов реакции, что и объясняет ее более быстрое протекание.
Опыт № 5. Влияние величины ПР электролита на его способность к химическому взаимодействию.
В первую пробирку мы налили 2 капли раствора FeSO4, а в другую 2 капли CuSO4, затем в каждую прилили по 3 капли (NH4)2S. Выпали осадки. К осадкам мы прилили по 6-7 капель HCl 2н. В результате этого растворился осадок CuS, а осадок FeS не растворился.
Реакции:
Это произошло из-за того, что ПР CuS < ПР FeS
Вывод: Из-за того, что для растворения ионов меди требутся небольшое число анионов хлора. Она растворяется при нормальных условиях.
Опыт №6. Получение одних малорастворимых соединений из других
В пробирку были добавлены раствор нитрата свинца (II) и раствор сульфата натрия. Получен белый осадок сульфата свинца (II).
К полученному осадку добавлен раствор сульфида аммония. Образовался черный осадок сульфида свинца.
Один осадок заменил собой другой так как ПРPbS = 6,8 * 10-29 меньше чем ПРPbSO4 = 2,2 * 10-8
Вывод: Если одно ПР> ПР другого, то при реакции замещения выпадает тот, у которого ПР меньше.
studfiles.net
Химик.ПРО — Вычислить произведение растворимости
Растворимость карбоната серебра (Ag2CO3) в воде при 25 0C равна 1,16 ⋅ 10-4 моль/л. Вычислить произведение растворимости его при этой температуре.
Решение задачи
Растворимость – это способность веществ равномерно распределяться в виде атомов, молекул или ионов по всему объему растворителя.
Равновесие в рассматриваемой системе может быть представлено уравнением:
Вычислить произведение растворимости. Из условия задачи определяем, что концентрация карбонат ионов (CO32-) в насыщенном растворе равна:
C (CO32-) = 1,16 ⋅ 10-4 (г-ион/л),
а концентрация ионов серебра (Ag+) вдвое больше, то есть:
C (Ag+) = 2 ⋅ 1,16 ⋅ 10-4 = 2,32 ⋅ 10-4 (г-ион/л).
Вычислить произведение растворимости
ПР (произведение растворимости) – постоянная величина, равная произведению концентраций ионов малорастворимого электролита в его насыщенном растворе.
Отсюда:
ПР = C2(Ag+) ⋅ C(CO32-) = (2,32 ⋅ 10-4)2 ⋅ (1,16 ⋅ 10-4) = 6,24 ⋅ 10-12.
Ответ:
произведение растворимости карбоната серебра 6,24 ⋅ 10-12.
Ввиду очень малой концентрации раствора и отсутствия других растворимых веществ концентрации ионов можно принять равными их активностям.
Похожие задачи по химии
himik.pro
12. Расчеты, связанные с растворимостью веществ
Расчетам растворимости уделяется важное место как при выполнении гравиметрического анализа, так и в методах очистки веществ (методы рекристаллизации и осаждение с коллектором). Эти вычисления позволяют подбирать необходимые пары: определяемое вещество – осадителm; рассчитать предполагаемые потери вещества в ходе осаждения.
а). Понятие произведения растворимости.
В системе раствор – осадок при постоянной
температуре между осадком
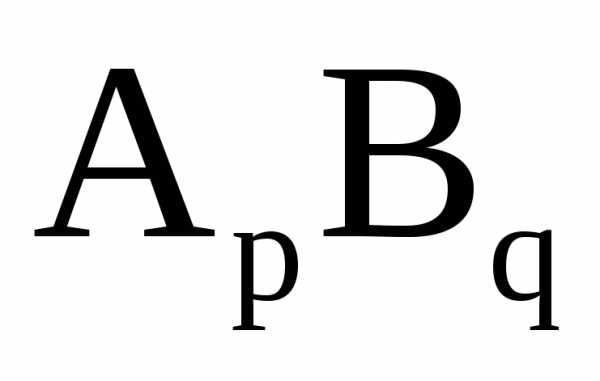 и его насыщенным раствором устанавливается
динамическое равновесие, характеризуемое
некоторой константой. Пусть малорастворимое
соединение (осадок)
и его насыщенным раствором устанавливается
динамическое равновесие, характеризуемое
некоторой константой. Пусть малорастворимое
соединение (осадок)
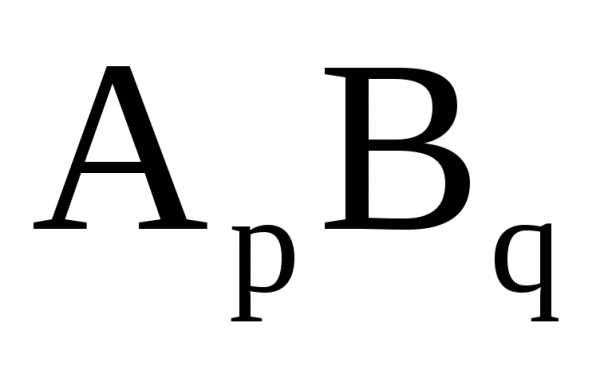 в растворе полностью диссоциирует по
уравнению:
в растворе полностью диссоциирует по
уравнению:
, (12.1)
тогда , (12.2)
где константа ПР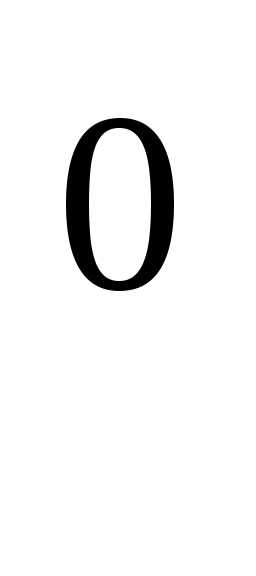 –
активностное, или термодинамическое
произведение растворимости;
–
активностное, или термодинамическое
произведение растворимости; и
и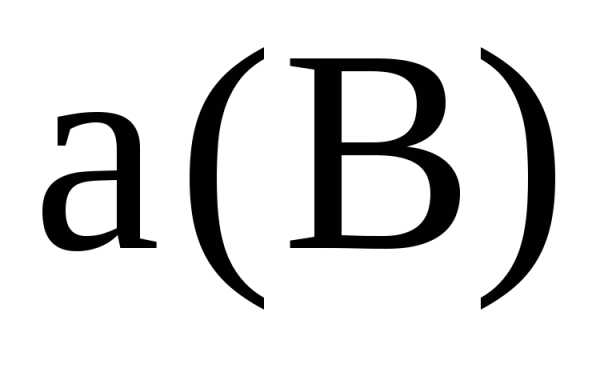 – активности ионов в насыщенном
равновесном растворе. Для разбавленных
растворов формула (9.2) примет вид:
– активности ионов в насыщенном
равновесном растворе. Для разбавленных
растворов формула (9.2) примет вид:
, (12.3)
где
 и
и – молярные равновесные концентрации
ионов осадка в растворе;
– молярные равновесные концентрации
ионов осадка в растворе;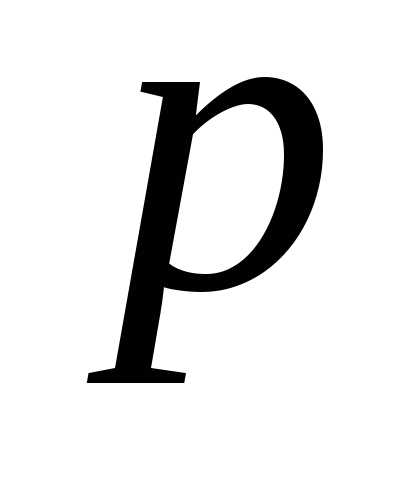 и
и – стехиометрические коэффициенты,
определяемые по уравнению (12.1).
Константа
– стехиометрические коэффициенты,
определяемые по уравнению (12.1).
Константа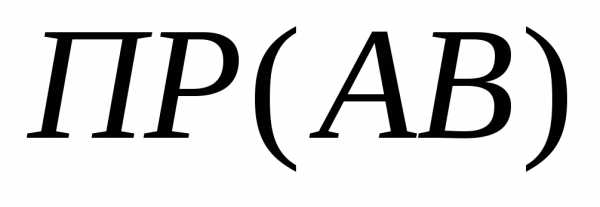 ,
рассчитанная по формуле (12.3), называетсяконцентрационным произведением
растворимости.
,
рассчитанная по формуле (12.3), называетсяконцентрационным произведением
растворимости.
б). Растворимость и ее виды; расчет растворимости.
Для практических расчетов при оценке
полноты осаждения пользоваться табличным
произведением растворимости не всегда
удобно, так как при одних и тех же
значениях
 концентрации в растворах различных
веществ могут существенно варьировать.
Гораздо проще сопоставлять содержание
веществ в насыщенных растворах по их
предельной концентрации (растворимости),
так как в ней не содержится стехиометрических
множителей.Растворимость характеризует
предельно возможную при данной температуре
концентрацию вещества в растворе до
начала образования осадка.Такие
растворы называют насыщенными, и они
также образуют с осадком равновесную
систему. В зависимости от способа
выражения предельной концентрации
различают несколько видов растворимости.
концентрации в растворах различных
веществ могут существенно варьировать.
Гораздо проще сопоставлять содержание
веществ в насыщенных растворах по их
предельной концентрации (растворимости),
так как в ней не содержится стехиометрических
множителей.Растворимость характеризует
предельно возможную при данной температуре
концентрацию вещества в растворе до
начала образования осадка.Такие
растворы называют насыщенными, и они
также образуют с осадком равновесную
систему. В зависимости от способа
выражения предельной концентрации
различают несколько видов растворимости.
1. Молярная растворимость показывает количество моль вещества осадка находящегося в 1 л его насыщенного раствора при данной температуре. Ее рассчитывают по формуле:
, (12.4)
где
 – объем насыщенного раствора в мл, а
– объем насыщенного раствора в мл, а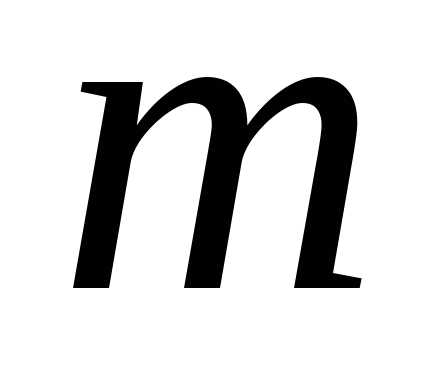 – масса неосажденного вследствие
растворимости вещества осадка.
– масса неосажденного вследствие
растворимости вещества осадка.
2. Растворимость по массе
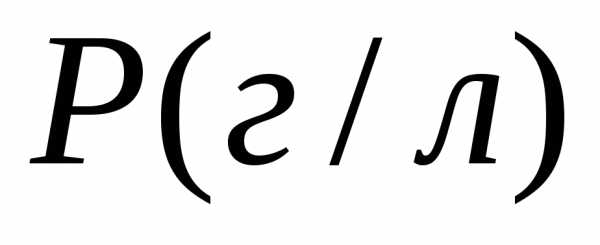 характеризует, сколько граммов данного
вещества содержится в 1 л его насыщенного
раствора. Растворимость по массе (
характеризует, сколько граммов данного
вещества содержится в 1 л его насыщенного
раствора. Растворимость по массе (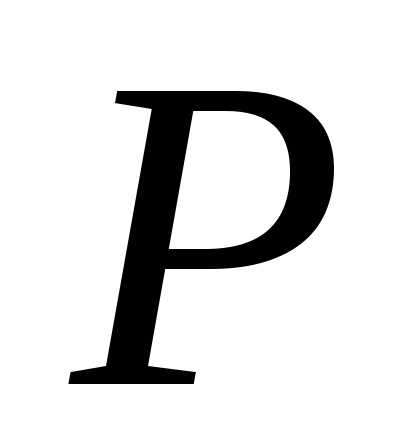 )
и молярная растворимость (
)
и молярная растворимость (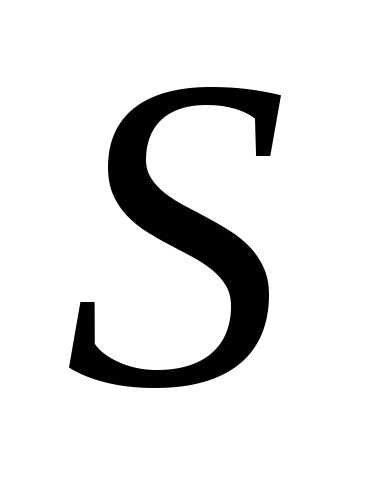 )
связаны между собой простым соотношением:
)
связаны между собой простым соотношением:
(г/л). (12.5)
Произведение растворимости малорастворимого
соединения
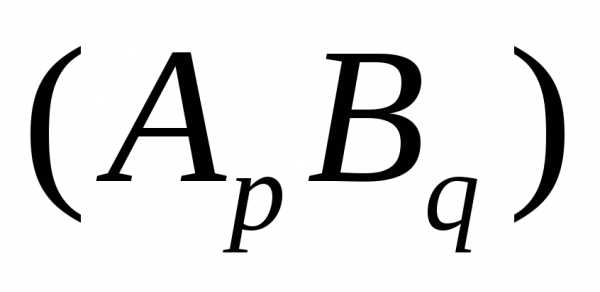 связано с его молярной растворимостью,
так как они характеризуют одну и ту же
систему раствор-осадок. Причем
растворимость – со стороны осадка, а
связано с его молярной растворимостью,
так как они характеризуют одну и ту же
систему раствор-осадок. Причем
растворимость – со стороны осадка, а – характеризует концентрацию ионов
осадка в насыщенном растворе. Выведем
эту взаимосвязь.
– характеризует концентрацию ионов
осадка в насыщенном растворе. Выведем
эту взаимосвязь.
Пусть растворимость осадка
 в насыщенном растворе составляет.
Запишем уравнение диссоциации молекул
осадка и выразим концентрации ионов в
насыщенном растворе, обозначив
растворимость
в насыщенном растворе составляет.
Запишем уравнение диссоциации молекул
осадка и выразим концентрации ионов в
насыщенном растворе, обозначив
растворимость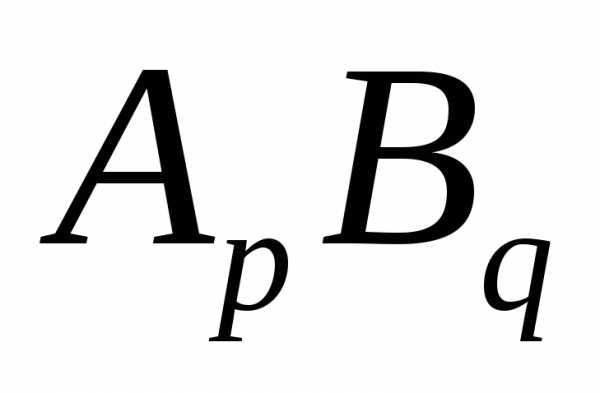 через:
через:
(12.6)
(12.7)
. (12.8)
Составим формулу и подставим в нее значения концентраций ионов из (12.7) и (12.8):
. (12.9)
Из (12.9) следует, что: (12.10)
Откуда:
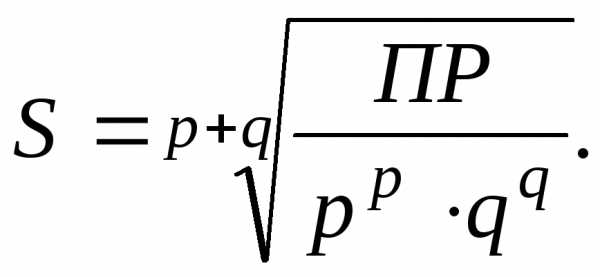 (12.11)
(12.11)
Соотношения (12.6) и (12.10) позволяют
рассчитать значение произведения
растворимости по величине растворимости
 и, наоборот. Зная молярную растворимость
легко вычислить по формулам (12.7) и (12.9)
остаточную концентрацию ионов в растворе
вследствие растворимости осадка и
оценить полноту осаждения. Зная молярную
растворимость, легко рассчитать и
растворимость по массеР.
и, наоборот. Зная молярную растворимость
легко вычислить по формулам (12.7) и (12.9)
остаточную концентрацию ионов в растворе
вследствие растворимости осадка и
оценить полноту осаждения. Зная молярную
растворимость, легко рассчитать и
растворимость по массеР.
Пример
Вычислить растворимость (г/л) осадка
и массу ионов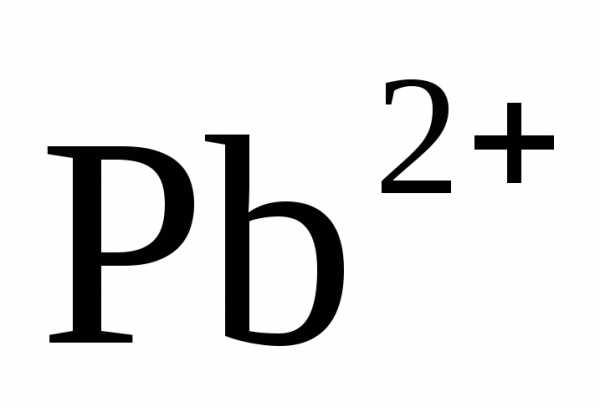 в 100 мл насыщенного водного раствора,
если.
в 100 мл насыщенного водного раствора,
если.
Решение.
1. Обозначим молярную растворимость
через .
.
2. Запишем уравнение диссоциации фосфата
свинца и определим стехиометрические
коэффициенты
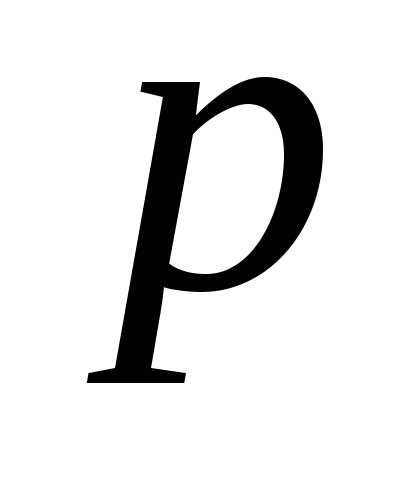 и
и :
:
; ;
; .
.
3. Выразим концентрацию ионов осадка через растворимость :
;
.
4. По уравнению диссоциации составим формулу ПР: .
5. Подставим в формулу
 концентрации ионов, выраженные через
растворимость осадка:
концентрации ионов, выраженные через
растворимость осадка:
.
6. Выразим молярную растворимость Sчерез ПР и найдем ее значение:
;.
7. Рассчитаем растворимость
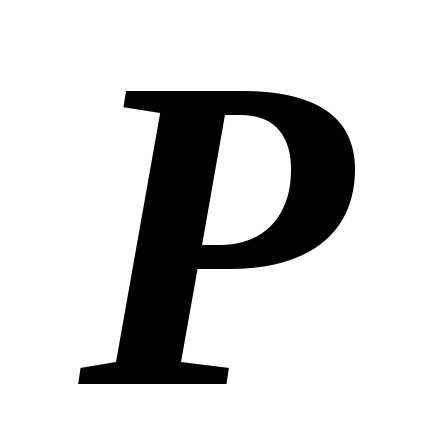 (г/л)
дляиз соотношения:
(г/л)
дляиз соотношения:
;
где – молярная масса соли;
.
8. Найдем массу неосажденных ионов
 ,
учитывая, чтопо формуле:
,
учитывая, чтопо формуле:
;
Задание 9. Вычислите растворимость (г/л) и массу неосажденного вещества.
(значение ПР приведенных веществ взять из приложения 2)
9.1. Определите растворимость Hg2SO4в водном растворе. Вычислите массу ионов ртути в 250 мл такого раствора.
9.2. Чему равна растворимость Ag2SO4(г/л) в водном растворе. Вычислите массу ионов серебра в 420 мл такого раствора.
9.3. Рассчитайте растворимость BaCrO4(г/л) в водном растворе и массу ионов бария в 350 мл такого раствора.
9.4. Вычислите растворимость PbMoO4(г/л) в водном растворе и массу неосажденного молибдата свинца в 100мл этого раствора.
9.5. Вычислите растворимость Ag2S(г/л) и массу не осажденного серебра в 400мл его водного раствора.
9.6. Рассчитайте растворимость (г/л) Ag2СO3в водном растворе. Вычислите массу ионов серебра в 250мл такого раствора.
9.7. Рассчитайте растворимость (г/л) AgBrO3в водном растворе. Вычислите массу серебра в 250мл такого раствора.
9.8. Рассчитайте растворимость MgF2(г/л) в водном растворе. Вычислите сколько грамм фтора содержит 400мл такого раствора.
9.9. Определите растворимость AgIO3(г/л) в водном растворе и вычислите массу неосажденных ионов серебра в 220мл такого раствора.
9.10. Определите растворимость (г/л) SrSO4в водном растворе. Вычислите массу сульфата стронция, оставшуюся не осажденной, в 300мл такого раствора.
9.11. Определите растворимость (г/л) Ag2CrO4в водном растворе. Вычислите массу ионов серебра в 125 мл такого раствора.
9.12. Рассчитайте растворимость Pb(JO3)2(г/л) в водном растворе. Вычислите массу ионов свинцав 240мл такого раствора.
9.13. Чему равна растворимость (г/л) соли BaS2O3в водном растворе. Вычислите массу ионов бария в 200мл такого раствора.
9.14. Рассчитайте растворимость Cu2P2O7(г/л) в водном растворе. Сколько грамм ионов меди содержит 800мл такого раствора?
studfiles.net
1. Равновесия в растворах малорастворимых соединений. Растворимость и произведение растворимости.
СПЕЦИАЛЬНОСТЕЙ 200503, 280202
ВЫПОЛНЯЮТСЯ ПО МЕТОДИЧЕСКИМ УКАЗАНИЯМ
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
УГАЭС
Кафедра Общей химии
Аналитическая химия
(методы химического анализа)
Уфа 2011
УДК 371.385.54
Составители: к.х.н., доцент О.Г.Горлевских
Методические указания: «Аналитическая химия. Методы химического анализа».- Уфа,УГАЭС 2011. 24 с.
Предназначены для студентов заочной формы обучения всех специальностей.
Рецензент:
Методические указания для студентов заочной формы обучения
Издательский центр УГАЭС 2011
Аналитическая химия — наука о методах изучения химического состава вещества. Аналитическая химия включает качественный и количественный анализ. Качественный анализ позволяет определять и идентифицировать состав вещества. Количественный анализ — определять содержание различных компонентов в анализируемой системе.
В качественном и количественном анализе используют химические, физические и физико-химические методы исследования. Химические методы анализа основаны на способности веществ вступать в химические взаимодействия. Физические методы основаны на измерении каких-либо физических параметров веществ. Физико-химические методы основаны на наблюдении за изменением физических свойств веществ, которые происходят в результате химической реакции.
В качественном анализе для обнаружения ионов и молекул используют химические и физико-химические методы.
При количественных определениях применяются химические методы (титриметрический и гравиметрический), физические и физико-химические (атомная и молекулярная абсорбционная спектроскопия, эмиссионный спектральный анализ, флуориметрия, поляриметрия,рефрактометрия, кондуктометрия, потенциометрия; полярография, кулонометрия, хроматография и т.д.). Несмотря на преимущества, которые имеют физические и физико-химические методы по сравнению с химическими методами количественного анализа, последний широко используются в практике научно-исследовательских и заводских лабораторий. Это объясняется простотой методики эксперимента и сочетанием правильности и воспроизводимости результатов анализа.
В настоящем пособии основное внимание уделено химическим методам количественного анализа, имеющим наибольшее значение для работников пищевых предприятий.
Пособие состоит из трех разделов:
1)равновесия в растворах труднорастворимых соединений;
2)гравиметрический анализ;
3)титриметрический анализ.
В начале каждого раздела кратко изложена теория, даны примеры решения задач. В конце каждого раздела приведены контрольные вопросы и задачи для выполнения контрольной работы. Варианты контрольных работ и справочные таблицы помещены в конце пособия.
Ионные равновесия, связанные с образованием осадков, являются обратимыми, подчиняются закону действующих масс и характеризуются константой равновесия, которую принято называть произведением растворимости (ПР). Произведение растворимости — постоянная величина. Она равна произведению активностей ионов в насыщенном растворе малорастворимого электролита.
Например, при образовании осадка хлорида серебра имеет место равновесие, которое описывается уравнением:
AgCl Аg+ + Сl—
Для приближенных раcчетов произведение растворимости AgCl можно записать в виде следующего выражения:
ПР(AgCl)=[Ag+] +[Cl—],
так как молярные концентрации ионов в данном случае мало отличаются от их активностей. Таким образом, для любой труднорастворимой соли МpAq можно записать в общем виде:
ПР (МpАq) =[M]p + [A]q
По опытным данным о растворимости труднорастворимых электролитов рассчитывают их произведение растворимости или на основании табличных данных о произведении растворимости решают обратную задачу. При этом необходимо, помнить, что растворимость вещества может быть выражена в любых единицах измерения, а ПР рассчитывается только по концентрациям, выраженным в моль/дм3 или в моль/л.
Все вычисления, связанные с образованием и растворением осадков, выполняют по следующей схеме:
составляют уравнения диссоциации электролитов;
составляют ионные уравнения образования осадков;
записывают выражение ПР в соответствии с ионным уравнени- ем, описывающим образование осадка и находят значение ПР по таб- лице;
вычисляют значения равновесных концентраций ионов по за- данным концентрациям сильных электролитов или с учетом Кдис. для слабых электролитов;
сопоставляя заданные концентрации и условия задачи, составляют алгебраическое уравнение, по которому определяют искомую величину.
Пример1. Вычислить ПР (BaSO4), если его растворимость равна 2,33 мг/л.
Решение:
Для вычисления
ПР (BaS04)=
[Ва2+]•[SO ]
необходимо рассчитать
концентрацию
BaS04
в
моль/л. Для этого нужно весовое колическтво
соли
BaSQ4,
равное 2,33 мг, выразить в молях, для чего
данное
его весовое количество надо разделить
на мольную массу
сульфата
бария, т.е. 233,4 г/мол:
]
необходимо рассчитать
концентрацию
BaS04
в
моль/л. Для этого нужно весовое колическтво
соли
BaSQ4,
равное 2,33 мг, выразить в молях, для чего
данное
его весовое количество надо разделить
на мольную массу
сульфата
бария, т.е. 233,4 г/мол:
0,00233г : 233,4 г/моль=10-5 моль.
Поскольку
концентрация соли BaS04
очень мала, то соль в растворе
диссоциирована полностью и тогда
концентрация ионов Ba2+
и
S0 будет равна 10-5
моль/л. Соответственно, произведение
растворимости
будет равна 10-5
моль/л. Соответственно, произведение
растворимости
ПР(BaSO )=
[Ва2+]•[SO
)=
[Ва2+]•[SO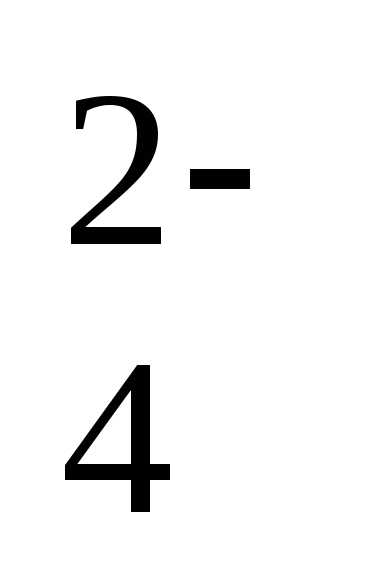 ]=
10-5
•10-5
= 10-10.
]=
10-5
•10-5
= 10-10.
Пример 2. Вычислить растворимость СаСО3 в граммах на 100 г насыщенного раствора, если ПР(СаСОз) =1,7•10 -8.
Решение: Записываем уравнение образования осадка:
Сa2+
+
CO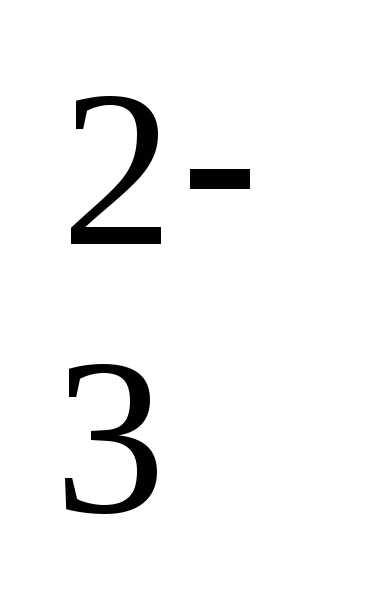 =
CaCO3
=
CaCO3
Согласно
уравнению [Сa
2+]•[
CO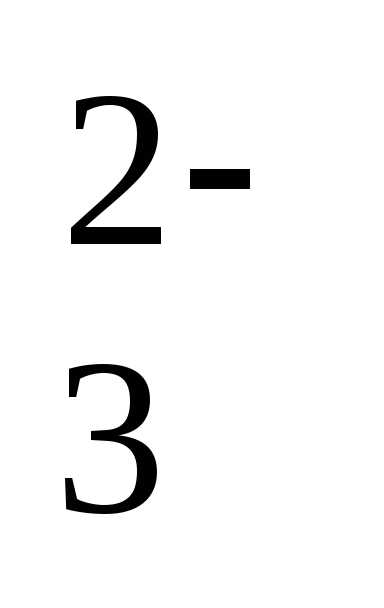 ]=
В
насыщенном растворе СаСОз равновесные
концентрации Са2+
и CO
]=
В
насыщенном растворе СаСОз равновесные
концентрации Са2+
и CO равны;
обозначим эту концентрацию «х»,
т.е. [Сa
2+]•[
CO
равны;
обозначим эту концентрацию «х»,
т.е. [Сa
2+]•[
CO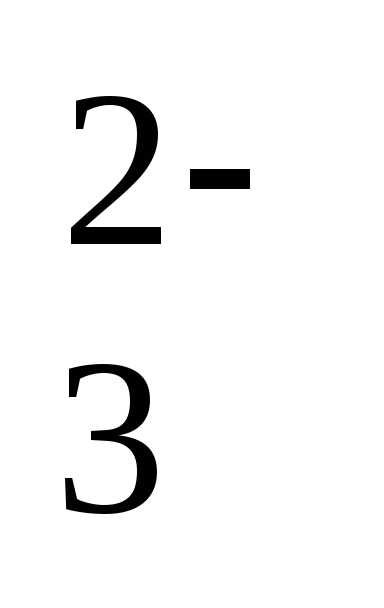 ]
=х.
Тогда
]
=х.
Тогда
[Сa
2+]•[
CO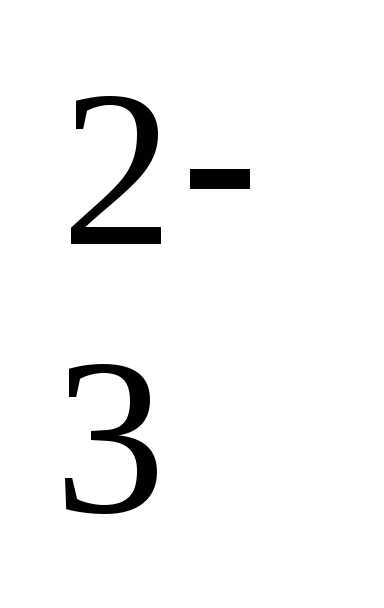 ]=1,7•10
-8
=
х2,
откуда
]=1,7•10
-8
=
х2,
откуда
х=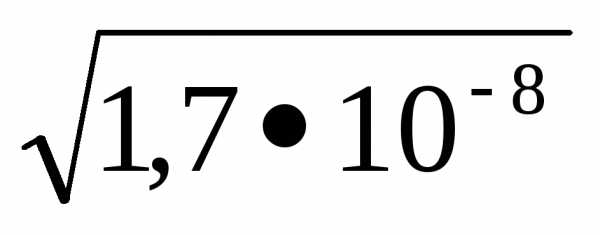 =
1,3•10-4моль/л.
=
1,3•10-4моль/л.
Следовательно, и концентрация СаСОз в насыщенном растворе равна 1,3•10-4 моль/л. Растворимость «а» СаСОз в г получим, умножив мольную концентрацию на молекулярную массу соли:
а=1,3•10-4•100=1,3•10-2 г/л, или 1,3•10-4 /10=1,3•10-3 г/100см3 .
Принимая плотность очень разбавленного раствора равной 1 г/см3, получим, что растворимость СаСОз равна 1,3•10-4г на 100 г раствора.
Радение данной задачи носит приближенный характер.
Условия образования и растворения осадков.
Следствием из определения произведения растворимости является вывод, что осадок выпадает из перенасыщенного раствора, т.е
когда произведение концентраций ионов выше ПР, взятых из справочных таблиц. Если произведение концентраций ионов — меньше ПР, то осадок не выпадает, и при внесении в такой раствор кристалликов твердой фазы этого вещества будет наблюдаться растворение твердого вещества.
Пример 3. Может ли образовываться осадок Mg(OH)2 , если смешать равные объёмы 0,5М раствора MgCl2 и 0,1М раствора NH4 OH?
Решение: За счет увеличения объёма при сливании растворов вдвое следует учитывать уменьшение начальных концентраций также вдвое, т.е. концентрация раствора MgCl2 станет равной 0,5М:2 – 0,25М/л, а концентрация NH4 OH — равной 0,1М:2 – 0,05 М/л.
Уравнения записываются в следующем виде:
Mg+2 + 2OH— Mg(OH)2
ПР(Mg(OH)2)=[ Mg+2] •[ OH—]2 .
Для ответа на вопрос, выпадает ли в осадок Mg(OH)2 , нужно знать концентрацию ионов Mg+2 и OH— . Концентрацию ионов магния принимаем равной 0,25 моль/л, учитывая, что хлорид магния является сильным электролитом и диссоциирует полностью.
Для вычисления концентрации ионов OH— используют выражение константы диссоциации:
NH4 OH NH4 + + OH—
К=[ NH4 +]•[ OH—]/[ NH4 OH]=1,8•10-5
Принимаем равновесные концентрации [ NH4 +]=[ OH—]=х и
[ NH4 OH]=0,05-х. Тогда х2 / (0,05-х)= 1,8•10-5 .
Решим уравнение в упрощенном виде, т.е. примем, что 0,05-х=0,05М/л. Теперь находим значение «х»:
х == 9,5•10-4моль/л.
Используя значения концентраций [ Mg+2] =0,25 моль/л и [ OH—]= 9,5•10-4моль/л для вычисления произведения начальных концентраций по выражению для ПР, получим:
[ Mg+2] •[ OH—]2 =0,25•(9,5•10-4)2 =2,25•10-7 .
Полученную величину сравниваем с табличным значением ПР(Mg(OH)2)= 5,2•10-12 . Очевидно, что рассчитанное произведение концентраций превышает табличное значение ПР(Mg(OH)2), следовательно, раствор пересыщен, и осадок должен выпадать.
Пример 4. При каком значении рН начнется выпадение осадка Fe(OH)2 из 0,1 М раствора FeSO4 при добавлении раствора NaOH?
Решение: Образование осадка описывается уравнением:
Fe2+ + 2OH— Fe(OH)2 ,
для которого выполняется условие
ПР(Fe (OH)2)=[ Fe 2+] •[ OH—]2 =1,1•10-15.
Принимая,
что соль FeSO4,
как сильный электролит, в растворе
диссоциирует полностью, равновесная
концентрация ионов [Fe2+]=0,1
моль/л.Исходя из выражения
ПP(Fe(OH)2)
получаем:
10-1]•[ОН—]2=
1,1•10-15;
[ОН—]=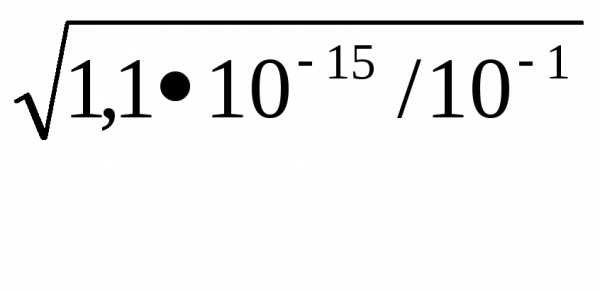 =10-7
моль/л.
=10-7
моль/л.
Учитывая, что рН=-lg [Н+],а [H+]•ОH—]=10-14, найдем, что концентрация ионов водорода равна 10-14/10-7моль/л и рН соответственно равно -lg•10-7=7
Таким образом, при pH=7 начинается выпадение осадка Fe(OH)2 из 0,1 М раствора FeSO4 при добавлении NaOH.
studfiles.net
Произведение растворимости
Гетерогенное равновесие: осадок ↔ насыщенный раствор
подчиняется правилу произведения растворимости – в насыщенном растворе трудно растворимого сильного электролита произведение концентраций (активностей) ионов, возведенных в степени стехиометрических коэффициентов, есть величина постоянная при данной температуре.
Если малорастворимый электролит распадается на ионы по уравнению:
Ca3(PO4)2 = 3Ca2+ + 2PO43−,
то выражение для произведения растворимости будет иметь вид:
ПР(Ca3(PO4)2) = a3(Ca2+) · a2 (PO43−) = fa(Ca2+)·[Ca2+]3· fa(PO43−)·[PO43−]2.
В разбавленных растворах, какими являются насыщенные растворы трудно растворимых электролитов, при fа =1, а =С, тогда: ПР(Ca3(PO4)2)= [Ca2+]3·[PO43−]2.
Отсюда вытекают два следствия:
1. Условие растворения осадка: произведение концентраций ионов возведенных в степень стехиометрических коэффициентов, должно быть меньше величины произведения растворимости ПР(Ca3(PO4)2) > [Ca2+]3·[PO43−]2.
2. Условие образования осадка: произведение концентраций ионов возведенных в степень стехиометрических коэффициентов, должно быть больше величины произведения растворимости ПР(Ca3(PO4)2)< [Ca2+]3·[PO43−]2.
Пример 1. Растворимость (S) карбоната кальция в воде при температуре 250 С составляет 6,9 ·10 −5 моль/л. Найти ПР(CaCO3). S S S
Решение. В насыщенном растворе карбоната кальция: CaCO3 ↔ Ca2++CO32−,
[Ca2+] = [CO32−] = S = 6,9 ·10 −5 моль/л. Отсюда, ПР(CaCO3) =[Ca2+]·[CO32−]=S·S= S2.
Подставляем числовые значения: ПР(CaCO3) = (6,9 ·10 −5)2 = 4,8·10 −9.
Пример 2. Произведение растворимости йодида свинца ПР(PbI2) = 1,1·10−9. Чему равна S (растворимость) йодида свинца? S S 2S
Решение. Запишем уравнение диссоциации: PbI2 ↔ Pb2+ + 2I−. Из каждой молекулы йодида свинца образуется один ион Pb2+ и два иона I−. Следовательно, в насыщенном растворе PbI2, растворимость ионов свинца [Pb2+] = S, а йодид –ионов [I−] = 2S. Отсюда получаем: ПР(PbI2) = [Pb2+]·[I−]2 = S·(2S)2 = 4S3. Растворимость йодида свинца
___________ __________
[PbI2]= S = 3√ ПР(PbI2) / 4 ; S= 3√ 1,1·10−9 / 4 = 6,5·10−4 моль/л.
Лабораторная работа № 4 Произведение растворимости
Опыт 1. Дробное осаждение.
Выполнение работы. В две пробирки внести по 1 капле 0,5 н раствора нитрата серебра (AgNO3). В пробирку №1 добавить 2 капли 0,5 н раствора хлорида калия (AgNO3+КС1→AgCl↓+KNO3), №2 — 2 капли 0,5 н раствора хромата калия (2AgNO3+K2CrO4→Ag2CrO4↓+2KNO3).
Написать ионные уравнения реакций, отметить цвет осадков хлорида и хромата серебра.
Какое вещество будет выпадать в осадок первым из раствора, содержащего ионы Cl−, CrO42− и Ag+ в равных концентрациях?
ПР(AgCl)=1,8∙10−10; ПР(Ag2CrO4) = 4∙ 10−12
Проверить предположение опытом, для чего в пробирку №3 внести сначала
2 капли 0,5 н раствора хлорида калия (КС1), затем 2 капли 0,5 н раствора хромата калия (K2CrO4), добавить 3 капли дистиллированной воды. Раствор тщательно перемешать. Осторожно прибавить к нему 1 каплю 0,5 н раствора нитрата серебра (AgNO3), перемешать. Какое вещество при этом образуется? Добавить ещё несколько капель раствора нитрата серебра, тщательно перемешать. Наблюдается ли образование хромата серебра? Отметить его образование при дальнейшем увеличении концентрации катионов серебра.
Запись данных опыта. Описать наблюдаемые явления. Написать выражения, произведений растворимости хлорида и хромата серебра. Объяснить, применив следствие правила произведения растворимости, последовательность образования осадков в данном опыте (пробирка №3), учитывая величины произведений растворимости хлорида и хромата серебра. На все вопросы ответить письменно.
Опыт 2. Условия растворения осадков.
а) Влияние величины произведения растворимости на растворение осадков.
Выполнение работы. В три пробирки внести по 1 капле0,5 н раствора нитрата серебра (AgNO3). Затем в первую пробирку добавить 1 каплю 0,5 н раствора хлорида калия (AgNO3+КС1→AgCl↓ +KNO3), во вторую – 1 каплю0,5 н раствора бромида калия (AgNO3+KBr→AgBr↓+KNO3), в третью – 1 каплю 0,5 н раствора йодида калия (AgNO3+KI→AgI↓+KNO3). Отметить цвет образовавшихся осадков. К осадкам в каждую пробирку добавлять по каплям 2 н водный раствор аммиака (NH3∙H2O), тщательно перемешивая полученные растворы. В какой пробирке осадок растворился быстрее? Осадок, какого вещества практически не растворим?
Запись данных опыта. Написать уравнения реакций растворения осадков, соответствующих галогенидов серебра в водном растворе аммиака, протекающих с образованием комплексного иона [Ag(NH3)2]+ (AgCl+2NH3∙H2O=[Ag(NH3)2]++ Cl−+2H2O.) Написать выражения произведений растворимости хлорида, бромида и йодида серебра (ПР(AgCl)=1,8∙10−10; ПР(AgBr)=6∙10−13; ПР(AgI)=1,1∙10−16). Как влияет величина произведения растворимости на растворимость сильных, но трудно растворимых электролитов?
studfiles.net
