Катализатор | Химическая энциклопедия
Одно из наиболее эффективных воздействий на химические реакции – это применение катализатора. Катализаторы – это вещества, ускоряющие химические реакции. Присутствие катализаторов изменяет скорость реакции в тысячи и даже миллионы раз. Катализаторы активно участвуют в химической реакции, но в отличие от реагентов в конце ее остаются неизменными.
Катализаторы – это вещества, которые изменяют скорость протекания реакции, но сами не расходуются в ходе реакции и не входят в состав конечных продуктов.
Важной характеристикой каталитической реакции (катализа) является однородность или неоднородность катализатора и реагирующих веществ. Различают гомогенные и гетерогенные каталитические процессы. При гомогенном (однородном) катализе между реагирующими веществами и катализатором отсутствует поверхность раздела. В данном случае катализ осуществляется через образование неустойчивых промежуточных продуктов.
Например, вещество A должно вступить в реакцию с веществом B. Однако для начала реакции необходимо сильное нагревание, и реакция далее протекает медленно. Тогда подбирают катализатор с таким расчетом, чтобы он с веществом A образовал активное промежуточное соединение, способное потом энергично реагировать с веществом B:
A + Кат. = A ∙ Кат.
A ∙ Кат. + B = AB ∙ Кат.
Кат.
A + B = AB
Процессы, в которых катализатор и катализируемые вещества находятся в разных агрегатных состояниях, относятся к гетерогенному (неоднородному) катализу. При адсорбции на поверхности катализатора газообразных или жидких реагентов ослабляются химические связи, возрастает способность этих веществ к взаимодействию.
Ускоряющее действие катализатора заключается в понижении энергии активации основной реакции. Каждый из промежуточных процессов с участием катализатора протекает с меньшей энергией активации, чем некатализируемая реакция. Катализ открывает иной пут протекания химической реакции от исходных веществ к продуктам реакции.
Опыт показывает, что катализаторы строго специфичны для конкретных реакций. Например, в реакции:
N2+3H2 =Fe 2NH3
Катализатором является металлическое железо, а в реакции окисления оксида серы(IV) в оксид серы(VI) катализатор – оксид ванадия(V) V2O5. Часто в качестве катализаторов используют платину, никель, палладий, оксид алюминия. Для ускорения процесса разложения пероксида водорода в качестве катализатора применяют оксид марганца(IV). Если в стакан с раствором пероксида водорода добавить немного оксида марганца(IV), сразу происходит бурное вспенивание жидкости в результате выделения кислорода.
Катализатором реакции взаимодействия алюминия и йода является обычная вода. Если к смеси алюминия и йода прилить воду, то вещества в смеси бурно реагируют.
Существуют вещества, способные замедлять химическую реакцию – осуществлять так называемый отрицательный катализ. Их называют ингибиторами. Такие вещества применяют при необходимости замедлит некоторые процессы, например коррозию металлов, окисление сульфидов при хранении и др.
abouthist.net
Катализатор. Что это такое, или кто это такой?
Катализатор[править]
Материал из Википедии — свободной энциклопедии
Катализа́тор — вещество, ускоряющие реакцию, но не входящее в состав продуктов реакции (Химическая энциклопедия) . Количество катализатора, в отличие от других реагентов, при реакции не изменяется. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно (сотни, миллионы раз) повторяется.
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный – образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества (Химическая энциклопедия) . Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO (Химическая энциклопедия) .
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.) .
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-востановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции (Имянитов, Temkin). Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа» , или катализ второго уровня (Имянитов) .
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
otvet.mail.ru
Катализаторы (в химии) — «Энциклопедия»
КАТАЛИЗАТОРЫ, функциональные материалы и вещества, ускоряющие или инициирующие химические реакции за счёт промежуточных химических взаимодействий с участниками реакции и восстановления своего химического состава после каждого цикла таких промежуточных взаимодействий (смотри в статье Катализ). По способу организации и фазовому составу реакционной системы принято различать гетерогенные и гомогенные катализаторы, а также катализаторы биологического происхождения — ферменты. В гетерогенном катализе катализаторы иногда называют контактами.
В общем случае носителем каталитической активности катализаторов (смотри в статьях Гетерогенный катализ, Гомогенный катализ) обычно является вещество, непосредственно вступающее в химическое взаимодействие, по крайней мере, с одним из исходных реагентов с образованием нестойких (в условиях проведения каталитической реакции) химических соединений, — активный компонент катализатора (для твёрдых гетерогенных катализаторов часто каталитическая активная фаза). Механизмы действия катализаторов достаточно разнообразны и зависят от типа осуществляемой каталитической реакции и природы вещества активного компонента катализатора; химическая природа активного компонента катализаторов также может быть самой разнообразной. Массовая доля активного компонента в катализаторах может варьировать от 100% до весьма малых величин (десятые доли процента).
Реклама
Основными характеристиками катализаторов являются каталитическая активность, селективность по отношению к целевым продуктам каталитических превращений, специфичность по отношению к реагентам каталитических реакций, стабильность, устойчивость к действию каталитических ядов; для промышленных катализаторов ещё и производительность (количество целевого продукта, полученного за единицу времени на единицу объёма или массы катализатора).
Обычно катализаторы подразделяют по типам каталитических процессов: глубокого и парциального (селективного) окисления, гидрирования, полимеризации, процессов нефтепереработки, органического синтеза и др. Типичными катализаторами окислительно-восстановительных реакций (окисления, гидрирования и пр.) являются переходные элементы в металлическом виде, а также их соли, комплексные соединения, оксиды и сульфиды. Типичными катализаторами кислотно-основных реакций (гидратации, дегидратации, алкилирования, полимеризации, крекинга и пр.) являются жидкие и твёрдые минеральные и органические кислоты и основания, кислые соли, алюмосиликаты, цеолиты и др.
В промышленности предпочитают использовать твёрдые гетерогенные катализаторы вследствие лёгкости их отделения от реакционной среды и возможности работы при повышенных температурах. Активный компонент (каталитически активная фаза) многих промышленных гетерогенных катализаторов является высокодисперсным и нередко нанесённым на прочный пористый носитель (обычно высокопористый углерод, оксид непереходного элемента, например, кремния, алюминия, титана, циркония, и др.). Для увеличения каталитической активности, селективности, химической устойчивости и термостабильности в катализаторы иногда вводят небольшое количество промотора (или активатора) — вещества, которое может не обладать самостоятельной каталитической активностью.
Твёрдые промышленные катализаторы должны обладать высокими каталитической активностью, специфичностью по отношению к заданной реакции, селективностью по отношению к целевому продукту, механической прочностью, термостойкостью, определённой теплопроводностью. Промышленные катализаторы должны быть также стойкими по отношению к дезактивации — снижению или полному подавлению их каталитической активности. Дезактивация катализаторов может происходить за счёт спекания или механического разрушения (например, истирания) активного компонента и/или вещества носителя, блокировки активных центров побочными продуктами процесса — плотными углеродными отложениями (коксом), смолистыми веществами и пр., отравления каталитическими ядами. Действие каталитических ядов обычно обусловлено блокировкой наиболее активных участков активного компонента катализаторов за счёт прочной хемосорбции и поэтому проявляется даже при наличии малых количеств ядов. Типичными каталитическими ядами являются соединения серы, азота, фосфора, мышьяка, свинца, ртути, цианистые соединения, кислород, монооксид углерода, производные ацетилена, иногда вода и др. В промышленности для предотвращения отравления катализаторов производят глубокую предварительную очистку реагирующих веществ от каталитических ядов. В промышленных каталитических процессах для восстановления каталитической активности катализаторы после их дезактивации регенерируют. Регенерацию катализаторов осуществляют, например, выжиганием кокса и смолистых веществ, промыванием водой или специально подобранными растворителями.
Каталитическая активность твёрдого катализатора зависит от величины и состояния доступной для реагентов поверхности катализатора, формы, размера и профиля пор катализатора (то есть его текстуры), что определяется способом приготовления катализатора и его предварительной обработкой. В условиях отсутствия диффузионных ограничений активность твёрдого катализатора прямо пропорциональна такой поверхности. Поэтому большинство промышленных гетерогенных катализаторов имеет развитую удельную поверхность, вплоть до нескольких сотен м2 на 1 г катализатора. Наиболее распространёнными методами получения активных твёрдых катализаторов являются осаждение гидроксидов и карбонатов металлов из растворов солей или комплексных соединений с последующим термическим разложением осадка до оксидов, разложение иных соединений на воздухе до оксидов, сплавление нескольких веществ с последующим выщелачиванием одного из них (так называемые сплавные, или «скелетные», катализаторы), а также нанесение активного компонента катализатора на носитель методом пропитки или из газовой фазы с последующей активацией катализатора. Типичными процедурами активации катализаторов являются их восстановление водородом, сульфидирование с помощью различных серосодержащих соединений и т.п.; для некоторых типов катализаторов используется термоактивация, осуществляемая с помощью прогрева катализатора до температуры формирования активной фазы. Механически прочные катализаторы изготавливают в виде прессованных таблеток, а также полученных специальными методами гранул, шариков, сплошных и полых цилиндров (колец Рашига), различного рода экструдатов и пр. В ряде случаев для снижения аэро- или гидродинамического сопротивления слоя катализаторов им придают и более специфические формы. Например, каталитические нейтрализаторы автомобильных выхлопов обычно изготавливают в виде керамических или металлических «сотовых» блоков со множеством параллельных каналов вдоль потока очищаемого газа. В промышленности применяют также суспензии катализаторов в жидкой фазе (суспензионный процесс) и пылевидные катализаторы, которые в ходе реакции оказываются взвешенными в парах компонентов реакции (так называемый флюид-процесс).
Стоимость катализатора зависит от его химического состава, способа приготовления и варьирует от 0,5 до нескольких тысяч долларов США за 1 кг катализатора. Тем не менее, в стоимости готовой продукции, полученной с помощью промышленных катализаторов, стоимость катализатора обычно составляет не более 0,1-1%.
Промышленные гетерогенные катализаторы являются мало- или среднетоннажной продукцией. Общий объём их годового потребления в России около 100 тысяч тонн.
Литературу смотри при статье Катализ.
В. Н. Пармон.
knowledge.su
Катализатор Википедия
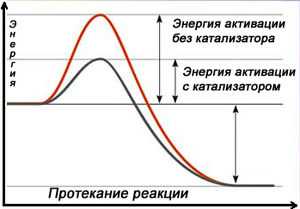 Схема протекания реакции с катализатором
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Противоположное понятие — ингибитор.
Катализаторы в химии[ | ]
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества[1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO[1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня[2].
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его деза
ru-wiki.ru
Катализаторы — это… Что такое Катализаторы?
Катализа́тор — вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции (Химическая энциклопедия). Количество катализатора, в отличие от других реагентов, при реакции не изменяется. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно (сотни, миллионы раз) повторяется.
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный – образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества (Химическая энциклопедия). Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO (Химическая энциклопедия).
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-востановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции (Имянитов, Temkin). Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
На дороги ежедневно выезжают миллионы автомобилей, и каждый из них — источник загрязнения воздуха. Особенно это чувствуется в крупных городах, где выхлопные газы автомобилей могут создавать большие проблемы.
В современных автомашинах присутствует каталитический преобразователь или автомобильный катализатор. Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счет неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.[1]
Источники
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru.
Литература
- Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443 — 1454. — 0132-344X.
- Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
Ссылки
См. также
Wikimedia Foundation. 2010.
dic.academic.ru
Катализатор Википедия
 Схема протекания реакции с катализатором
Схема протекания реакции с катализатором
Катализа́тор — химическое вещество, ускоряющее реакцию, но не расходующееся в процессе реакции.
Противоположное понятие — ингибитор.
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества[1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO[1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции[2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня[2].
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
См. также
Примечания
- ↑ 1 2 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ 1 2 Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе (неопр.). AutoRelease.ru. Архивировано 25 августа 2011 года.
Ссылки
wikiredia.ru
Катализатор
Химия — Катализатор
01 марта 2011Оглавление:
1. Катализатор
2. Катализаторы в автомобилях
Схема протекания реакции с катализатором
химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции. Количество катализатора, в отличие от других реагентов, после реакции не изменяется. Важно понимать, что катализатор участвует в реакции. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно повторяется.
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества . Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO .
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе.
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения. В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла. Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции . Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня.
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Просмотров: 2855
| Каталитическая грелка |
4108.ru
