Электролитическая диссоциация
Вещества, растворы (или расплавы) которых проводят электрический ток, называются э л е к т р о л и т а м и. Нередко электролитами называют и сами растворы этих веществ. Эти растворы (расплавы) электролитов являются проводниками второго рода, так как передача электричества осуществляется в них движением и о н о в — заряженных частиц. Частица, заряженная положительно называется катионом (Са+2), частица несущая отрицательный заряд — анионом (ОН־). Ионы могут быть простые (Са+2, Н+) и сложные (РО4 ־3, НСО3־2).
Основоположником теории электролитической диссоциации является шведский ученый С. Аррениус. Согласно теории
Свой вклад в развитие этой теории внесли русские ученые: Д.И. Менделеев, И. А. Каблуков – сторонники химической теории растворов, обращавшие внимание на влияние растворителя в процессе диссоциации. Каблуков утверждал, что растворенное вещество взаимодействует с растворителем (процесс с о л ь в а т а ц и и) образуя продукты переменного состава (с о л ь в а т ы).
Сольват представляет собой ион, окруженный молекулами растворителя (сольватная оболочка), которых может быть разное количество (именно за счет этого достигается переменный состав). Если растворителем является вода, то процесс взаимодействия молекул растворенного вещества и растворителя называется г и д р а т а ц и е й, а продукт взаимодействия — г и д р а т о м.
Таким образом, причиной электролитической диссоциации является сольватация (гидратация). И именно сольватация (гидратация) ионов препятствует обратному соединению в нейтральные молекулы.
Количественно процесс диссоциации характеризуется величиной степени электролитической диссоциации (α), которая представляет собой отношение количества распавшегося на ионы вещества к общему количеству растворенного вещества. Отсюда следует, что для сильных электролитов α = 1 или 100 % (в растворе присутствуют ионы растворенного вещества), для слабых электролитов 0 < α < 1 (в растворе присутствуют наряду с ионами растворенного вещества и его недиссоциированные молекулы), для неэлектролитов
Если растворителем является вода, к сильным электролитам относятся:
1) все соли;
2) следующие кислоты: HCl, HBr, HI, H2SO4, HNO3, HClO4;
3) следующие основания: LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2.
Процесс электролитической диссоциации является обратимым, следовательно, его можно охарактеризовать величиной константы равновесия, которая, в случае слабого электролита, называется константой диссоциации (КД).
Чем больше эта величина, тем легче электролит распадается на ионы, тем больше его ионов в растворе. Например: HF ═ H + + F־
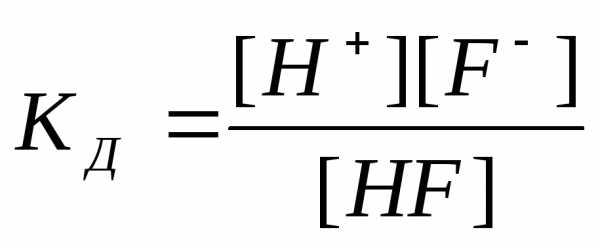 .
.
Эта величина постоянная при данной температуре и зависит от природы электролита, растворителя.
Многоосновные кислоты и многокислотные основания диссоциируют ступенчато. Например, молекулы серной кислоты в первую очередь отщепляют один катион водорода:
H2SO4 ═ Н+ + HSO4־.
Отщепление второго иона по уравнению
HSO4־═ Н+ + SO4־2
идет
уже значительно труднее, так как ему
приходится преодолевать притяжение со
стороны двухзарядного иона SO4־2,
который, конечно, притягивает к себе
ион водорода сильнее, чем однозарядный
ион HSO
Основания, содержащие более одной гидроксильной группы в молекуле, тоже диссоциируют ступенчато. Например:
Ba(OH)2 ═ BaOH+ + OH— ;
BaOH+ = Ba2+ + OH—.
Средние (нормальные) соли всегда диссоциируют на ионы металлов и кислотных остатков:
CaCl2 = Ca2+ + 2Cl— ;
Na2SO4 = 2Na+ + SO42-.
Кислые соли, подобно многоосновным кислотам, диссоциируют ступенчато. Например:
NaHCO3 = Na+ + HCO3— ;
HCO3— = H + + CO32-.
Однако степень диссоциации по второй ступени очень мала, так что раствор кислой соли содержит лишь незначительное число ионов водорода.
Основные соли диссоциируют на ионы основных и кислотных остатков. Например:
Fe(OH)Cl2 = FeOH2+ + 2Cl—.
Вторичной диссоциации ионов основных остатков на ионы металла и гидроксила почти не происходит.
studfiles.net
Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
Все вещества делятся на 2 большие группы: электролитыинеэлектролиты.
Электролитами называются вещества (исключая металлы), растворы или расплавы которых проводят электрический ток. К электролитам относятся соединения, образованные ионными или ковалентными полярными связями. Это сложные вещества: соли, основания, кислоты, оксиды металлов (проводят электрический ток только в расплавах).
Неэлектролитаминазываются вещества, растворы или расплавы которых электрический ток не проводят. К ним относятся простые и сложные вещества, образованные малополярными или неполярными ковалентными связями.
Свойства растворов и расплавов электролитов впервые объяснил в конце XIXвека шведский учёный Сванте Аррениус. Им была создана специальнаятеория электролитической диссоциации, основные положения которой, доработанные и развитые другими учёными, в настоящее время формулируются следующим образом.
1. Молекулы (или формульные единицы) электролитов в растворах или расплавах распадаются на положительно и отрицательно заряженные ионы. Этот процесс называется электролитической диссоциацией. Общая сумма зарядов положительных ионов равна сумме зарядов отрицательных ионов, поэтому растворы или расплавы электролитов в целом остаются электронейтральными. Ионы могут быть какпростые, состоящие только из одного атома (Na+,Cu2+,Cl–,S2-), так исложные, состоящие из атомов нескольких элементов (SO42–,PO43–,NH4+, [Al(OH)4]–).
Простые ионы по своим физическим, химическим и физиологическим свойствам существенно отличаются от нейтральных атомов, из которых они образовались. В первую очередь, ионы являются гораздо более устойчивыми частицами, чем нейтральные атомы, и могут существовать в растворах или расплавах неограничено долгое время, не вступая в необратимое взаимодействие с окружающей средой.
Такое различие в свойствах атомов и ионов одного и того же элемента объясняется разным электронным строением этих частиц.
Так, простые ионы s- иp-элементов находятся в более устойчивом состоянии, чем нейтральные атомы, потому что имеют завершённую электронную конфигурацию внешнего слоя, например:
|
Nao |
– 1ē |
Na+ | |
|
1s22s22p63s1 |
1s22s22p6 | ||
|
нейтральный атом натрия; на внешнем электронном слое находится один электронов |
положительно заряженный ион натрия; на внешнем электронном слое находится 8 электронов (как у ближайшего благородного газа неона) | ||
|
Fo |
+ 1ē |
F– | |
|
1s22s22p5 |
1s22s22p6 | ||
|
нейтральный атом фтора; на внешнем электронном слое находится 7 электронов |
отрицательно заряженный ион фтора; на внешнем электронном слое находится 8 электронов | ||
Распад электролитов на ионы в расплавах осуществляется за счёт действия высоких температур, а в растворах за счёт действия молекул растворителя.
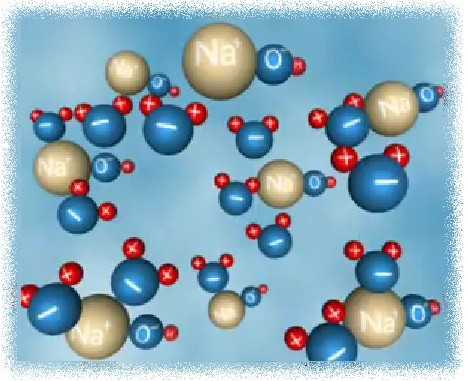
Особенностью ионных соединений является то, что в узлах их кристаллической решётки имеются уже готовые ионы и в процессе таких веществ растворения диполям растворителя (воды) остаётся только разрушить эту ионную решётку (рис. 18).
Вещества, образованные полярными ковалентными связями, переходят в раствор в виде отдельных молекул, которые, как и молекулы Н2О, представляют собой диполи, например:

 + –
+ –
В этом случае диполи Н2О, ориентируясь соответствующим образом вокруг растворенной молекулы электролита, вызывают в ней дальнейшую поляризацию ковалентной связи, а затем и её окончательный гетеролитический разрыв (рис. 29).
H–ClH++Cl
Рис. 29.Схема электролитической диссоциации в растворе полярной молекулыHCl
Процесс электролитической диссоциации протекает одновременно с процессом растворения веществ, и поэтому в растворах все ионы находятся в гидратированном состоянии (окружены оболочками из молекул Н2О).
Однако для простоты в уравнениях химических реакций ионы изображаются без окружающих их гидратных оболочек: H+,NO3–,K+и т.д.
2. Ионы электролитов в растворе или расплаве за счёт теплового движения хаотически перемещаются по всем направлениям. Но если в раствор или расплав опустить электроды и пропустить электрический ток, то положительно заряженные ионы электролита начинают двигаться к отрицательно заряженному электроду – катоду (поэтому они иначе называются катионами), а отрицательно заряженные ионы – к положительно заряженному электроду – аноду (поэтому они иначе называются анионами).
Таким образом, электролиты являются проводниками второго рода. Они переносят электрический заряд за счёт направленного движения ионов. Металлы же являются проводниками первого рода, т.к. проводят электрический ток за счёт направленного движения электронов.
3. Процесс электролитической диссоциации обратим. Наряду с распадом молекул на ионы всегда протекает обратный процесс – соединение ионов в молекулы или ассоциация. Поэтому в уравнениях реакций электролитической диссоциации веществ вместо знака равенства «=» ставят знак обратимости «», например:
HF H+ + F–
CH3COOH CH3COO– + H+
studfiles.net
Электролитическая диссоциация — как ее понять?
Вы никогда не задумывались над тем, почему одни растворы проводят электричество, а другие — нет? Например, всем известно, что лучше не принимать ванну, одновременно укладывая волосы феном. Ведь вода — неплохой проводник электрического тока, и если работающий фен упадет в воду, то короткого замыкания не избежать. На самом деле, вода — не такой уж и хороший проводник тока. Есть растворы, которые проводят электричество гораздо лучше. Такие вещества называют электролитами. К ним можно отнести кислоты, щелочи и растворимые в воде соли.
Электролиты — кто они?
Возникает вопрос: почему растворы одних веществ пропускают электричество, а других — нет? Все дело в заряженных частицах — катионах и анионах. При растворении в воде электролиты распадаются на ионы, которые при действии электрического тока движутся в заданном направлении. Положительно заряженные катионы движутся к отрицательному полюсу — катоду, а отрицательно заряженные анионы движутся к положительному полюсу — аноду. Процесс распада вещества на ионы при расплавлении или растворении в воде носит гордое название — электролитическая диссоциация.
Этот термин ввел в обращение шведский ученый С.Аррениус, когда изучал свойства растворов пропускать электричество. Для этого он замыкал электрическую цепь через раствор какого-либо вещества и следил загорается лампочка при этом или нет. Если лампочка накаливания загорается — значит раствор проводит электричество, из чего следует вывод, что это вещество является электролитом. Если лампочка остается потухшей — то раствор не проводит электричество, следовательно это вещество — неэлектролит. К неэлетролитам относятся растворы сахара, спирта, глюкозы. А вот расторы поваренной соли, серной кислоты и гидроксида натрия прекрасно проводят электрический ток, следовательно в них протекает электролитическая диссоциация.
Как протекает диссоциация?
Впоследствии теорию электролитической диссоциации развили и дополнили русские ученые И.А. Каблуков и В.А. Кистяковский, применив к ее обоснованию химическую теорию растворов Д.И. Менделеева.
Эти ученые выяснили, что электролитическая диссоциация кислот, щелочей и солей протекает в следствие гидратации электролита, то есть его взаимодействия с молекулами воды. Ионы, катионы и анионы, образующиеся в результате этого процесса будут гидратированными, то есть связанными с молекулами воды, которые их окружают плотным кольцом. Их свойства значительно отличаются от негидратированных ионов.
Итак, в растворе нитрата стронция Sr(NO3)2, а также в растворах гидроксида цезия CsOH, протекает электролитическая диссоциация. Примеры этого процесса можно выразить следующими уравнениями реакции:
Sr(NO3)2 = Sr2+ + 2NO3 -,
т.е. при диссоциации одной молекулы нитрата стронция образуется один катион стронция и 2 нитрат-аниона;
CsOH = Cs+ + OH-,
т.е. при диссоциации одной молекулы гидроксида цезия образуется один катион цезия и один гидроксид-анион.
Электролитическая диссоциация кислот происходит аналогично. Для йодоводородной кислоты этот процесс можно выразить следующим уравнением:
HJ = H+ + CJ-,
т.е. при диссоциации одной молекулы йодоводородной кислоты образуется один катион водорода и один анион йода.
Механизм диссоциации.
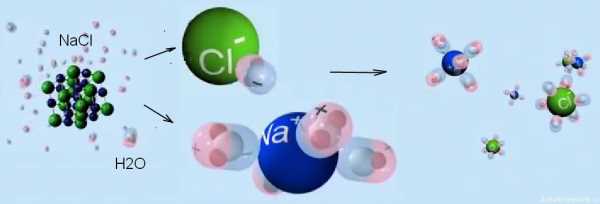
Электролитическая диссоциация веществ-электролитов протекает в несколько стадий. Для веществ с ионным типом связи, таких как NaCl, NaOH этот процесс включает в себя три последовательных процесса:
вначале молекулы воды, имеющие 2 разноименных полюса (положительный и отрицательный) и представляющие собой диполь, ориентируются у ионов кристалла. Положительным полюсом они прикрепляются к отрицательному иону кристалла, и наоборот, отрицательным полюсом — к положительному у ионов кристалла;
затем происходит гидратация ионов кристалла диполями воды,
и только после этого гидратированные ионы как бы расходятся в разные стороны и начинают двигаться в растворе или расплаве хаотично до тех пор, пока на них не подействуют электрическим полем.
Для веществ с ковалентной полярной связью, таких как HCl и другие кислоты, процесс диссоциации аналогичен, за исключением того, что на начальном этапе происходит переход ковалентной связи в ионную за счет действия диполей воды. Таковы основные моменты теории диссоциации веществ.
fb.ru
Электролитическая диссоциация веществ | Дистанционные уроки
09-Апр-2014 | комментариев 8 | Лолита Окольнова
Все вещества делятся на те, которые проводят электрический ток и те, которые не проводят, проще говоря, на электролиты и неэлектролиты.
Электролиты — вещества, распадающиеся на ионы в растворах или расплавах и потому проводящие электрический ток.
Неэлектролиты — вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят.
|
Электролиты |
Неэлектролиты |
|
|
Распад электролитов на ионы при растворении их в воде называется
электролитической диссоциацией.
Как происходит электролитическая диссоциация веществ?
Молекулы воды полярны.
Когда в воду попадает вещество, само имеющее положительные и отрицательные заряды, то между зарядами вещества и водой возникают силы притяжения .
Притяжение между зарядами внутри кристаллической решетки ослабевает.
Эти заряды переходят в раствор в виде гидратированных ионов, частиц, связанных с молекулами воды.
Электролитическая диссоциация веществ — процесс обратимый,
в растворах электролитов наряду с их ионами присутствуют и молекулы.
Поэтому растворы электролитов характеризуются степенью диссоциации.
Степень диссоциации — это отношение числа распавшихся на ионы молекул N’ к общему числу растворенных молекул N:
- если количество ионов больше, то α близка к 1 — ионов в растворе больше, чем молекул — значит, вещество — сильный электролит;
- если молекул больше, чем ионов, значит, вещество неохотно диссоциирует — слабый электролит.
|
Сильные электролиты |
слабые электролиты |
|
1) кислоты:
(сильная кислота — сильный электролит) 2) основания: все растворимые в воде, например, NaOH 3) соли — растворимые в воде |
1) вода H2O 2) кислоты: все органические кислоты;
3) основания: Nh5OH, мало-и нерастворимые основания 4) мало- и нерастворимые соли, соли органических кислот |
- в ЕГЭ это вопрос А22 — Ионный обмен и диссоциация
- в ГИА (ОГЭ) это А7 — Электролиты и неэлектролиты
Еще на эту тему:
Обсуждение: «Электролитическая диссоциация веществ»
(Правила комментирования)distant-lessons.ru
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ЭЛЕКТРОЛИТЫ | Энциклопедия Кругосвет
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ЭЛЕКТРОЛИТЫ. Дождливый день. На остановке троллейбуса люди складывают зонтики и заходят в салон. Вот один из них поставил ногу на ступеньку и тут же отпрянул: «Ой, током бьет!» Как же ток добрался до пассажира?
Еще на заре изучения электрических явлений ученые заметили, что ток могут проводить не только металлы, но и растворы. Но не всякие. Так, водные растворы поваренной соли и других солей, растворы сильных кислот и щелочей хорошо проводят ток. Растворы уксусной кислоты, углекислого и сернистого газа проводят его намного хуже. А вот растворы спирта, сахара и большинства других органических соединений вовсе не проводят электрический ток. Английский физик Майкл Фарадей еще в 30-е годы XIX века, изучая закономерности прохождения электрического тока через растворы, ввел термины «электролит», «электролиз», «ион», «катион», «анион». Электролит – вещество, раствор которого проводит электрический ток. Происходит это в результате движения в растворе заряженных частиц – ионов. Спустя много лет и в другой стране был придуман забавный стишок, позволяющий запомнить заряд ионов:
Для двух ребят подарков груз
ИОН взвалил себе на спину:
Для КАТИ ОН несет свой плюс,
Для АНИ ОН несет свой минус.
Причина появления в растворах заряженных частиц была совершенно непонятной. Само название «электролит» (от греч. lysis – разрушение, растворение) предполагало, что ионы появляются в растворе при пропускании через него электрического тока.
Изучение растворов методами физической химии, например, с помощью измерения oсмотического давления и криоскопии (см. также МОЛЕКУЛЯРНОЙ МАССЫ ОПРЕДЕЛЕНИЕ), показало, что растворах электролитов число частиц больше, чем дают расчеты, основанные на концентрации растворенного вещества. Получалось, например, что в разбавленных растворах поваренной соли число частиц вдвое больше, чем вычисленное по формуле NaCl, в растворах CaCl2 – втрое больше и т.д. Это можно было бы объяснить, предположив, что указанные соединения при растворении в воде распадаются на несколько частей – как говорят химики, претерпевают диссоциацию (от латинского dissociatio – разъединение, разделение).
Явления диссоциации химикам были известны; например, при нагревании хлорида аммония: он возгоняется с одновременной диссоциацией на две молекулы: NH4Cl ® NH3+ HCl. Но распад при нагревании было объяснить намного легче: энергия, необходимая для диссоциации, черпается за счет тепловой энергии. А вот откуда берется энергия при растворении соли в воде при комнатной температуре, никто объяснить не мог (температура раствора часто почти не меняется). Более того, при растворении некоторых солей в воде раствор сильно нагревается! Непонятно было также, как и на что может распадаться в растворе поваренная соль – ведь не на натрий же и хлор!
В 1887 году шведский физико-химик Сванте Аррениус, исследуя электропроводность водных растворов, высказал предположение, что в таких растворах вещества распадаются на заряженные частицы – ионы, которые могут передвигаться к электродам – отрицательно заряженному катоду и положительно заряженному аноду. Это и есть причина электрического тока в растворах. Данный процесс получил название электролитической диссоциации (дословный перевод – расщепление, разложение под действием электричества). Такое название также предполагает, что диссоциация происходит под действием электрического тока. Дальнейшие исследования показали, что это не так: ионы являются только переносчиками зарядов в растворе и существуют в нем независимо от того, проходит через раствор ток или нет.
Теория Аррениуса, с одной стороны, объясняла, почему растворы электролитов проводят ток, с другой стороны – объясняла увеличение числа частиц в растворе. Например, в растворе сульфат алюминия Al2(SO4)3 распадается сразу на пять ионов: два катиона алюминия Al3+ и три сульфат-аниона SO42–. За создание теории электролитической диссоциации Аррениус в 1903 году был удостоен Нобелевской премии по химии.
По степени диссоциации на ионы электролиты стали относить к сильным (полный распад на ионы) и к слабым (на ионы распадается только часть растворенного вещества). К сильным электролитам относятся щелочи, многие кислоты (серная, азотная, соляная), большинство солей. К слабым электролитам относятся уксусная СН3СООН, азотистая HNO2, сероводородная H2S, угольная Н2СО3, сернистая H2SO3, большинство органических кислот. Воду также можно отнести к слабым электролитам, так как лишь очень небольшая часть ее молекул находится в растворах в виде катионов Н+ и анионов ОН–. Фосфорная кислота Н3РО4 – электролит средней силы. Тело человека также содержит растворы электролитов и проводит электрический ток. Прохождение через тело тока силой всего 0,1 ампера может быть смертельным.
Многие ученые – современники Аррениуса, вначале не приняли его теорию. У многих из них то время еще не было четкого понимания, чем ионы отличаются от нейтральных атомов. Им казалось невероятным, как, например, хлорид натрия в воде может существовать в виде отдельных ионов натрия и хлора: как известно, натрий бурно реагирует с водой, а раствор хлора имеет желто-зеленый цвет и ядовит. В результате диссертация Аррениуса получила ряд отрицательных отзывов. К числу самых непримиримых противников Аррениуса принадлежал и Д.И.Менделеев, создавший «химическую» теорию растворов, в отличие от «физической» теории Аррениуса. Менделеев считал, что в растворах происходят по сути химические взаимодействия между растворенным веществом и растворителем, тогда как теория Аррениуса представляла водные растворы как механическую смесь ионов и воды. В 1889 году Менделеев опубликовал Заметку о диссоциации растворенных веществ, в которой ставился под сомнение сам факт распада на ионы в растворах электролитов. «Сохраняя все то, что приобретено в отношении к пониманию растворов, – писал Менделеев, – мне кажется, можно оставить в стороне гипотезу об особом виде диссоциации – на ионы, совершающейся с электролитами при образовании слабых растворов».
Хотя Менделеев, критикуя Аррениуса, во многом был не прав, в его рассуждениях была значительная доля истины. Как это часто бывает в науке, в ожесточенном споре между приверженцами физической и химической теории правыми оказались обе стороны. Очень сильное химическое взаимодействие между ионами и молекулами растворителя дает ту энергию, которая необходима для разрушения кристаллической решетки или молекул электролитов. В случае водных растворов эта энергия называется энергией гидратации (hydor по-гречески вода) и она может достигать очень больших значений; так, энергия гидратации катионов Na+ почти вдвое больше, чем энергия разрыва связи в молекуле Cl2. Чтобы разъединить катионы и анионы в кристаллах электролитов, тоже требуется затратить немало энергии (она называется энергией кристаллической решетки). В результате если суммарная энергия гидратации катионов и анионов при образовании раствора больше энергии кристаллической решетки (или энергии связи между атомами в таких электролитах, как HCl, H2SO4), растворение будет сопровождаться нагреванием, а если меньше – охлаждением раствора. Именно поэтому при растворении в воде таких веществ как LiCl, безводный CaCl2 и многих других раствор нагревается, а при растворении KCl, KNO3, NH4NO3 и некоторых других – охлаждается. Охлаждение может быть таким сильным, что стакан, в котором готовят раствор, покрывается снаружи росой и может даже примерзнуть к мокрой подставке!
Механизм электролитической диссоциации можно рассмотреть на примере хлороводорода. Связь H–Cl – ковалентная, полярная (см. МОЛЕКУЛ СТРОЕНИЕ), молекулы HCl – диполи с отрицательным полюсом на атоме Cl и положительным на атоме Н. Полярны и молекулы воды. В водном растворе молекулы HCl окружены со всех сторон молекулами воды так, что положительные полюса молекул Н2О притягиваются к отрицательным полюсам молекул HCl, а отрицательные полюса – к положительным полюсам молекул HCl. В результате связь H–Cl сильно поляризуется и разрывается с образованием гидратированных катионов H+ и анионов Cl–: диполи Н2О как бы растаскивают молекулы HCl на отдельные ионы. Каждый катион H+ в растворе окружен со всех сторон диполями Н2О, направленными к нему своими отрицательными полюсами, а каждый анион Cl– окружен противоположно ориентированными диполями Н2О. Аналогичные процессы происходят в воде с молекулами H2SO4, другими молекулами с полярными ковалентными связями, а также с ионными кристаллами. В них уже имеются «готовые» ионы, и роль диполей воды сводится к отделению катионов от анионов.
Ионы резко отличаются по своим физическим и химическим свойствам от нейтральных атомов. Например, атомы Na реагируют с водой, а катионы Na+ – нет; хлор – сильный окислитель и ядовит, а анионы Cl– не являются окислителем и не ядовиты. Цвет ионов при гидратации может измениться. Например, негидратированные ионы меди бесцветны (безводный CuSO4), а гидратированные – голубые.
Учитывая диссоциацию в растворах, уравнения многих реакций можно записать в сокращенном ионном виде. Ионное уравнение показывает, какие именно ионы участвуют в реакции. Например, полное уравнение реакции AgNO3 + NaCl ® AgCl + NaNO3 можно записать в сокращенном ионном виде: Ag+ + Cl– ® AgCl. Суть реакции состоит в образовании осадка AgCl при встрече ионов Ag+ и Cl–, тогда как ионы Na+ и NO3– остаются в растворе и фактически не принимают участия в реакции.
Илья Леенсон
www.krugosvet.ru
Электролитическая диссоциация » HimEge.ru
Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
 В начале XIX века была замечена способность растворов многих веществ проводить электрический ток (была обнаружена Майклом Фарадеем). Исследование электропроводности растворов показало, что растворы и расплавы многих веществ (например, поваренной соли) проводят электрический ток. Зато дистиллированная вода, кристаллические вещества и растворы некоторых других веществ (например, сахарозы) не проводит электрический ток – лампочка не горит, если замкнуть цепь.
В начале XIX века была замечена способность растворов многих веществ проводить электрический ток (была обнаружена Майклом Фарадеем). Исследование электропроводности растворов показало, что растворы и расплавы многих веществ (например, поваренной соли) проводят электрический ток. Зато дистиллированная вода, кристаллические вещества и растворы некоторых других веществ (например, сахарозы) не проводит электрический ток – лампочка не горит, если замкнуть цепь.
Вещества, которые проводят электрический ток назвали электролитами, вещества, непроводящие ток – неэлектролиты. Электролиты делятся на сильные и слабые. Сильные хорошо проводят ток, лампочка горит ярко, слабые – плохо проводят ток, лампочка горит тускло, например, в растворе уксусной кислоты (см. рисунок).
В чем же причина электропроводности? Почему одни вещества проводят электрический ток, а другие нет?
Электрический ток – это направленно движение заряженных частиц под действием разности потенциалов. Электрический ток в металлах осуществляется за счет электронов, именно электроны являются носителями заряда. А в растворах и расплавах заряд переносят ионы. Вещества, которые распадаются на ионы в растворе или расплаве и проводят электрический ток называются электролитами.
Запомнить! Электролиты – вещества, которые проводят электрический ток в растворах. Электролиты в растворах распадаются на заряженные частицы – ионы, которые могут передвигаться к электродам. Это и есть причина электрического тока в растворах.
Химическая связь в электролитах — ионная или ковалентная сильнополярная (соли, кислоты, основания).
Неэлектролиты – вещества, которые не проводят электрический ток в растворах. Связь в таких веществах — ковалентная неполярная и слабополярная. При растворении они образуют не ионы, а молекулы, которые не способны переносить электрический ток, например, органические вещества (сахароза, бензин, спирт).
Теория электролитической диссоциации была сформулирована Сванте Аррениусом в 1887 году, но актуальна и по сей день. Основные положения этой теории:
- При растворении в воде (или расплавлении) электролиты распадаются на положительно и отрицательно заряженные ионы (подвергаются электролитической диссоциации).
- Под действием электрического тока катионы двигаются к катоду (-), а анионы – к аноду (+).
- Электролитическая диссоциация — процесс обратимый.
- Сила электролита ( на сколько полно происходит распад на ионы) определяется степенью диссоциации, обозначается α (альфа) . Она показывает отношение числа молекул, распавшихся на ионы (n) к общему числу молекул, введенных в раствор (N). Изменяется от 0 до 1, или в прощентах от 0 до 100% 0 означает – совсем не распадается на ионы, 1 или 100% — все молекулы распались на ионы.
Степень электролитической диссоциации (α) зависит от природы электролита и растворителя, температуры и концентрации.
В зависимости от значения степени диссоциации, электролиты можно разделить на сильные, средние и слабые.

Сильные электролиты имеют степень диссоциации α > 30%, средние от 3 – 30%, а слабые – меньше 3%.
К сильным относят все раств. соли, все щелочи и некоторые кислоты. В растворе эти соединения практически полностью распадаются на ионы.
При написании уравнений диссоциации помните, что суммарный заряд катионов и анионов должен быть равен нулю.
Эти реакции распада на ионы протекают необратимо (только в одну сторону), ионы обратно не соединяются в кристаллическую решетку, препятствуют молекулы воды, окружающие эти ионы (гидратные оболочки).
К электролиам средней силы относят гидроксид магния, сернистую и фосфорную кислоты.
К слабым электролитам, которые лишь частично распадаются на ионы, α < 3%, относят гидроксид аммония, угольную кислоту, сероводородную, уксусную кислоты и воду. Диссоциация слабых электролитов – обратимые процесс.

himege.ru
Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
Все вещества делятся на 2 большие группы: электролитыинеэлектролиты.
Электролитами называются вещества (исключая металлы), растворы или расплавы которых проводят электрический ток. К электролитам относятся соединения, образованные ионными или ковалентными полярными связями. Это сложные вещества: соли, основания, кислоты, оксиды металлов (проводят электрический ток только в расплавах).
Неэлектролитаминазываются вещества, растворы или расплавы которых электрический ток не проводят. К ним относятся простые и сложные вещества, образованные малополярными или неполярными ковалентными связями.
Свойства растворов и расплавов электролитов впервые объяснил в конце XIXвека шведский учёный Сванте Аррениус. Им была создана специальнаятеория электролитической диссоциации, основные положения которой, доработанные и развитые другими учёными, в настоящее время формулируются следующим образом.
1. Молекулы (или формульные единицы) электролитов в растворах или расплавах распадаются на положительно и отрицательно заряженные ионы. Этот процесс называется электролитической диссоциацией. Общая сумма зарядов положительных ионов равна сумме зарядов отрицательных ионов, поэтому растворы или расплавы электролитов в целом остаются электронейтральными.Ионы могут быть какпростые, состоящие только из одного атома (Na+,Cu2+,Cl–,S2-), так исложные, состоящие из атомов нескольких элементов (SO42–,PO43–,NH4+, [Al(OH)4]–).
Простые ионы по своим физическим, химическим и физиологическим свойствам существенно отличаются от нейтральных атомов, из которых они образовались. В первую очередь, ионы являются гораздо более устойчивыми частицами, чем нейтральные атомы, и могут существовать в растворах или расплавах неограничено долгое время, не вступая в необратимое взаимодействие с окружающей средой.
Такое различие в свойствах атомов и ионов одного и того же элемента объясняется разным электронным строением этих частиц.
Так, простые ионы s- иp-элементов находятся в более устойчивом состоянии, чем нейтральные атомы, потому что имеют завершённую электронную конфигурацию внешнего слоя, например:
|
Nao |
– 1ē |
Na+ | |
|
1s22s22p63s1 |
1s22s22p6 | ||
|
нейтральный атом натрия; на внешнем электронном слое находится один электронов |
положительно заряженный ион натрия; на внешнем электронном слое находится 8 электронов (как у ближайшего благородного газа неона) | ||
|
Fo |
+ 1ē |
F– | |
|
1s22s22p5 |
1s22s22p6 | ||
|
нейтральный атом фтора; на внешнем электронном слое находится 7 электронов |
отрицательно заряженный ион фтора; на внешнем электронном слое находится 8 электронов | ||
Распад электролитов на ионы в расплавах осуществляется за счёт действия высоких температур, а в растворах за счёт действия молекул растворителя.
Особенностью ионных соединений является то, что в узлах их кристаллической решётки имеются уже готовые ионы и в процессе таких веществ растворения диполям растворителя (воды) остаётся только разрушить эту ионную решётку (рис. 18).
Вещества, образованные полярными ковалентными связями, переходят в раствор в виде отдельных молекул, которые, как и молекулы Н2О, представляют собой диполи, например:

 + –
+ –
В этом случае диполи Н2О, ориентируясь соответствующим образом вокруг растворенной молекулы электролита, вызывают в ней дальнейшую поляризацию ковалентной связи, а затем и её окончательный гетеролитический разрыв (рис. 29).
H–ClH++Cl
Рис. 29.Схема электролитической диссоциации в растворе полярной молекулыHCl
Процесс электролитической диссоциации протекает одновременно с процессом растворения веществ, и поэтому в растворах все ионы находятся в гидратированном состоянии (окружены оболочками из молекул Н2О).
Однако для простоты в уравнениях химических реакций ионы изображаются без окружающих их гидратных оболочек: H+,NO3–,K+и т.д.
2. Ионы электролитов в растворе или расплаве за счёт теплового движения хаотически перемещаются по всем направлениям. Но если в раствор или расплав опустить электроды и пропустить электрический ток, то положительно заряженные ионы электролита начинают двигаться к отрицательно заряженному электроду – катоду (поэтому они иначе называются катионами), а отрицательно заряженные ионы – к положительно заряженному электроду – аноду (поэтому они иначе называются анионами).
Таким образом, электролиты являются проводниками второго рода. Они переносят электрический заряд за счёт направленного движения ионов. Металлы же являются проводниками первого рода, т.к. проводят электрический ток за счёт направленного движения электронов.
3. Процесс электролитической диссоциации обратим. Наряду с распадом молекул на ионы всегда протекает обратный процесс – соединение ионов в молекулы или ассоциация. Поэтому в уравнениях реакций электролитической диссоциации веществ вместо знака равенства «=» ставят знак обратимости «», например:
HF H+ + F–
CH3COOH CH3COO– + H+
studfiles.net
