Соли — Википедия
У этого термина существуют и другие значения, см. Соль (значения). Соль со дна Мёртвого моряСо́ли — сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков[1]. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов[2]. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды[3].
Кроме катионов металлов в солях могут находиться катионы аммония NH4+, фосфония PH4+ и их органические производные, а также комплексные катионы и т. д. Анионами в солях выступают анионы кислотного остатка различных кислот Брёнстеда — как неорганических, так и органических, включая карбанионы и комплексные анионы
ru.wikipedia.org
Что такое соль? Формула, свойства соли (химия) :: SYL.ru
Для того чтобы ответить на вопрос, что такое соль, обычно долго задумываться не приходится. Это химическое соединение в повседневной жизни встречается достаточно часто. Об обычной поваренной соли и говорить не приходится. Подробное внутреннее строение солей и их соединений изучает неорганическая химия.
Определение соли
Четкий ответ на вопрос, что такое соль, можно найти в трудах М. В. Ломоносова. Такое имя он присвоил хрупким телам, которые могут растворяться в воде и не воспламеняются под воздействием высоких температур или открытого огня. Позднее определение выводили не из их физических, а из химических свойств данных веществ.
Школьные учебники неорганической химии дают достаточно ясное понятие того, что такое соль. Так называются продукты замещения химической реакции, при которой атомы водорода кислоты в соединении замещаются на металл. Примеры типичных соединений солей: NaCL, MgSO4. Легко увидеть, что любую эту запись можно разделить на две половины: в левой составляющей формулы всегда будет записан металл, а в правой – кислотный остаток. Стандартная формула соли выглядит следующим образом:
MenmКислотный остатокmn.
Физические свойства соли
Химия, как точная наука, вкладывает в название того или иного вещества всю возможную информацию о его составе и возможностях. Так, все наименования солей в современной интерпретации состоят из двух слов: одна часть имеет название металлического составляющего в именительном падеже, вторая — содержит описание кислотного остатка.
Эти соединения не имеют молекулярного строения, поэтому при обычных условиях они представляют собой твердые кристаллические вещества. Многие соли обладают кристаллической решеткой. Кристаллы этих веществ тугоплавки, поэтому для их плавления нужны очень высокие температуры. Например, сульфид бария плавится при температуре около 2200о С.
По растворимости соли делятся на растворимые, малорастворимые и нерастворимые. Примером первых могут служить хлорид натрия, нитрат калия. К малорастворимым относят сульфит магния, хлорид свинца. Нерастворимые – это карбонат кальция. Информация о растворимости того или иного вещества содержится в справочной литературе.
Рассматриваемый продукт химической реакции обычно не имеет запаха и обладает разным вкусом. Предположение о том, что все соли соленые — ошибочно. Чистый соленый вкус имеет только один элемент этого класса – наша старая знакома поваренная соль. Существуют сладкие соли бериллия, горькие – магния и безвкусные – например, карбонат кальция (мел обыкновенный).
Большинство данных веществ бесцветно, но среди них имеются и такие, которые имеют характерные окрасы. Например, железа (II) сульфат отличается характерным зеленым цветом, калия перманганат – фиолетовый, а кристаллы хромата калия – ярко-желтые.
Классификация соли
Химия разделяет все виды неорганических солей на несколько основных признаков. Соли, получающиеся при полном замещении водорода в кислоте, называют нормальными или средними. Например, сульфат кальция.
Соль, которая является производной от реакции неполного замещения, называется кислой или основной. Примером такого образования может быть реакция гидросульфата калия:
Основная соль получается при такой реакции, в которой гидроксогруппа не полностью замещается на кислотный остаток. Вещества данного вида могут быть образованны теми металлами, чья валентность равна двум или больше. Типичная формула соли этой группы может быть выведена из такой реакции:
Нормальные, средние и кислые химические соединения образуют классы солей и являются стандартной классификацией этих соединений.
Двойная и смешанная соль
Химия неорганических веществ показывает, что данный продукт может быть образован двумя металлами и одной кислотой. В этом случае кислота должна иметь основность больше или равной 2. Такое соединение называют двойная соль. Химические соли этой группы – алюмокалиевые квасцы, их еще называют сульфат калия-алюминия.
Примером смешанной является кальциевая соль соляной и хлорноватистой кислоты: CaOCl2.
Номенклатура
Соли, образованные металлами с переменной валентностью, имеют дополнительное обозначение: после формулы в скобках пишут римскими цифрами валентность. Так, существует сульфат железа FeSO4 (II) и Fe2 (SO4)3 (III). В названии солей имеется приставка гидро-, если в ее составе существуют незамещенные атомы водорода. Например, гидрофосфат калия обладает формулой K2HPO4 .
Свойства солей в электролитах
Теория электролитической диссоциации дает собственное толкование химическим свойствам. В свете этой теории соль может быть определена как слабый электролит, который в растворенном виде диссоциирует (распадается) в воде. Таким образом, раствор соли можно представить как комплекс положительных отрицательных ионов, причем первые – это не атомы водорода Н+, а вторые – не атомы гидроксогруппы ОН—. Ионов, которые присутствовали бы во всех видах растворов солей, не существует, поэтому какими-либо общими свойствами они не обладают. Чем меньше заряды ионов, образующих раствор соли, тем лучше они диссоциируют, тем лучше электропроводимость такой жидкой смеси.
Растворы кислых солей
Кислые соли в растворе распадаются на сложные отрицательные ионы, представляющие собой кислотный остаток, и простые анионы, являющиеся положительно заряженными частицами металла.  Например, реакция растворения гидрокарбоната натрия ведет к распаду соли на ионы натрия и остаток НСО3—.
Например, реакция растворения гидрокарбоната натрия ведет к распаду соли на ионы натрия и остаток НСО3—.
Полная формула выглядит таким образом: NaHCO3 = Na+ + HCO3—,HCO3 — = H+ + CO32-.
Растворы основных солей
Диссоциация основных солей ведет к образованию анионов кислоты и сложных катионов, состоящих из металлов и гидроксокрупп. Эти сложные катионы, в свою очередь, также способны распадаться в процессе диссоциации. Поэтому в любом растворе соли основной группы присутствуют ионы ОН— . Например, диссоциация хлорида гидроксомагния протекает следующим образом: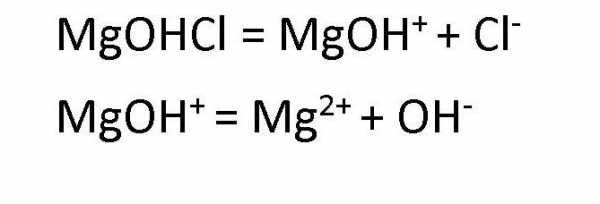
Распространение солей
Что такое соль? Этот элемент является одним из самых распространенных химических соединений. Всем известны поваренная соль, мел (карбонат кальция) и прочее. Среди солей карбонатной кислоты самым распространенным является карбонат кальция. Он является составной частью мрамора, известняка, доломита. А еще карбонат кальция — основа для формирования жемчуга и кораллов. Это химическое соединение является неотъемлемой составляющей для формирования твердых покровов у насекомых и скелетов у хордовых животных.
Поваренная соль известна нам с детства. Врачи предостерегают от ее чрезмерного употребления, но в умеренных количествах она крайне необходима для осуществления жизненных процессов в организме. А нужна она для поддержания правильного состава крови и вырабатывания желудочного сока. Физрастворы, неотъемлемая часть инъекций и капельниц, есть не что иное, как раствор поваренной соли.
www.syl.ru
Формула поваренной соли в химии
Определение и формула поваренной соли
Молярная масса равна г/моль.
Физические свойства – мелко- или грубодисперсные белые или бесцветные кристаллики.
В незначительной степени впитывает влагу.
Пищевая соль принимает участие в поддержании и регулировании водного баланса в организме.
Поваренная соль по химическому строению и составу на состоит из хлорида натрия .
Поваренную соль можно добывать разными способами, например: из «соляных водопадов» путём природного испарения морской воды.
Каменная соль добывается методом разработки шахт.
Химические свойства поваренной соли
- Хлорид натрия в составе поваренной соли реагирует с кислотами с выделением газообразного хлороводорода:
- Взаимодействует с солями минеральных кислот. Образующийся продукт должен выпадать в осадок:
Применение
Основным направлением потребления является пищевая промышленность. Находится в различных видах и формах: очищенная и неочищенная (каменная соль), крупного и мелкого помола, чистая и йодированная.
Также применяется в качестве консерванта.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Формула и свойства поваренной соли. Применение поваренной соли :: SYL.ru
Поваренная соль, формула которой NaCl, является пищевым продуктом. В неорганической химии данное вещество называют хлоридом натрия. В измельченном варианте поваренная соль, формула которой приведена выше, представляет собой белые кристаллы. Несущественные серые оттенки могут появляться при наличии иных минеральных солей в качестве примесей.
Производят ее в различных видах: неочищенном и очищенном, мелком и крупном, йодированном.

Биологическое значение
Кристалл поваренной соли, имеющий ионную химическую связь, необходим для полноценной жизни и деятельности человека, иных живых организмов. Хлорид натрия принимает участие в регулировании и поддержании водно-солевого баланса, щелочного обмена. Биологические механизмы контролируют постоянство концентрации хлористого натрия в различных жидкостях, например, в крови.
Разность концентраций NaCl внутри клетки и снаружи – основной механизм для попадания внутрь питательных веществ, а также вывода продуктов жизнедеятельности. Аналогичный процесс применяется в генерации и передаче нейронами импульсов. Также анион хлора в данном соединении – основной материл для образования соляной кислоты, важнейшего компонента желудочного сока.
Дневная потребность в этом веществе составляет от 1,5 до 4 граммов, а для жаркого климата доза хлорида натрия возрастает в несколько раз.
Организм нуждается не в самом соединении, а в катионе Na+ и анионе Cl-. При недостаточном количестве этих ионов происходит разрушение мышечной и костной тканей. Появляются депрессии, психические и нервные заболевания, нарушения в деятельности сердечно-сосудистой системы и процессах пищеварения, спазмы мускулатуры, анорексия, остеопороз.
Хроническая нехватка ионов Na+ и Cl- приводит к смерти. Биохимик Жорес Медведев отмечал, что при полном отсутствии в организме соли можно продержаться не больше 11 суток.
Племена скотоводов и охотников еще в древности для удовлетворения потребности организма в соли, употребляли в сыром виде мясопродукты. Земледельческие племена потребляли растительную пищу, в которой незначительное количество хлористого натрия. В качестве признаков, сигнализирующих о нехватке соли, выделяют слабость и головную боль, тошноту, головокружение.

Особенности производства
В далеком прошлом добыча соли осуществлялась путем сжигания в кострах определенных растений. Образующуюся золу применяли в виде приправы.
Очистка поваренной соли, полученной путем выпаривания морской воды, не проводилась, полученное вещество сразу же употреблялось в пищу. Такая технология возникла в странах с жарким и сухим климатом, где подобный процесс происходил без вмешательства человека, а затем, когда его переняли иные страны, морская вода стала подогреваться искусственным путем.
На берегах Белого моря строились солеварни, в которых путем выпаривания и замораживания получали концентрированный рассол и пресную воду.

Природные месторождения
Среди мест, характеризующихся большими запасами поваренной соли, выделим:
- Артемовское месторождение, расположенное в Донецкой области. Здесь осуществляется добыча соли шахтовым способом;
- озеро Баскунчак, перевоз ведется по специально построенной железной дороге;
- калийные соли в большом количестве обнаружены в Верхнекамском месторождении, где шахтовым способом идет добыча этого полезного ископаемого;
- в Одесских лиманах велась добыча до 1931 года, в настоящее время месторождение не используется в промышленных объемах;
- в Сереговском месторождении проводится выпаривание рапы.
Соляная шахта
Биологические свойства поваренной соли сделали ее важным экономическим объектом. На 2006 год на российском рынке использовалось порядка 4,5 миллионов тонн данного минерала, причем 0,56 млн тонн шло на пищевые расходы, а оставшиеся 4 миллиона тонн уходили на нужды химической промышленности.

Физические характеристики
Рассмотрим некоторые свойства поваренной соли. Данное вещество достаточно хорошо растворяется в воде, причем на процесс влияет несколько факторов:
- температура;
- наличие примесей.
Кристалл поваренной соли содержит примеси в виде катионов кальция, магния. Именно поэтому хлорид натрия впитывает воду (сыреет на воздухе). Если такие ионы не входят в состав поваренной соли, такое свойство отсутствует.
Температура плавления поваренной соли — 800,8 °С, что свидетельствует о прочной кристаллической структуры данного соединения. При смешивании мелкого порошка хлорида натрия с измельченным льдом получают охладитель высокого качества.
Например, 100 г льда и 30 г поваренной соли могут снижать температуру до −20 °C. Причина подобного явления в том, что раствор поваренной соли замерзает при температуре ниже 0 °C. Лед, для которого это значение является температурой плавления, плавится в подобном растворе, поглощая тепло окружающей среды.
Высокая температура плавления поваренной соли объясняет ее термодинамические характеристики, а также высокую диэлектрическую проницаемость – 6,3.

Получение
Учитывая, насколько важны биологические и химические свойства поваренной соли, ее существенные природные запасы, нет необходимости разрабатывать вариант промышленного производства данного вещества. Остановимся на лабораторных вариантах получения хлорида натрия:
- Данное соединение можно получить в качестве продукта при взаимодействии сульфата меди (2) с хлоридом бария. После удаления осадка, в качестве которого выступает сульфат бария, выпаривания фильтрата, можно получить кристаллы поваренной соли.
- При экзотермическом соединении натрия с газообразным хлором также образуется хлористый натрий, причем процесс сопровождается выделением существенного количества тепла (экзотермический вид).
Взаимодействия
Каковы химические свойства поваренной соли? Данное соединение образовано сильным основанием и сильной кислотой, поэтому гидролиз в водном растворе не протекает. Нейтральность среды и объясняет применение поваренной соли в пищевой промышленности.
При электролизе водного раствора данного соединения на катоде выделяется газообразный водород, а на аноде идет процесс образования хлора. В межэлектродном пространстве накапливается гидроксид натрия.
Учитывая, что получаемая щелочь – вещество, востребованное в различных производственных процессах, это также объясняет применение поваренной соли в промышленных масштабах на химическом производстве.
Плотность поваренной соли составляет 2,17 г/см3. Кубическая гранецентрированная кристаллическая решетка характерна для многих минералов. Внутри ее преобладают ионные химические связи, образуемые за счет действия сил электростатического притяжения и отталкивания.

Галит
Так как плотность поваренной соли в этом соединении достаточно высока (2,1—2, 2 г/см³), галит – твердый минерал. Процентное содержание катиона натрия в нем составляет 39,34 %, аниона хлора – 60, 66%. Помимо этих ионов, в составе галита есть в виде примесей ионы брома, меди, серебра, кальция, кислорода, свинца, калия, марганца, азота, водорода. Этот прозрачный бесцветный минерал, имеющий стеклянный блеск, образуется в замкнутых водоемах. Галит является продуктом сгона на кратерах вулканов.
Каменная соль
Он представляет собой горную осадочную породу из группы эвапоритов, которая состоит более чем на 90 процентов из галита. Для каменной соли характернее белоснежный цвет, лишь в исключительных случаях присутствие глины дает минералу серый оттенок, а наличие оксидов железа придает соединению желтый, оранжевый цвет. В каменной соли присутствует не только хлорид натрия, но и множество иных химических соединений магния, кальция, калия:
- иодиды;
- бораты;
- бромиды;
- сульфаты.
В зависимости от условий формирования, основные месторождения каменной соли подразделяют на несколько видов:
- подземные соляные воды;
- рассолы современных бассейнов;
- залежи минеральных солей;
- ископаемые месторождения.
Морская соль
Она является смесью сульфатов, карбонатов, хлоридов калия и натрия. В процессе ее испарения при диапазоне температур от +20 до +35 °C первоначально происходит кристаллизация менее растворимых солей: карбонатов магния и кальция, а также сульфата кальция. Далее в осадок выпадают растворимые хлориды, а также сульфаты магния и натрия. Последовательность кристаллизации этих неорганических солей может меняться с учетом температурного показателя, скорости процесса испарения, иных условий.
В промышленных объемах морская соль получается из воды морей путем выпаривания. Она существенно отличается по микробиологическим и химическим показателям от каменной соли, имеет большое процентное содержание йода, магния, калия, марганца. Из-за различного химического состава есть отличия и в органолептических показателях. Применяют морскую соль в медицине в качестве средства при лечении кожных заболеваний, например, псориаза. Среди распространенных продуктов, предлагаемых в аптечной сети, выделим соль Мертвого моря. Также морская соль в очищенном виде предлагается и в пищевой промышленности как йодированная.
Обычная поваренная соль имеет слабые антисептические свойства. При процентном содержании данного вещества в диапазоне 10-15 процентов можно предотвратить появление гнилостных бактерий. Именно для этих целей хлорид натрия добавляют в виде консерванта к пище, а также иным органических массам: древесине, клею, коже.

Злоупотребление солью
По информации Всемирной организации здравоохранения, избыточное потребление хлорида натрия приводит к существенному повышению кровяного давления, в результате чего нередко развиваются болезни почек и сердца, желудка, формируется остеопороз.
Вместе с другими солями натрия хлорид натрия является причиной появления заболеваний глаз. Поваренная соль задерживает внутри организма жидкость, что приводит к повышению внутриглазного давления, формированию катаракты.
Вместо заключения
Хлорид натрия, называемый в повседневной жизни поваренной солью, является широко распространенным в природе неорганическим минералом. Этот факт существенно упрощает его применение в пищевой, химической промышленности. Нет необходимости тратить временные и энергетические ресурсы на промышленное получение данного вещества, что сказывается на его стоимости. Для того чтобы не допускать переизбытка данного соединения в организме, необходимо контролировать ежедневное употребление соленых продуктов.
www.syl.ru
Какова формула сахара, соли, воды, спирта, уксуса и прочих веществ?
Химические формулы распространённых в быту веществ полезно знать не только как часть школьного курса химии, но и просто для общей эрудиции. Формулу воды или поваренной соли знают практически все, однако насчёт спирта, сахара или уксуса — немногие смогут сразу попасть в точку. Давайте пойдём от простого к сложному.
Какова формула воды?
Эту жидкость, благодаря которой на планете Земля появилась удивительная живая природа, знают и пьют все. Более того, она составляет около 70% нашего с вами тела. Вода является простейшим соединением атома кислорода с двумя атомами водорода.
Химическая формула воды: H2O
Какова формула поваренной соли?
Поваренная соль является не только незаменимым кулинарным блюдом, но и одной из главных составляющих морской соли, запасы которой в Мировом Океане составляют миллионы тонн. Формула поваренной соли проста и легка для запоминания: 1 атом натрия и 1 атом хлора.
Химическая формула поваренной соли: NaCl
Какова формула сахара?
Сахар — белый кристаллический порошок, без которого ни один сладкоежка в мире не сможет прожить и дня. Сахар является сложным органическим соединением, формулу которого сразу не запомнишь: 12 атомов углерода, 22 атома водорода и 11 атомов кислорода образуют сладкую и сложную структуру.
Химическая формула сахара: C12H22O11
Какова формула уксуса?
Уксус — раствор уксусной кислоты, который используют в пищу, а также для очистки металлов от налёта. Молекула уксусной кислоты имеет сложную структуру, состоящую из двух атомов углерода, к одному из которых крепятся три атома водорода, а к другому — два атома кислорода, один из которых прихватил себе ещё один водород.
Химическая формула уксусной кислоты: CH3COOH
Какова формула спирта?
Начнём с того, что спирты бывают разные. Тот спирт, что используется для приготовления вин, водки и коньяков, называется по-научному этанол. Помимо этанола есть ещё куча спиртов, которые используются в медицине, автомобилестроении и авиации.
Химическая формула этанола: C2H5OH
Какова формула пищевой соды?
Пищевая сода называется по-научному гидрокарбонатом натрия. Из этого названия любой начинающий химик поймёт, что в молекуле соды есть натрий, углерод, кислород и водород.
Химическая формула пищевой соды: NaHCO3
Сегодня 9 ноября 2018 года. А вы знаете, какой сегодня праздник?
Расскажите Какова формула сахара, соли, воды, спирта, уксуса и прочих веществ друзьям в социальных сетях:
| Оцените качество ответа: |
Рекомендуем также почитать:
navopros.ru
Соли: классификация и химические свойства
Солями называются сложные вещества, молекулы которых, состоят из атомов металлов и кислотных остатков (иногда могут содержать водород). Например, NaCl – хлорид натрия, СаSO 4 – сульфат кальция и т. д.
 Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Na+Cl– – хлорид натрия
Ca2+SO42– – сульфат кальция и т.д.
Соль является продуктом частичного или полного замещения металлом атомов водорода кислоты. Отсюда различают следующие виды солей:
1. Средние соли – все атомы водорода в кислоте замещены металлом: Na2CO3, KNO3 и т.д.
2. Кислые соли – не все атомы водорода в кислоте замещены металлом. Разумеется, кислые соли могут образовывать только двух- или многоосновные кислоты. Одноосновные кислоты кислых солей давать не могут: NaHCO3, NaH2PO4 ит. д.
4. Соли основные можно рассматривать как продукты неполного, или частичного, замещения гидроксильных групп оснований кислотными остатками: Аl(OH)SO4 , Zn(OH)Cl и т.д.
По международной номенклатуре название соли каждой кислоты происходит от латинского названия элемента. Например, соли серной кислоты называются сульфатами: СаSO4 – сульфат кальция, Mg SO4 – сульфат магния и т.д.; соли соляной кислоты называются хлоридами: NaCl – хлорид натрия, ZnCI2 – хлорид цинка и т.д.
В название солей двухосновных кислот добавляют частицу «би» или «гидро»: Mg(HCl3)2 – бикарбонат или гидрокарбонат магния.
При условии, что в трехосновной кислоте замещён на металл только один атом водорода, то добавляют приставку «дигидро»: NaH 2PO4 – дигидрофосфат натрия.
Соли – это твёрдые вещества, обладающие самой различной растворимостью в воде.
Химические свойства солей
Химические свойства солей определяются свойствами катионов и анионов, которые входят в их состав.
1. Некоторые соли разлагаются при прокаливании:
CaCO3 = CaO + CO2↑
2. Взаимодействуют с кислотами с образованием новой соли и новой кислоты. Для осуществление этой реакции необходимо, чтобы кислота была более сильная чем соль, на которую воздействует кислота:
2NaCl + H2 SO4 → Na2SO4 + 2HCl↑.
3. Взаимодействуют с основаниями, образуя новую соль и новое основание:
Ba(OH)2 + Mg SO4 → BaSO4↓ + Mg(OH)2.
4. Взаимодействуют друг с другом
NaCl + AgNO3 → AgCl + NaNO3 .
5. Взаимодействуют с металлами, которые стоят в раду активности до металла, который входит в состав соли:
Fe + CuSO4 → FeSO4 + Cu↓.
Остались вопросы? Хотите знать больше о солях?
Чтобы получить помощь репетитора – зарегистрируйтесь.
Первый урок – бесплатно!
Зарегистрироваться
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
Поваренная соль формула — Какая химическая формула у соли? — 22 ответа
формула соли в химии
В разделе Образование на вопрос Какая химическая формула у соли? заданный автором Black Angel лучший ответ это Какой соли? Если повареной — NaCl, соды — Na2CO3 питьевой соды — NaHCO3 и т. д. А вообще соли — это вещества, которые можно получить из основания и кислоты, например, Na2SO4
Ответ от 22 ответа[гуру]Привет! Вот подборка тем с ответами на Ваш вопрос: Какая химическая формула у соли?
Ответ от шеврон[гуру]
Соли чего? И какой кислоты? Соли соляной- NaCl, KCl, натрия и калия соответственно, серной NaSO4 и так далее.. . Простая бытовая соль имеет формулу NaCl но обычно имеет добавки йода иногда магния …
Ответ от Особенный[эксперт]
NaCl
Ответ от Вопросить[мастер]
Na2SO4 — сульфат натрия
Ответ от Ирина Кулик[гуру]
В составе любой соли — атомы металла и кислотные остатки. В составе кислой соли — дополнительно — незамещённые атомы водорода, а в составе основной — незамещённые гидроксогруппы. Если имелась в виду формула пищевой или поваренной соли, то это NaCl!
Ответ от Ѐуслан Алиев[активный]
ПОВАРЕНА ТО NACI СОДА NANCO3 ПИТЬЕВАЯ СОДА NAHCO3 ИТД
Ответ от Максим дурманов[активный]
ВОТ ПАЦАНЫ… круто кушать Натрий перемешанный в Хлоре !!!ахахах )) 🙂
Ответ от Ёветлана Терентьева[новичек]
СОЛЕЙ МНОГО!!! ОЧЕНЬ ОЧЕНЬ МНОГО, ТАК ЧТО ПИШИ НАЗВАНИЕ!!!!
Ответ от Peregrinator[активный]
NaCl вроде
Ответ от Bkmz[гуру]
100% натрий хлор
NaCl!!!
Ответ от ЇАВ[гуру]
В точности NaCl
Ответ от AJA[гуру]
NaCl
Ответ от 2 ответа[гуру]
Привет! Вот еще темы с нужными ответами:
Поваренная соль на Википедии
Посмотрите статью на википедии про Поваренная соль
Софийская церковь в Савине на Википедии
Посмотрите статью на википедии про Софийская церковь в Савине
Хлорид натрия на Википедии
Посмотрите статью на википедии про Хлорид натрия
Ответить на вопрос:
22oa.ru
