Что такое моль в химии :: SYL.ru
Понятие моль используют для измерения химических веществ. Выясним особенности этой величины, приведем примеры расчетных заданий с ее участием, определим важность данного термина.
Определение
Моль в химии – это единица вычисления. Она представляет собой количество определенного вещества, в котором находится столько структурных единиц (атомов, молекул), сколько содержится в 12 граммах атома углерода.

Число Авогадро
Количество вещества связано с числом Авогадро, которое составляет 6*10^23 1/моль. Для веществ молекулярного строения считают, что один моль включает именно число Авогадро. Если нужно посчитать число молекул, содержащееся в 2 молях воды, то необходимо умножить 6*10^23 на 2 , получаем 12*10^23 штук. Давайте рассмотрим, какую роль играет моль в химии.
Количество вещества
Вещество, которое состоит из атомов, содержит число Авогадро. Например, для атома натрия это 6*10*23 1/моль. Каково его обозначение? Моль в химии обозначают греческой буквой «ню» или латинской «n». Для проведения математических вычислений, связанных с количеством вещества, используют математическую формулу:
n=N/N(A), где n – количество вещества, N(A) – число Авогадро, N – количество структурных частиц вещества.
При необходимости можно вычислить число атомов (молекул):
N=N(A) * n
Фактическая масса моля называется молярной. Если количество вещества определяют в молях, то величина молярной массы имеет единицы измерения г/моль. В численном выражении она соответствует значению относительной молекулярной массы, которую можно определить путем суммирования относительных атомных масс отдельных элементов.

Например, для того чтобы определить молярную массу молекулы углекислого газа, необходимо провести следующие расчеты:
M (CO2)=Ar(C)+2Ar(O)=12+2*16=44
При вычислении молярной массы оксида натрия получаем:
M (Na2O)=2*Ar(Na)+Ar(O)=2*23+16=62
При определении молярной массы серной кислоты суммируем две относительные атомные массы водорода с одной атомной массой серы и четырьмя относительными атомными массами кислорода. Их значения всегда можно найти в периодической таблице Менделеева. В итоге получаем 98.
Моль в химии позволяет проводить разнообразные расчеты, связанные с химическими уравнениями. Все типовые расчетные задачи в неорганической и органической химии, которые предполагают нахождение массы и объема веществ, решаются именно через моли.
Примеры расчетных задач
Молекулярная формула любого вещества указывает на количество молей каждого элемента, включенного в его состав. Например, один моль фосфорной кислоты содержит три моля атомов водорода, один моль атомов фосфора и четыре моля атомов кислорода. Все достаточно просто. Моль в химии является переходом из микромира молекул и атомов в макросистему с килограммами и граммами.
Задача 1. Определите число молекул воды, содержащихся в 16,5 молях.
Для решения используем связь между числом Авогадро (количество вещества). Получаем:
16,5*6,022*1023 = 9,9*1024 молекул.

Задача 2. Рассчитайте число молекул, содержащихся в 5 г углекислого газа.
Сначала необходимо вычислить молярную массу данного вещества, воспользовавшись ее связью с относительной молекулярной массой. Получаем:
M (CO2)=Ar(C)+2Ar(O)=12+2*16=44.
Далее вычисляем число молекул, используя формулу, приведенную выше:
N=5/44*6,023*1023=6,8*1023 молекул.
Алгоритм задач на химическое уравнение
При вычислении массы или продуктов реакции по уравнению используют определенный алгоритм действий. Сначала определяют, какое из исходных веществ в недостатке. Для этого находят их количество в молях. Далее составляют уравнение процесса, обязательно расставляют стереохимические коэффициенты. Над веществами записывают исходные данные, под ними указывают количество вещества, взятое в молях (по коэффициенту). В случае необходимости осуществляют перевод единиц измерения, пользуясь формулами. Далее составляют пропорцию и решают ее математическим способом.

Если предлагается более сложная задача, то предварительно вычисляют массу чистого вещества, убирая примеси, потом уже приступают к определению его количества (в молях). Ни одна задача в химии, связанная с уравнением реакции, не решается без такой величины, как моль. Кроме того с помощью данного термина, легко можно определить количество молекул или атомов, воспользовавшись для таких вычислений постоянным числом Авогадро. Расчетные задания включены в тестовые вопросы по химии для выпускников основной и средней общеобразовательной школы.
www.syl.ru
Урок 5. Моль и молярная масса – HIMI4KA
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.

Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·1023 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·1023 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·1023).

Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·1023атомов. Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·1023молекул. Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·1023; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·1023 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·1023 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·1023 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·1023 × 0,25 = 1,505·1023 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·1023 молекул/моль, что равно 2,99·1026 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Что такое моль в химии? Определение и формулы
С понятием «моль» сталкивается каждый школьник, который начинает изучать химию. С более сложными понятиями, такими как молярная масса, молярная концентрация, молярность растворителя, тяжело разобраться, не зная, что такое моль. Можно сделать вывод, что моль — одно из важнейших понятий в химии. Многие задачи нельзя решить, не определив количество молей.
Определение
Так что такое моль в химии? Пояснение дать довольно просто: это единица, в которой выражается количество вещества, одна из единиц СИ. Определение того, что такое моль в химии, можно сформулировать и таким образом: 1 моль эквивалентен такому количеству вещества, сколько содержится структурных частиц в 12 г карбона-12.
Как было установлено, в 12 г этого изотопа содержится количество атомов, численно равное постоянной Авогадро.
Происхождение понятия
Немного разобравшись с тем, что такое моль в химии с помощью определений, обратимся к истории этого понятия. Как принято считать, термин «моль» ввел немецкий химик Вильгельм Освальд, получивший Нобелевскую премию в 1909 году. Слово «моль», очевидно, происходит от слова «молекула».

Интересный факт — гипотеза Авогадро о том, что при одинаковых условиях в одинаковых объемах разных газов содержится одно и то же количество вещества, было выдвинута задолго до Освальда, да и сама константа была подсчитана Авогадро еще в начале XIX века. То есть хоть понятия «моль» и не существовало, само представление о количестве вещества уже было.
Основные формулы

Количество вещества находится по-разному, в зависимости от данных задачи. Такой вид имеет самая распространенная формула, в которой эта величина выражается отношением массы к молярной массе:
n=m/M
Стоит сказать, что количество вещества — величина аддитивная. То есть, чтобы посчитать значение этой величины для смеси, нужно сначала определить количество вещества для каждого ее элемента и сложить их.
Другая формула применяется, если известно количество частиц:
n=N/Na
Если в задаче указано, что процесс происходит при нормальных условиях, можно воспользоваться следующим правилом: при нормальных условиях любой газ занимает инвариантный объем — 22,4 л. Тогда можно воспользоваться следующим выражением:
n-V/Vm
Количество вещества выражается из уравнения Клапейрона:
n=pV/(RT)
Знание того, что такое моль в химии и основных формул для определения количества молей вещества, дает возможность значительно быстрее решать многие задачи. Если известно количество вещества, можно найти массу, объем, плотность и другие параметры.
fb.ru
Моль — это… Что такое Моль?
- Эта статья посвящена единице измерения.
Моль (русское обозначение: моль; международное: mol) — единица измерения количества вещества в Международной системе единиц (СИ), одна из семи основных единиц СИ[1].
Моль принят в качестве единицы СИ XIV Генеральной конференцией по мерам и весам в 1971 году. Точное определение моля формулируется так[2]:
Моль есть количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц.
Из определения моля непосредственно следует, что молярная масса углерода-12 равна 12 г/моль точно.
Количество специфицированных структурных элементов в одном моле вещества называется числом Авогадро, обозначаемом обычно как
1/12 массы атома углерода-12 называют атомной единицей массы (обозначение а. е. м.). Отсюда следует, что 1 а. е. м. = 0,001/NA кг.
Из определения а. е. м. вытекает, что молярная масса вещества, выраженная в граммах на моль, численно равна массе молекулы этого вещества, выраженной в атомных единицах массы.
При нормальных условиях объём одного моля идеального газа составляет 22,413 996(39) л[4].
Кратные и дольные единицы
Десятичные кратные и дольные единицы образуют с помощью стандартных приставок СИ. Причём, единица измерения йоктомоль может использоваться лишь формально, так как столь малые количества вещества должны измеряться отдельными частицами (1 имоль формально равен 0,602 частицы).
| Кратные | Дольные | ||||||
|---|---|---|---|---|---|---|---|
| величина | название | обозначение | величина | название | обозначение | ||
| 101 моль | декамоль | дамоль | damol | 10−1 моль | децимоль | дмоль | dmol |
| 102 моль | гектомоль | гмоль | hmol | 10−2 моль | сантимоль | смоль | cmol |
| 103 моль | киломоль | кмоль | kmol | 10−3 моль | миллимоль | ммоль | mmol |
| 106 моль | мегамоль | Ммоль | Mmol | 10−6 моль | микромоль | мкмоль | µmol |
| 109 моль | гигамоль | Гмоль | Gmol | наномоль | нмоль | nmol | |
| 1012 моль | терамоль | Тмоль | Tmol | 10−12 моль | пикомоль | пмоль | pmol |
| 1015 моль | петамоль | Пмоль | Pmol | 10−15 моль | фемтомоль | фмоль | fmol |
| 1018 моль | эксамоль | Эмоль | Emol | 10−18 моль | аттомоль | амоль | amol |
| 1021 моль | зеттамоль | Змоль | Zmol | 10−21 моль | зептомоль | змоль | zmol |
| 1024 моль | йоттамоль | Имоль | Ymol | 10−24 моль | йоктомоль | имоль | ymol |
| применять не рекомендуется | |||||||
См. также
Примечания
dic.academic.ruОбъяснение что такое «моль», «молярная масса» и «количество вещества»
Вчера обещал объяснить это доступным языком. Вещь важная для понимания химии. Если один раз понять, то потом уже не забудешь.Химия имеет свой язык, как и любая наука. 2H2 + O2 → 2H2O — на химическом языке запись реакции образования воды из простых веществ, водорода (H) и кислорода (O). Маленькие цифры относятся к количеству атомов (Они стоят после символа химического элемента), большие — к количеству молекул. Из уравнения видно что две молекулы водорода соединяются с одной молекулой кислорода и в результате выходит две молекулы воды. Внимание — это очень важно понять! Соединяются именно молекулы с молекулами, не «грамм с граммом», а молекула с молекулой.
Эта пропорция сохранится всегда:
| 2 молекулы водорода | соединятся с одной молекулой кислорода | и получится | 2 молекулы воды |
| 200 молекул водорода | соединятся с 100 молекул кислорода | и получится | 200 молекулы воды |
| 2000 молекул водорода | соединятся с 1000 молекул кислорода | и получится | 2000 молекулы воды |
| 2 миллиона молекул водорода | соединятся с миллионом молекул кислорода | и получится | 2 миллиона молекул воды |
Всё бы хорошо, но есть две проблемы. Первая — в реальной жизни мы не сможем отмерить один миллион молекул кислорода или водорода. Мы сможем отмерить один грамм или одну тонну реактивов. Вторая — молекулы очень маленькие. В одном стакане воды их 6,7·1024 штук. Или, в обычной записи 6,7 триллионов триллионов (именно так — почти семь триллионов раз по триллиону молекул). Оперировать такими цифрами неудобно.
Какой же выход? Молекулы ведь тоже имеют массу, пускай очень маленькую. Мы просто берём массу одной молекулы, умножаем на количество молекул и получаем нужную нам массу. Договорились так — берём очень большое количество молекул (600 миллиардов триллионов штук) и изобретаем для этого количества специальную единицу измерения моль. Как для 12 штук чего-либо есть специальное название «дюжина», и когда говорят о «десяти дюжинах», то имеют в виду 120 штук. 5 дюжин яиц = 60 штук. Так и с молями. 1 моль — это 600 миллиардов триллионов молекул или, в математической нотации, 6,02·1023 молекул. То есть когда нам говорят «1 моль» водорода, мы знаем что речь идёт о 600 миллиардах триллионов молекул водорода. Когда говорят о 0,2 молях воды, то мы понимаем что речь идёт 120 миллиардах триллионов молекул воды.
Ещё раз — моль это просто такая счётная единица, только специально для молекул. Как «десяток», «дюжина» или «миллион», только гораздо больше.
Продолжая таблицу выше, можно написать:
| 2 моля водорода | соединятся с одним молем кислорода | и получится | 2 моля воды |
| 20 молей водорода | соединятся с 10 молями кислорода | и получится | 20 молей воды |
| 1000 молей водорода | соединятся с 500 молями кислорода | и получится | 1000 молей воды |
Первую проблему мы решили, писать 1 моль или 2 моля гораздо удобнее чем 600 миллиардов триллионов молекул или 1,2 триллиона триллионов молекул. Но для одного удобства не стоило огород городить. Вторая проблема, как помним, переход от количества молекул (не считать же их поштучно!) к массе вещества, к тому что мы можем отмерить на весах. Такое количество молекул в одном моле (оно ведь немного странное, некруглое — 6,02·1023 молекул) выбрано неспроста. Один моль молекул углерода весит ровно 12 грамм.
Понятно что все молекулы разные. Есть большие и тяжелые — в них может быть много атомов, или не очень много, но зато сами атомы тяжелые. А есть маленькие и легкие молекулы. Для каждого атома и для многих молекул есть в справочниках таблицы с их молярной массой. То есть с весом одного моля таких молекул (если нет, можно легко самим посчитать, сложив молярные массы всех атомов, из которых составлена молекула). Молярная масса измеряется в грамм/моль (сколько грамм весит один моль, то есть сколько грамм весят 6,02·1023 молекул). Мы помним ведь что моль — просто счётная единица. Ну как если бы в справочнике писали — 1 дюжина куриных яиц весит 600 грамм, а 1 дюжина страусиных весит 19 килограмм. Дюжина — просто количество (12 штук), а сами яйца, куриное или страусиное, весят по-разному. И дюжина таких или других яиц тоже по-разному весит.
Так и с молекулами. 1 моль маленьких и лёгких молекул водорода весит 2 грамма, а 1 моль больших молекул серной кислоты — 98 грамм. 1 моль кислорода весит 32 грамма, 1 моль воды — 18 грамм. Вот картинка для примера, где видны маленькие молекулы водорода и большие молекулы кислорода. Эта картинка — графическое отображение реакции 2H2 + O2 → 2H2O.
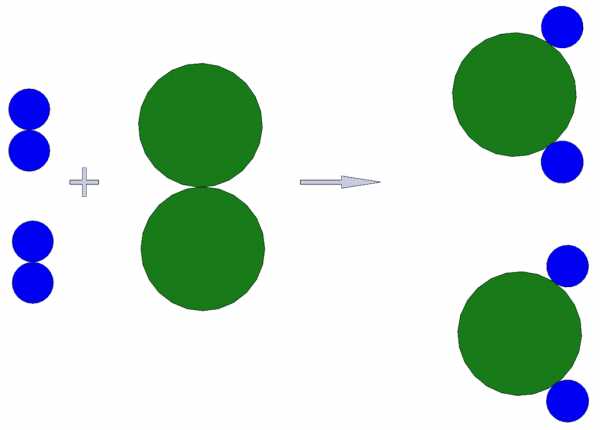
Продолжаем заполнять таблицу:
| 2 моля водорода | соединятся с одним молем кислорода | и получится | 2 моля воды |
| 4 грамма водорода (т.к. 1 моль водорода весит два грамма) | соединятся с 32 граммами кислорода | и получится | 36 грамм воды |
Видите переход от количества молекул к их массе? Видите что выполняется закон сохранения вещества? 4 грамма + 32 грамма дали 36 грамм.
Теперь мы можем решать простые задачи по химии. Вот самая примитивная: Было 100 молекул кислорода и 100 молекул водорода. Что произойдёт в результате реакции? Мы знаем что на 1 молекулу кислорода нужно 2 молекулы водорода. Поэтому прореагируют все 100 молекул водорода (и образуется 100 молекул воды), а вот кислород прореагирует не весь, ещё 50 молекул останется. Кислород в избытке.
Молекулы штуками, как я уже сказал выше, никто не считает. Вещества обычно отмеряют граммами. Теперь задача из школьного учебника: есть 10 г. водорода и 64 г. кислорода, что будет если их смешать? Мы для начала должны перевести массы в моли (то есть в количество молекул или количество вещества, как говорят химики). 10 г. водорода — это 5 моль водорода (1 моль водорода весит 2 грамма). 64 г. кислорода — это 2 моля (1 моль весит 32 грамма). Мы знаем что на 1 моль кислорода при реакции уходит 2 моля водорода. Значит, в нашем случае прореагирует весь кислород (2 моля) и 4 моля водорода из пяти. Получится 4 моля воды и ещё останется один моль водорода.
Переведём ответ снова в граммы. Прореагирует весь кислород (64 грамма) и 8 грамм водорода (4 моля * 2 г/моль). 1 моль водорода останется не прореагировавшим (это 2 грамма) и получится 72 грамма воды (4 моля * 18 г/моль). Закон сохранения вещества опять выполняется — 64 + 10 = 72 + 2.
Думаю что теперь уже всем должно быть понятно. 1 моль — просто количество молекул. Молярная масса — это масса одного моля. Она нужна для того чтобы переходить от массы вещества (с которой мы работаем в реальном мире) к количеству молекул, или количеству вещества, нужному для реакций.
Снова повторимся:
а) вещества реагирует в соотношении n молекул одного к m молекул другого. Это пропорция будет одинаковой и для 100 молекул исходного вещества, и для ста триллионов, или для ста триллионов триллионов.
б) для удобства, чтобы не считать молекулы штуками, придумали специальную счётную единицу — моль, то есть сразу 6,02·1023 молекул. Количество этих молей называют обычном «количество вещества»
в) моль каждого вещества весит по-разному, т.к. молекулы и атомы, из которых состоит вещества, сами весят по-разному. Масса одного моля вещества называется его молярной массой. Ещё один пример — обычные и силикатные кирпичи весят по-разному. Если мы проведём аналогию, то «вес тысячи кирпичей» — это «молярная масса» (с тем отличием что молекул не 1000, а больше). Масса этой «тысячи кирпичей» разная для силикатных и обычных кирпичей.
г) весь этот огород городим для того чтобы легко можно было переходить от массы реактивов к количеству вещества (количеству молекул, количеству молей) и обратно. А переходить туда/обратно нужно потому что в реальном мире мы отмеряем реактивы граммами, а химические реакции идут пропорционально не массе, а количеству молекул.
P.S. Химикам и прочим — я здесь специально многое упрощал. Не нужно мне объяснять что 12 грамм весит не 1 моль углерода, а 1 моль молекул изотопа С12, или про то что вместо «молекул» нужно было бы писать «структурных единиц» (молекул, ионов, атомов…), специально не упомянул что 1 моль газа занимает одинаковый объём при одинаковых условиях и ещё про многое другое
Что мне не нравилось в учебниках — только формальное определение моля, без указания смысла этого понятия и для чего это нужно.
chva.livejournal.com
Моль (единица измерения) — Циклопедия
Моль. Количество вещества // Химия – Просто [5:52]Моль — единица количества вещества в СИ. Другое название — грамм-молекула. Моль является одной из семи базовых единиц СИ.
1 моль — это количество вещества, содержащее число Авогадро (6,02214179±(30)×1023) структурных формульных единиц — реальных частиц, таких как атомы, молекулы, ионы или радикалы.
По формальному определению моль — это количество вещества, выраженное в граммах, численно равное ее молекулярной массе и отличается тем, что одному молю любого вещества соответствует одинаковое количество молекул. В частности, 1 моль содержит столько молекул (атомов, ионов, других структурных элементов вещества), сколько атомов в 12 г 126C, то есть равна постоянной Авогадро.
Обозначение «моль» ввел в 1893 году Вильгельм Оствальд, как производное от слова «молекула». Как базовую единицу СИ моль утвердила в 1971 году 14 Генеральная конференция мер и весов. Несмотря на то, что моль широко использовался в химии, были возражения, в частности, противники указывали на то, что моль — это все количество, которое можно выразить числом.
Рассматривается предложение[1] переопределения многих единиц СИ, в частности постоянной Авогадро. Если постоянная Авогадро получит фиксированное числовое значение, то для определения моля не надо будет привязываться к атомам, в частности атомам углерода-12.
[править] Связанный термин
Молярный — связан с грамм-молекулой:
- молярный раствор — раствор, в 1 л которого содержится одна грамм-молекула растворенного вещества;
- молярная доля — отношение количества молей данного растворенного вещества к сумме молей всех растворенных веществ и растворителя.
cyclowiki.org
Что такое моль в химии
Химические вещества можно измерять не только в килограммах или миллилитрах, но и в молях. Моль – единица количества вещества, появившаяся благодаря тому факту, что вещества состоят из молекул и атомов.Что такое моль в химии: определение
Моль представляет собой такое количество вещества, которое вмещает в себя столько же частиц (молекул или атомов), сколько атомов содержится в 12 г углерода C. Чтобы найти число частиц в 12 г углерода, надо разделить общую массу вещества (0,012 кг) на абсолютную массу углеродного атома, составляющую 19,93×10^(-27) кг.В итоге получается 6,02×10^23 частиц. Найденное число равно числу молекул или атомов в одном моле всякого вещества и называется числом Авогадро. Его размерность – 1/моль, или моль «в минус первой степени».Если химическое вещество состоит из молекул, в одном моле этого вещества будет содержаться 6,02×10^23 молекул. Так, 1 моль водорода h3 – это 6,02×10^23 молекул h3, 1 моль воды h3O – это 6,02×10^23 молекул h3O, 1 моль глюкозы C6h22O6 – это 6,02×10^23 молекул C6h22O6.Если вещество состоит из атомов, в одном моле этого вещества будет содержаться то же Авогадрово число атомов — 6,02×10^23. Это относится, к примеру, к 1 молю железа Fe или серы S.
О чем говорит количество вещества
Итак, 1 моль любого химического вещества содержит Авогадрово число частиц, составляющих данное вещество, т.е. около 6,02×10^23 молекул или атомов. Общее количество вещества (число молей) обозначается латинской буквой n или греческой буквой «ню». Его можно найти по отношению общего количества молекул или атомов вещества к числу молекул в 1 моле – числу Авогадро:n=N/N(A), где n – количество вещества (моль), N – количество частиц вещества, N(A) – число Авогадро.Отсюда же можно выразить и число частиц в заданном количестве вещества:N=N(A) x n.Фактическую массу одного моля вещества называют его молярной массой и обозначают букой M. Она выражается в «граммах на моль» (г/моль), но численно равна относительной молекулярной массе вещества Mr (если вещество состоит из молекул) или относительной атомной массе вещества Ar, если вещество состоит из атомов.Относительные атомные массы элементов можно найти по таблице Менделеева (обычно при расчетах их округляют). Так, для водорода это 1, для лития – 7, для углерода – 12, для кислорода – 16 и т.д. Относительные молекулярные массы складываются из относительных атомных масс составляющих молекулы атомов. К примеру, относительная молекулярная масса воды h3OMr(h3O)=2xAr(H)+Ar(O)=2×1+16=18.Относительные атомные и молекулярные массы – безразмерные величины, поскольку выражают массу атома и молекулы относительно условной единицы – 1/12 массы атома углерода.В типовых задачах обычно требуется найти, сколько молекул или атомов содержится в заданном количестве вещества, какую массу составляет заданное количество вещества, сколько молекул в заданной массе. Важно понимать, что молекулярная формула вещества указывает на число молей каждого элемента, входящего в его состав. То есть 1 моль серной кислоты h3SO4 содержит 2 моля атомов водорода H, 1 моль атомов серы S, 4 моля атомов кислорода O.
completerepair.ru
