|
|
|
|
Сегодня 20.06.2021
Быстрые ссылки
|
||||||
Бытовая химия. Товары в METRO Cash and Carry
О качестве
Чистота – залог здоровья. Особенно если наводить ее при помощи эффективных чистящих средств. METRO предлагает широкий выбор бытовой химии от ведущих мировых производителей для поддержания в чистоте офисов, кафе, ресторанов, отелей, хостелов и других помещений. В наших торговых центрах представлена продукция компаний, лидирующих в области товаров для поддержания чистоты.
Вся бытовая химия соответствует требованиям законодательства РФ, имеет все необходимые документы в области качества и безопасности, а также отвечает высоким требованиям бренда. Наши средства помогут бережно и надежно защитить свой дом или рабочее место.
Какие чистящие средства представлены в нашем ассортименте?
УНИВЕРСАЛЬНЫЕ. Успешно справляются со всеми видами загрязнений на различных поверхностях: кафель, плитка, дерево, керамика, стекло и т.д.
ДЛЯ КУХНИ. Жироудалители для избавления от стойких и пригоревших жиров, концентрированные средства, очистители холодильников, чистящее средство для кухонных поверхностей. Удаляют загрязнения и помогают продлить срок службы оборудования.
ДЛЯ ВАННОЙ И САНУЗЛА. Удаляют ржавчину и известковый камень, дезинфицируют, продлевают срок службы поверхностей и нейтрализуют неприятные запахи.
ДЛЯ СТЕКЛА. В основном выпускаются в виде жидкостей, имеют удобную форму пульверизатора для быстрого и легкого нанесения средства на вертикальную поверхность. Эффективно очищают, защищают стекла и зеркала от царапин.
ДЛЯ ПОЛА. Поддерживают отличный внешний вид линолеума, ламината, ковролина: удаляют пятна, формируют защитное покрытие.
ДЛЯ ПОСУДЫ. Гелеобразные пенящиеся средства удобно наносятся на посуду и хорошо смываются.
ДЛЯ ДЕТСКОЙ ПОСУДЫ. Изготовлены преимущественно из натуральных компонентов без использования отдушек, консервантов и красителей.
ДЛЯ ПОСУДОМОЕЧНЫХ МАШИН. Порошки, таблетки и капсулы эффективно очищают посуду от жира и грязи, придают ей блеск и защищают от разводов и коррозии. А очистители посудомоечных машин поддерживают устройство в рабочем состоянии и устраняют неприятные запахи.
ДЛЯ СТИРКИ. Стиральные порошки, концентрированные средства, средства в больших упаковках, пятновыводители, кондиционеры. А также специальные средства и добавки: ловушки для грязи и цвета, салфетки для предотвращения окрашивания вещей, антинакипины и др.
Подробнее
Ярославский государственный технический университет
О программе
Специалитет. Направление подготовки «04.05.01. Фундаментальная и прикладная химия».
Будете уметь
Пользоваться нормативной документацией, регламентирующей производство и проверку качества лекарственных препаратов; выполнять качественное и количественное определение лекарственных веществ различными физико-химическими методами анализа, прогнозировать на основе химического строения физико-химические свойства, возможный характер фармакологической активности оптимальные условия хранения лекарственных препаратов.
Будете работать
На предприятиях фармацевтической отрасли, в научных организациях и в образовательных учреждениях.
* Количество мест указано для направления подготовки 44.05.01. Фундаментальная и прикладная химия
Помощь лучшим студентам
ЯГТУ реализует программу «Поддержка лучших», включающую:
— выплату повышенной стипендии на первый семестр студентам первого курса очной формы обучения, поступившим по результатам ЕГЭ и набравшим высокие баллы по предметам, установленным в качестве вступительных испытаний;
— скидки по оплате обучения для некоторых категорий абитуриентов, поступающих для обучения на очной форме на основе договора.
Как поступить
Поступление на 1 курс бакалавриата и специалитета происходит по результатам баллов ЕГЭ или по результатам прохождения тест-экзамена ЯГТУ (для некоторых категорий).
ЯГТУ начисляет дополнительные баллы за индивидуальные спортивные, творческие, общественные достижения абитуриента: победы в соревнованиях, олимпиадах различных уровней, успехи в учебе, волонтерской деятельности, творческих конкурсах.
При поступлении в магистратуру формой проведения вступительных экзаменов является письменный экзамен по профилю направления. Для участия в вступительных испытаниях требуется наличие высшего образования.
Опубликованы результаты пригласительного этапа ВсОШ по химии
В пригласительном этапе всероссийской олимпиады по химии приняли участие 18 482 школьника из 82 субъектов России. В лидерах по числу участников – Самарская, Нижегородская, Тамбовская, Оренбургская области, Республика Татарстан. Задачи тура также порешали 958 учителей, родителей и других взрослых.
Результаты участников доступны в тестирующей системе по ссылке из заявки в личном кабинете. На странице тура опубликованы задания, ответы. Видеоразборы, в которых эксперты олимпиады объясняют решения и типичные ошибки участников доступны на канале «Сириуса».
Уже состоялись туры по астрономии и биологии. Результаты по этим предметам будут объявлены 9 и 14 мая соответственно.
Пригласительный школьный онлайн-этап олимпиады еще продолжается. И вы можете зарегистрироваться на него на сайте siriusolymp.ru. Принять участие в интеллектуальном состязании могут ученики 3–10-х классов из всех регионов России, а также учителя и все, кто хочет порешать интересные задачи и проверить свои знания.
Туры пройдут:
12 – 14 мая математика
17 – 18 мая физика
24 – 25 мая информатика
Образовательный центр «Сириус» второй год подряд проводит онлайн пригласительный этап всероссийской олимпиады по шести дисциплинам, приоритетным для Стратегии научно-технологического развития страны: химии, астрономии, биологии, математике, физике и информатике. Дистанционный формат обеспечивает равный доступ к интеллектуальному соревнованию всех школьников России и помогает им открыть знакомые предметы с новой стороны.
Учебный отдел — Институт химии СПбГУ
Учебное управление ректората СПбГУ
Николаева Дина Николаевна — заместитель начальника Учебного управления по направлениям математика, механика, процессы управления, физика и химия
эл. почта [email protected]
телефон 4284208
кабинет 3519 (Университетский пр., д. 28)
Часы приёма:
- Вт: 11:00–13:00
- Чт: 11:00–13:00
Учебный отдел по направлению химия
Захарова Ирина Витальевна — начальник учебного отдела
эл, почта [email protected]
телефон 4284032
кабинет 313 (Университетский пр., д. 26)
Часы приема: Пн – Пт 09:00–16:00 (обеденный перерыв 13:40–14:25)
- Байкова Наталья Львовна — ведущий специалист;
- Никонорова Марина Викторовна — специалист;
- Иванова Евгения Эдуардовна — ведущий специалист.
эл. почта [email protected]
телефон 4284032
кабинет 313 (Университетский пр., д. 26).
Часы работы: Пн – Пт 09:00–17:45 (обеденный перерыв 13:40–14:25).
Чернышова Мария Алексеевна — ведущий специалист (аспирантура)
эл. почта [email protected]
телефон 4284589
кабинет 106 (Университетский пр., д. 26).
Часы работы: Пн – Пт 09:00–17:45 (обеденный перерыв 13:40–14:25).
Отдел планирования учебных занятий и аттестаций
Котова Наталья Леонидовна — ведущий специалист
эл. почта [email protected]
телефон 4284032
кабинет 313 (Университетский пр., д. 26).
Часы работы: Пн – Пт 09:00–17:45 (обеденный перерыв 13:40–14:25).
Если вам необходимо получить какой-либо документ или справку, рекомендуем ознакомиться с ответами на часто задаваемые вопросы по документам и справкам.
Контактная информация
Приемная ректора
ул. Большая Морская, д. 18, каб. 313
Тел.: +7 (812) 315-75-25
Факс: +7 (812) 315-75-25
E-mail: [email protected]
Приемная президента
ул. Большая Морская, д. 18, каб. 313
Тел.: +7 (812) 571-97-55
Факс: +7 (812) 571-95-84
E-mail: [email protected]
Институты
Институт текстиля и моды
Иванов Олег Михайлович
ул. Большая Морская, д. 18, каб. 435 А
Телефон/факс: +7 (812) 315-16-79, Часы приема: пн — ср. 10:00 — 18:00, вт — чт. 10:00 — 18:30
Эл. почта: [email protected]
Институт прикладной химии и экологии
Новоселов Николай Петрович
ул. Большая Морская, д. 18, каб. 428
Телефон/факс: +7 (812) 315-06-65, Часы приема: пн — чт. 13:00 — 17:00, пт. 13:00 — 16:00
Эл. почта: [email protected]
Институт графического дизайна
Сухарева Алина Михайловна
ул. Большая Морская, д. 18, каб. 431
Телефон/факс: +7 (812) 315-08-85, Часы приема: пн — чт. 11:00 — 17:00
Эл. почта: [email protected]
Высшая школа технологии и энергетики
Институт информационных технологий и автоматизации
Марковец Алексей Владимирович
ул. Большая Морская, д. 18, каб. 425
Телефон/факс: +7 (812) 315-12-77
Эл. почта: [email protected]
Институт экономики и социальных технологий
Иванова Светлана Юрьевна
(по вопросам обучения по направлению: 44.03.04 Профессиональное обучение)
ул. Большая Морская, д. 18, каб. 415
Часы приема: пн — пт. 10:00 — 17:00
Тел.: +7 (812) 571-98-10
(по вопросам обучения по направлениям: 38.03.01 Экономика, 38.03.02 Менеджмент, 39.03.02 Социальная работа)
Вознесенский пр.,46, каб. 363
Часы приема: пн — пт. 10:00 — 17:00
Тел.: +7 (812) 310-37-44
ул. Большая Морская, д. 18, каб. 433, каб. 421a
Часы приема: пн — пт. 10:00 — 17:00
Телефон/факс: +7 (812) 315-03-92,
Эл. почта: [email protected]
Высшая школа печати и медиатехнологий
Лезунова Наталья Борисовна
Институт бизнес-коммуникаций
Рожков Николай Николаевич
ул. Большая Морская, д. 18
Часы приема: пн — ср. 15:00 — 17:00; вт — чт. 11:00 — 17:00 (обед: 14:00 — 15:00)
Кабинет 424:
- Oчное, заочное отделение – направления 43.03.02 Туризм
- Очное отделение – направления 42.03.01 Реклама и связи с общественностью
E-mail: [email protected]
Тел.: +7 (812) 571-42-00
Кабинет 424:
- Oчное, заочное, очно-заочное отделения – направления 38.03.02 Менеджмент
E-mail: [email protected]
Тел.: +7 (812) 571-42-00
Кабинет 426:
- Заочное отделение – направления 42.03.01 Реклама и связи с общественностью, 46.03.02 Документоведение и архивоведение
E-mail: [email protected]
Телефон/факс: +7 (812) 314-71-00
Институт дизайна костюма
Гамаюнов Петр Петрович
ул. Садовая, д. 54, каб. 718
Телефон/факс: +7 (812) 310-35-45, Часы приема: вт. 11:00 — 13:00, чт. 15:00 — 17:00
Эл. почта: [email protected]
Институт дизайна пространственной среды
Ветрова Юлия Николаевна
ул. Моховая, д. 26, каб. 412
Телефон/факс: +7 (812) 272-73-62, Часы приема: пн — чт. 13:00 — 17:00, перерыв 14:00 — 15:00
Эл. почта: [email protected]
Институт прикладного искусства
Жукова Любовь Тимофеевна
ул. Садовая, д. 54, каб. 604
Телефон/факс: +7 (812) 314-11-74, Часы приема: пн — чт. 11:00 — 17:00
Эл. почта: [email protected]
Институт дизайна и искусств
Санжаров Владимир Борисович
ул. Большая Морская, д. 18, каб. 422
Телефон/факс: +7 (812) 315-13-49, Часы приема: пн — пт. 11:00 — 16:00
Эл. почта: [email protected]
Региональный институт непрерывного профессионального образования
Лебедева Галина Георгиевна
Вознесенский пр., д. 46, каб. 415
Телефон/факс: +7 (812) 315-12-74, Часы приема: вт. 11:00 — 13:00, чт. 15:00 — 17:00
Эл. почта: [email protected]
Институт дополнительного профессионального образования
Тюрина Елена Витальевна
Колледжи
Колледж технологии, моделирования и управления
Кукушкина Наталия Георгиевна
Инженерная школа одежды (колледж)
Вершигора Анна Владимировна
празеодим | химический элемент | Britannica
Празеодим (Pr) , химический элемент, редкоземельный металл лантаноидного ряда периодической таблицы.
Британская энциклопедия, Inc.Британская викторина
Периодическая таблица элементов
Проверьте свою связь с периодической таблицей элементов в этой викторине по всем 118 химическим элементам и их символам.Возможно, вы знакомы с химическими символами водорода и кислорода, но можете ли вы сопоставить такие низкопрофильные элементы, как гадолиний и эрбий, с их соответствующими символами?
Празеодим — умеренно мягкий, пластичный и ковкий серебристо-белый металл. Он быстро вытесняет водород из воды в разбавленных кислотах (кроме плавиковой кислоты [HF]) и медленно окисляется на воздухе, образуя зеленовато-желтоватое оксидное покрытие со сложной и меняющейся стехиометрией, которую можно выразить с помощью общей формулы PrO x ( 1.5 ≤ x ≤ 2). Металл лучше всего хранить запечатанным в пластиковой оболочке в вакууме или в инертной атмосфере. Празеодим сильно парамагнитен, и недеформированный монокристаллический образец будет иметь антиферромагнитный порядок при 0,03 К (-273,12 ° C или -459,62 ° F). Однако, если празеодим деформирован, он может упорядочиваться при температурах до 20 К (-253 ° C или -424 ° F).
Празеодим был обнаружен в дидимии, смеси нескольких оксидов редкоземельных элементов. Из него путем многократной фракционной кристаллизации нитрата аммония дидимия австрийский химик Карл Ауэр фон Вельсбах в 1885 году отделил соли элементов празеодима (зеленая фракция) и неодима (розовая фракция).Празеодим встречается в таких минералах, как монацит и бастнасит, и как один из продуктов ядерного деления.
Природный празеодим полностью представляет собой стабильный изотоп празеодим-141. Сообщается о 38 радиоактивных изотопах празеодима, исключая ядерные изомеры. Они имеют массу от 121 до 159 и имеют период полураспада от 10 миллисекунд (празеодим-121) до 13,57 дней (празеодим-143).
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту.Подпишитесь сейчасЭтот элемент коммерчески отделяется и очищается методами жидкостно-жидкостной экстракции или ионным обменом. Металл получают электролизом плавленых безводных галогенидов или металлотермическим восстановлением фторида или хлорида кальцием. Празеодим существует в двух аллотропных (структурных) формах. Α-фаза представляет собой двойную плотноупакованную гексагональную форму с a, = 3,6721 Å и c, = 11,8326 Å при комнатной температуре. Β-фаза является объемно-центрированной кубической с a = 4.13 Å при 821 ° C (1510 ° F).
Празеодим является второстепенным компонентом миш-металла, который используется для изготовления более легких кремней и в качестве легирующих добавок к черным и цветным сплавам. Этот металл также используется в качестве добавки к сплавам постоянных магнитов Nd 2 Fe 14 B, что приводит к снижению количества необходимого неодима. Оксид циркония, стабилизированный празеодимом (ZrO 2 ), является основой синтетических драгоценных камней зеленого цвета. Смесь празеодима и неодима является активным компонентом дидимия стекла, используемого в защитных очках для защиты глаз стеклодувов и сварщиков.Соединения празеодима также используются для получения керамики и других стекол от светло-зеленого до желтого цвета.
Празеодим образует трехвалентные соединения, такие как оливково-зеленый оксид Pr 2 O 3 , который легко растворяется в кислотах с образованием зеленых солей трехвалентного празеодима. Четырехвалентный черновато-фиолетовый диоксид PrO 2 известен, но ион Pr 4+ в водном растворе неизвестен.
| атомный номер | 59 | ||
|---|---|---|---|
| атомный вес | 140. | ||
| точка плавления | 931 ° C (1708 ° F) | ||
| точка кипения | 3520 ° C (6368 ° F) | ||
| удельный вес | 6,773 (24 ° C, или 75 ° F) | ||
| Степени окисления | +3, +4 | ||
| электронная конфигурация | [Xe] 4 f 3 6 s 2 | ||
| Празеодим Празеодим — мягкий ковкий металл серебристо-желтого цвета.Он является членом группы лантанидов периодической таблицы элементов. Он медленно реагирует с кислородом: при контакте с воздухом образует зеленый оксид, который не защищает его от дальнейшего окисления. Он более устойчив к коррозии на воздухе, чем другие редкие металлы, но его все же необходимо хранить в масле или покрывать пластиком. Быстро реагирует с водой. Приложения В основном этот металл используется в пирофорном сплаве, который используется в кремнях для зажигалок. Соединения празеодима используются по-разному: оксид используется в угольных электродах для зажигания дуги, и он известен своей способностью придавать стеклу приятный желтый цвет.Это стекло фильтрует инфракрасное излучение, поэтому его используют в очках, защищающих глаза сварщиков. Соли используются для окрашивания эмали и стекла. Празеодим можно использовать в качестве легирующего агента с магнием для создания металлов высокой прочности, которые используются в авиационных двигателях. Празеодим — одно из редких химических веществ, которое можно найти в домах в таком оборудовании, как цветные телевизоры, люминесцентные лампы, энергосберегающие лампы и очки. Все редкие химические вещества обладают сопоставимыми свойствами.Использование празеодима все еще растет из-за того, что он подходит для производства катализаторов и полировки стекла. Празеодим в окружающей среде Празеодим — один из наиболее распространенных редкоземельных элементов. Его в четыре раза больше, чем олова. Празеодим обычно встречается только в двух разных типах руд. Основными промышленными рудами, в которых обнаружен празеодим, являются монацит и бастнасит. Основные районы добычи — Китай, США, Бразилия, Индия, Шри-Ланка и Австралия.Запасы празеодима оцениваются примерно в 2 миллиона тонн. Мировое производство празеодима составляет около 2500 тонн в год.
Вернуться к таблице периодических элементов | |
Празеодим — Информация об элементе, свойства и использование
Расшифровка:
Химия в ее элементе: празеодим
(Promo)
Вы слушаете Химию в ее элементе, представленную вам Chemistry World , журналом Королевского химического общества.
(Окончание акции)
Крис Смит
Привет, два по цене одного на этой неделе. Вот Андреа Селла.
Андреа Селла
Будучи аспирантом, я запечатывал образцы ЯМР в вакууме. Когда стекло нагревается факелом, пламя вспыхивает ярким оранжевым светом натрия, скрывающегося в пирексе. Это было все, что я мог выдувать. Для чего-то более серьезного требовалось спуститься на первый этаж, чтобы увидеть нашего волшебника-стеклодува Джеффри Уилкинсона, милого негодяя из Черной страны, заразительно смеющегося и остроумного, как бритва.
Однажды, когда он стоял у токарного станка, и перед ним бушевал оранжевый ад, я спросил его, в каких очках он был одет. «Didymium», — загадочно ответил он, а затем, заметив мой пустой взгляд, добавил: «Выключите свет. Попробуйте их». Он передал мне свои очки, линзы любопытного зеленовато-серого цвета. Я надел их, и внезапно пламя погасло. Все, что я мог видеть, это раскаленный кусок вращающегося стекла, не заслоненный ярким светом. Я смотрела в изумлении, пока Джефф не снял очки с моего лица, сказав: «Верни их, дурак», и не вернулся к своей работе.
Didymium — это не то имя, которое в наши дни можно встретить в учебниках. Это название пары элементов, которые расположены рядом друг с другом в ряду лантаноидов или редкоземельных элементов — то, что раньше было Диким Западом периодической таблицы. Четырнадцать элементов, составляющих серию, примечательны своим сходством. Нигде больше нельзя найти группу элементов, которые так похожи друг на друга по своим химическим свойствам. Следовательно, эти элементы оказалось невероятно трудно отделить друг от друга и очистить.И что еще хуже, в отличие от других металлов, цвета соединений редкоземельных металлов были бледными, мало менялись от одного соединения к другому, что еще больше затрудняло определение чистоты вашего материала. Среди множества заявлений об открытии новых элементов был отчет в 1839 году шведского химика Карла Густава Мосандера о предполагаемом элементе, который он назвал «Дидимий» — в честь греческого слова «близнец».
Изобретение спектроскопии Густовым Кирхгофом и Робертом Бунзеном (да, он же из горелки Бунзена) теперь вступило в силу.Вскоре стало ясно, что спектр редкоземельных элементов очень характерен с резкими газофазными линиями как в твердом теле, так и в растворе. Наконец-то появилось средство установления чистоты.
Бунзен, который к 1870-м годам был ведущим мировым авторитетом в области спектроскопии редкоземельных элементов, поставил этот элемент в качестве проблемы для одного из своих учеников Карла Ауэра, который начал проводить сотни фракционных кристаллизации, необходимых для его получения. чистый. К 1885 году стало ясно, что у Ауэра на руках не один, а два элемента — голубовато-сиреневый, который он назвал «неодимом», новый близнец, и зеленый, который он назвал «празеодимом» — зеленый двойник, каждый со своим спектром. которые в совокупности были такими же, как и в материалах Мосандера.Бунзен был в восторге и сразу одобрил работу своего ученика.
Но только в 1940-х годах будут разработаны быстрые и эффективные методы разделения лантаноидов. Вместо серии мучительно утомительных кристаллизации американские химики во главе с Фрэнком Спеддингом описали методы ионного обмена, и затем в течение нескольких лет экстракция растворителем стала преобладающей и произвела килограммовые количества этих элементов. Внезапно коммерческие приложения стали реальной перспективой.
Поскольку сами ионы имеют неспаренные электроны, их магнитные свойства оказались интересными для ученых и прибыльными для предпринимателей. Сплав неодима, железа и бора, открытый в 1980-х годах, является ферромагнитным, что дает постоянные магниты в 1000 раз сильнее, чем когда-либо ранее. Неодимовые ионно-борадные магниты используются не только в почти миллиардах электродвигателей и электронных устройств по всему миру, но и в чудесных игрушках для детей.
С другой стороны, резкие спектральные линии, которые так очаровывали Бунзена и поколения спектроскопистов с тех пор, предполагают очень точные электронные состояния. Внедрение неодима в синтетические драгоценные камни, такие как гранат, привело к созданию неодимового: YAG-лазера, рабочей лошадки для промышленных лазерных режущих инструментов с блестящими инфракрасными линиями. Ваш персональный iPod, вероятно, был выгравирован YAG. В сочетании с кристаллом удвоения частоты YAG дает нам ярко-зеленую лазерную указку, которой некоторые лекторы любят хвастаться.
Но нестандартное мышление в 1940-х годах химиками из Corning Glassworks в США привело к изобретению, которое навсегда изменило выдувание стекла. Кто-то заметил, что и празеодим, и неодим имеют линии поглощения, почти точно соответствующие этой раздражающе яркой оранжевой линии натрия. Компания Corning начала производить «дидимиевое стекло», которое действует как оптический режекторный фильтр, чтобы вырезать блики, и эффект остается для меня таким же удивительным, как и в первый раз, когда я его видел. Когда несколько лет назад один из наших стеклодувов в UCL вышел на пенсию, он позвонил мне в свой последний день работы.«У меня есть кое-что для тебя», — загадочно сказал он. Я спустился в подвал и пожал ему руку, чтобы пожелать ему всего наилучшего. А затем, к моему удовольствию, он вручил мне свои очки. «Дидимиум, — сказал он, — тебе это понадобится».
Крис Смит
Андреа Селла с историей дидимиума, два элемента в одном лице. И Андреа возвращается на следующей неделе со вкусом металла, который тает во рту и, возможно, также в ваших руках.
Андреа Селла
Но я уверен, вы действительно хотите знать, если это действительно элемент M&M, каков он на вкус? Я знал, что ты спросишь.Так что пару дней назад я быстро лизнул, и ответ такой, если честно, на самом деле это не так уж и много. Слегка терпкий и металлический привкус остается на языке на несколько часов. А когда он расплавится, извините, я оставлю этот эксперимент для кого-то более бесстрашного, чем я.
Крис Смит
И вы можете уловить историю о галлии, который он ел, с Андреа Селла на следующей неделе. Химия в своей стихии, это, конечно, при условии, что его выходки поедания стихии не отравили его тем временем.Я Крис Смит, спасибо за внимание и до свидания.
(Промо)
(Окончание промо)
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Портал круглого стола по фармацевтике ACS GCI »Портал круглого стола по фармацевтике ACS GCI
О Круглом столе
В 2005 году ACS Green Chemistry Institute® и глобальные фармацевтические корпорации разработали Круглый стол по фармацевтике ACS GCI для поощрения инноваций и одновременного ускорения интеграции зеленой химии и зеленой инженерии в фармацевтическую промышленность.С самого начала Круглый стол уделял приоритетное внимание сотрудничеству с академическими исследователями, предоставляя информацию о ключевых возможностях исследований в области зеленой химии и создавая программу грантов. Изучая этот сайт, вы можете узнать о возможностях получения грантов, предстоящих семинарах и онлайн-обучении, а также получить доступ к инструментам, которые помогут вам в разработке более экологичных процессов.
Темы
Медицинская химия
Биофарма
Аналитическая химия
Проточная химия
Пептиды и олигонуклеотиды
И многое другое
Новости
Барометр химической активности вырос в мае
Не скорректированные данные показывают 1.Рост на 0% в мае после роста на 0,9% в апреле. Индекс диффузии в мае достиг 100%. Индекс распространения отмечает количество положительных вкладчиков по отношению к общему количеству отслеживаемых показателей. Показатель CAB за апрель был пересмотрен в сторону повышения на 0,91 пункта, а показатель за март — на 0,16 пункта. Данные за май являются предварительными и могут быть пересмотрены.
«Последние данные CAB соответствуют заметному расширению коммерции, торговли и промышленности», — сказал Кевин Свифт, главный экономист ACC.
CAB состоит из четырех основных компонентов, каждый из которых состоит из множества показателей: 1) производство; 2) цены на акции; 3) цены на продукцию; 4) запасы и другие показатели.
В мае производственные показатели были положительными. Несмотря на некоторую недавнюю слабость в жилищном строительстве — отражение более высоких процентных ставок и цен, а также ограничений со стороны рабочей силы и предложения — тенденции в строительных смолах и связанных с ними химических характеристиках были устойчивыми. Благодаря успеху на автомобильных рынках, смолы и химия, используемые в других товарах длительного пользования, были сильными.Прирост в области пластиковых смол, используемых в упаковке, а также в потребительских и институциональных областях, был положительным. Химические показатели для промышленности были в основном положительными. Экспорт был положительным, в то время как цены на акции выросли, достигнув новых рекордов. Цены на продукцию и вводимые ресурсы были положительными, так же как и товарные запасы и другие показатели цепочки поставок.
CAB — это ведущий экономический индикатор, полученный на основе сводного индекса деятельности химической промышленности. Благодаря своему раннему положению в цепочке поставок, химическая промышленность неизменно занимает лидирующие позиции в США.Бизнес-цикл S. Economics и барометр можно использовать для определения поворотных моментов и вероятных тенденций в экономике в целом. Месячные движения могут быть нестабильными, поэтому предоставляется трехмесячная скользящая средняя значения CAB. Это дает более последовательную и наглядную картину тенденций в национальной экономике.
Если применить CAB еще к 1912 году, было показано, что он обеспечивает опережение от двух до 14 месяцев со средним опережением в восемь месяцев на пиках цикла, как определено Национальным бюро экономических исследований.Среднее преимущество также составило восемь месяцев. При минимальных значениях экономического цикла CAB опережает на срок от одного до семи месяцев, а в среднем — четыре месяца. Среднее преимущество составляло три месяца. CAB перебазируется до среднего опережения (в месяцах) в среднем 100 в базовом году (использовался 2012 год) контрольного временного ряда. Последний — это индекс промышленного производства Федеральной резервной системы.
| Барометр химической активности за последние шесть месяцев и месяц назад *
|
|||||||
| |
Май-20 |
Дек-20 |
21 января |
21 февраля |
21 марта |
21 апреля |
21 мая |
| |
|
|
|
|
|
|
|
| КАБИНА (3MMA) |
108.60 |
121,63 |
123,58 |
124,67 |
126,12 |
127,34 |
128,81 |
| % M / M |
-4,2 |
1,3 |
1,6 |
0,9 |
1.2 |
1,0 |
1,2 |
| % Г / Г |
-11,3 |
-0,6 |
0,4 |
1,1 |
5,3 |
12,3 |
18,6 |
| |
|
|
|
|
|
|
|
| КАБИНА |
108.75 |
123,23 |
125,11 |
125,67 |
127,59 |
128,76 |
130,07 |
| % M / M |
3,6 |
0,7 |
1,5 |
0,4 |
1.5 |
0,9 |
1,0 |
| % Г / Г |
-11,1 |
0,4 |
0,7 |
2,2 |
13,9 |
22,6 |
19,6 |
|
* Изменения в процентах могут не отражать значения индекса из-за округления. |
|||||||
CAB включает показатели, относящиеся к производству хлора и других щелочей, пигментов, пластмассовых смол и других выбранных основных промышленных химикатов; данные о запасах химической компании; часы, отработанные в химикатах; информация о ценах на химические вещества из открытых источников; объем продаж конечным потребителям (или потребителям) в товарно-материальные запасы; и несколько более широких ведущих экономических мер (разрешения на строительство и новые заказы).Каждый месяц ACC предоставляет номер барометра, отражающий данные о деятельности за текущий месяц, а также трехмесячную скользящую среднюю. CAB был разработан экономическим отделом ACC.
Не скорректированные показания CAB за текущий месяц основаны на еженедельных и ежедневных данных с высокой частотой. Например, мы используем данные по капиталу за четверг перед датой выпуска. Использование данных за середину месяца может привести к большим пересмотрам, если условия заметно изменятся во второй половине месяца. Мы перенесли даты выпуска CAB на последний вторник каждого месяца.Мы надеемся, что это минимизирует количество исправлений.
Полный набор данных можно найти на сайте https://www.americanchemistry.com/CAB-vs-Industrial-Production/. Следующая CAB запланирована на 29 июня 2021 года в 9:10 по восточному времени.
CAB разработан и подготовлен в соответствии с антимонопольными директивами ACC и рекомендациями FTC Safe Harbor; не использует информацию о ценах для конкретной компании в качестве входных данных; данные агрегируются таким образом, что невозможно определить данные по компании и продукту. Примечание. ACC постарался подготовить эту публикацию, чтобы предоставить наилучшую доступную информацию. Однако ни Американский химический совет, ни его сотрудники, агенты или другие правопреемники не дают никаких гарантий, явных или подразумеваемых, и не принимают на себя никаких обязательств или ответственности за любое использование или результаты такого использования любой информации или данных, раскрытых в этот материал .
ИСТОЧНИК Американский химический совет
Ссылки по теме
www.americanchemistry.com
празеодим | Химия | Фэндом
| Общие | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Имя, символ, номер | Утюг, пр., 59 | ||||||||||||||
| Химическая серия | лантаноидов | ||||||||||||||
| Группа, период, блок | н / д, 6, ж | ||||||||||||||
| Внешний вид | Серовато-белый | ||||||||||||||
| Атомная масса | 140.908 (2) г / моль | ||||||||||||||
| Электронная конфигурация | [Xe] 4f 3 6s 2 | ||||||||||||||
| Электронов на оболочку | 2, 8, 18, 21, 8, 2 | ||||||||||||||
| Физические свойства | |||||||||||||||
| Фаза | твердый | ||||||||||||||
| Плотность (около комнатной) | 6,77 г · см −3 | ||||||||||||||
| Плотность жидкости при т.пл. | 6,5 г · см −3 | ||||||||||||||
| Температура плавления | 1208 K (935 ° C, 1715 ° F) | ||||||||||||||
| Температура кипения | 3134 К (2861 ° C, 5182 ° F) | ||||||||||||||
| Теплота плавления | 6.89 кДж · моль −1 | ||||||||||||||
| Теплота испарения | 331 кДж · моль −1 | ||||||||||||||
| Теплоемкость | (25 ° C) 27,2 Дж · моль −1 · K −1 | ||||||||||||||
| |||||||||||||||
| Атомные свойства | |||||||||||||||
| Кристаллическая структура | объемно-центрированная кубическая a = 286.65 вечера; [1] гранецентрированный кубик между 1185–1667 K | ||||||||||||||
| Степени окисления | 2, 3 , 4, 6 (амфотерный оксид) | ||||||||||||||
| Электроотрицательность | 1,83 (шкала Полинга) | ||||||||||||||
| Энергии ионизации (подробнее) |
1-й: 762,5 кДж · моль −1 | ||||||||||||||
| 2-я: 1561,9 кДж · моль −1 | |||||||||||||||
| 3-я: 2957 кДж · моль −1 | |||||||||||||||
| Атомный радиус | 140 вечера | ||||||||||||||
| Атомный радиус (расч.) | 156 часов | ||||||||||||||
| Ковалентный радиус | 125 вечера | ||||||||||||||
| Разное | |||||||||||||||
| Магнитный заказ | ферромагнетик | ||||||||||||||
| Удельное электрическое сопротивление | (20 ° C) 96,1 нОм · м | ||||||||||||||
| Теплопроводность | (300 K) 80,4 Вт · м −1 · K −1 | ||||||||||||||
| Тепловое расширение | (25 ° C) 11,8 мкм · м −1 · K −1 | ||||||||||||||
| Скорость звука (тонкий стержень) | (г.т.) (электролитический) 5120 м · с −1 | ||||||||||||||
| Модуль Юнга | 211 ГПа | ||||||||||||||
| Модуль сдвига | 82 ГПа | ||||||||||||||
| Объемный модуль | 170 ГПа | ||||||||||||||
| Коэффициент Пуассона | 0,29 | ||||||||||||||
| Твердость по Моосу | 4,0 | ||||||||||||||
| Твердость по Виккерсу | 608 МПа | ||||||||||||||
| Твердость по Бринеллю | 490 МПа | ||||||||||||||
| Регистрационный номер CAS | 7439-89-6 | ||||||||||||||
| Избранные изотопы | |||||||||||||||
| Список литературы | |||||||||||||||
Празеодим (атомный символ Pr ) — 59-й элемент периодической таблицы.Это малотоксичный лантаноид.
- Атомный вес: 140.908
- Температура плавления: 1204 K (931 ° C или 1708 ° F)
- Температура кипения: 3793 K (3520 ° C или 6368 ° F)
- Плотность: 6,77 г / куб.см
- Фаза (при комнатной температуре): твердый
Празеодим содержится в минералах монацит и бастнасит.
Празеодим используется в сплаве с магнием для создания металлов повышенной прочности для авиационных двигателей. 1 Кроме того, празеодим составляет 5% Misch Metal, сплава, используемого в кремнях зажигалок.Кроме того, он используется в углеродных дугах в киноиндустрии для студийного освещения и проекции. Празеодим также входит в состав дидимиевого стекла, которое используется для изготовления определенных типов защитных очков для сварщиков и стеклодувов, поэтому желтый свет от выдувания стекла отфильтровывается. Соли этого элемента используются для окрашивания стекла и эмали, поэтому они приобретают необычно насыщенный и чистый желтый цвет.
Празеодим происходит от греческих слов празиос и дидимос, которые вместе означают «зеленый близнец».«Он был открыт в 1885 году Карлом Ф. (бароном) Ауэром фон Вельсбахом.
- Примечание.

 4
4 1·10-12
1·10-12 79
79 0·10-50
0·10-50 5·10-12
5·10-12 3
3 0·10-10
0·10-10 4
4 3·10-22
3·10-22 3·10-23
3·10-23 57
57 6·10-58
6·10-58 0·10-12
0·10-12 0·10-9
0·10-9 75·10-25
75·10-25 4
4 8·10-21
8·10-21 9·10-21
9·10-21 4
4 4·10-6
4·10-6 5·10-10
5·10-10 0·10-9
0·10-9 1·10-46
1·10-46 8·10-21
8·10-21 1
1 3
3 6
6 3·10-18
3·10-18 6·10-23
6·10-23 8·10-7
8·10-7 3
3 6·10-9
6·10-9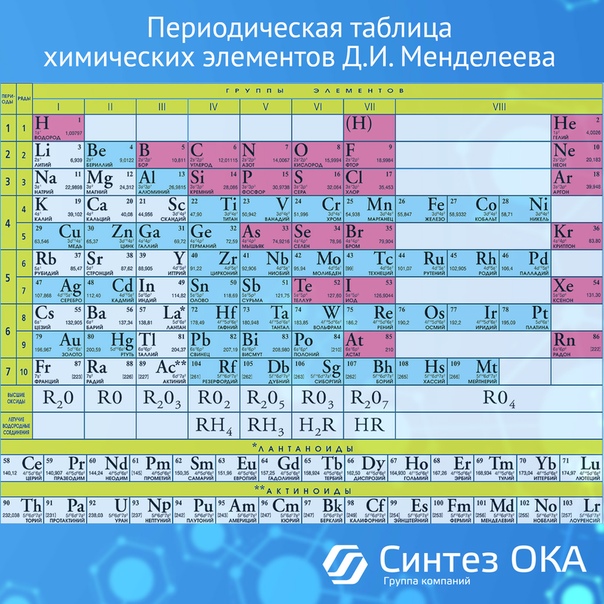 37
37 2·10-11
2·10-11 9·10-5
9·10-5 4
4 07
07 1·10-12
1·10-12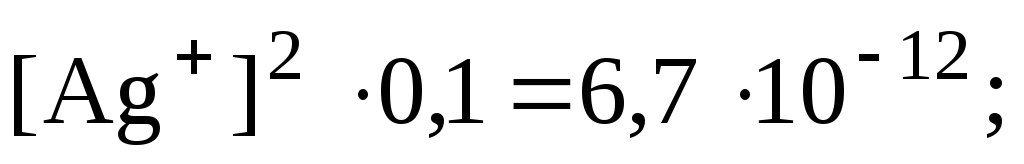 3
3 5·10-10
5·10-10 5
5 1·10-26
1·10-26