| 1. |
Число протонов и заряд ядра
Сложность: лёгкое |
1 |
| 2. |
Число электронов
Сложность: лёгкое |
1 |
3.
|
Число нейтронов в атоме
Сложность: лёгкое |
1 |
| 4. |
Основные понятия
Сложность: лёгкое |
1 |
5.
|
Сложность: среднее |
2 |
| 6. |
Число нейтронов и электронов в нуклиде
Сложность: среднее |
2 |
7.
|
Состав атома
Сложность: среднее |
2 |
| 8. |
Количество нейтронов
Сложность: сложное |
3 |
9.
|
Определи элемент
Сложность: сложное |
3 |
| 10. |
Молекулярные массы хлоридов
Сложность: сложное |
4 |
Урок 1.
 химический элемент. нуклиды. изотопы. законы сохранения массы и энергии в химии — Химия — 11 класс
химический элемент. нуклиды. изотопы. законы сохранения массы и энергии в химии — Химия — 11 класс
Химия, 11 класс
Урок № 1. Химический элемент. Нуклиды. Изотопы. Законы сохранения массы и энергии в химии
Перечень вопросов, рассматриваемых в теме
Урок посвящён изучению основных понятий химии (химический элемент, изотоп, нуклид) и двум важнейшим законам природы – закону сохранения массы и закону сохранения энергии. Учащиеся узнают о важнейших характеристиках химического элемента, смогут назвать различие между понятиями «химический элемент», «нуклид», «изотоп» и научатся применять закон сохранения массы веществ при составлении уравнений химических реакций.
Глоссарий
Атом – это наименьшая частица химического элемента, которая несет все его свойства.
Изотопы – это нуклиды с одинаковым зарядом ядра, но разным массовым числом и числом нейтронов
Нейтрон – это незаряженная элементарная частица.
Нуклиды – это различные виды ядер, которые отличаются зарядом или массовым числом.
Протон – это положительно заряженная элементарная частица.
Элементарная частица – это объект, который нельзя разделить на более мелкие составляющие.
Радиоактивный распад – это превращение ядер нуклидов, сопровождающиеся изменением числа протонов или нейтронов в ядре и испусканием элементарных частиц, гамма-квантов или кластеров.
Химический элемент – это вид атомов с определенным зарядом ядра.
Электроны – это отрицательно заряженные элементарные частицы, которые движутся по орбиталям вокруг ядра.
Ядро – это положительно заряженная центральная часть атома.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Одним из основных понятий химии является атом. Атом – это наименьшая частица химического элемента, которая несет все его свойства. Согласно планетарной модели, атом состоит из ядра и электронов. Электроны – это отрицательно заряженные элементарные частицы, которые движутся по орбиталям вокруг ядра. Ядро – это положительно заряженная центральная часть атома. Ядра атомов превращаются друг в друга в ходе ядерных реакций.
Ядро состоит из двух типов элементарных частиц: протонов (Z) и нейтронов (N). Заряд нейтронов равен нулю. Протоны обладают зарядом +1. Общее число нейтронов и протонов в ядре называется массовым числом (А). Оно близко, но не равно по значению к атомной массе элемента, указанной в Периодической таблице. Заряд ядра равен числу протонов и порядковому номеру элемента в Периодической системе.
Вид атомов с определенным зарядом ядра называется химическим элементом. Химический элемент существует в виде простого вещества (металла или неметалла) или соединений с другими элементами. К характеристикам химического элемента относятся: атомный номер, относительная атомная масса, изотопный состав, положение в Периодической системе, строение атома, электроотрицательность, степени окисления, валентность, энергия ионизации, сродство к электрону, распространенность в природе.
Нуклидами называют различные виды ядер, которые отличаются зарядом или массовым числом. Они обозначаются следующим образом: вверху перед символом нуклида пишется массовое число, внизу – порядковый номер элемента. Нуклиды с одинаковым зарядом ядра, но разным массовым числом и числом нейтронов называются изотопами. Изотопы одного элемента обладают одинаковыми химическими свойствами и почти не отличаются по физическим свойствам. Элементы представляют собой совокупность изотопов с разными массовыми числами, поэтому атомные массы многих элементов представлены дробными числами.
Нуклиды с одинаковым зарядом ядра, но разным массовым числом и числом нейтронов называются изотопами. Изотопы одного элемента обладают одинаковыми химическими свойствами и почти не отличаются по физическим свойствам. Элементы представляют собой совокупность изотопов с разными массовыми числами, поэтому атомные массы многих элементов представлены дробными числами.
Химические реакции подчиняются законам сохранения массы и энергии. Закон сохранения массы веществ впервые сформулировал великий ученый М.В. Ломоносов. Экспериментально его доказал А.Л. Лавуазье. Формулируется закон следующим образом: масса исходных веществ, вступивших в химическую реакцию, равна массе продуктов реакции. В ходе реакции атомы веществ только перегруппировываются.
В двадцатом веке ученые обнаружили, что закон сохранения массы не соблюдается в случае ядерных реакций. После того, как А. Эйнштейн открыл взаимосвязь между массой и энергией, выраженную в его знаменитой формуле E=mc2, стало понятно, что закон сохранения массы лишь частный случай закона сохранения энергии. Закон сохранения энергии гласит: в изолированной системе энергия системы не исчезает и не появляется, а только переходит из одного вида в другой. Для составления ядерных реакций важно помнить, что суммарный заряд ядер и массовое число сохраняются.
Закон сохранения энергии гласит: в изолированной системе энергия системы не исчезает и не появляется, а только переходит из одного вида в другой. Для составления ядерных реакций важно помнить, что суммарный заряд ядер и массовое число сохраняются.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Решение задачи на работу с Периодической системой.
Условие задачи: Введите формулу простого вещества, при бета-распаде которого образуется висмут.
Решение: Висмут – элемент с порядковым номером 83. При бета распаде один из нейтронов превращается в протон, таким образом заряд ядра атома увеличивается на единицу. Следовательно, химический элемент, образующий исходное вещество, находится на одну клетку левее висмута. Это свинец.
Ответ: Pb.
2.Решение задачи на закон сохранения массы или закон сохранения числа атомов.
Условие задачи: Расставьте коэффициенты в реакции и выберите правильное значение их суммы.
Al + S = Al2S3
А) 3
Б) 5
В) 6
Г) 10
Решение: Составим электронный баланс. Каждый атом алюминия присоединил 3 электрона, а каждый атом серы отдал два электрона. Тогда коэффициенты 2Al + 3S = Al2S3
Каждый атом алюминия присоединил 3 электрона, а каждый атом серы отдал два электрона. Тогда коэффициенты 2Al + 3S = Al2S3
Сумма коэффициентов = 6.
Ответ: В.
Урок 44. движение как качественное изменение. ядерные реакции — Естествознание — 10 класс
Естествознание, 10 класс.
Урок 44. Движение как качественное изменение. Ядерные реакции
Перечень вопросов, рассматриваемых в теме: Могут ли одни химические элементы превращаться в другие? Когда было открыто явление радиоактивности и как оно изучалось? Каковы особенности процесса радиоактивного распада? Как происходят ядерные реакции?
Глоссарий по теме:
Химический элемент – вид атомов с одинаковым зарядом ядра.
Нуклид (от лат. nucleus – ядро) – вид атомов с определенным значением заряда ядра Z (число протонов в ядре) и массового числа А (сумма числа протонов и нейтронов в ядре).
Изотопы (от греч.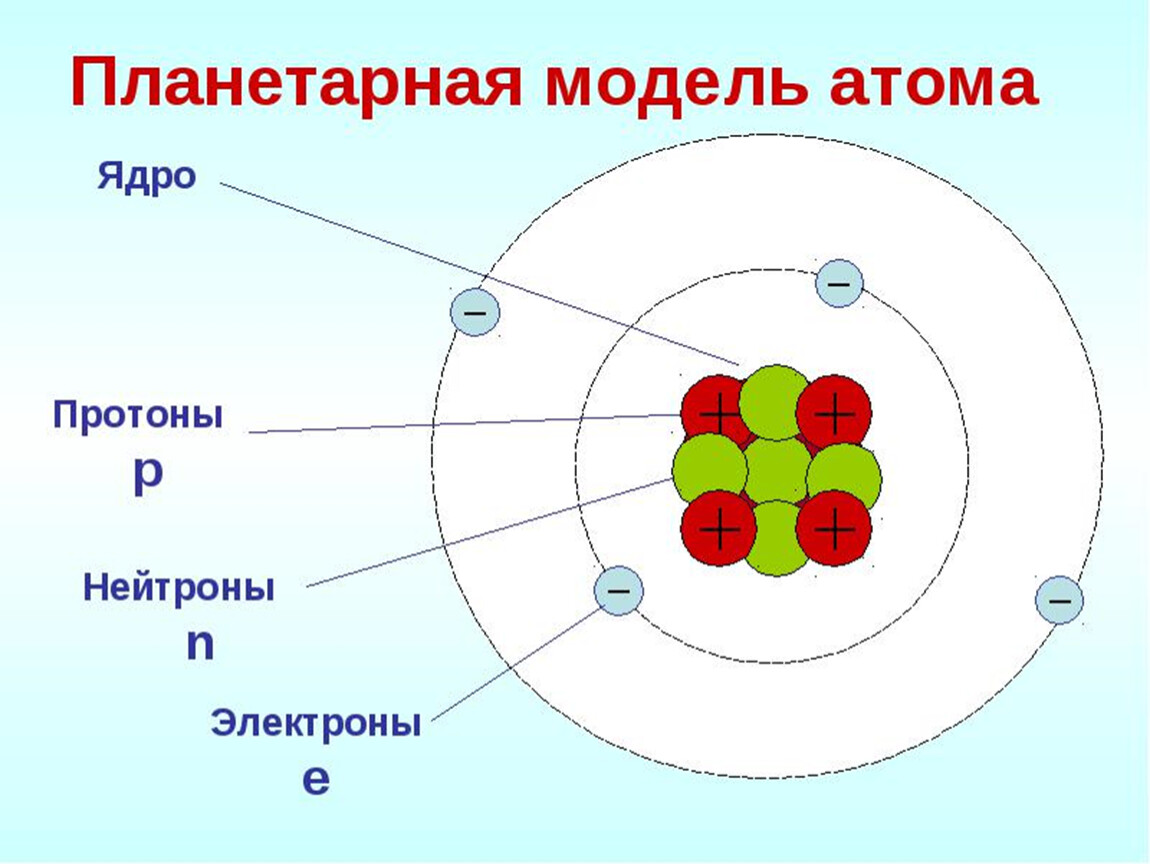 isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
Атомное ядро – положительно заряженная центральная часть атома, состоящая из протонов и нейтронов (нуклонов).
Ядерная физика – раздел физики, изучающий структуры и свойства атомных ядер и их превращений – процессов радиоактивного распада и ядерных реакций.
Радиоактивность (от лат. radio – испускаю, излучаю и actives – действенный) – свойство атомных ядер самопроизвольно изменять свой состав путем испускания элементарных частиц или ядер.
Радиоактивный распад – спонтанное изменение состава нестабильных атомных ядер путем испускания элементарных частиц или ядерных фрагментов.
Период полураспада – это время, в течение которого распадается половина исходного числа радиоактивных атомов.
Ядерные реакции – это превращение атомных ядер при взаимодействии их с элементарными частицами, гамма-квантами или друг с другом.
Деление ядер – процесс, при котором из одного ядра возникают два ядра близких по массе.
Цепные ядерные реакции – это ядерные реакции, в которых частицы, вызывающие их, образуются и как продукты этих реакций.
Основная и дополнительная литература по теме урока:
1. Естествознание. 10 класс: учебник для общеобразоват. организаций: базовый уровень / И.Ю. Алексашина, К.В. Галактионов, И.С. Дмитриев, А.В. Ляпцев и др. / под ред. И.Ю. Алексашиной. – 3-е изд. – М.: Просвещение, 2017. – С. 193-195.
2. Энциклопедия для детей. Том 16. Физика Ч. 1. Биография физики. Путешествие в глубь материи. Механическая картина мира / Глав. ред. В.А. Володин. – М.: Аванта+, 2000. – С. 243-257..
3. Энциклопедия для детей. Том 16. Физика. Ч. 2. Электричество и магнетизм. Термодинамика и квантовая механика. Физика ядра и элементарных частиц / Глав. ред. В.А. Володин. – М.: Аванта+, 2000. – С. 275-291.
Открытые электронные ресурсы по теме урока:
Статья: Радиоактивный распад // Научно-популярный портал «Элементы». URL: http://elementy.ru/trefil/21197/Radioaktivnyy_raspad
URL: http://elementy.ru/trefil/21197/Radioaktivnyy_raspad
Статья: Ядерный распад и синтез // Научно-популярный портал «Элементы». URL: http://elementy.ru/trefil/21178/Yadernyy_raspad_i_sintez
Теоретический материал для самостоятельного изучения
Столетиями алхимики, веря в трансмутацию, пытались найти средство, позволяющее превращать одни элементы в другие, но сделать это в ходе химических превращений оказалось невозможным. Превращать одни химические элементы в другие стало возможным только в XX столетии, когда человек научился осуществлять ядерные реакции. Изучением структуры и свойств атомных ядер и их превращений – процессов радиоактивного распада и ядерных реакций, занимается ядерная физика.
В конце XIX века французский физик Антуан Анри Беккерель (1852 – 1908), изучая флуоресценцию солей урана, обнаружил, что эти соединения испускают неизвестное излучение, засвечивающее завёрнутую в чёрную бумагу фотопластинку. При этом обнаруженное излучение соли урана испускали независимо от того облучались они светом или нет. Новым явлением заинтересовались французские учёные Пьер Кюри (1859 – 1906) и Мария Склодовская-Кюри (1867 – 1934). В 1897 – 1898 гг. они установили, что обнаруженное излучение является свойством урана, которое не зависит от того, в каком соединении этот элемент содержится. Исследуя в 1898 г. урановую руду, учёные открыли два новых химических элемента – полоний и радий, которые также обладали радиоактивностью – такое название они предложили для обнаруженного самопроизвольного испускания атомами излучения (от лат. radio – испускаю, излучаю и actives – действенный).
Новым явлением заинтересовались французские учёные Пьер Кюри (1859 – 1906) и Мария Склодовская-Кюри (1867 – 1934). В 1897 – 1898 гг. они установили, что обнаруженное излучение является свойством урана, которое не зависит от того, в каком соединении этот элемент содержится. Исследуя в 1898 г. урановую руду, учёные открыли два новых химических элемента – полоний и радий, которые также обладали радиоактивностью – такое название они предложили для обнаруженного самопроизвольного испускания атомами излучения (от лат. radio – испускаю, излучаю и actives – действенный).
Изучение радиоактивного излучения позволило обнаружить его неоднородность. Так в 1899 г. английский физик Эрнест Резерфорд (1871 – 1937) установил, что магнитное поле разделяет излучение на две составляющие, обладающие положительными и отрицательными зарядами. Эти составляющие радиоактивного излучения получили название альфа-лучи и бета-лучи (по первым буквам греческого алфавита). В 1900 г. французский физик и химик Поль Виллар (1860 – 1934) сумел выделить еще одну составляющую, которая не отклонялась магнитным полем – гамма-лучи.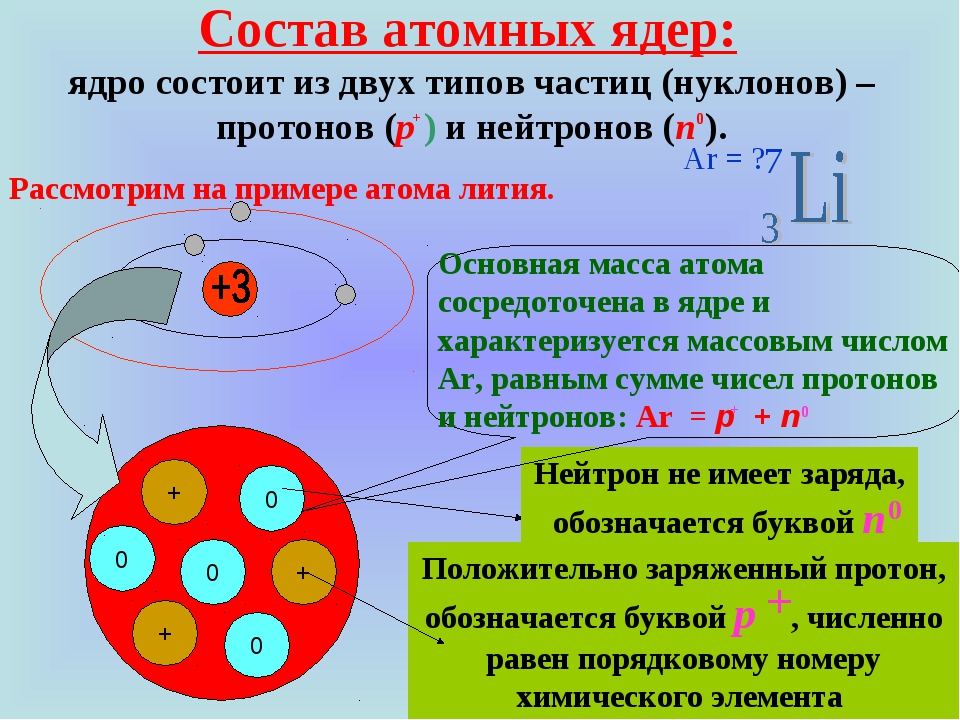 Анри Беккерелем было установлено, что бета-лучи представляют собой поток электронов. В 1908 г. Э. Резерфордом совместно с немецким физиком Хансом Гейгером (1882 – 1945) было доказано, что альфа-частицы являются ядрами атома гелия (заряд Z = +2 и массовое число A = 4).
Анри Беккерелем было установлено, что бета-лучи представляют собой поток электронов. В 1908 г. Э. Резерфордом совместно с немецким физиком Хансом Гейгером (1882 – 1945) было доказано, что альфа-частицы являются ядрами атома гелия (заряд Z = +2 и массовое число A = 4).
Радиоактивное излучение свидетельствует о том, что ядра атомов претерпевают распад, в результате которого они превращаются в ядра новых химических элементов. Выяснилось, что радиоактивностью обладают многие элементы, присутствующие в земной коре. Более того, все химические элементы, расположенные в периодической системе за висмутом, радиоактивны: все их нуклиды нестабильны. Нуклидом (от лат. nucleus – ядро) называют вид атомов с определенным значением заряда ядра и массой. Для обозначения нуклида используют название химического элемента, к которому через дефис записываю массовое число (например, уран-238) или знак химического элемента, рядом с которым наверху указывают массовое число, а внизу заряд ядра (например, 23892U). Разные нуклиды одного элемента по отношению друг к другу являются изотопами. Изотопы (от греч. isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
Разные нуклиды одного элемента по отношению друг к другу являются изотопами. Изотопы (от греч. isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
На рубеже XIX –XX вв. было установлено, что существует три вида самопроизвольных ядерных превращений (позже были обнаружены и другие виды, но они менее распространены).
Альфа-распад (α-распад) – самопроизвольное (спонтанное) изменение состава нестабильных атомных ядер, сопровождающееся испусканием α-частиц, каждая из которых состоит из двух протонов и двух нейтронов (ядро атома гелия 42He). Примером такого распада может служить превращение радия-226 в радон-222: 22688Ra → 22286Rn + 42α (где 42α – альфа-частица или ядро атома гелия).
Бета-распад (β-распад) происходит в результате того, что один из нейтронов нестабильного атомного ядра превращается в протон, при этом ядро испускает электрон и легкую частицу, называемую антинейтрино. Записать процесс можно следующим образом: 10n → 11p + -1e + ~ν. Примером такого радиоактивного распада может быть превращение тория-234 в протактиний-234: 23490Th → 23491Pa + -1e + ~ν.
Записать процесс можно следующим образом: 10n → 11p + -1e + ~ν. Примером такого радиоактивного распада может быть превращение тория-234 в протактиний-234: 23490Th → 23491Pa + -1e + ~ν.
Гамма-распад (γ-распад) представляет собой процесс испускания возбужденным ядром атома излучения с очень малой длиной волны – гамма-квантов. При этом изменение заряда ядра атома не происходит.
При всех этих распадах энергия ядра уменьшается. А что при этом происходит с зарядом ядра и массой? При α-распаде массовое число уменьшается на четыре единицы, а заряд ядра элемента – на две. При β-распаде атомный номер элемента увеличивается на единицу, а массовое число не изменяется. При γ-излучении, которое часто (но не всегда) сопутствует α- и β-распаду, ни атомный номер, ни массовое число не изменяются.
В ходе радиоактивного распада число имеющихся исходных атомов постепенно убывает. Изучая процессы радиоактивного распада во времени, Э. Резерфорд обнаружил, что через определенный промежуток времени – различающийся для разных элементов, количество того или иного радиоактивного элемента уменьшается в два раза. Этот промежуток времени, в течение которого распадается половина исходного числа радиоактивных атомов, был назван периодом полураспада Т1/2. Период полураспада характеризует скорость радиоактивного процесса и различается для разных радиоактивных изотопов. Если изотоп распадается быстро, то он называется короткоживущим. Значения Т1/2 для таких изотопов могут составлять 10-12 – 10-10 с и даже меньше. Примером может служить сверхлегкий изотоп кислорода-12, период полураспада которого составляет 10–21 с, или изотоп свинца-210 с периодом полураспада 1,5·10–4 с. Период полураспада долгоживущих, медленно распадающихся атомов, может достигать миллиардов лет. Так, например, для урана-238 период полураспада составляет 4,47·109 лет, для тория-232 – 1,405·1010 лет.
Изучая процессы радиоактивного распада во времени, Э. Резерфорд обнаружил, что через определенный промежуток времени – различающийся для разных элементов, количество того или иного радиоактивного элемента уменьшается в два раза. Этот промежуток времени, в течение которого распадается половина исходного числа радиоактивных атомов, был назван периодом полураспада Т1/2. Период полураспада характеризует скорость радиоактивного процесса и различается для разных радиоактивных изотопов. Если изотоп распадается быстро, то он называется короткоживущим. Значения Т1/2 для таких изотопов могут составлять 10-12 – 10-10 с и даже меньше. Примером может служить сверхлегкий изотоп кислорода-12, период полураспада которого составляет 10–21 с, или изотоп свинца-210 с периодом полураспада 1,5·10–4 с. Период полураспада долгоживущих, медленно распадающихся атомов, может достигать миллиардов лет. Так, например, для урана-238 период полураспада составляет 4,47·109 лет, для тория-232 – 1,405·1010 лет. Следует отметить, что скорость распада не зависит от внешних условий. Радиоактивный распад является статистическим процессом, поэтому нельзя определить, какой именно атом распадется в данный момент времени. Т.е ядро данного радиоактивного изотопа, родившееся только что, и ядро этого же изотопа, просуществовавшее миллионы лет имеют одинаковую вероятность распасться. Можно определить только среднее время жизни радиоактивного атома, если имеется большое число таких атомов. Изменение числа атомов в процессе радиоактивного распада описывается законом радиоактивного распада: N = N0 2–t/T1/2, где N0 – число радиоактивных атомов в начальный момент времени t=0, N – число нераспавшихся атомов к моменту времени t, Т1/2 – период полураспада.
Следует отметить, что скорость распада не зависит от внешних условий. Радиоактивный распад является статистическим процессом, поэтому нельзя определить, какой именно атом распадется в данный момент времени. Т.е ядро данного радиоактивного изотопа, родившееся только что, и ядро этого же изотопа, просуществовавшее миллионы лет имеют одинаковую вероятность распасться. Можно определить только среднее время жизни радиоактивного атома, если имеется большое число таких атомов. Изменение числа атомов в процессе радиоактивного распада описывается законом радиоактивного распада: N = N0 2–t/T1/2, где N0 – число радиоактивных атомов в начальный момент времени t=0, N – число нераспавшихся атомов к моменту времени t, Т1/2 – период полураспада.
В 1919 г. изучая воздействие альфа-излучения на различные газы, Э. Резерфорд обнаружил, что в результате бомбардировки альфа-частицами атомов азота получаются атомы кислорода. Этот процесс можно описать следующим образом: 147N + 42α → 178O + 11p (где 11p – протон или ядро атома водорода 11H). Таким образом, Резерфордом было осуществлено первое искусственное превращение элементов – ядерная реакция. Напомним, что ядерной реакцией называются превращение атомных ядер при взаимодействии их с элементарными частицами, гамма-квантами или друг с другом. От химической ядерная реакция отличается тем, что в ходе её изменяются ядра атомов, т.е. атомы одних элементов, превращаются в атомы других химических элементов. И ядерная реакция, и радиоактивный распад являются превращением одного атомного ядра (химического элемента) в другое ядро. Но если радиоактивный процесс происходит самопроизвольно и не зависит от внешнего воздействия, то ядерная реакция, наоборот, вызывается воздействием на атомное ядро других частиц (ядер, протонов, нейтронов, гамма-квантов).
Этот процесс можно описать следующим образом: 147N + 42α → 178O + 11p (где 11p – протон или ядро атома водорода 11H). Таким образом, Резерфордом было осуществлено первое искусственное превращение элементов – ядерная реакция. Напомним, что ядерной реакцией называются превращение атомных ядер при взаимодействии их с элементарными частицами, гамма-квантами или друг с другом. От химической ядерная реакция отличается тем, что в ходе её изменяются ядра атомов, т.е. атомы одних элементов, превращаются в атомы других химических элементов. И ядерная реакция, и радиоактивный распад являются превращением одного атомного ядра (химического элемента) в другое ядро. Но если радиоактивный процесс происходит самопроизвольно и не зависит от внешнего воздействия, то ядерная реакция, наоборот, вызывается воздействием на атомное ядро других частиц (ядер, протонов, нейтронов, гамма-квантов).
Бомбардировкой альфа-частицами ядер различных атомов удалось осуществить множество ядерных превращений. В 1932 г. при бомбардировке альфа-частицами атомов бериллия английским физиком Джеймсом Чедвиком (1891 – 1974) был открыт нейтрон. Происходящий ядерный процесс можно изобразить следующим образом: 94Ве + 42α → 126С + 10n (где 10n – нейтрон). В 1934 г. французскими физикам Ирен Жолио-Кюри (1897 – 1956) и Фредериком Жолио-Кюри (1900 – 1958) была открыта искусственная радиоактивность – самопроизвольный распад нестабильных атомных ядер, полученных в ходе ядерных реакций. При облучении альфа-частицами алюминия им удалось получить не существующий в природе радиоактивный изотоп фософра-30. Уравнение, протекающей ядерной реакции можно представить следующим образом: 2713Al + 42α → 3015P + 10n. Период полураспада изотопа фосфора-30 составляет около 2,5 минут, при этом в ядре этого изотопа один из протонов превращается в нейтрон с испусканием позитрона (античастица электрона +1e) и нейтрино: 11p → 10n + +1e + ν. Процесс, происходящий с ядрами изотопа фосфора-30 можно записать следующим образом: 3015Р → 3014Si + +1e + ν.
Период полураспада изотопа фосфора-30 составляет около 2,5 минут, при этом в ядре этого изотопа один из протонов превращается в нейтрон с испусканием позитрона (античастица электрона +1e) и нейтрино: 11p → 10n + +1e + ν. Процесс, происходящий с ядрами изотопа фосфора-30 можно записать следующим образом: 3015Р → 3014Si + +1e + ν.
Дальнейшие исследования показали, что с помощью ядерных реакций можно не только одни химические элементы превращать в другие, но и синтезировать новые элементы. Так в 1937 г. при облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые искусственно получен, а не выделен из природных соединений, химический элемент технеций Тс, получивший свое название от греческого слова «techne» – искусство, ремесло. В 1940 г. предсказанный Д.И. Менделеевым «экаиод» – химический элемент астат At, был получен искусственным путем в ходе ядерной реакции 20983Bi + 42α → 21185At + 2 10n.
Положительно заряженные частицы (протон, альфа-частица и др.), используемые в ядерных реакциях, испытывают сильное отталкивание при приближении к ядрам атомов, с которыми они должны взаимодействовать. Чтобы преодолеть это отталкивание альфа-частицы, протоны и т.д. должны обладать достаточно большой энергией, для этого их разгоняют с помощью специальных устройств – ускорителей. Первый ускоритель (циклотрон) был создан в 1931 году американским физиком Эрнестом Орландо Лоуренсом (1901 – 1958). С помощью циклотрона стало возможным проводить разнообразные ядерные реакции. Так, в 1932 г. Джоном Кокрофтом и Эрнестом Уолтоном была проведена первая ядерная реакция на быстрых протонах. Бомбардируя протонами литий, учёным удалось расщепить его на две альфа-частицы: 73Li + 11H → 42He + 42He.
Наибольший интерес представляют реакции, проводимые с использованием нейтронов. Лишенные заряда нейтроны не испытывают отталкивания атомных ядер и легко в них проникают. Потоки нейтронов получают в результате ядерных реакций в ускорителях и в ядерных реакторах. Приведем несколько примеров ядерных реакций, вызываемых нейтронами: 2311Na + 10n → 2411Na + γ,
Потоки нейтронов получают в результате ядерных реакций в ускорителях и в ядерных реакторах. Приведем несколько примеров ядерных реакций, вызываемых нейтронами: 2311Na + 10n → 2411Na + γ,
5927Co + 10n → 6027Co + γ. Подобные реакции применяются для получения новых изотопов: 3517Cl + 10n → 3516S + 11p или 2713Al + 10n → 2411Na + 42He.
Большой практический интерес представляют реакции, вызываемые бомбардировкой нейтронами ядер урана-235 23592U. После поглощения нейтрона 23592U + 10n → 23692U ядро урана испытывает вынужденное деление, что приводит к образованию двух новых ядер и одновременно освобождается 2 или 3 нейтрона 10n. В результате такой реакции образуется смесь изотопов с массовыми числами равными приблизительно половине массового числа делящегося урана (смесь изотопов 9236Kr, 14156Ba и др.). Например: 23592U + 10n→ 23692U*→14456Ва + 8936Kr + 3 10n. При делении каждого ядра урана выделяется энергии порядка 200 МэВ. Процесс, при котором из одного атомного ядра возникает два близких по массе ядра, называют делением ядер.
В результате такой реакции образуется смесь изотопов с массовыми числами равными приблизительно половине массового числа делящегося урана (смесь изотопов 9236Kr, 14156Ba и др.). Например: 23592U + 10n→ 23692U*→14456Ва + 8936Kr + 3 10n. При делении каждого ядра урана выделяется энергии порядка 200 МэВ. Процесс, при котором из одного атомного ядра возникает два близких по массе ядра, называют делением ядер.
Ядерный реактор оказался настоящей фабрикой радиоактивных изотопов.
Ядра изотопа 23592U могут захватывать нейтроны с небольшой энергией около 5 – 10 эВ (500 – 1000 кДж) – так называемые тепловые нейтроны, а нейтроны, образующиеся при делении ядра 23692U, обладают в миллионы раз большей энергией. Поэтому, чтобы реакция шла дальше за счет вылетающих при делении ядра нейтронов, их необходимо замедлить. Тогда пойдет цепная реакция деления урана – выделившиеся нейтроны, после замедления, будут захватываться другими ядрами 23592U и т. д. Ядерные реакции, в которых частицы, вызывающие их, образуются и как продукты этих реакций называются цепными ядерными реакциями. Осуществление таких реакций сопровождается выделением энергии и имеет большое практическое значение.
Тогда пойдет цепная реакция деления урана – выделившиеся нейтроны, после замедления, будут захватываться другими ядрами 23592U и т. д. Ядерные реакции, в которых частицы, вызывающие их, образуются и как продукты этих реакций называются цепными ядерными реакциями. Осуществление таких реакций сопровождается выделением энергии и имеет большое практическое значение.
Резюме теоретической части.
1. В природе существуют разновидности атомов одного и того же элемента – изотопы, отличающиеся массами из-за разного содержания в ядрах их атомов нейтронов. В природе существуют радиоактивные изотопы, способные самопроизвольно изменять состав своих ядер. Все изотопы химических элементов, следующих за висмутом Bi в периодической системе химических элементов, являются радиоактивными. Многие химические элементы были получены искусственным путем в ходе ядерных реакций.
2. Превращение атомов одних химических элементов в другие возможно входе процессов радиоактивного распада и ядерных реакций. Изучением этих процессов занимается ядерная физика, зарождение которой началось на рубеже XIX – XX веков.
Изучением этих процессов занимается ядерная физика, зарождение которой началось на рубеже XIX – XX веков.
3. Процессы радиоактивного распада протекают самопроизвольно. В результате у ядер атомов изменятся состав и испускаются элементарные частицы, гамма-кванты или ядерные фрагменты. Наиболее распространенными являются α-распад, β-распад и γ-распад. Скорость радиоактивного процесса не зависит от внешних условий и характеризуется периодом полураспада, который сильно различается для радиоактивных изотопов разных химических элементов. Радиоактивный распад является статистическим процессом, который количественно описывается законом радиоактивного распада.
4. Ядерные реакции, в отличие от процессов радиоактивного распада, протекают под внешним воздействием – атомные ядра бомбардируют другими ядрами, элементарными частицами или гамма-квантами. Бомбардирующие частицы чаще всего разгоняют с помощью специальных устройств – ускорителей. Наибольший интерес представляют ядерные реакции, проводимые с использованием нейтронов, потоки которых получают в результате ядерных реакций в ускорителях и в ядерных реакторах.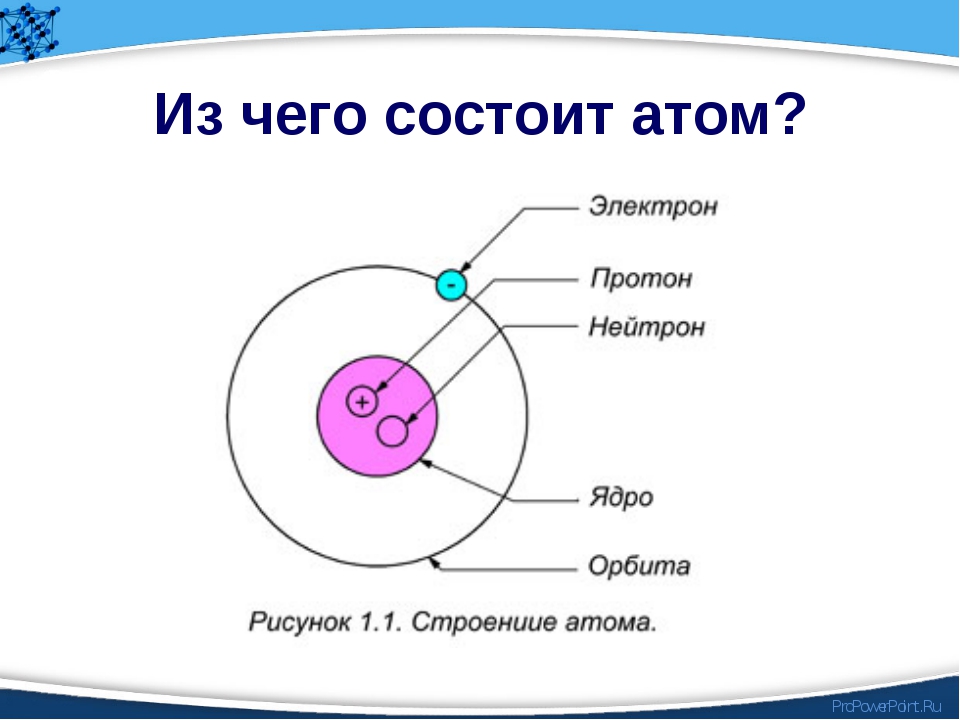 Открытие деления ядер урана привело к осуществлению цепных ядерных реакций, которые имеют большое практическое значение.
Открытие деления ядер урана привело к осуществлению цепных ядерных реакций, которые имеют большое практическое значение.
5. Качественные изменения, происходящие с атомными ядрами в ходе процессов радиоактивного распада и ядерных реакций, можно рассматривать как одну из форм движения материи.
Примеры и разбор решения заданий тренировочного модуля:
1. Укажите верные утверждения:
Утверждение | Правильный ответ и пояснение |
А. Ядерные реакции приводят к превращению атомов одних химических элементов в другие. | Правильное утверждение. Химический элемент – это вид атомов с одинаковым зарядом ядра. В ходе ядерных реакций происходят изменения ядер атомов, в большинстве случаев меняется число протонов в ядре. Следовательно, в этих случаях происходит превращение атомов одних химических элементов в другие. |
Б. Радиоактивность атома химического элемента зависит от того, в каком химическом соединении он находится. | Неправильное утверждение. Радиоактивность – это свойство атомного ядра химического элемента, поэтому это свойство никак не зависит от того, в каком химическом соединении атом данного элемента находится. |
В. В ходе альфа-распада образуется атомное ядро с зарядом на две единицы и массой на четыре единицы меньше, чем у исходного атомного ядра. | Правильное утверждение. Альфа-распад сопровождается испусканием атомным ядром альфа-частиц – ядер атома гелия 42He, состоящих из двух протонов и двух нейтронов. Испустив альфа-частицу и потеряв два протона и два нейтрона, образовавшееся атомное ядро будет иметь массу на четыре единицы, а заряд на две единицы меньше, чем исходное ядро. |
2. Установление соответствие между элементами двух множеств. К каждой позиции первого столбца подберите соответствующую позицию второго.
Описание процесса | Вид явления |
1. | А. Явление радиоактивности Б. Ядерная реакция |
2. В результате испускания ядром изотопа радия-226 альфа-частицы образуется изотоп радона-222. | |
3. При захвате ядром алюминия-27 нейтрона образуется ядро натрия-24 и альфа-частица. |
Правильный ответ:1 – Б; 2 – А; 3 – Б.
Описание процесса | Вид явления |
1. При облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые был искусственно получен химический элемент технеций Тс. | Б. Ядерная реакция |
2. В результате испускания ядром изотопа радия-226 альфа-частицы образуется изотоп радона-222. | А. Явление радиоактивности |
3. | Б. Ядерная реакция |
Строение и химия Земли – аналитический портал ПОЛИТ.РУ
Облик нашей планеты и ее эволюция обусловлены процессами, которые происходят в ее глубинах. Каков химический состав мантии и ядра Земли? Каковы температуры и давления там? Из каких химических веществ они состоят, и каковы их свойства? Есть ли связь между химией высоких давлений и появлением жизни на Земле (а также периодическими глобальными вымираниями)? Что нового мы узнали о своей планете благодаря изучению ее вещества при высоких температурах и давлениях? Об этом и пойдет речь в лекции Артёма Оганова, химика, кристаллографа-теоретика, профессора РАН, члена Европейской Академии, профессора Сколтеха.
Сегодня я расскажу вам об одном из основных своих направлений работы. У меня несколько направлений, одно — это дизайн материалов, а другое — изучение вещества в недрах планеты. Тема на самом деле общая — мы изучаем вещество, его строение, и то, как это строение обуславливает свойства и поведение вещества. Найдя ключ к пониманию строения вещества, научившись предсказывать строение вещества, мы можем изучать вещество на самых разных просторах — от приборов и технологий до недр планет.
Тема на самом деле общая — мы изучаем вещество, его строение, и то, как это строение обуславливает свойства и поведение вещества. Найдя ключ к пониманию строения вещества, научившись предсказывать строение вещества, мы можем изучать вещество на самых разных просторах — от приборов и технологий до недр планет.
Поговорим немного о планетах — какие они бывают, какое место среди них занимает наша Земля. В Солнечной системе планеты бывают каменные (их также называют планетами земного типа) — это Меркурий, Венера, Земля, Марс, и газовые гиганты — Юпитер, Сатурн, Уран, Нептун. Уже известно несколько тысяч планет за пределами Солнечной системы, их называют экзопланетами. Кстати, среди каменных экзопланет известны планеты намного более крупные, чем Земля — вплоть до 20 земных масс, их называют суперземлями.
Мы знаем температуру и давление внутри Земли — например, давление в центре Земли 3,64 млн атмосфер, а температура примерно 6 тыс градусов Кельвина. Менее точно мы знаем давление и температуру в недрах других планет.
Артем Оганов / Фото: Алексей Никодимов
Юпитер и Сатурн состоят в основном из смеси водорода и гелия, и характеризуются — в особенности Сатурн — большим избыточным тепловым потоком. То есть Сатурн излучает больше тепла, чем получает от Солнца. И этому есть объяснение: при высоких давлениях, которые создаются в недрах этой гигантской планеты, водород становится металлическим, а гелий — нет. И эта смесь разделяется на две компоненты: более легкий металлический водород и более тяжелый неметаллический гелий. И вот более тяжелый гелий образует капельки, которые падают в гравитационном поле Сатурна. И гравитационная энергия переходит в тепловую посредством трения этих капелек об жидкие «внутренности» Сатурна. За счет этого «гелиевого дождя» и производится тепло в недрах этой планеты. В Юпитере это тоже происходит, но в меньшем масштабе, поскольку недра Юпитера более горячие и гелий с водородом лучше смешиваются.
Уран и Нептун — другие. Они состоят из смеси воды, метана и аммиака. Из этих двух планет Нептун тоже характеризуется большим избытком теплового потока. Предполагают, что в недрах Нептуна образуются алмазы. Нептун и Уран — это тоже жидкие планеты, газово-жидкие. В недрах Нептуна, как считают, образуется алмаз — он плотный, твердый, эти кристаллики падают в недрах Нептуна в огромных количествах, и за счет этого генерируется тепло. За счет падения огромного количества алмазов. Пока еще эта гипотеза вызывает вопросы, но это пока что лучшее, что у нас есть.
Из этих двух планет Нептун тоже характеризуется большим избытком теплового потока. Предполагают, что в недрах Нептуна образуются алмазы. Нептун и Уран — это тоже жидкие планеты, газово-жидкие. В недрах Нептуна, как считают, образуется алмаз — он плотный, твердый, эти кристаллики падают в недрах Нептуна в огромных количествах, и за счет этого генерируется тепло. За счет падения огромного количества алмазов. Пока еще эта гипотеза вызывает вопросы, но это пока что лучшее, что у нас есть.
Вот такие удивительные миры скрываются за пределами нашей планеты. Посмотрим на шкалу давлений, которая существует внутри планет Солнечной системы, в гигапаскалях, ГПа. 1 ГПа — это десять тысяч атмосфер, а давления в центре планет порядка сотен гигапаскалей. Чтобы создать давление в 100 ГПа, то есть 1 миллион атмосфер, вам нужно поймать 200 слонов, и их совокупный вес приложить к площади в один квадратный сантиметр. Давление в центре Земли — почти 4 млн атмосфер. Давление в центре Венеры примерно такое же. Давление в центре Марса чуть ниже, в центре Юпитера или Сатурна значительно выше. При такого рода давлениях можно ожидать фундаментального изменения в химических связях между атомами. Мы ожидаем, что атомы будут вести себя совсем не так, как при нормальных условиях. Например, кислород под давлением является сверхпроводником. При нормальных условиях кислород не является металлом, а при давлении в миллион атмосфер он становится сверхпроводящим металлом. Ну, и много других подобных «сюрпризов».
Давление в центре Марса чуть ниже, в центре Юпитера или Сатурна значительно выше. При такого рода давлениях можно ожидать фундаментального изменения в химических связях между атомами. Мы ожидаем, что атомы будут вести себя совсем не так, как при нормальных условиях. Например, кислород под давлением является сверхпроводником. При нормальных условиях кислород не является металлом, а при давлении в миллион атмосфер он становится сверхпроводящим металлом. Ну, и много других подобных «сюрпризов».
Если мы посмотрим на уникальные данные, которые собрали советские физики в 1960-е годы, мы увидим, что при очень высоких давлениях нарушается даже периодический закон Менделеева. Посмотрим на изменение атомного объема с порядковым номером. Вы видите пилообразную периодическую зависимость — классическое подтверждение закона Менделеева. При давлении в 3 млн атмосфер мы все еще наблюдаем эту «пилу», но она значительно «приглушена»; при давлении в 10 млн атмосфер «пилы» уже нет, фактически можно говорить, что и периодического закона тут нет. Но есть какая-то «шероховатость» в зависимости атомного объёма от атомного номера. А при давлении в 30 млн атмосфер даже «шероховатости» нет, есть плавное изменение физических и химических изменений свойств элементов с порядковым номером. Химия в таких условиях сверхвысоких давлений оказывается не действенной. Вместо электронов на атомных s-, p-, d-, f- орбиталях, мы имеем электроны, размазанные в «картофельное пюре» — электронный газ. И привычная химия с периодическим законом уступает физике электронного газа.
Но есть какая-то «шероховатость» в зависимости атомного объёма от атомного номера. А при давлении в 30 млн атмосфер даже «шероховатости» нет, есть плавное изменение физических и химических изменений свойств элементов с порядковым номером. Химия в таких условиях сверхвысоких давлений оказывается не действенной. Вместо электронов на атомных s-, p-, d-, f- орбиталях, мы имеем электроны, размазанные в «картофельное пюре» — электронный газ. И привычная химия с периодическим законом уступает физике электронного газа.
Артем Оганов / Фото: Алексей Никодимов
В этой лекции мы говорим про давления на один-два порядка меньше, чем те, при которых это происходит. При такого рода давлениях химия по-прежнему существует, но значительно меняется. Например, мы нашли — теоретически и экспериментально — новую стабильную структуру бора, где один тип атомов бора отдает электроны, а другие атомы бора притягивают электроны на себя. В результате часть атомов заряжена положительно, часть — отрицательно, но это атомы одного и того же элемента, просто они играют разную роль в кристаллической структуре. А вот еще более удивительное предсказание, тоже подтвержденное экспериментом: что при высоких давлениях натрий перестает быть металлом. Мы привыкли называть натрий и другие элементы I группы щелочными металлами, но под давлением натрий уже не металл, а прозрачный диэлектрик. И здесь вы видите экспериментальный образец натрия в просвечивающем свете, и видно, что он, действительно, прозрачен и имеет оранжевый цвет. Это совершенно удивительные предсказания и их экспериментальные подтверждения.
А вот еще более удивительное предсказание, тоже подтвержденное экспериментом: что при высоких давлениях натрий перестает быть металлом. Мы привыкли называть натрий и другие элементы I группы щелочными металлами, но под давлением натрий уже не металл, а прозрачный диэлектрик. И здесь вы видите экспериментальный образец натрия в просвечивающем свете, и видно, что он, действительно, прозрачен и имеет оранжевый цвет. Это совершенно удивительные предсказания и их экспериментальные подтверждения.
Итак, химия под давлением меняется очень сильно. Мы говорим про давления, присущие недрам Земли. Из чего она состоит, как устроена? Мы знаем это из разных источников. Конечно, мы можем изучать горные породы и минералы с поверхности Земли, даже пробурить внутрь Земли, но это нас заведет не очень далеко. Самая глубокая скважина — Кольская сверхглубокая — имеет глубину чуть больше 12 километров (а радиус Земли почти 6400 км), и пробурить даже на 12 км было очень трудно. Таким образом, мы должны исходить из каких-то косвенных данных. Самый важный метод косвенного изучения недр Земли — сейсмология, когда мы изучаем прохождение упругих волн через недра нашей планеты. Волны достаточной мощности генерируются в землетрясениях. Когда у вас есть сейсмическая волна, упругая или звуковая волна — это одно и то же — она распространяется по всем направлениям, следуя, как ни странно, законам геометрической оптики: отражаясь или преломляясь от границ сред с разными скоростями распространения волн. И вот, применяя законы геометрической оптики для распространения в данном случае сейсмических волн, и решая обратную задачу, мы много смогли узнать о недрах Земли. Где находится сейсмическая граница между, скажем, ядром и мантией, или между внутренним ядром и внешним ядром, и так далее. Все эти границы удалось достаточно точно локализовать и описать. Как меняются свойства вещества при пересечении каждой из этих границ? Например, как меняется плотность? Удалось построить сейсмическую модель Земли. Надо сказать, что эта история до сих продолжается, хотя самые великие геофизические открытия, наверное, уже были сделаны за последние 100 лет. Эта эпопея началась чуть больше 100 лет назад, но последние важные открытия были сделаны в начале 2000-х годов, то есть, люди до сих пор находят что-то новое.
Самый важный метод косвенного изучения недр Земли — сейсмология, когда мы изучаем прохождение упругих волн через недра нашей планеты. Волны достаточной мощности генерируются в землетрясениях. Когда у вас есть сейсмическая волна, упругая или звуковая волна — это одно и то же — она распространяется по всем направлениям, следуя, как ни странно, законам геометрической оптики: отражаясь или преломляясь от границ сред с разными скоростями распространения волн. И вот, применяя законы геометрической оптики для распространения в данном случае сейсмических волн, и решая обратную задачу, мы много смогли узнать о недрах Земли. Где находится сейсмическая граница между, скажем, ядром и мантией, или между внутренним ядром и внешним ядром, и так далее. Все эти границы удалось достаточно точно локализовать и описать. Как меняются свойства вещества при пересечении каждой из этих границ? Например, как меняется плотность? Удалось построить сейсмическую модель Земли. Надо сказать, что эта история до сих продолжается, хотя самые великие геофизические открытия, наверное, уже были сделаны за последние 100 лет. Эта эпопея началась чуть больше 100 лет назад, но последние важные открытия были сделаны в начале 2000-х годов, то есть, люди до сих пор находят что-то новое.
Мы узнали кое-что о составе Земли, хотя и не можем добурить до центра, но все же кое-что знаем. Модели состава Земли основаны на составе особого типа метеоритов, углистых хондритов CI, которые, как считается, представляют первичное вещество Вселенной. И считается, что этот состав соответствует составу вещества Земли и вещества Солнца (если брать нелетучие элементы). В Солнце, конечно, очень много летучих элементов — водород, гелий, но если вы уберете эти летучие элементы, то соотношение всех остальных элементов на Земле и на Солнце будет одинаково, потому что они произошли из одного и того же газово-пылевого облака.
Итак, у нас есть представление о среднем составе всей Вселенной. Если мы уберем водород и гелий, а также и другие летучие элементы, то получим то, что считаем составом Земли. И то же самое касается Солнца и метеоритов. Но состав Земли очень сильно дифференцирован. Средний состав — это если бы мы взяли всю Землю, перемешали бы ее на миксере, и провели химический анализ. На самом деле, земная кора, земное ядро, земная мантия имеют совершенно разные составы. Мы знаем, что земное ядро — это, грубо говоря, железо-никелевый сплав. Это сильно сжатое и горячее железо в сплаве с никелем. А мантия Земли — это, в основном, силикаты магния. А земная кора — это, в основном, продукты выплавления из мантии, обогащенные щелочными металлами и другими элементами — например, фосфором, литием, бором, ураном, а также обогащенные элементами жизни — углеродом, водородом, азотом.
Артем Оганов / Фото: Алексей Никодимов
Важную роль играет динамика мантии и ядра Земли. В мантии потоки горячего вещества идут вверх, холодные потоки мантийного вещества идут вниз. Этот процесс протекает на больших масштабах. Благодаря этому процессу , например, континенты дрейфуют друг относительно друга. Южная Америка и Африка раньше были одним континентом, но благодаря этим мантийным потокам они дрейфуют в противоположные стороны, их как бы «разрывает». Благодаря этой конвекции индийская плита «врезалась» в евразийскую.
Это очень важный процесс, который формирует нашу жизнь: землетрясения, вулканизм, дрейф континентов — все это происходит благодаря конвекции в мантии Земли. Сам по себе этот процесс очень интересен, потому что мантия Земли не является жидкостью или газом. Мы привыкли к конвекции в жидкости или газе, мы видим конвекцию в воздухе у костра или в чашке чая. В твердой мантии Земли конвекция тоже происходит, но с меньшей скоростью, примерно сантиметр в год. Казалось бы, пустяк, но если помножить эту скорость на геологические масштабы времени, на сотни миллионов лет, и станет понятно, что за это время вещество земной мантии может много раз пройти по кругу как через мясорубку.
Конвекция также присуща ядру Земли. Внешнее ядро Земли жидкое, расплавленное, а внутреннее — кристаллическое, твердое. И внешнее ядро Земли находится в состоянии довольно быстрой конвекции. Эта конвекция расплавленного электропроводящего вещества и генерирует наше магнитное поле. Оно связано не с тем, что ядро железное, а железо магнитное, нет. При давлениях и температурах ядра Земли железо уже немагнитное. Ядро создает магнитное поле не потому, что там магнитное железо, железо там размагнитилось, а благодаря тому, что там есть конвективное движение электропроводящей жидкости.Например, Юпитер обладает еще более сильным магнитным полем, чем Земля. Скорее всего, там нет или почти нет железного ядра, зато там есть вихревые потоки металлического водорода. Экспериментально магнитные поля планет изучают, помещая расплавленные металлы, такие, например, как натрий, в большие объемы, где происходит их помешивание. Помешивая расплавленный металл, вы можете сгенерировать магнитное поле примерно такого же типа, как у Земли. Магнитное поле Земли очень важно, потому то оно защищает нашу планету от потока заряженных частиц, в частности, от солнечного ветра. Если бы магнитного поля не было, то солнечный ветер — этот поток заряженных частиц — уничтожил бы жизнь. Собственно, он не дал бы ей даже зародиться. Поэтому мы знаем, что жизнь могла возникнуть только на планете, на которой есть магнитное поле.
Если говорить про минералы, то на поверхности Земли известно около 5000 минеральных видов, но доминирующими минералами являются полевые шпаты и кварц — больше 80% объема земной коры. Когда мы спускаемся ниже, считается, что минеральное разнообразие уменьшается. Минералы, которые мы предполагаем найти в недрах Земли, можно уже пересчитать по пальцам. В верхней мантии это оливин, пироксены, гранаты. В переходной зоне появляется новый минерал — вадслеит. Когда мы пересекаем границу 670 км и попадаем в нижнюю мантию Земли, то минералогия и химия претерпевают большие изменения, и тут доминируют перовскиты. Кстати, собственно перовскит это титанат кальция, встречающийся в маленьких количествах на поверхности Земли. В нижней мантии Земли возникают магниевый и кальциевый силикатные перовскиты. Магний-силикатный перовскит это минерал бриджманит, и это самый важный минерал на Земле, составляющий примерно 40% от объема всей Земли или же около 80% объёма нижней мантии. На поверхности Земли этот минерал был найден всего лишь несколько лет назад. И недавно открыли (с моим участием) минерал пост-перовскит, из самой нижней мантии Земли, он составляет примерно 80% объёма слоя D», у самой границы мантии с ядром.
Минералогические превращения обусловливает множество интересных вещей. В частности, некоторые глубинные землетрясения на Земле, вероятно, связаны с ними. Землетрясения малых глубин связаны просто с хрупкой деформацией — одна плита надвигается на другую, происходит хрупкая деформация. Глубинные землетрясения так не объяснить, потому что вещество становится гораздо более пластичным. Как считается, происходит фазовое превращение минералов. Например, минерал как серпентин, содержащий довольно много воды, на глубине обезвоживается, и это резкое обезвоживание и связанное с ним изменение объёма может объяснить некоторые из глубинных землетрясений.
Лекция на красной площади / Фото: Алексей Никодимов
Поговорим немного про ядро. Внешнее ядро — жидкое, расплавленное, а внутреннее — кристаллическое. И до сих пор ведутся жесточайшие дискуссии — какова же кристаллическая структура железа в условиях ядра Земли. Ядро это железо-никелевый сплав, но там также порядка 15% более легких элементов. Каких? Сера, кремний, углерод, кислород, водород. В какой пропорции — не знает никто. Множество моделей, но друг с другом они никак не сходятся. Перед вами полушуточный график, из которого видно, что на 1995-й год «лидировала» сера — большинство авторов предпочитало серу, на втором месте внезапно оказался кислород, который до того был достаточно непопулярен. Демократия в науке не работает, решается вопрос не большинством голосов, а логичностью выводов и их согласованностью с фактами.
До недавнего времени кристаллические структуры веществ можно было изучать только экспериментально. Предсказывать, какую структуру будет иметь ещё не полученное вещество, считалось невозможным. Эту задачу нам удалось решить, разработав эволюционный метод USPEX, где компьютер генерирует разные модели кристаллических структур, отбраковывает наименее стабильные из них, а на основе более стабильных конструирует новые модели кристаллических структур, пока не находит наилучшую. Это оказался эффективный метод, который даже при небольших ресурсах позволяет решать сложные задачи. Используют его уже тысячи ученых, как для предсказания новых материалов, так и для изучения вещества в экстремальных условиях.
Вот силикат магния при давлении 120 ГПа, то есть, 1,2 млн атмосфер. Мы начинаем со случайных структур, взятых «из ниоткуда», и наш эволюционный алгоритм генерирует новые модели структуры до тех пор, пока не находит наилучшую. В результате получается структура, в точности соответствующая стабильной структуре силиката магния. Что нам это дает? Ни много ни мало, как объяснение геофизических аномалий, которые были известны начиная с 1930-х годов. Много десятилетий были известны эти аномалии, но никто не мог их объяснить. Эта новая модификация силиката магния, которую мы назвали пост-перовскитом, доминирует в составе слоя D», на схеме строения Земли вы видите, что этот слой имеет крайне нерегулярные контуры. В каких-то местах он отсутствует, в каких-то достигает примерно 300 км в толщину. Все остальные оболочки Земли имеют более-менее ровные контуры, а этот слой — нет. И вещество этого слоя анизотропно, то есть сейсмические волны распространяются в разных направлениях с разной скоростью. Это необычно.
Лекция на Красной площади / Фото: Виктор Чернышов
А объясняется это тем, что образуется новая структура, вот этот самый пост-перовскит, который я только что вам показал. И эта структура слоистая и, разумеется, в любой слоистой структуре свойства будут различаться в разных направлениях. И если эти кристаллы ориентировать неким образом, то свойства будут зависеть от направления. Удалось выяснить еще много чего. С помощью предсказанного поля стабильности этой фазы удалось объяснить, почему этот загадочный слой имеет такую сильно меняющуюся толщину. Дело в том, что область стабильности этой фазы зависит от температуры. Если температура высокая, то пост-перовскит устойчив в очень маленьком диапазоне давлений, а там, где температура низкая, он устойчив в большем диапазоне давлений. Это объяснило, почему в каких-то местах этот слой отсутствует, а в каких-то местах он очень толстый. Мы видим, что с ростом температуры стабильность пост-перовскита падает. Когда Земля еще только-только образовалась и была очень горячей, температуры были такими высокими, что этого слоя не было. Этот слой родился в процессе охлаждения Земли, и даже до сих пор этот слой растет. Мы знаем еще одну оболочку Земли, которая растёт в процессе охлаждения Земли — твердое внутреннее ядро, по мере охлаждения Земли оно медленно выкристаллизовывается из жидкого ядра. Из условий, необходимых для стабильности пост-перовскита, можно заключить, что нет никакого пост-перовскита на таких планетах, как Марс или Меркурий. Он может быть на Венере, которая таких же размеров, как Земля, он есть на Земле. Он будет на более крупных планетах, но не на более мелких.
Кстати говоря, свойства этого самого пост-перовскита позволили объяснить еще одну загадку: периодическое изменение продолжительности суток. С периодом около 10 лет она меняется на несколько миллисекунд. И это связано с тем, что пост-перовскитовый слой D» имеет высокую электропроводность, и его взаимодействие с магнитным полем Земли оказывает влияние на скорость вращения Земли вокруг своей оси. Это было показано геофизиками достаточно давно, но не было известно, откуда берется эта электропроводность. Сейчас мы знаем, что за неё отвечает пост-перовскит.
Кстати, фазовый переход из перовскита в пост-перовскит должен ускорять конвекцию Земли. Есть фазовые переходы, которые являются барьерами для этой конвективной динамики, а есть переходы, которые ее подстегивают — и пост-перовскитовый переход относится именно к этому типу. Это означает, что в тот момент, когда пост-перовскит возник — не с момента образования Земли, а через сколько-то сотен миллионов лет, и точнее пока что сказать нельзя, ведь мы пока еще не очень хорошо понимаем, как менялись температуры в ходе эволюции Земли — динамика Земли изменилась. Конвективное движение должно было ускориться. Возможно, в тот момент возникла тектоника плит. Что это означает для нас? Эта самая конвекция и является механизмом, который приносит летучие элементы к поверхности Земли — углерод, водород, кислород, азот, и многие другие. Без этого не возникла бы жизнь. Это красивая идея, которую высказали японские учёные. Если так, то именно благодаря пост-перовскиту жизнь и возникла, потому что с его появлением был ускорен механизм экстракции летучих элементов из глубин на поверхность Земли. Что мне нравится в нашей науке и в науке вообще — удивительные связи между, казалось бы, несвязанными вещами. Казалось бы, где жизнь и мы с вами, и где пост-перовскит. Но без него, возможно, и нас бы не было.
Как я уже сказал, поведение элементов меняется, они ведут себя под давлением совсем не так, как обычно. Мы научились с помощью нашего метода предсказывать стабильные химические составы — и оказывается, что под давлением возникают соединения, о которых мы даже и не подумали бы, что они возможны. Например, сплавы железа с разными элементами — кремнием, серой, углеродом, водородом, кислородом. Изучая эти системы и сравнивая результаты моделирования с измеренными свойствами внутреннего кристаллического ядра Земли, можно сделать первую гипотезу о том, каков может быть состав. Можно правдоподобно описать внутреннее ядро, используя только углерод. Можно, используя только кислород. Есть еще также модели, в которых содержится кремний и водород, или сера и водород. Нам удалось еще сузить пространство поиска. Вот здесь показана одна из лучших моделей — 88% железо-никелевого сплава, 5% серы, 5% водорода и 2% кислорода. Это одна из лучших моделей на сегодняшний день, но мы продолжаем и дальше ограничивать пространство возможных составов. Может быть, в скором времени у нас будет возможность представить на ваш суд окончательную модель состава ядра.
Лекция на Красной площади / Фото: Виктор Чернышов
В системах Fe-H и Fe-C возникает множество необычных соединений. Но самая яркая иллюстрация к таким необычным соединениям — это система Na-Cl. Мы привыкли, что хлорид натрия — это соль, NaCl. Другого состава классическая химия нам не разрешает. Под давлением образуются новые соединения. Вот результаты предсказаний, полученных с помощью нашего метода: под давлением возникают Na2Cl, Na3Cl, Na4Cl3, NaCl3, NaCl7, большинство из которых являются — подумайте! — металлами, то есть соединениями, проводящими электроны. Можно сказать, что это металлический сплав. И это не та химия, к которой мы привыкли. Удивительно. Эти соединения были получены экспериментально.
Такого рода необычные соединения возникают практически во всех химических системах при достаточно высоких давлениях. Любая система, если ее хорошенечко сдавить, тоже даст такие странные соединения.
Система Si-O — тут возникают SiO и SiO3. При нормальных условиях стабиле только SiO2, а под давлением SiO3 и SiO тоже будут стабильны. Смотрим на систему Mg-O: при нормальных условиях только MgO стабилен, а при высоких давлениях также стабильны МgO2, MgO3, Mg3O2.
Очень любопытное предсказание, и вновь подтверждённое экспериментом — это соединение FeO2, это предсказание было сделано китайскими учёными с помощью моей программы. Этот FeO2 возникает в условиях мантии Земли и может служить своего рода аккумулятором кислорода. Идея про кислородный аккумулятор в ее изначальном виде уже опровергнута, но она настолько красива, что, может быть, в каком-то виде и воскреснет. В чем идея? Под давлением становится стабильным соединение FeO2, это экспериментально доказано, это факт. Входящий в состав осадочных пород гидроксид железа (фактически, ржавчина) опускается в ходе субдукции плит, и на глубине преобразуется в FeO2 с выделением водорода. Но вещество мантии Земли находится в состоянии круговорота и пласты, содержащие FeO2, в какой-то момент снова всплывут к поверхности, где давления недостаточны для существования FeO2, и это вещество распадётся с образованием FeO или Fe2O3 и выделением кислорода. То есть, возникает процесс, при котором в глубоких недрах Земли запасается кислород в виде FeO2, и когда это вещество оказывается на меньших глубинах, этот кислород выбрасывается в атмосферу.
Это было использовано для объяснения удивительного явления в истории, серии так называемых «кислородных катастроф», самая важная из которых случилась чуть больше 2 миллиардов лет назад. Здесь есть график, который показывает содержание кислорода в нашей атмосфере. Когда Земля была молодая, никакого кислорода в атмосфере не было (зато было много метана). Кислород появился в больших количествах 2,2 млрд лет назад и с тех пор его содержание росло почти монотонно. Откуда он взялся и почему его содержание росло, вообще говоря, неизвестно. Главенствует гипотеза, что это сине-зеленые водоросли сгенерировали кислород в качестве продукта своей жизнедеятельности, в качестве продукта фотосинтеза. Другое объяснение — FeO2, который выходит с глубин Земли и выделяет этот кислород. Это привело к массовому вымиранию, потому что первичная жизнь была бескислородная; более того, кислород для той первичной жизни был ядом. И жизни на Земле пришлось довольно долго приспосабливаться к кислородной атмосфере. Видно, что в истории Земли был всплеск содержания кислорода в атмосфере, соответствующий грубо жизни динозавров. И это не случайно — такие огромные животные требовали большого количества кислорода для выработки достаточного количества энергии. А потом содержание кислорода пошло на спад. Циклические глобальные вымирания, приходы и уходы живых видов, возможно, связаны с содержанием кислорода в атмосфере.
Вот ещё один совершенно новый поворот: мы предсказали и экспериментально доказали, что под давлением гелий образует соединения Na2He, очень устойчивое и полученное экспериментально. Мы также предсказали, что гелий вступит в реакцию с оксидом натрия Na2O, и образует соединение Na2HeO. После нашей работы вышел ряд работ, в которых было показано, что гелий реагирует с такими соединениями, как H2O, SiO2, MgF2, CaF2, FeO2. Напомню, что геохимики до недавних пор считали, что гелий химически абсолютно инертен и не может удерживаться в недрах Земли — очевидно, что эти представления ошибочны, и гелий под давлением способен образовывать множество устойчивых соединений. Напомню, что гелий — распространённости элемент во Вселенной.
Я надеюсь, что то, что я вам рассказал сегодня, доказало то, что наука едина: химия, физика, геология, астрономия — границы между ними достаточно сильно размыты. Изучая строение и свойства вещества, в частности, при высоких давлениях, мы можем понять очень много и про нашу планету, и про другие миры.
строительные блоки молекул / Хабр
Если молекулы –
основные структуры, задействованные в химии – это слова, из которых состоят все окружающие нас материалы, тогда атомы – это буквы, строительные блоки молекул. Слова бывают разной длины, и типичная молекула тоже может содержать несколько атомов, или несколько сотен, или даже сто тысяч атомов. Молекула столовой соли NaCl состоит из двух атомов, натрия Na и хлора Cl. Молекула воды H
2O содержит два атома водорода и один кислорода. Молекула столового сахара C
12H
22O
11содержит 12 атомов углерода, 11 кислорода и 22 водорода, организованных определённым образом.
Откуда нам известно о существовании атомов? Иногда их можно «видеть», так же, как мы видим молекулы, которые они могут формировать. Не глазами, но более продвинутыми устройствами. Один из методов использует сканирующий туннельный микроскоп, способный показывать атомы в кристалле или даже передвигать их по одному. Другой метод использует нашу возможность захвата ионов (немного изменённых атомов – подробности ниже).
На фото – три иона, пойманных одновременно. На них падает свет, они поглощают его и снова испускают. Повторно испущенный свет можно обнаружить, благодаря чему мы можем увидеть, где находятся ионы – примерно так отражение света от небольшого, но яркого бриллианта может помочь нам найти его.
Сколько же типов атомов существует? Типы называются «химическими элементами» и точное их количество зависит от того, как их считать. Но допустим, что атомный алфавит состоит из примерно сотни химических элементов, а к тонкостям подсчёта вернёмся позже. Так же, как мы могли назначить буквам алфавита от А до Я номера от 1 до 33, каждому элементу назначается не только имя, но и атомный номер (обозначается «Z»). Самые простые атомы – у водорода, их атомный номер = 1. Самые сложные в изобилии встречаются в природе, это уран с атомным номером 92. Другие – кислород (8), азот (7), кальций (20), криптон (36), лантан (57), платина (78). Полный список ищите в периодической системе элементов Менделеева. У каждого элемента своя химия – то, как он ведёт себя внутри молекул – примерно так, как у каждой буквы есть свои правила, по которым она может встречаться в словах.
Вопросы, которые можно задать об атомах:
1. Из чего состоят атомы?
2. В чём смысл атомного номера?
3. Каков главный источник различий в химическом поведении атомов разных элементов?
4. До какой степени разные атомы одного элемента схожи между собой?
5. Как части атома удерживаются вместе?
6. Почему атомы удерживаются вместе и образуют молекулы?
Оказывается, на все эти вопросы лучше всего отвечать, начав с первого: из чего состоят атомы? Атомы состоят из того, что обычно называют «субатомными частицами» (к сожалению, этот термин некорректен, поскольку у этих «частиц» есть некоторые свойства, частицам не присущие). Конкретнее, атомы состоят из набора небольших и очень лёгких электронов, окружающих крохотное, но тяжёлое атомное ядро, в котором содержится большая часть массы атома. Ядро состоит из других «частиц», в свою очередь также состоящих из других «частиц», и мы до них ещё доберёмся.
Рисованный атом
Частенько мы видим изображения атомов, нарисованные на книгах по химии, на рекламках и предупреждающих знаках. Пример – рис. 1. Он передаёт очень грубую идею того, как устроен атом: снаружи у него есть определённое количество электронов (синие), и они вращаются вокруг центрального атомного ядра. Ядро – это скопление протонов (красные) и нейтронов (белые).
Рис. 1
Теперь мы можем ответить на 2-й вопрос: что означает атомное число Z? Это просто количество протонов в ядре. У кислорода атомный номер 8, и у него в ядре 8 протонов.
В простейших условиях атомное число также равняется количеству электронов атома. С количеством нейтронов всё сложнее, мы вернёмся к этому позже. У электронов отрицательный электрический заряд (-е), а у протонов – положительный (+е). Нейтроны нейтральны, электрического заряда у них нет. Когда количество электронов и протонов совпадает, их заряды взаимно уничтожаются, и у атома электрического заряда не наблюдается – такой атом нейтрален.
Но нет ничего необычного – к примеру, в процессе формирования молекул – если атом приобретёт или потеряет один или несколько внешних, валентных электронов. В этом случае электрические заряды электронов и протонов не уничтожаются, и получившийся заряженный атом называют ионом.
Более реалистичный атом
Хотя рис. 1 примерно описывает архитектуру атома – электроны действительно находятся снаружи, а ядро, состоящее из протонов и нейтронов, в середине – он совершенно не передаёт реальную форму и суть атома, поскольку он выполнен не в масштабе, а мы живём в квантовом мире, в котором объекты ведут себя так, что их сложно нарисовать или представить.
С проблемой масштаба можно разобраться, нарисовав более точное (хотя всё ещё несовершенное) изображение, рис. 2.
Рис 2. Атом – по большей части пуст (серая область). По нему быстро движутся электроны (голубые точки, нарисованы не в масштабе, а гораздо больше). В центре находится тяжёлое ядро (красные и белые точки, нарисованы больше, чем в масштабе).
Вот, что я попытался передать этим изображением. Во-первых, электроны очень, очень малы, настолько малы, что мы так и не смогли измерить их размер – может статься, что они точечные и не имеют размера, но они точно не больше, чем 1/100 000 000 от диаметра атома. Во-вторых, ядра (и протоны с нейтронами, их составляющие) также крайне малы, хотя они и больше, чем электроны. Их размер измерен, и он примерно в 10 000 – 100 000 раз меньше диаметра атома. Атом немного похож на деревню. Протоны и нейтроны в ядре – большие дома, находящиеся в центре деревни, а электроны – далеко разбросанные фермерские домики. На большей части сельской местности растут зерновые культуры и нет домов. И хотя территория, считающаяся частью деревни, может быть большой, реально занимаемая домами площадь очень мала.
Но эта аналогия не полная, поскольку электроны, в отличие от фермерских домиков, очень быстро двигаются по серому региону на картинке и вокруг ядра со скоростями порядка 1% от скорости света. Покрываемая ими территория обычно не сферическая, а более сложной формы, кроме того не все электроны перемещаются по одной и той же территории.
Но, как я вас предупреждал, рис. 2 тоже не точный. Во-первых, нужно было бы нарисовать ядро в тысячи раз меньше, а электроны – в миллионы раз меньше, только тогда их не было бы видно. Если бы атом был размером с вашу спальню, то его ядро было бы размером с пылинку. По сравнению со своими компонентами, атомы огромны! В каком-то смысле большую часть атома составляет пустота!
Во-вторых, изображение не передаёт мутную природу квантовой механики. Уравнения квантовой механики описывают и предсказывают поведение молекул, атомов и субатомных частиц, и эти уравнения говорят нам, что у этих частиц могут быть очень странные и неинтуитивные свойства. Хотя электроны в каком-то смысле точечные (допустим, если вы захотите столкнуть два электрона друг с другом, то обнаружите, что можете сдвинуть их вместе на сколь угодно малое расстояние, и они ничем не выдадут своей внутренней структуры, если она вообще есть), есть возможность сделать так, что они, будучи оставленными в покое, будут распространяться как волна и заполнят всё серое пространство на рис. 2. Если это звучит странно, это не оттого, что вы чего-то не поняли: это странно и об этом тяжело думать. Я-то уж точно не знаю, как нарисовать атом, чтобы не вводить вас в заблуждение, и эксперты всё ещё спорят о том, как лучше всего о нём думать. Так что пока просто примите это как странный факт.
Размер электрона слишком мал для измерения, и его масса настолько мала, что электрон может распространиться по всему атому. А вот у ядра есть вполне измеренный и известный размер, а его масса так велика – больше 99,9% массы всего атома – что оно вообще не распределяется в пространстве. Ядро сидит в середине серой области.
Атом и его химия
Лучший приходящий мне в голову способ описать атом: большая часть массы атома содержится в ядре, находящемся в его центре, вокруг которого распределились чрезвычайно мелкие электроны гораздо меньшей массы, причём сделали это совершенно не так, как ведут себя частицы, заполнив всю серую область рис. 2.
Небольшой размер ядра по отношению к полному размеру атома, и то, что оно обычно находится в его центре, объясняет, почему оно играет относительно слабую роль в химии. Химия происходит – то есть, формируются и меняются молекулы – когда атомы приближаются друг к другу, а это происходит, когда внешние, валентные электроны одного атома близко подходят к внешним электронам другого – когда край серой области одного атома приближается к краю серой области другого. В химических процессах атомное ядро остаётся в центрах атомов, и никогда не приближается к другим ядрам. Основная роль ядра – обеспечение положительного заряда, удерживающего электроны, и большей части массы (определяющей, как сложно другим объектам передвигать этот атом).
Это отвечает на 3-й вопрос: химию атома в основном определяют подробности, связанные с его внешними электронами. Эти детали можно узнать (сложным способом, через уравнения квантовой механики), исходя из атомного номера Z.
Вместо того, чтобы заняться химией – темой, которой хватит на целый курс – мы перейдём на уровень ниже, к субатомным частицам, по пути отвечая на другие вопросы. Перечислим вопросы, с которыми мы разобрались, и вопросы, которые ещё предстоит изучить.
1. Из чего состоят атомы? Снаружи – электроны, в центре – атомное ядро (из протонов и нейтронов).
2. В чём смысл атомного номера? Это количество протонов в ядре атома, которое, в обычных условиях равно количеству электронов, его окружающих.
3. Каков главный источник различий в химическом поведении атомов разных элементов? Свойства внешних электронов, определяемые общим количеством электронов у каждого элемента, к примеру, атомным номером.
4. До какой степени разные атомы одного элемента схожи между собой? Обсудим это в статье про изотопы.
5. Как части атома удерживаются вместе? Обсудим это в статье о роли электрических сил и квантовой механики.
6. Почему атомы удерживаются вместе и образуют молекулы? Обсудим это в статье о роли электронов и электрических сил в построении молекул из атомов.
А вот вам ещё вопрос, который мог возникнуть при изучении рис. 2:
Если атом – по большей части пуст, почему объекты кажутся твёрдыми? Почему нельзя протянуть руку через экран компьютера, если экран состоит из атомов, по большей части пустых?
Радионуклид — Что такое Радионуклид?
Радионуклид — радиоактивный атом с данным массовым числом и атомным номером а для изомерных атомов — и с определенным энергетическим состоянием атомного ядра.Радионуклиды представляют собой радиоактивные изотопы химических элементов
с разными массовыми числами.
Радионуклиды широко применяются в народном хозяйстве, технике, науке и медицине.
С их помощью изучают физиологические и биохимические процессы в норме и при патологии, а так же закономерности миграции и обмена химических элементов в окружающей среде, организме животных и человека.
Радиоактивные изотопы по свойствам относятся к разным категориям.
Радиоизотопы делятся на:
- природные;
- искусственные, образующиеся в результате проводимых ядерных реакций за счет деятельности человека.
Общее количество их достигает 2000 и продолжает увеличиваться.
Естественных элементов намного меньше, около 100.
По устойчивости ядер радионуклиды классифицируются на:
- короткоживущие – с периодом полураспада менее 10 суток;
- долгоживущие – с большим периодом полураспада.
с периодом полного распада в несколько минут, что делает их практически безвредными.
По радиационной токсичности радионуклиды делятся на 4 категории:
- А – самые высокотоксичные для человека. Это изотопы тяжелых элементов,
- ядра которых подвержены самопроизвольному распаду. У них относительно большие периоды полураспада. Также эти радиоактивные вещества имеют склонность к накоплению
- в разных органах тела;
- Б – радионуклиды высокой токсичности;
- В – радиоизотопы средней токсичности;
- Г – радиационные изотопы малой токсичности.
Радионуклиды попадают в ткани и органы человека и животных через вдыхание воздуха, прием пищи, царапины, раны, ожоги.
От истории химии до величайших вымыслов: вся правда о Менделееве
Как известно, в 2019 году мир отмечал 185-летие со дня рождения Д.И. Менделеева и 150-летие Периодической системы химических элементов. В честь памятных дат ведущие ученые проводили в «Сириусе» научно-популярные лекции по химии и ее истории. Подводя итоги года, мы вспоминаем самые интересные факты и вымыслы, связанные с великими открытиями.
Открытие Менделеевым таблицы химических элементов стало настоящей революцией в науке. Но история этого открытия до сих пор окутана легендами, мифами и легендами. Правда ли, что великому ученому приснился сон о том, как систематизировать знания о химических элементах? А верить ли слухам, что он торговал чемоданами в Гостином дворе в Санкт-Петербурге и придумал формулу спирта?
Развенчивает стереотипы и подтверждает догадки, а также рассказывает об истории химии – старший преподаватель кафедры радиохимии СПбГУ Евгений Калинин.
С чего начинается химия
Основа всей современной химии – наши представления об атоме. Именно на уровне атома (носителя свойств вещества) человечество может объяснить фундаментальные свойства химических элементов – электронное строение атома, масса и заряд ядра, валентность, степени окисления и многое другое.
Из школьной программы мы, конечно, помним, что:
- атом – мельчайшая частица, в состав которой входят отрицательно заряженные электроны» и «положительно заряженное» ядро. А ядро – это центр атома, который играет в его строении самую существенную роль и вокруг которого вращаются все электроны.
Но изучена ли природа мельчайшей структурной единицы досконально? Если подумать, мы в точности не знаем, как устроен атом и можем рассуждать о его строении лишь опосредованно, утверждает Евгений Калинин.
Тем не менее, история химии изучает и описывает долгий процесс накопления научных знаний, начиная с древних времен. Например, еще греческие философы были рассуждали о важных вопросах о делимости материи. Первым стал рассуждать на эту тему Левкипп, учитель Демокрита.
Атомизм Левкиппа-Демокрита
Философа интересовало: можно ли каждую часть материи, которая обладает определенными свойствами, бесконечно делить на еще более мелкие части?
Например, камень, расколотый пополам или растолченный в порошок, все равно останется тем же камнем. А что, если взять каждую его крупинку и раздробить на еще меньшие частички – до какого предела можно проводить такое деление и существует ли вообще такой предел?
Левкипп пришел к выводу:
- в конечном счете это приведет к исчезновению прежних свойств и появлению новых.
Эту мысль за своим наставником стал развивать и Демокрит. Он придумал мельчайшим частицам название: «атомос», то есть «неделимые». Термин, который ввел философ, унаследовала и современная химия. Учение о том, что деление материи допустимо только до определенного предела, стало называться атомистикой, или атомистической теорией.
Таким образом, Левкипп и Демокрит обрисовали важную мысль о том, что все состоит из атомов – невидимых и неделимых сфер материи бесконечного типа и числа.
Попытка точных измерений
Тщательным экспериментальным исследованиям физических и химических явлений дал жизнь ирландский химик XVII века Роберт Бойль – автор многих фундаментальных открытий. Вы о них точно слышали:
— Бойль предпринял первые попытки точных измерений при описании изменения вещества в экспериментах по сжатию и расширению газов;
— Именно Бойль установил, что воздух под давлением ртути умеет сжиматься, правда, не бесконечно (такое свойство воздуха в 1651 году было названо упругостью). Открытая ученым обратная зависимость объема от давления получила название закона Бойля. Занимаясь изучением химических процессов, он ввел в науку понятие анализа состава тел и прославился своими взглядами на строение вещества.
Как-то охарактеризовать невидимые атомы предложил английский естествоиспытатель Джон Дальтон. Изучая составы химических соединений, он установил:
- Два элемента могут соединяться друг с другом в строго определенных соотношениях (соотношение малых целых чисел) и обобщил результаты своих исследований, сформулировав закон кратных отношений – важнейшее открытие в химии.
Дальтон исследовал многие распространенные бинарные соединения (гидриды и оксиды) и сгруппировал первую таблицу относительных атомных весов.
Тропинка к Менделееву
В истории развития химии важными являются и труды Йенса Якоба Берцелиуса. В попытке точно определить элементный состав различных соединений ученый провел не менее 2000 анализов и в итоге получил новую таблицу относительных атомных весов. К слову, во времена Берцелиуса было открыто уже 54 элемента.
- Метод, как их упорядочить и систематизировать, обнаружил Иоганн Деберейнер, объединивший элементы в группы. Он наблюдал за изменением их химических свойств и поведением атомного веса.
- Но впервые расположил их в порядке возрастания Джон Ньюлендс. Он придумал вертикальные столбцы и вставил по семь элементов в каждый. Также ученый определил, что похожие элементы часто попадают в одни и те же горизонтальные ряды.
- Позже немец Лотар Майер опубликовал научный труд, в котором рассматривал объемы, занимаемые весовыми количествами элемента, численно равными их атомным весам. Он первым предложил термин «периодичность».
И наконец, фундаментальный вклад в развитие науки – создание периодической системы химических элементов и формулировка Периодического закона Менделеева. К этой задаче российский ученый подошел вплотную: в 1867-1868 годах он подготовил первое издание учебника «Основы химии», где обобщал все химические свойства всех известных тогда элементов.
Спустя три года Менделеев предложил новый вариант Периодической системы, уже в известном нам виде. Особенностью этого исследования было то, что в этой системе ученый предугадал открытие новых элементов.
- По мнению Менделеева, в одном столбце должны находиться элементы с одинаковой валентностью, поэтому он решил в своей таблице оставить пустые клетки, при этом тщательно изучая динамику возрастания атомных весов. Потом он соотносил это с валентностями в типических соединениях и химическими свойствами элементов.
Интересный факт: сперва коллеги Менделеева с недоверием отнеслись к его теории о недостающих элементах, но в течение 15 лет новые элементы – галлий, скандий и германий – были открыты, их свойства в точности отвечали признакам, описанным Менделеевым. После этого сомнений в значимости Периодической системы у скептиков не осталось.
Легенды и мифы о Менделееве
Миф 1. Таблица Менделеева ученому приснилась
Историю о том, что Периодическая система элементов привиделась химику во сне, слышал чуть ли не каждый изучающий химию школьник. Эта легенда появилась благодаря товарищу Менделеева Александру Иностранцеву, русскому геологу и профессору Петербургского университета. Сам Менделеев такого не подтверждал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
Миф 2. Изобретение 40-градусной водки
Есть мнение, что Дмитрий Иванович Менделеев изобрел традиционную русскую водку. Слухи породила его революционная научная работа на тему «Рассуждение о соединении спирта с водою», и строго говоря, к алкогольному напитку эта работа имела весьма косвенное отношение – ученый в своей диссертации заложил основы гидратной теории растворов спирта с водой при различных температурах.
Миф 3. Чемоданных дел мастер
Еще один интересный миф говорит о том, что Менделеев изготавливал чемоданы и торговал ими в Гостином дворе в Санкт-Петербурге. Ученый действительно научился переплетному и картонажному делу еще в юности и, имея огромный архив личных и научных документов, самостоятельно переплетал их и клеил для них картонные ящики. Кроме того, он мастерски делал оригинальные рамки для фотографий. Материалы для любимого занятия Менделеев покупал в том самом петербуржском Гостином дворе.
А легенду породила одна история. Однажды, когда ученый зашел в хозяйственную лавку, он услышал за своей спиной следующий диалог:
– Кто этот почтенный господин? – спросили у лавочника.
– Неужели не знаете? – удивился тот. – Да это же известный чемоданных дел мастер Менделеев! – с уважением в голосе ответил продавец.
Так люди узнали, что Менделеев любил не только изобретать, но и заниматься «приземленными ремеслами».
Ядро аналитической химии — Исследовательский центр Суперфонда Университета Дьюка
Что нам делать?
Ядро аналитической химии (ACC) является неотъемлемой частью обеспечения высококачественного химического анализа для всех проектов в Исследовательском центре Duke’s Superfund. Ядро преследует четыре цели:
- Регулярный количественный анализ органических и неорганических загрязнителей
Органические аналиты: ACC выполняет экстракцию и анализ следов органических соединений, включая: хлорорганические и органофосфатные пестициды, ПАУ, антипирены (ПБДЭ и заменители) и гормоны щитовидной железы.Мы можем проводить эти анализы в широком диапазоне сред, включая ткани, отложения, почвы и водные суспензии.
Неорганические аналиты: Доктор Хсу-Ким ACC также анализирует отдельные микроэлементы, включая щелочные и щелочноземельные металлы, переходные металлы, селен, мышьяк, лантаноиды, ртуть / метилртуть.
2. Проведение нецелевых химических анализов
Для характеристики и количественной оценки продуктов, образовавшихся в результате разложения химикатов Superfund и смесей загрязняющих веществ, ACC выполняет нецелевые анализы с использованием массы с высоким разрешением и точной массой (HRAM).Эта работа особенно важна для Проекта 5, который изучает эффективность методов биоремедиации грибков и бактерий для химикатов Суперфонда.
Ненаправленный анализ также может использоваться после наводнения или других стихийных бедствий для оценки рисков для здоровья окружающей среды от множества известных и неизвестных источников загрязнения. После урагана Флоренция в сентябре 2018 года д-р Фергюсон и д-р Джойс собрали пробы паводковой воды для нецелевого анализа.
3. Служить обучающим и консультационным ресурсом для стажеров и исследователей DUSRC
ACC поддерживает потребности в аналитической химии ИП и стажеров, работающих над проектами, связанными с SRC. Это включает помощь в разработке экспериментов, а также обучение работе с оборудованием, используемым для сбора данных и химического анализа. Формальное обучение также предоставляется на курсах для выпускников по экологической аналитической химии, которые ведет доктор Фергюсон.
4. Разработка новых аналитических методов для дополнительных «представляющих интерес химических веществ»
Персонал ACC разрабатывает новые методы измерения новых вызывающих озабоченность химических веществ, которые интересны исследователям Duke Superfund по мере необходимости.
Некоторые примеры аналитических услуг, предоставляемых ACC, включают:
- Количественное определение гормонов щитовидной железы в биологических тканях
- Анализ и определение характеристик существующих и новых галогенированных антипиренов (например, ПБДЭ и заменителей) в экологических и биологических пробах
- Количественное определение пестицида хлорпирифоса и продуктов его разложения в естественных и искусственно созданных системах
- Широкий спектр полициклических ароматических углеводородов (ПАУ) в отложениях и воде
- Идентификация и характеристика продуктов трансформации ПАУ в тканях рыб
- Анализ основных и микроэлементов в почве, воде и биологических тканях
- Анализ на содержание ртути (Hg), мышьяка (As), селена (Se), кадмия (Cd) и свинца (Pb) в цельной крови и других биологических тканях
- Биодоступные формы микроэлементов в почвах и частицах
Аналитические ресурсы, доступные ACC для этих анализов, включают: ВЭЖХ-МС / МС, ВЭЖХ-МС / МС с орбитальной ловушкой высокого разрешения, МС-МС с орбитальной ловушкой высокого разрешения, ГХ-МС, ГХ-ECD, ВЭЖХ-УФ-FLD и анализ микроэлементов с помощью систем ICP-MS и атомной флуоресцентной спектроскопии.
Исследование пенополиуретана
В рамках наших постоянных усилий по изучению воздействия на человека огнестойких химикатов мы предлагаем бесплатное тестирование пенополиуретана из бытовой мебели. Наше тестирование определит, присутствуют ли в мебельной пене 9 распространенных антипиренов. Это бесплатное тестирование открыто для всех, и каждая семья может отправить до 5 образцов мебели или других бытовых товаров с пенополиуретаном. Для получения дополнительной информации о том, почему мы это делаем, что мы делаем и как вы можете участвовать, посетите веб-сайт проекта .
–
Кто мы?
Доктор Ли Фергюсон — соучредитель
Доктор Хизер Стэплтон — соучредитель
Доктор Хейлин Хсу-Ким — соучредитель
Доктор Эбигейл Джойс — руководитель отдела аналитической химии
Доктор Нельсон Ривера — вспомогательный персонал целевого анализа неорганических веществ
Эмина Ходзич, BS — Техник-исследователь II
–
Связаться
Для получения дополнительной информации о ядре аналитической химии или для запроса услуг, пожалуйста, свяжитесь с Dr.Эбигейл Джойс: [email protected]
Химические расчеты показывают внутреннее ядро Земли | Research
Теоретические расчеты подтвердили, что ядро Земли содержит значительную долю кислорода. Это было предложено ранее, но новое исследование подтверждает это с точностью, которая ранее была невозможна. Присутствие кислорода можно использовать для ограничения моделей формирования Земли, предполагая, что ранняя Земля могла быть более горячей и богатой кислородом средой, чем предсказывают некоторые модели.
Измеряя момент инерции Земли и глядя на метеориты, сделанные из материала, похожего на планету, ученые подсчитали, что ядро в основном сделано из сплава, в котором железа в 16 раз больше, чем в никеле. Однако сейсмические волны проходят через ядро быстрее, чем через чистый железо-никелевый сплав, что подразумевает присутствие некоторых более легких элементов. Были предложены сера, кремний, углерод и кислород.
Невозможно получить образец ядра Земли, поэтому группа из Французского национального центра научных исследований и Университетского колледжа Лондона использовала теорию функционала плотности для предсказания плотности и сейсмических скоростей железо-никелевого сплава в сочетании с различными количествами. этих легких элементов.Они обнаружили, что каждая комбинация, удовлетворяющая всем четырем граничным условиям, содержала значительное количество кислорода. Внутреннее ядро также содержит кремний, но кристаллическая решетка твердого железа отклоняет атомы кислорода. По их лучшей оценке, в дополнение к сплаву железо-никель, внешнее ядро Земли содержит 3,7% кислорода, 1,9% кремния и не содержит серы или углерода.
Автор Джон Бродхольт говорит, что идея о том, что ядро содержит кислород и кремний, не является революционной, но геофизики в настоящее время отдают предпочтение различным возможным составам.«Мы не предлагаем совершенно другие элементы, о которых никогда не думали раньше, — говорит Бродхольт, — мы просто связываем это гораздо лучше». Поступая таким образом, он говорит, они также ограничивают возможные условия в которое ядро Земли отличало от мантии. Кислород плохо растворяется в железе при низких температурах, объясняет Бродхольт, поэтому эти результаты «предполагают относительно окислительную и потенциально более теплую раннюю Землю».
Теоретик электронной структуры и ученый-геолог Артем Оганов из Университета Стоуни-Брук, США, говорит, что группа UCL предложила аналогичный состав для активной зоны еще в 2002 году, и «выводы их работы полностью подтверждаются этой статьей».Хотя он согласен с тем, что внешнее ядро содержит кислород, он скептически относится к тому, что сера полностью или почти полностью отсутствует. «Если вы посмотрите на железные метеориты, которые представляют собой ядра разрушившихся планет в Солнечной системе, они содержат много серы», — говорит он. «Я никогда не встречал человека, который думал, что ядро Марса содержит менее 20% серы. Почему ядро Земли должно быть таким другим? »
SOCC Home
Ядро синтетической органической химии (SOCC) в UTMB было создано в 1998 году для изучения и разработки новых методов и протоколов синтеза модифицированных нуклеозидов, представляющих известные повреждения ДНК, и для превращения этих нуклеозидов в фосфорамидиты, которые могут быть удобно и сайт-специфично включены в синтетические последовательности ДНК.SOCC также разрабатывает методы включения участков поражения в олигонуклеотиды с помощью методов и протоколов пост-синтеза для очистки и анализа этих определенных продуктов. Предоставляемые синтетические органические услуги также были адаптированы и расширены за последние 18 лет, чтобы удовлетворить растущую потребность в синтезе и очистке других малых молекул и биоконъюгатов, которые представляют интерес для исследователей биомедицины и гигиены окружающей среды в UTMB и других местах. Эта область синтеза продолжает быстро расти с расширением Центра комплексной оценки воздействия и разработки биомаркеров Центра комплексных медицинских наук и его фокусом на разработке анализов для мониторинга воздействия и заболеваний.
SOCC выполняет две основные задачи:
Обеспечить рентабельную установку химического синтеза на территории кампуса с опытом в синтезе определенных химических повреждений ДНК, недоступных в других местах или непомерно дорогих на коммерческой основе, а также других недоступных органических молекул, биоконъюгатов и биомаркеров для биологического, медицинского и экологического здоровья исследовать.
Для снижения затрат на эту услугу за счет совместного использования этих ресурсов и их обслуживания в масштабах университетского городка между несколькими исследовательскими группами, которые используют объект.Техническое обслуживание оборудования SOCC осуществляется ежедневно обученным и квалифицированным персоналом с минимальными затратами для исследователей за счет возвратных платежей за услуги.
Программа SOCC для достижения этих целей использует известные из литературы методы и при необходимости разрабатывает новые методы и протоколы. SOCC специализируется на синтезе модифицированных нуклеозидов, представляющих известные сайт-специфические повреждения ДНК, а также в разработке методов и протоколов очистки и анализа этих определенных продуктов.
Химия — Core
Приведенный график предназначен только для студентов первого курса, которые прошли предварительный расчет. Студенты, у которых не было предварительных расчетов и переводных студентов, должны обсудить свое расписание с консультантом факультета.
Версия PDF
| Основной вариант и типовой график | |
|---|---|
| ПЕРВЫЙ ГОД | |
| Осень | Пружина |
| Лекция по общей химии (4.0 кр) 1 01: 160: 161 ИЛИ 01: 160: 163 |
Лекция по общей химии (4.0 кр) 01: 160: 162 OR 01: 160: 164 |
| Лаборатория общей химии (1.0 cr) 01: 160: 171 Осенью или весной |
|
| Исчисление I (4,0 кр) 01: 640: 151 |
Исчисление II (4,0 кр) 01: 640: 152 |
| ВТОРОЙ ГОД | |
| Осень | Пружина |
|
Лекция по органической химии (4.0 кр)
Аналитическая химия (3,0 кр)
Общая физика (3,0 кр)
Лаборатория общей физики (1.0 cr)
Многопараметрическое исчисление (4,0 кр) |
Лекция по органической химии (4,0 кр)
Лаборатория органической химии 3 (2.5 кр)
Общая физика (3,0 кр)
Лаборатория общей физики (1.0 cr)
Линейная алгебра (3,0 кр) |
| ТРЕТИЙ ГОД | |
| Осень | Пружина |
|
Лекция по физической химии (3.0 кр)
Лаборатория органической химии 2 (2,5 кр)
Химическое соединение (1,5 кр)
Инструментальный анализ (3,0 кр) |
Лекция по физической химии (3,0 кр)
Экспериментальная физическая химия (2.5 кр)
Неорганическая химия (3,0 кр) |
| ГОД ЧЕТВЕРТЫЙ | |
| Осень | Пружина |
| Семинар (1.0 кр) 01: 160: 491 |
Семинар (1.0 кр) 01: 160: 492 |
Основной вариант: примечания к курсу / расписанию
1 Предварительное условие для проведения исчисления
2 Только по приглашению
3 309 предлагается только в пружине ; Chem 310 предлагается осенью . только
4 327 и 341 имеют математику 251 как обязательное условие, а не как сопутствующее.
327 и 328 приемлемы для всех специальностей по химии
341 и 342 рекомендуются для студентов ориентирована на естественные науки
5 348 имеет 251 в качестве необходимого условия, которое предлагается только в осеннем ряду ; 251 предлагается как осень , так и пружина
6 361 и 371 могут быть отложены на один или два семестра, по желанию.Оба курса предлагаются осенью и весной . Chem 371 имеет Chem 361 и Chem 308 или 316 в качестве предварительных условий.
Центр передовых исследований гликонауки | Аналитические и биофизические исследования химии Core
Гликонаука — важная и быстро развивающаяся область биомедицинской науки, и сложный характер исследований гликологии требует инструментов и опыта, которые обычно не встречаются в сообществе биомедицинских исследователей. Более того, биомедицинское сообщество быстро растет, чтобы оценить важную роль углеводов, и исследователи, не входящие в самоидентифицированное сообщество «гликозайн», сталкиваются с необходимостью решать сложные вопросы гликонауки в рамках своих биомедицинских исследований.Ядро аналитических и биофизических исследований ориентировано на три аспекта:
Обучение
GlyCORE предлагает обучение правильной подготовке проб и обращению с ними, чтобы обеспечить приемлемые результаты. Обучение и консультация проводится в индивидуальном порядке.
Целевой анализ
GlyCORE предлагает целенаправленный анализ различных видов, чтобы помочь как в качественном, так и в количественном анализе как обогащенных соединений, так и выбранных соединений, присутствующих в сложных смесях.GlyCORE поддерживает множество распространенных анализов, в том числе: количественный анализ с метками и без меток; анализ углеводов для определения состава и структуры; анализ последовательности белков для определения мутаций и / или посттрансляционных модификаций; структурный анализ белков более высокого порядка для определения изменений в топографии или границах связывания белков; и измерение комплексов белок-лиганд.
Исследования, основанные на открытиях
GlyCORE предлагает услуги в области качественной и дифференциальной количественной гликомики, протеомики и метаболомики, чтобы предложить исследователям взгляды на системные изменения при возмущении их экспериментальной системы.Анализ данных доступен для протеомики через программное обеспечение Byonic. Анализ данных для гликомики и метаболомики поддерживается с помощью бесплатного академического программного обеспечения. Доступно взаимодействие с ядром вычислительной химии и биоинформатики GlyCORE для поддержки более сложных потребностей анализа данных.
По вопросам обращайтесь к нашему основному менеджеру, доктору Сандипу Мисре ([email protected]). Чтобы запросить услуги через Ядро, заполните наш образец формы запроса, чтобы отправить запрос (-ы) Менеджеру ядра.
Основная лаборатория клинической химии | Пенсильванский университет
Обзор
Выполняя 10 миллионов диагностических тестов в год, лаборатории Penn Medicine используют современную технологию тестирования, предварительно подключенную к полностью электронной системе заказа врачей, с последующей беспроблемной передачей и распределением в различные системы электронных медицинских карт с использованием любого из настольных компьютеров. или мобильные приложения.
Основная лаборатория, расположенная на территории 7 Founders, обслуживает большое количество пациентов стационаров и отделений неотложной помощи, одновременно поддерживая сеть амбулаторных клиник и специализированных онкологических служб.Лаборатория клинической химии выполняет анализы сыворотки, плазмы, мочи, спинномозговой жидкости и других биологических жидкостей. Запросы статистики с использованием образцов плазмы позволяют получить результат менее 30 минут, что очень важно для оказания неотложной помощи и других пациентов в критическом состоянии. Основная лаборатория стала одной из самых загруженных и производительных лабораторий университетских больниц в стране.
Ключом к успешной обработке большого ежедневного объема проб являются анализаторы с высокой пропускной способностью и резервными возможностями, которые позволяют бесперебойно предоставлять жизненно важные услуги пациентам при техническом обслуживании инструментов или непредвиденных простоях.Эта лаборатория большого объема работает с минимальным участием технолога. Подавляющее большинство образцов помещается на стеллажи в начальной точке короткого пути по автоматизированной системе треков к анализатору с последующей доставкой в автоматизированную систему холодильного хранения. Результаты, прошедшие определенные параметры скрининга (настроенные медицинским руководителем), автоматически подтверждаются лабораторным компьютером, а затем немедленно передаются в медицинскую карту пациента. Многократные проверки идентификации и качества образцов на протяжении всего пути следования образцов обеспечивают высочайшее качество результатов.Процесс, напоминающий высокотехнологичную сборочную линию, спроектирован и настроен так, чтобы максимизировать производительность тестирования при сохранении точности тестирования.
Основные моменты
• Основная лаборатория имеет обширное меню химических тестов, включающее примерно 135 различных анализов для основных типов образцов (сыворотка / плазма, моча, спинномозговая жидкость и биологические жидкости).
• Разработанные для выполнения максимального количества тестов с минимальным объемом образца, химические анализаторы могут выполнять 32 отдельных биохимических анализа на 1/3 мл (около 7 капель) крови.
• Оптимизация протоколов работы с образцами сводит к минимуму время выполнения работ для всех критически важных областей обслуживания больницы.
• Интеграция обслуживания клиентов с высококачественными анализаторами позволяет проводить полный спектр лабораторных испытаний как для исследований, так и для повседневной клинической помощи
Центр фотомедицины Веллмана: Факультетские лаборатории
Основная лаборатория синтетической химии была добавлена к центру Wellman в июне 2009 года. Центр химии предоставляет услуги в области синтетической, а также аналитической химии исследователям в центре Wellman и за его пределами.
Химическое ядро оснащено:
— Оборудование для нестандартного синтеза
— Газовый хроматограф (ГХ)
— Магнит ЯМР Bruker 300 МГц
— Масс-спектрометр Bruker Microflex MALDI-TOF
— Системы ВЭЖХ для нормальной и обращенно-фазовой хроматографии
Анализ и очистка. Наши ВЭЖХ оснащены колонками с обращенной фазой C18 для аналитического разделения и разделения в предварительном масштабе.Матрица фотодиодов и детекторы показателя преломления покрывают полный диапазон обнаружения при длине волны 200-800 нм
Химический синтез. Ядро полностью оборудовано для многоступенчатого органического синтеза. Эти услуги предоставляются бесплатно исследователям центра Wellman. Мы предполагаем сотрудничество с другими основными химическими лабораториями в районе Бостона, чтобы предоставить индивидуальные решения для индивидуальных проблем.
Спектроскопия ЯМР. ЯМР-магнит Bruker 300 МГц обеспечит такие возможности, как:
— 1D и 2D ЯМР спектроскопия
— ЯМР с переменной температурой
— Гетероядерный ЯМР
— Кинетические исследования
— Диффузионно-упорядоченная спектроскопия
Мы также будем предоставлять услуги ЯМР исследователям за пределами центра Wellman с оплатой за образец
Масс-спектроскопия.Наша система Bruker Microflex MALDI-TOF универсальна для анализа проб от малых молекул до крупных белков и полимеров. Обычно требуется всего несколько микрограммов аналита. Прибор оснащен как линейным, так и рефлекторным детекторами, способными анализировать последовательность пептидов
.
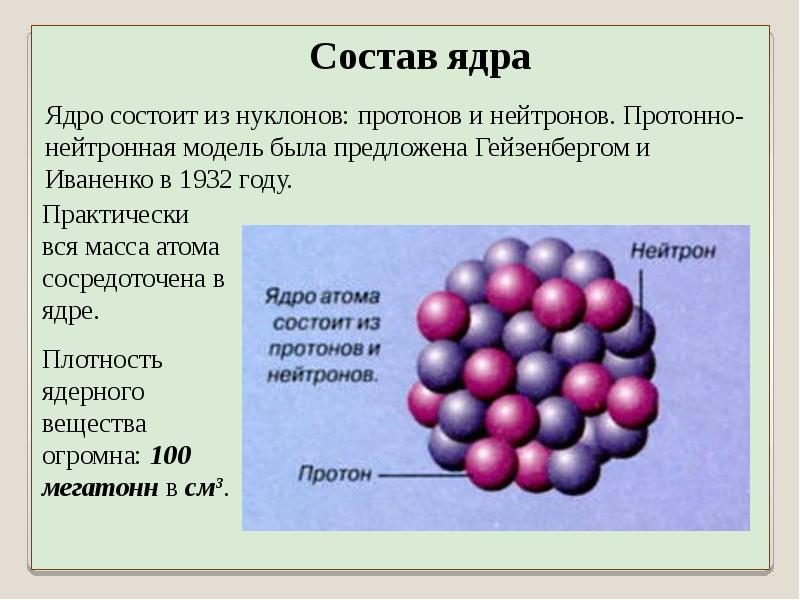
 При облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые был искусственно получен химический элемент технеций Тс.
При облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые был искусственно получен химический элемент технеций Тс. При захвате ядром алюминия-27 нейтрона образуется ядро натрия-24 и альфа-частица.
При захвате ядром алюминия-27 нейтрона образуется ядро натрия-24 и альфа-частица.