Формула спирта в химии
Определение и формула спирта
Спирты можно рассматривать как производные воды , в которых один атом водорода замещен на органическую функциональную группу.

Общая формула спиртов:
Структурная формула метанола, простейшего спирта,
Соединения, в которых гидроксильная группа связана с ненасыщенным атомом углерода, по номенклатуре ИЮПАК (IUPAC) называются енолы (гидроксильная группа связана с двойной связью C=C). Соединения, в которых гидроксильная группа связана с бензольным или любым другим ароматическим циклом называются фенолы.
Классификация и структура спиртов
Формулы разных спиртов
Общая формула предельных одноатомных спиртов:
Общая формула двухатомных спиртов (гликолей, диолов):
Общая формула трехатомных спиртов (триолов):
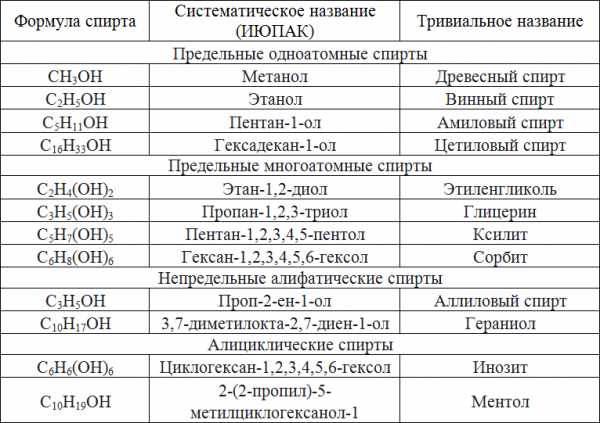
Для многих спиртов наряду с систематическими часто употребляются тривиальные названия:
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Физические и химические свойства спиртов
Общая формула гомологического ряда предельных одноатомных спиртов CnH2n+1OH . В названии спиртов присутствует суффикс – ол.
В зависимости от числа гидроксильных групп спирты делят на одно- (CH3OH — метанол, C2H5OH — этанол), двух- (CH2 (OH)-CH2-OH — этиленгликоль) и трехатомные (CH 2(OH)-CH(OH)-CH2-OH — глицерин). В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают первичные (R-CH2-OH), вторичные (R2CH-OH) и третичные спирты (R3C-OH).
Для предельных одноатомных спиртов характерна изомерия углеродного скелета (начиная с бутанола), а также изомерия положения гидроксильной группы (начиная с пропанола) и межклассовая изомерия с простыми эфирами.
СН3-СН2-СН2-СН2-ОН (бутанол – 1)
СН3-СН(СН3)- СН2-ОН (2-метилпропанол – 1)
СН3-СН(ОН)-СН2-СН3 (бутанол – 2)
СН3-СН2-О-СН2-СН3 (диэтиловый эфир)
Химические свойства спиртов
1. Реакция, протекающие с разрывом связи О-Н:
— кислотные свойства спиртов выражены очень слабо. Спирты реагируют с щелочными металлами
2C2H5OH + 2K → 2C2H5OK + H2
но не реагируют с щелочами. В присутствии воды алкоголяты полностью гидролизуются:
C2H5OK + Н2О → C2H5OH + KOH
Это означает, что спирты – более слабые кислоты, чем вода
— образование сложных эфиров под действием минеральных и органических кислот:
CH3-CO-OH + H-OCH3 ↔ CH3COOCH3 + H2O
— окисление спиртов под действием дихромата или перманганата калия до карбонильных соединений. Первичные спирты окисляются в альдегиды, которые, в свою очередь, могут окисляться в карбоновые кислоты.
R-CH 2-OH + [O] → R-CH = O + [O] → R-COOH
Вторичные спирты окисляются в кетоны:
R-CH(OH)-R’ + [O] → R-C(R’) = O
Третичные спирты более устойчивы к окислению.
2. Реакция с разрывом связи С-О.
— внутримолекулярная дегидратация с образованием алкенов (происходит при сильном нагревании спиртов с водоотнимающими веществами (концентрированная серная кислота)):
CH3-CH2-CH2-OH → CH3-CH = CH2 + H2O
— межмолекулярная дегидратация спиртов с образованием простых эфиров (происходит при слабом нагревании спиртов с водоотнимающими веществами (концентрированная серная кислота)):
2C2H5OH → C2H5-O-C2H5 + H2O
— слабые основные свойства спиртов проявляются в обратимых реакциях с галогеноводородами:
C2H5OH + HBr →C2H5Br + H2O
Физические свойства спиртов
Низшие спирты (до С15) – жидкости, высшие – твердые вещества. Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в оде падает. Спирты имеют высокие температуры кипения и плавления за счет образования водородных связей.
Получение спиртов
Получение спиртов возможно с помощью биотехнологического (брожение) способа из древесины или сахара.
К лабораторным способам получения спиртов относятся:
— гидратация алкенов (реакция протекает при нагревании и в присутствии концентрированной серной кислоты)
СН2 = СН2 + Н2О → СН3ОН
— гидролиз алкилгалогенидов под действием водных растворов щелочей
СН3Br + NaOH → CH3OH + NaBr
СН3Br + Н2О → CH3OH + HBr
— восстановление карбонильных соединений
CH3-CH-O + 2[H] → CH3– CH2-OH
Примеры решения задач
ru.solverbook.com
Х и м и я
Органическая химия
Спирты.
Спирты – это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами (ОН).
Так метиловый спирт СН3-ОН представляет собой гидроксильное производное метана СН4, этиловый спирт С2Н5-ОН – производное этана.
Название спиртов образуется добавлением окончания «-ол» к названию соответствующего углеводорода (метанол, этанол и т.д)
Название спирта | Формула спирта | Формула углеводорода |
|---|---|---|
| Метанол | СН3-ОН | СН4— метан |
| Этанол | С2Н5-ОН | С2Н6 — этан |
| Пропанол | С3Н7-ОН | С3Н8 — пропан |
| Бутанол | С4Н9-ОН | С4Н10 — бутан |
Производные ароматических углеводородов с группой ОН в бензольном ядре называются фенолами.
Свойства спиртов.
Подобно молекулам воды, молекулы низших спиртов связываются между собой водородными связями. По этой причине температура кипения спиртов выше, чем температура кипения соответствующих углеводородов.
Общим свойством спиртов и фенолов является подвижность водорода гидроксильной группы. При действии на спирт щелочного метала этот водород вытесняется металом и получаются твёрдые, растворимые в спирте соединения, называемые алкоголятами.
Спирты взаимодействуют с кислотами, образуя сложные эфиры.
Спирты значительно легче окисляются, чем соответствующие углеводороды. При этом образуются альдегиды и кетоны.
Спирты практически не являются электролитами, т.е. не прводят электрический ток.
Метиловый спирт.
Метиловый спирт (метанол) СН3ОН – бесцветная жидкость. Весьма ядовит: приём небольших его доз вутрь вызывает слепоту, а больших – смерть.
Метиловый спирт получают в больших количествах синтезом из окиси углерода и водорода при высоком давлении (
Метиловый спирт образуется при сухой перегонке дерева; поэтому его также называют древесным спиртом.
Он применяется как растворитель, а также для получения других органических веществ.
Этиловый спирт.
Этиловый спирт (этанол) С2Н5ОН – одно из важнейших исходных веществ в современной промышленности органического синтеза.
Для получения его издавна пользуются различными сахаристыми веществами, которые путём брожения превращаются в этиловый спирт. Брожение вызывается действием ферментов (энзимов), вырабатываемых дрожжевыми грибками.
В качестве сахаристых веществ используют виноградный сахар или глюкозу :
Глюкоза в свободном виде содержится, например, в виноградном соке, при брожении которого получается виноградное вино с содержанием спирта от 8 до 16%.
Исходным продуктом для получения спирта может служить полисахарид крахмалл, cодержащийся, например в клубнях картофеля, зерна ржи, пшеницы, кукурузы. Для превращения в сахаристые вещества (глюкозу) крахмал предварительно подвергают гидролизу.
В настоящее время осахариванию подвергается также другой полисахарид – целюлозу (клетчатку), образующую главную массу древесины. Целюлозу (например, древесные опилки) также предварительно подвергают гидролизу в присутствии кислот. Полученный таким образом продукт также содержит глюкозу и сбраживается на спирт при помощи дрожжей.
Наконец, этиловый спирт может быть получен синтетическим путём из этилена. Суммарная реакция заключается в присоединении воды к этилену.
Реакция протекает в присутствии катализаторов.
Многоатомные спирты.
До сих пор мы рассматривали спирты с одной гидроксильной группой (ОН). Такие спирты называются алкоголями.
Но также известны спирты, молекулы которых содержат несколько гидроксильных групп. Такие спирты называются многоатомными.
Примерами таких спиртов могут служить двухатомный спирт этиленгликоль и трёхатомный спирт глицерин:
Этиленгликоль и глицерин – жидкости сладковатого вкуса, смешивающиеся с водой в любых соотношениях.
Использование многоатомных спиртов.
Этиленгликоль применяется в качестве составной части, так называемых антифризов, т.е. веществ с низкой температурой замерзания, заменяющих воду в радиаторах автомобильных и авиационных моторов в зимнее время.
Также, этиленгликоль используют в производстве целлофана, полиуретанов и ряда других полимеров, как растворитель красящих веществ, в органическом синтезе.
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника.
Глицерин относится к группе стабилизаторов. При этом, он обладает свойствами сохранять и увеличивать степень вязкости различных продуктов, и таким образом менять их консистенцию. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
xn—-7sbb4aandjwsmn3a8g6b.xn--p1ai
строение, изомерия, свойства и примеры
В зависимости от числа гидроксильных групп спирты делят на одно- (CH3OH — метанол, 2H5OH — этанол), двух- (CH2(OH)-CH2-OH — этиленгликоль) и трехатомные (CH2(OH)-CH(OH)-CH2-OH — глицерин). В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают первичные (R-CH2-OH), вторичные (R2CH-OH) и третичные спирты (R3C-OH). В названии спиртов присутствует суффикс – ол.
Одноатомные спирты
Общая формула гомологического ряда предельных одноатомных спиртов CnH2n+1OH.
Изомерия
Для предельных одноатомных спиртов характерна изомерия углеродного скелета (начиная с бутанола), а также изомерия положения гидроксильной группы (начиная с пропанола) и межклассовая изомерия с простыми эфирами.
СН3-СН2-СН2-СН2-ОН (бутанол – 1)
СН3-СН(СН3)- СН2-ОН (2-метилпропанол – 1)
СН3-СН(ОН)-СН2-СН3 (бутанол – 2)
СН3-СН2-О-СН2-СН3 (диэтиловый эфир)
Физические свойства
Низшие спирты (до С15) – жидкости, высшие – твердые вещества. Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в оде падает. Спирты имеют высокие температуры кипения и плавления за счет образования водородных связей.
Получение спиртов
Получение спиртов возможно с помощью биотехнологического (брожение) способа из древесины или сахара.
К лабораторным способам получения спиртов относятся:
— гидратация алкенов (реакция протекает при нагревании и в присутствии концентрированной серной кислоты)
СН2=СН2 + Н2О → СН3ОН
— гидролиз алкилгалогенидов под действием водных растворов щелочей
СН3Br + NaOH → CH3OH + NaBr
СН3Br + Н2О → CH3OH + HBr
— восстановление карбонильных соединений
CH3-CH-O + 2[H] → CH3 – CH2-OH
Химические свойства
1. Реакция, протекающие с разрывом связи О-Н:
— кислотные свойства спиртов выражены очень слабо. Спирты реагируют с щелочными металлами
2C2H5OH + 2K → 2C2H5OK + H2
но не реагируют с щелочами. В присутствии воды алкоголяты полностью гидролизуются:
C2H5OK + Н2О → C2H5OH + KOH
Это означает, что спирты – более слабые кислоты, чем вода
— образование сложных эфиров под действием минеральных и органических кислот:
CH3-CO-OH + H-OCH3 ↔ CH3COOCH3 + H2O
— окисление спиртов под действием дихромата или перманганата калия до карбонильных соединений. Первичные спирты окисляются в альдегиды, которые, в свою очередь, могут окисляться в карбоновые кислоты.
R-CH2-OH + [O] → R-CH=O + [O] → R-COOH
Вторичные спирты окисляются в кетоны:
R-CH(OH)-R’ + [O] → R-C(R’)=O
Третичные спирты более устойчивы к окислению.
2. Реакция с разрывом связи С-О.
— внутримолекулярная дегидратация с образованием алкенов (происходит при сильном нагревании спиртов с водоотнимающими веществами (концентрированная серная кислота)):
CH3-CH2-CH2-OH → CH3-CH=CH2 + H2O
— межмолекулярная дегидратация спиртов с образованием простых эфиров (происходит при слабом нагревании спиртов с водоотнимающими веществами (концентрированная серная кислота)):
2C2H5OH → C2H5-O-C2H5 + H2O
— слабые основные свойства спиртов проявляются в обратимых реакциях с галогеноводородами:
C2H5OH + HBr →C2H5Br + H2O
Примеры решения задач
ru.solverbook.com
Спирты — номенклатура, получение, химические свойства » HimEge.ru

Спиртами (или алканолами) называются органические вещества, молекулы которых содержат одну или несколько гидроксильных групп (групп —ОН), соединенных с углеводородным радикалом.
Классификация спиртов
По числу гидроксильных групп (атомности) спирты делятся на:
Одноатомные, например:
Двухатомные (гликоли), например:
Трехатомные, например:
По характеру углеводородного радикала выделяют следующие спирты:
Предельные, содержащие в молекуле лишь предельные углеводородные радикалы, например:
Непредельные, содержащие в молекуле кратные (двойные и тройные) связи между атомами углерода, например:
Ароматические, т. е. спирты, содержащие в молекуле бензольное кольцо и гидроксильную группу, связанные друг с другом не непосредственно, а через атомы углерода, например:
Органические вещества,содержащие в молекуле гидроксильные группы, связанные непосредственно с атомом углерода бензольного кольца, существенно отличаются по химическим свойствам от спиртов и поэтому выделяются в самостоятельный класс органических соединений-фенолы.
Например:
Существуют и полиатомные (многоатомные спирты),содержащие более трех гидроксильных групп в молекуле. Например, простейший шестиатомный спирт гексаол (сорбит)
Номенклатура и изомерия спиртов
При образовании названий спиртов к названию углеводорода,соответствующего спирту,добавляют (родовой) суффикс-ол.
Цифрами после суффикса указывают положение гидроксильной группы в главной цепи, а префиксами ди-, три-,тетра- и т.д.-их число:
В нумерации атомов углерода в главной цепи положение гидроксильной группы приоритетно перед положением кратных связей:
Начиная с третьего члена гомологического ряда, у спиртов появляется изомерия положения функциональной группы (пропанол-1 и пропанол-2), а с четвертого — изомерия углеродного скелета (бутанол-1, 2-метилпропанол-1). Для них характерна и межклассовая изомерия- спирты изомерны простым эфирам:
Давайте дадим название спирту, формула которого указана ниже:
Порядок построения названия:
1. Углеродная цепь нумеруется с конца к которому ближе находится группа –ОН.
2. Основная цепь содержит 7 атомов С, значит соответствующий углеводород — гептан.
3. Число групп –ОН равно 2, префикс – «ди».
4. Гидроксильные группы находятся при 2 и 3 атомах углерода, n = 2 и 4.
Название спирта: гептандиол-2,4
Физические свойства спиртов
Спирты могут образовывать водородные связи как между молекулами спирта, так и между молекулами спирта и воды. Водородные связи возникают при взаимодействии частично положительно заряженного атома водорода одной молекулы спирта и частично отрицательно заряженного атома кислорода другой молекулы.Именно благодаря водородным связям между молекулами спирты имеют аномально высокие для своей молекулярной массы температуры кипения.Так, пропан с относительной молекулярной массой 44 при обычных условиях является газом, а простейший из спиртов-метанол,имея относительную молекулярную массу 32, в обычных условиях-жидкость.
Низшие и средние члены ряда предельных одноатомных спиртов,содержащих от 1 до 11 атомов углерода-жидкости.Высшие спирты(начиная с C12H25OH) при комнатной температуре-твердые вещества. Низшие спирты имеют алкогольный запах и жгучий вкус,они хорошо растворимы в воде.По мере увеличения углеродного радикала растворимость спиртов в воде понижается, а октанол уже не смешивается с водой.
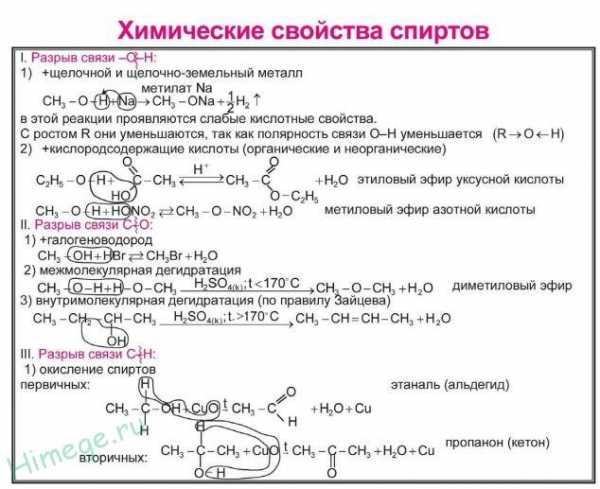
Химические свойства спиртов
Свойства органических веществ определяются их составом и строением. Спирты подтверждают общее правило. Их молекулы включают в себя углеводородные и гидроксильные группы, поэтому химические свойства спиртов определяются взаимодействием друг на друга этих групп.
Характерные для данного класса соединений свойства обусловлены наличием гидроксильной группы.
- Взаимодействие спиртов со щелочными и щелочноземельными металлами. Для выявления влияния углеводородного радикала на гидроксильную группу необходимо сравнить свойства вещества, содержащего гидроксильную группу и углеводородный радикал,с одной стороны, и вещества,содержащего гидроксильную группу и не содержащего углеводородный радикал,-с другой. Такими веществами могут быть,например, этанол (или другой спирт) и вода. Водород гидроксильной группы молекул спиртов и молекул воды способен восстанавливаться щелочными и щелочноземельными металлами(замещаться на них)
- Взаимодействие спиртов с галогеноводородами. Замещение гидроксильной группы на галоген приводит к образованию галогеналканов. Например:
Данная реакция обратима. - Межмолекулярная дегидратация спиртов- отщепление молекулы воды от двух молекул спиртов при нагревании в присутствии водоотнимающих средств:
В результате межмолекулярной дегидратации спиртов образуются простые эфиры.Так, при нагревании этилового спирта с серной кислотой до температуры от 100 до 140°С образуется диэтиловый (серный) эфир. - Взаимодействие спиртов с органическими и неорганическими кислотами с образованием сложных эфиров( реакция этерификации)
Реакция этерификации катализируется сильными неорганическими кислотами. Например, при взаимодействии этилового спирта и уксусной кислоты образуется-этилацетат:
- Внутримолекулярная дегидратация спиртов происходит при нагревании спиртов в присутствии водоотнимающих средств до более высокой температуры,чем температура межмолекулярной дегидратации. В результате образуются алкены. Эта реакция обусловлена наличием атома водорода и гидроксильной группы при соседних атомах углерода. В качестве примера можно привести реакцию получения этена (этилена) при нагревании этанола выше 140°С в присутствии концентрированной серной кислоты:
- Окисление спиртов обычно проводят сильными окислителями, например, дихроматом калия или перманганатом калия в кислой среде. При этом действие окислителя направляется на тот атом углерода, который уже связан с гидроксильной группой. В зависимости от природы спирта и условий проведения реакции могут образовываться различные продукты. Так, первичные спирты окисляются сначала в альдегиды, а затем в карбоновые кислоты: При окислении вторичных спиртов образуются кетоны:
Третичные спирты достаточно устойчивы к окислению. Однако в жестких условиях (сильный окислитель, высокая температура) возможно окисление третичных спиртов, которое происходит с разрывом углерод-углеродных связей, ближайших к гидроксильной группе. - Дегидрирование спиртов. При пропускании паров спирта при 200-300 °С над металлическим катализатором, например медью, серебром или платиной, первичные спирты превращаются в альдегиды, а вторичные — в кетоны:
- Качественная реакция на многоатомные спирты.
Присутствием в молекуле спирта одновременно нескольких гидроксильных групп обусловлены специфические свойства многоатомных спиртов, которые способны образовывать растворимые в воде ярко-синие комплексные соединения при взаимодействии со свежеполученным осадком гидроксида меди (II). Для этиленгликоля можно записать:
Одноатомные спирты не способны вступать в эту реакцию. Поэтому она является качественной реакцией на многоатомные спирты.
Получение спиртов:
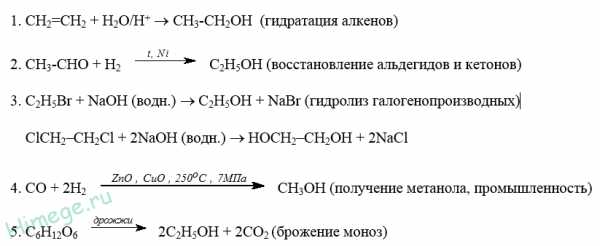
Применение спиртов
Метанол (метиловый спирт СН3ОН) — бесцветная жидкость с характерным запахом и температурой кипения 64,7 °С. Горит чуть голубоватым пламенем. Историческое название метанола — древесный спирт объясняется одним из путей его получения способом перегонки твердых пород дерева (греч. methy — вино, опьянеть; hule — вещество, древесина).
Метанол требует осторожного обращения при работе с ним. Под действием фермента алкогольдегидрогеназы он превращается в организме в формальдегид и муравьиную кислоту, которые повреждают сетчатку глаза, вызывают гибель зрительного нерва и полную потерю зрения. Попадание в организм более 50 мл метанола вызывает смерть.
Этанол (этиловый спирт С2Н5ОН) — бесцветная жидкость с характерным запахом и температурой кипения 78,3 °С. Горюч. Смешивается с водой в любых соотношениях. Концентрацию (крепость) спирта обычно выражают в объемных процентах. «Чистым» (медицинским) спиртом называют продукт, полученный из пищевого сырья и содержащий 96 % (по объему) этанола и 4 % (по объему) воды. Для получения безводного этанола — «абсолютного спирта» этот продукт обрабатывают веществами, химически связывающими воду (оксид кальция, безводный сульфат меди (II) и др.).
Для того чтобы сделать спирт, используемый в технических целях, непригодным для питья, в него добавляют небольшие количества трудноотделимых ядовитых, плохо пахнущих и имеющих отвратительный вкус веществ и подкрашивают. Содержащий такие добавки спирт называют денатурированным, или денатуратом.
Этанол широко используется в промышленности для производства синтетического каучука, лекарственных препаратов, применяется как растворитель, входит в состав лаков и красок, парфюмерных средств. В медицине этиловый спирт — важнейшее дезинфицирующее средство. Используется для приготовления алкогольных напитков.
Небольшие количества этилового спирта при попадании в организм человека снижают болевую чувствительность и блокируют процессы торможения в коре головного мозга, вызывая состояние опьянения. На этой стадии действия этанола увеличивается водоотделение в клетках и, следовательно, ускоряется мочеобразование, в результате чего происходит обезвоживание организма.
Кроме того, этанол вызывает расширение кровеносных сосудов. Усиление потока крови в кожных капиллярах приводит к покраснению кожи и ощущению теплоты.
В больших количествах этанол угнетает деятельность головного мозга (стадия торможения), вызывает нарушение координации движений. Промежуточный продукт окисления этанола в организме — ацетальдегид — крайне ядовит и вызывает тяжелое отравление.
Систематическое употребление этилового спирта и содержащих его напитков приводит к стойкому снижению продуктивности работы головного мозга, гибели клеток печени и замене их соединительной тканью — циррозу печени.
Этандиол-1,2 (этиленгликоль) — бесцветная вязкая жидкость. Ядовит. Неограниченно растворим в воде. Водные растворы не кристаллизуются при температурах значительно ниже О °С, что позволяет применять его как компонент незамерзающих охлаждающих жидкостей — антифризов для двигателей внутреннего сгорания.
Пролактриол-1,2,3 (глицерин) — вязкая сиропообразная жидкость, сладкая на вкус. Неограниченно растворим в воде. Нелетуч. В качестве составной части сложных эфиров входит в состав жиров и масел.
Широко используется в косметике, фармацевтической и пищевой промышленностях. В косметических средствах глицерин играет роль смягчающего и успокаивающего средства. Его добавляют к зубной пасте, чтобы предотвратить ее высыхание.
К кондитерским изделиям глицерин добавляют для предотвращения их кристаллизации. Им опрыскивают табак, в этом случае он действует как увлажнитель, предотвращающий высыхание табачных листьев и их раскрошивание до переработки. Его добавляют к клеям, чтобы предохранить их от слишком быстрого высыхания, и к пластикам, особенно к целлофану. В последнем случае глицерин выполняет функции пластификатора, действуя наподобие смазки между полимерными молекулами и, таким образом, придавая пластмассам необходимую гибкость и эластичность.
himege.ru
Спирты — Популярная химия
Спирты – разнообразный и обширный класс химических соединений.Спирты – это химические соединения, молекулы которых содержатся гидроксильные группы ОН, соединённые с углеводородным радикалом.
Углеводородный радикал состоит из атомов углерода и водорода. Примеры углеводородных радикалов — СН3 — метил, С2Н5 – этил. Часто углеводородный радикал обозначают просто буквой R. Но если в формуле присутствуют разные радикалы, их обозначают R’, R», R»’ и т.д.
Названия спиртов образуются путём добавления суффикса –ол к названию соответствующего углеводорода.
Классификация спиртов

Спирты бывают одноатомные и многоатомные. Если в молекуле спирта только одна гидроксильная группа, то такой спирт называется одноатомным. Если же количество гидроксильных групп 2, 3, 4 и т.д., то это многоатомный спирт.
Примеры одноатомных спиртов: СН3-ОН – метанол или метиловый спирт, СН3СН2-ОН – этанол или этиловый спирт.
Соответственно, в молекуле двухатомного спирта присутствуют две гидроксильные группы, в молекуле трёхатомного – три и т.д.
Одноатомные спирты
Общую формулу одноатомных спиртов можно представить как R-OH.
По типу свободного радикала, входящего в молекулу, одноатомные спирты делятся на предельные (насыщенные), непредельные (ненасыщенные) и ароматические спирты.
В насыщенных углеводородных радикалах атомы углерода соединены простыми связями С – С. В ненасыщенных радикалах присутствуют одна или несколько пар атомов углерода, соединённых двойными С = С или тройными С ≡ С связями.
В состав предельных спиртов входят предельные радикалы.
CH3CH2CH2—OH – предельный спирт пропанол-1 или пропиленовый спирт.
Соответственно, непредельные спирты содержат непредельные радикалы.
CH2=CH—CH2—OH – непредельный спирт пропенол 2-1 (аллиловый спирт)
А в молекулу ароматических спиртов входит бензольное кольцо C6H5.
C6H5—CH2—OH – ароматический спирт фенилметанол (бензиловый спирт).
В зависимости от типа атома углерода, связанного с гидроксильной группой, спирты делятся на первичные ((R—CH2—OH), вторичные (R—CHOH—R’) и третичные (RR’R»C—OH) спирты.
Химические свойства одноатомных спиртов

1. Спирты горят, образуя углекислый газ и воду. При горении выделяется тепло.
C2H5OH + 3O2 → 2CO2 + 3H2O
2. При реакции спиртов со щелочными металлами образуется алкоголят натрия и выделяется водород.
C2H5-OH + 2Na → 2C2H5ONa + H2
3. Реакция с галогеноводородом. В результате реакции образуется галогеноалкан (бромэтан и вода).
C2H5OH + HBr → C2H5Br + H2O
4. Внутримолекулярная дегидратация происходит при нагревании и под воздействием концентрированной серной кислоты. В результате получается непредельный углеводород и вода.
Н3 – СН2 – ОН → СН2 = СН2 + Н2О
5. Окисление спиртов. При обычной температуре спирты не окисляются. Но при помощи катализаторов и при нагревании окисление происходит.
Многоатомные спирты
Как вещества, содержащие гидроксильные группы, многоатомные спирты имеют химические свойства, схожие со свойствами одноатомных спиртов, но реакция у них идёт сразу по нескольким гидроксильным группам.
Многоатомные спирты вступают в реакцию с активными металлами, с галогеноводородными кислотами, с азотной кислотой.
Получение спиртов

Рассмотрим способы получения спиртов на примере этанола, формула которого С2Н5ОН.
Наиболее старый из них – отгонка спирта из вина, где он образуется в результате брожения сахаристых веществ. Сырьём для получения этилового спирта служат также крахмалосодержащие продукты, которые с помощью процесса брожения превращают в сахар, который затем сбраживают в спирт. Но производство этилового спирта таким способом требует большого расхода пищевого сырья.
Гораздо совершеннее синтетический способ получения этилового спирта. В этом случае проводят гидратацию этилена водяным паром.
С2Н4+ Н2О → С2Н5ОН
Среди многоатомных спиртов наиболее известен глицерин, который получают расщеплением жиров или синтетическим способом из пропилена, который образуется при высокотемпературной переработке нефти.
ximik.biz
Спирты
Классификация спиртов
— одноатомные R-OH; например:
— двухатомные (гликоли, диолы) R(OH)2; например:
— трехатомные (триолы) R(OH)3; например:
Двух-, трех- и т. д. спирты называются многоатомными.
— алициклические; например:
— ароматические; например, бензиловый спирт (см. выше).
— первичные RCH2OH: группа -ОН связана с первичным атомом углерода;
СН3-ОН; СН3-СН2-ОН; СН3-СН2-СН2-ОН
метанол; этанол; пропанол-1.
— вторичные RR’CHOH: группа -ОН связана с вторичным атомом углерода;
— третичные RR’R’COH: группа -ОН связана с третичным атомом углерода.
Предельные одноатомные спирты (алканолы)
Общая формула гомологического ряда предельных одноатомных спиртов — CnH2n+1OH; CnH2n+2O или R-OH.
Изомерия и номенклатура
Изомерия одноатомных спиртов связана со строением углеродного скелета (например, бутанол-2 и 2-метилпропанол-2) и с положением группы ОН (пропанол-1 и пропанол-2).
Названия спиртов образуют, добавляя окончание -ол к названию углеводорода с самой длинной углеродной цепью, включающей гидроксильную группу. Нумерацию цепи начинают с того края, ближе к которому расположена гидроксильная группа. Кроме того, широко распространена заместительная номенклатура, по которой название спирта производится от соответствующего углеводородного радикала с добавлением, слова «спирт», например: C2H5OH — этанол или этиловый спирт.
Электронное строение молекул алканолов
Молекулы алканолов содержат полярные связи С-Н, С-О, О-Н. Наиболее полярной является связь О-Н; поэтому электронная плотность на атоме водорода в группе ОН оказывается пониженной, а на атоме кислорода — повышенной. Тем не менее, в водных растворах ионизация этой связи не происходит, следовательно, спирты являются неэлектролитами.
Физические свойства
Первые десять членов гомологического ряда алканолов являются жидкостями, высшие спирты — твердые вещества. Таким образом, спирты обладают аномально высокими температурами кипения по сравнению с алканами. Это объясняется ассоциацией молекул спиртов вследствие образования межмолекулярных водородных связей:
Все алканолы легче воды, бесцветны. Метанол, этанол и пропанол неограниченно растворяются в воде; с увеличением числа атомов углерода растворимость спиртов уменьшается.
Химические свойства алканолов
2C2H5O-H + 2Na → 22H6ONa + H2↑
этанол → этилат натрия (этоксид натрия)
Алкоголяты подвергаются практически необратимому гидролизу:
2C2H5ONa + H2O → 22H5OH + HOH
Необратимость этой реакции доказывает, что спирты не проявляют кислотных свойств (точнее, что кислотные свойства спиртов выражены слабее, чем у воды).
Спирты можно превратить в галогеналканы также действием галогенидов фосфора и тионилхлорида:
4. Замещение гидроксильной группы на аминогруппу (образуются амины)
1. Межмолекулярная дегидратация (образуются простые эфиры)
(Правило Зайцева!)
3. Дегидрирование (образуются альдегиды в случае первичных спиртов и кетоны — в случае вторичных спиртов)
Третичные спирты не дегидрируются.
1. Горение
(Реакция идет с выделением большого количества теплоты; на этом основано применение лабораторных спиртовок.)
2. Неполное окисление под действием различных окислителем (образуются альдегиды в случае первичных спиртов и кетоны в случае вторичных спиртов)
При неполном окислении спиртов образуются те же продукты, что и при их дегидрировании. Таким образом, реакции дегидрирования по своей сути являются реакциями окисления.
Образующиеся при окислении первичных спиртов альдегиды далее легко окисляются до карбоновых кислот, поэтому можно записывать суммарные уравнения, например:
5С2Н5ОН + 4КМnO4 + 6H2SO4 → 5СН3СООН + 2K2SO4 + 4MnSO4 + 11Н2O
этанол → уксусная кислота
1. Гидратация алкенов
См. «Алкены»
2. Щелочной гидролиз галогеналканов
СН3СН2СН2Вг + КОН → СН3СН2СН2ОН + КВr
1-бромпропан → пропанол-1
(Обратите внимание на отличие этой реакции от взаимодействия галогеналканов со спиртовыми р-рами щелочей, в результате которого образуются алкены.)
3. Гидрирование альдегидов и кетонов
Гидрирование альдегидов и кетонов является их восстановлением.
4. Гидролиз сложных эфиров (кислотный и щелочной)
1. Синтез из водяного газа
2. Спиртовое брожение глюкозы
examchemistry.com
