Растворимость твердых веществ в воде — Науколандия
Растворимость — это способность веществ растворяться в воде. Одни вещества очень хорошо растворяются в воде, некоторые даже в неограниченных количествах. Другие — лишь в небольших количествах, а третьи — вообще почти не растворяются. Поэтому вещества делят на растворимые, малорастворимые и практически нерастворимые.
К растворимым относятся такие вещества, которые в 100 г воды растворяются в количестве больше 1 г (NaCl, сахар, HCl, KNO3). Малорастворимые вещества растворяются в количестве от 0,01 г до 1 г в 100 г воды (Ca(OH)2, CaSO4). Практически нерастворимые вещества не могут раствориться в 100 г воды в количестве больше 0,01 г (металлы, CaCO3, BaSO4).
При протекании химических реакций в водных растворах могут образовываться нерастворимые вещества, которые выпадают в осадок или находятся во взвешенном состоянии, делая раствор мутным.
Существует таблица растворимости в воде кислот, оснований и солей, где отражено является ли соединение растворимым. Все соли калия и натрия, а также все нитраты (соли азотной кислоты) хорошо растворимы в воде. Из сульфатов (солей серной кислоты) малорастворим сульфат кальция, нерастворимы сульфаты бария и свинца. Хлорид свинца малорастворим, а хлорид серебра нерастворим.
Если в клетках таблицы растворимости стоит черточка, это значит, что соединение реагирует с водой, в результате чего образуются другие вещества, т. е. соединение в воде не существует (например, карбонат алюминия).
Все твердые вещества, даже хорошо растворимые в воде, растворяются лишь в определенных количествах. Растворимость веществ выражают числом, которое показывает наибольшую массу вещества, которая может раствориться в 100 г воды при определенных условиях (обычно имеется в виду температура). Так при 20 °C в воде растворяется 36 г поваренной соли (хлорида натрия NaCl), более 200 г сахара.
С другой стороны, вообще нерастворимых веществ нет. Любое практически нерастворимое вещество хотя бы в очень незначительных количествах, но растворяется в воде. Например, мел растворяется в 100 г воды при комнатной температуре в количестве 0,007 г.
Большинство веществ с повышением температуры лучше растворяются в воде. Однако NaCl почти одинаково растворим при любой температуре, а Ca(OH)2 (известь) лучше растворяется при более низкой температуре. На основе зависимости растворимости веществ от температуры строят кривые растворимости.
Если в растворе при данной температуре еще можно растворить какое-то количество вещества, то такой раствор называют ненасыщенным. Если же достигнут придел растворимости, и больше вещества растворить нельзя, то говорят, что раствор насыщенный.
Когда охлаждают насыщенный раствор, то растворимость вещества понижается, и, следовательно, оно начинает выпадать в осадок. Часто вещество выделяется в виде кристаллов. Для разных солей кристаллы имеют свою форму. Так кристаллы поваренной соли имеют кубическую форму, у калийной селитры они похожи на иголки.
scienceland.info
Глина в воде растворяется или нет. Растворимость различных веществ
Вода – универсальный растворитель. Из-за этого она никогда не бывает чистой. В ней всегда присутствуют какие-то вещества. Это свойство воды используется человеком для приготовления различных растворов. Они применяются во всех отраслях промышленности, в медицине и даже в быту. Но не все вещества одинаково растворяются в воде. Многие люди узнают об этом опытным путем, кто-то — из специальной литературы или от знакомых. Особенно часто задается такой вопрос: «Глина в воде растворяется или нет?» Это вещество также очень распространено в природе. Глина часто используется человеком. Интересуют многих также особенности растворения крахмала, сахара, соли и соды. Это самые часто применяемые людьми вещества.
Что такое растворимость
Процесс растворения различных веществ представляет собой механическое перемешивание их частиц с молекулами воды. Это не только физическое явление, но и химическое. При смешивании некоторых веществ могут происходить химические реакции. Чаще всего способность их растворяться улучшается с повышением температуры.  Свойство воды образовывать различные смеси с другими жидкостями, газами и твердыми веществами человек использует в своих целях. Чаще всего растворы применяются в кулинарии: растворяется соль и сахар для улучшения вкуса продуктов, крахмал и желатин – для придания им определенной консистенции, углекислый газ – для создания напитков. Растворимость веществ в воде широко используется в медицине. Например, для приготовления различных эмульсий и суспензий, растворов лекарственных веществ и взвесей нерастворимых субстанций для их лучшего воздействия на организм. Именно для этих целей люди часто ищут ответ на вопрос, растворяется ли глина в воде, ведь она используется для лечебных целей.
Свойство воды образовывать различные смеси с другими жидкостями, газами и твердыми веществами человек использует в своих целях. Чаще всего растворы применяются в кулинарии: растворяется соль и сахар для улучшения вкуса продуктов, крахмал и желатин – для придания им определенной консистенции, углекислый газ – для создания напитков. Растворимость веществ в воде широко используется в медицине. Например, для приготовления различных эмульсий и суспензий, растворов лекарственных веществ и взвесей нерастворимых субстанций для их лучшего воздействия на организм. Именно для этих целей люди часто ищут ответ на вопрос, растворяется ли глина в воде, ведь она используется для лечебных целей.
Особенности разных растворов
Прежде чем ответить на вопрос: «Глина в воде растворяется или нет?» — нужно понять, что в итоге должно получиться. Раствор – это однородная субстанция, в которой частицы растворенного вещества перемешаны с молекулами воды. Иногда они становятся полностью незаметными, но часто можно определить, что находится в жидкости. В зависимости от этого все растворы можно разделить на несколько групп.
1. Собственно раствор, который остается прозрачным, как вода, но имеет привкус или запах растворенного вещества. Так перемешиваются с жидкостью соль, сахар, некоторые газы и минеральные вещества. Такое свойство часто используют в приготовлении пищи.
2. Растворы, которые приобретают не только вкус и запах вещества, но и его цвет. Например, вода, подкрашенная марганцовкой или йодом.
3. Иногда получаются мутные растворы, называемые взвесями. О них узнают те, кто ищет ответ на вопрос, глина в воде растворяется или нет. Такие растворы можно разделить на две группы:
— суспензия, в которой частицы вещества равномерно распределены между молекулами воды, например, смесь глины с водой;
— эмульсия – это раствор какой-либо жидкости или масла в воде, например, бензина.
Растворяется ли глина в воде
Есть вещества растворимые и нерастворимые. Если проводить опыт, можно увидеть, что при смешивании песка, глины и некоторых других частиц с жидкостью образуется мутная взвесь. Через некоторое время можно наблюдать, как вода постепенно становится прозрачной. Это происходит из-за того, что частицы песка или глины оседают на дно. Но такие растворы также находят применение. Например, смесь глины с водой намного лучше усваивается организмом при приеме внутрь или при использовании для масок и компрессов.  Частички глины, перемешанные с жидкостью, становятся более пластичными и лучше проникают через кожу, оказывая свое положительное воздействие. О возможностях глины лечить многие заболевания известно давно. Но использовать ее можно только в виде раствора различной концентрации. Именно для этих целей люди чаще всего и ищут ответ на вопрос «глина в воде растворяется или нет?».
Частички глины, перемешанные с жидкостью, становятся более пластичными и лучше проникают через кожу, оказывая свое положительное воздействие. О возможностях глины лечить многие заболевания известно давно. Но использовать ее можно только в виде раствора различной концентрации. Именно для этих целей люди чаще всего и ищут ответ на вопрос «глина в воде растворяется или нет?».
Растворение соды, соли и сахара
1. Соду в воде растворяют также в основном для лечебных целей. Такими смесями показано полоскать рот или горло, делать примочки или компрессы. Полезно принимать ванны в растворе соды. Частицы этого вещества полностью перемешиваются с молекулами воды, оказывая лечебное действие на организм.
2. Раствор соли человек использует давно. Она способна полностью растворяться в воде. Именно это свойство широко применяется в кулинарии. Более насыщенные соляные растворы используются для полосканий и компрессов в медицине.
3. Сахар – это вещество, которое также легко растворяется в воде полностью. Эту сладкую смесь используют в кулинарии и для приготовления различных лекарств.
Растворяется ли крахмал
Глина, сода в воде используются немного реже, в основном для лечебных целей. А вот крахмал – довольно распространенный пищевой продукт. Но, в отличие от сахара и соли, он не растворяется в воде. Он образует суспензию, почти как глина. Но у этих веществ есть и определенные различия. Растворяется в воде глина и крахмал одинаково при комнатной температуре. Образуется взвесь, в которой при отстаивании частички твердого вещества оседают на дно. Но при повышении температуры воды крахмал ведет себя по-особому. Он набухает и образует коллоидный раствор – клейстер. Это его свойство используется при приготовлении киселей и различных других блюд.
Как большинство людей узнают о растворимости веществ
Еще в начальной школе детям рассказывают об этом. Часто им это показывают на наглядных примерах. Проводятся опыты, в которых видно, что соль полностью растворяется, а песок постепенно оседает на дно. Способность некоторых веществ перемешиваться с жидкостями проверяется каждый день. Например, ни у кого не возникает вопроса, растворяется ли сахар или соль. Но те вещества, которые используются реже, могут вызывать недоумение. Поэтому и интересуются люди, растворяется ли в воде глина и крахмал, как правильно развести марганцовку или как приготовить суспензию для компресса.
fb.ru
Растворимость веществ в, воде — Справочник химика 21
Растворимостью вещества в воде называется максимальное количество этого вещества, выраженное, например, в граммах, которое растворится в некотором количестве воды (например, 100 г) при некоторой температуре. Растворимость нитрата калия, например, может быть выражена в граммах на 100 г воды при определенной температуре. [c.53]Растворимость веществ в воде (в граммах безводного вещества в 100 г раствора) [c.208]
Для химика-органика большое значение имеет знакомство с методами, позволяющими индивидуализировать и определять органические соединения. Еще более важным является для него глубокое понимание структурной формулы соединения он должен уметь по структурной формуле составить себе представление о физических и химических свойствах изображенного формулой соединения. Так, например, наличие в молекуле карбоксильной или аминогруппы свидетельствует о том, что вещество обладает кислым или, соответственно, основным характером большой вес углеводородной части молекулы указывает на малую растворимость вещества в воде и значительную растворимость его в органических растворителях. Обратное заключение можно сделать при большом числе гидроксильных или сульфо-групп. Из рассмотрения структурной формулы часто становятся ясными такие свойства соединения, как легкая окисляемость, способность подвергаться гидролитическому расщеплению наличие характерных хромофорных групп (азогруппы, хиноидные системы и др.) показывает, что соединение обладает окраской [c.631]
Экстрагированием называется метод разделения веществ, при котором вещество извлекают из водного раствора с помощью органического растворителя, не смешивающегося с водой, т. е. в основе метода лежит различная растворимость веществ в воде и в органических растворителях. Например, часто для определения иодидов исследуемый водный раствор обрабатывают подходящим окислителем и выделившийся иод извлекают органическим растворителем (хлороформом, бензолом, четыреххлористым углеродом и т. п.), так как иод значительно лучше растворяется в этих растворителях, чем в воде.
РАСТВОРИМОСТЬ ВЕЩЕСТВ В ВОДЕ [c.235]
Растворение в воде. Обработку анализируемой смеси водой проводят при перемешивании и нагревании на водяной бане. Растворимость вещества в воде проверяют после отделения не-растворившегося остатка центрифугированием, выпаривая каплю центрифугата на (предметном стекле. Если вещество растворилось хотя бы частично, водную вытяжку повторяют до полного его растворения. [c.49]
Медико-биологическое значение соединений с гидроксильной группой и их применение в народном хозяйстве. Введение гидроксильной группы в молекулу повышает растворимость вещества в воде и увеличивает его физиологическую активность (токсичность и наркотическое действие). Последняя возрастает с удлинением углеродной цепи, проходя через максимум при Се—Се, с ее разветвлением, а также при переходе от первичных спиртов к вторичным и третичным. Введение галогенов или кратных связей в молекулу спирта усиливает его наркотическое действие. [c.158]
Растворимость веществ в воде при комнатной температуре 250 [c.4]
Эта реакция более универсальна, чем реакция с бромом. Скорость ее зависит от растворимости вещества в воде. Если вещество нерастворимо в воде, реакцию ведут в ацетоне. Однако КМпОд окисляет вещества и других классов, например первичные и вторичные спирты, альдегиды, тиоспирты, ароматические амины, фенолы и др. [c.250]
Растворимость веществ в воде 68—69, 173. [c.187]
Различная растворимость веществ в воде и разный характер ее зависимости от температуры лежат в основе процесса перекристаллизации, который заключается в растворении вещества или смеси веществ и последующей его кристаллизации. Чем ниже температура, при которой проводится кристаллизация, тем большее количество осадка выделяется в твердую фазу. Если в насыщенном горячем растворе есть механические нерастворимые примеси, его фильтруют через воронку для горячего фильтрования.
Растворимость вещества в воде и других растворителях является их индивидуальной особенностью. Одни вещества растворяются хорошо, другие, наоборот, плохо. Растворимость большинства неорганических веществ в воде при нагревании, как правило, увеличивается. [c.31]
Для понижения растворимости веществ в воде применяют разные методы, самым простым является осаждение спиртами. [c.300]
Извлечение (экстракцию) растворителем очень часто применяют для выделения вещества из растворов или из смесей. При подборе растворителя руководствуются общим принципом накопление в молекуле гидроксильных, карбоксильных и аминогрупп обычно увеличивает растворимость вещества в воде, и, наоборот, накопление атомов галоида или углеводородных радикалов повышает растворимость в эфире и в неполярных органических растворителях— бензоле и т. п. [c.43]
Растворимость веществ в воде [c.102]
Растворимость веществ в воде в значительной мере зависит от температуры. Растворимость твердых веществ и жидкостей с повышением температуры, как правило, возрастает. Однако температурная зависимость растворимости разных веществ самая различная. Например, растворимость хлорида калия с увеличением температуры растет очень сильно, а хлорида натрия — незначительно. Растворимость анилина при обычной температуре очень мала, но выше 40° С он растворяется в воде в неограниченных количествах. Правда, имеются твердые вещества, растворимость которых с повышением температуры падает, например уксуснокислый кальций, известь и др.
Анализ полученного продукта, несмотря на его светло-желтую окраску, дает удовлетворительные результаты. Бесцветное вещество может быть получено путем повторного кипячения с угле.м, что однако заметно снижает выход вследствие значительной растворимости вещества в воде. [c.42]
Эта реакция более универсальна, чем реакция с бромом. Скорость ее зависит от растворимости вещества в воде. Если вещество не раство- [c.215]
Растворимость веществ в воде. Концентрация растворов. [c.150]
Как влияет карбоксильная группа на растворимость веществ в воде [c.192]
При достаточной растворимости вещества в воде его можно вводить животным с питьевой водой из обычных автоматических поилок. Концентрацию раствора подбирают исходя из необходимой дозы и суточного потребления воды, которое для мышей составляет около 2 мл и для крыс около 10 мл в сутки. [c.273]
Растворимость веществ в воде 150 Диссоциация солей, кислот и оснований в воде. Ионные уравнения. Условия 186 протекания реакций обмена до конца [c.1]
При проверке растворимости веществ в воде следует определять реакцию раствора или суспензии на лакмус или фенолфталеин. [c.33]
Кристаллизацию веществ из насыщенного раствора методом охлаждения проводят для таких веществ, у которых сильно различаются растворимости при разных температурах. Для веществ с мало различающейся растворимостью (например, ЫаС1 — см. табл. VI) этот метод мало эффективен. В таких случаях к водному раствору добавляют вещества, понижающие растворимость веществ в воде (например, спирт, ацетон, концентрированную соляную кислоту и др.). [c.50]
Не растворимых веществ в воде, ие более. … в соляной кислоте, не более. [c.395]
Чем меньше растворимость вещества в воде, тем больше предельный коэффициент — -Сн,о)- Если концентрации выражены в миллимолях на 1 кг, то вычисление производится по формуле
К этому трудоемкому методу приходится прибегать в тех редких случаях, когда а) малая растворимость вещества в воде не позволяет применить потенциометрию или б) спектры поглощения молекул и ионов либо мало отличаются между собой, либо лежат за пределами надежного количественного измерения, что не позволяет применить спектрофотометрический метод. [c.104]
В последнее время С. Д. Заугольников -и др. (1973) разработали классификацию степени опасности веществ для воды водоем-oiB (табл. 33) ib соответствии с указанными выше кла-ссами опасности -профессиональных ядов. Показателем опасн-о-сти веществ в этом случае (поступление per os) служит логар-ифм отношений растворимости веществ в воде (820°) к их ПДК. [c.101]
В задание 16 включены вопросы, отвечая на которые учащиеся приобретают умения пользоваться таблицей, показывающей растворимость веществ в воде, определять характерные с. юйства гидроксидов разных групп и практически возможные способы их получения. [c.93]
chem21.info
Растворимость веществ в воде — РАСТВОРЫ
Часть И. ОБЩАЯ ХИМИЯ
Раздел 5. РОЗЧИНИ.ТЕОРІЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
§ 5.2. Растворимость веществ в воде
Растворимость — это свойство вещества растворяться в воде или другом растворителе. В воде могут растворяться твердые, жидкие и газуваті вещества.
По растворимостью в воде все вещества делятся на три группы: 1) хорошо растворимые; 2) малорастворимые и 3) практически нерастворимые. Последние называются также нерастворимыми веществами. Однако следует отметить, что абсолютно нерастворимых веществ нет. Если погрузить в воду стеклянную палочку или кусок золота или серебра, то они в ничтожно малых количествах все же таки растворяются в воде. Как известно, растворы аргентуму или ауруму в воде убивают микробы. Стекло, серебро, золото — это примеры практически не растворимых в воде веществ (твердые вещества). К ним относятся также керосин, масло (жидкие вещества), благородные газы (газуваті вещества). Многие вещества в воде растворяются достаточно хорошо. Примером таких веществ могут быть сахар, медный купорос, гидроксид натрия (твердые вещества), спирт, ацетон (жидкие вещества), хлороводень, аммиак (газуваті вещества).
Из приведенных примеров следует, что растворимость прежде всего зависит от природы веществ, кроме того, она зависит от температуры и давления. Сам процесс растворения обусловлен взаимодействием частиц растворенного вещества и растворителя; это самопроизвольный процесс.
Процесс растворения твердых веществ в жидкостях можно представить так: под влиянием растворителя от поверхности твердого вещества постепенно отрываются отдельные ионы или молекулы и равномерно распределяются в всем объеме растворителя. Если растворитель контактирует с большим количеством вещества, то через некоторое время раствор становится насыщенным.
Насыщенным называется такой раствор, который находится в динамическом равновесии с избытком растворенного вещества.
Чтобы приготовить насыщенный раствор, нужно в воду при данной температуре добавлять при перемешивании вещество до тех пор, пока не образуется осадок, то есть избыток вещества останется нерастворимым. В Этом случае установится динамическое равновесие между раствором и избытком вещества, растворяется: сколько частиц вещества переходит в раствор, столько же их будет выделяться (кристаллизоваться) из раствора. В насыщенном растворе при данной температуре содержится максимально возможное количество растворенного вещества.
В ненасыщенном растворе содержится меньше веществ, а в пресыщенному — больше, чем в насыщенном. Пересыщенные растворы довольно неустойчивы. Легкое встряхивание сосуда или добавления к раствору кристалла соли вызывает выпадение в осадок избытка растворенного вещества. Пересыщенные растворы образуют сахароза, Na2SO4 ∙ 10Н2О, Na2S2O3∙ 5Н2О, СН3СООNа, Na2B4O7 ∙10Н2О и др.
Часто малорастворимые и практически нерастворимые вещества объединяют одним названием — малорастворимые. В этом случае говорят только о растворимые и малорастворимые вещества. Количественно растворимость выражается концентрацией насыщенного раствора. Чаще всего ее выражают максимальным числом граммов вещества, которое можно растворить в 100 г растворителя при данной температуры. Это количество вещества иногда называют коэффициентом растворимости, или просто растворимостью вещества. Например, при 18 °С в 100 г воды растворятся 51,7 г соли нитрата свинца(II) Гb(NО3)2, то есть растворимость этой соли при 18°С равна 51,7. Если при этой же температуре более это количество добавить еще соли нитрата свинца(II), то она не растворится, а выпадет в виде осадка.
Говоря о растворимости вещества, следует указывать температуру растворения. Чаще всего растворимость твердых веществ с повышением темпераpатуpи сpостає. Это наглядно изображается помощью кривых растворимости (рис. 5.2). На оси абсцисс откладывают температуру, а на оси ординат — коэффициент растворимости. Однако растворимость некоторых веществ при повышении температуры возрастает незначительно (например NaCl, АlСl3) или даже уменьшается [например, Са(OН)2, Li2SO4, Са(СН3СОО)2]. На коэффициент растворимости твердого тела в воде давление влияет в незначительной степени, поскольку во время растворения не происходит заметного изменения объема системы. С помощью кривых растворимости легко вычислить, сколько соли выпадет из раствора при его охлаждении. Например, если взять 100 г воды и приготовить при 45°С насыщенный раствор нитрата калия, а затем охладить его до 0°С, то, как следует из кривой растворимости (см. рис. 5.2), должно выпасть 60 г кристаллов соли. По кривым растворимости легко определяют коэффициент растворимости веществ по различных температур.
Выделение вещества из раствора при снижении температуры называется кристаллизацией. Если в растворе содержались примеси, то вследствие кристаллизации вещество всегда добывается чистой, поскольку в отношении примесей раствор остается ненасыщенным даже при снижении температуры, и примеси не выпадают в осадок. На этом базируется метод очистки веществ, называется перекристаллизацией.
Во время растворения газов в воде выделяется теплота. Поэтому согласно принципу Ле Шателье при повышении
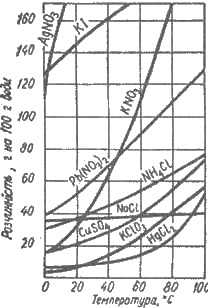
Рис. 5.2. Кривые растворимости твердых веществ
температуры растворимость газов уменьшается, а при снижении — увеличивается (рис. 5.3). Растворимость газов возрастает при повышении давления. Поскольку объем газа, растворяется в данном объеме воды, не зависит от давления, то растворимость газа обычно выражают количеством миллилитров, которое растворяется в 100 г растворителя (см. рис. 5.3).
Рис. 5.3. Кривые растворимости газов
na-uroke.in.ua
Растворение. Растворимость веществ в воде
Растворы играют ключевую роль в природе, науке и технике. Вода – основа жизни, всегда содержит растворенные вещества. Пресная вода рек и озер содержит мало растворенных веществ, в то время как морская вода содержит около 3,5% растворенных солей.
Первичный океан (во время зарождения жизни на Земле), по предположениям, содержал всего 1% растворенных солей.
«Именно в этой среде впервые развивались живые организмы, из этого раствора они черпали ионы и молекулы, которые необходимы для их дальнейшего роста и развития… Со временем живые организмы развивались и преображались, поэтому они смогли оставить водную среду и перебраться на сушу и затем подняться в воздух. Они получили эти способности, сохранив в своих организмах водный раствор в виде жидкостей, которые содержат жизненно важный запас ионов и молекул» – именно такими словами описывает роль растворов в природе знаменитый американский химик, лауреат Нобелевской премии Лайнус Полинг. Внутри каждого из нас, в каждой клетке нашего организма – содержатся воспоминания о первичном океане, месте в котором зародилась жизнь, — водном растворе, обеспечивающем саму жизнь.
В любом живом организме постоянно течет по сосудам – артериям, венам и капиллярам – необычный раствор, который составляет основу крови, массовая доля солей в нем такая же, как в первичном океане, – 0,9%. Сложные физико-химические процессы, протекающие в организме человека и животного, также взаимодействуют в растворах. Процесс усвоения пищи связан с переводом высокопитательных веществ в раствор. Природные водные растворы напрямую связаны с процессами почвообразования, снабжением растений питательными веществами. Такие технологические процессы в химической и многих других отраслях промышленности, например производство удобрений, металлов, кислот, бумаги, происходят в растворах. Современная наука занимается изучением свойств растворов. Давайте выясним, что же такое раствор?
Растворы отличаются от других смесей тем, что частицы составных частей располагаются в них равномерно, и в любом микрообъеме подобной смеси состав будет одинаков.
Именно поэтому под растворами понимали однородные смеси, которые состоят из двух или более однородных частей. Такое представление исходило из физической теории растворов.
Приверженцы физической теории растворов, которой занимались Вант-Гофф, Аррениус и Оствальд, считали, что процесс растворения является результатом диффузии.
Д. И. Менделеев и сторонники химической теории считали, что растворение является результатом химического взаимодействия растворенного вещества с молекулами воды. Таким образом, будет точнее определить раствор как однородную систему, которая состоит из частиц растворенного вещества, растворителя, а также продуктов их взаимодействия.
Вследствие химического взаимодействия растворенного вещества с водой образуются соединения – гидраты. Химическое взаимодействие обычно сопровождается тепловыми явлениями. К примеру, растворение серной кислоты в воде проходит с выделением такого колоссального количества тепла, что раствор может закипеть, именно поэтому кислоту льют в воду, а не наоборот. Растворение таких веществ как хлорид натрия, нитрат аммония, сопровождается поглощением тепла.
М. В. Ломоносов доказал, что растворы превращаются в лед при более низкой температуре, чем растворитель.
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
Свойство воды и растворимость веществ в ней
В обычной неассоциированной жидкости, например в такой, как бензин, молекулы свободного скользят одна вокруг другой. В воде же они скорее катятся, чем скользят. Молекулы воды, как известно, соединены между собой водородными связями, поэтому прежде чем произойдет какое-либо смещение, нужно разорвать хотя бы одну из этих связей. Эта особенность и определяет вязкость воды.
Диэлектрической постоянной воды называется ее способность нейтрализовать притяжение, существующее между электрическими зарядами. Растворение твердых веществ в воде — сложный процесс, который обусловливается взаимодействием частиц растворенного вещества и частиц воды.
При изучении строения веществ с помощью рентгеновских лучей было установлено, что большинство твердых тел имеет кристаллическое строение, т. е. частицы вещества расположены в пространстве в определенном порядке. Частицы одних веществ расположены так, будто бы они находятся в углах крошечного куба, частицы других — в углах, центре и в середине сторон тетраэдра, призмы, пирамиды и пр. Каждая из этих форм является мельчайшей ячейкой более крупных кристаллов аналогичной формы. У одних веществ в узлах их кристаллической решетки находятся молекулы (у большинства органических соединений), у других (например, у неорганических солей) — ионы, т. е. частицы, состоящие из одного или нескольких атомов, имеющих положительные или отрицательные заряды. Силами, удерживающими ионы в определенном, ориентированном в пространстве порядке кристаллической решетки, являются силы электростатического притяжения разноименно заряженных ионов, составляющих кристаллическую решетку.
Если, например, растворить в воде хлористый натрий, то положительно заряженные ионы натрия и отрицательно заряженные ионы хлора будут отталкиваться друг от друга.
Это отталкивание происходит потому, что у воды высокая диэлектрическая постоянная, т. е. выше, чем у любой другой жидкости. Она уменьшает силу взаимного притяжения между противоположно заряженными ионами в 100 раз. Причину сильно нейтрализующего действия воды нужно искать в расположении ее молекул. Водородный атом в них не делит поровну свой электрон с тем атомом кислорода, к которому он прикреплен. Этот электрон всегда ближе к кислороду, чем к водороду. Поэтому водородные атомы заряжены положительно, а кислородные — отрицательно.
Когда какое-либо вещество, растворяясь, распадается на ионы, кислородные атомы притягиваются к положительным ионам, а водородные — к отрицательным. Молекулы воды, окружающие положительный ион, направляют к нему свои кислородные атомы, а молекулы, которые окружают отрицательный ион, устремляются к нему своими атомами водорода. Таким образом молекулы воды образуют как бы решетку, которая отделяет ионы друг от друга и нейтрализует их притяжение (рис. 12). Чтобы оторвать друг от друга ионы, находящиеся в кристаллической решетке, и перевести их в раствор, необходимо преодолеть силу притяжения этой решетки. При растворении солей такой силой является притяжение ионов решетки молекулами воды, характеризуемое так называемой энергией гидратации. Если при этом энергия гидратации по сравнению с энергией кристаллической решетки будет достаточно велика, то ионы будут отрываться от последней и перейдут в раствор.
Взаимосвязь между молекулами воды и ионами, оторванными от решетки, в растворе не только не ослабевает, а становится еще теснее.
Рис. 12. Разрушение ионной решетки кристалла NaCl полярными молекулами воды при растворении.
Как уже отмечалось, в растворе ионы окружаются и разобщаются молекулами воды, которые, ориентируясь на них своими противоположными по заряду частями, образуют так называемую гидратную оболочку (рис. 13). Величина этой оболочки различна у разных ионов и зависит от заряда иона, его размера и, кроме того, от концентрации ионов в растворе.
В продолжение нескольких лет физико-химики изучали воду в основном как растворитель электролитов. В результате получено много сведений об электролитах, но очень мало о самой воде. Как ни странно, но только в последние годы появились работы, посвященные изучению отношения воды к веществам, которые в ней практически не растворяются.
Наблюдалось немало поразительных явлений. Например, однажды труба, по которой шел природный газ при t = 19°С, оказалась забитой, мокрым снегом с водой. Стало ясным, что дело здесь не в температуре, а в других свойствах воды. Возник ряд вопросов: почему вода замерзла при столь высокой температуре, как вода могла соединиться с веществами, которые в ней нерастворимы.
Эта тайна еще не была раскрыта, когда обнаружилось, что даже такие благородные газы, как аргон и ксенон, которые не вступают ни в какие химические реакции, могут связываться с водой, образуя некоторое подобие соединений.
Рис. 13. Разъединение ионов Na+ и С1— полярными молекулами воды, образующими вокруг них гидратную оболочку.
Интересные результаты по растворимости в воде метана были получены в Иллинойсе. Молекулы метана не образуют ионов в воде и не воспринимают водородных связей; притяжение между ними и молекулами воды очень слабое. Однако метан все же, хотя и плохо, растворяется в воде, и его диссоциированные молекулы образуют с ней соединения — гидраты, в которых несколько молекул воды присоединены к одной молекуле метана. При этой реакции высвобождается в 10 раз больше тепла, чем при растворении метана в гексане (метан растворяется в гексане лучше, чем в воде).
Факт растворения метана в воде представляет большой интерес. Ведь по объему молекула метана вдвое больше молекулы воды. Чтобы метан растворился в воде, между ее молекулами должны образоваться довольно большие «дырки». Для этого требуется значительная затрата энергии, большая чем для испарения воды (примерно 10 000 калорий на каждый моль). Откуда же появляется столько энергии? Силы притяжения между молекулами метана и воды слишком слабы, они не могут дать столько энергии. Поэтому существует другая возможность: структура поды изменяется в присутствии метана. Предположим, что молекула растворенного метана окружена оболочкой из 10-20 молекул воды. При образовании таких ассоциаций молекул выделяется теплота. В пространстве, занятом молекулой метана, исчезают силы взаимного притяжения между молекулами воды, а значит, и внутреннее давление. В таких условиях, как мы видели, вода замерзает при температуре выше нуля.
Вот почему молекулы, находящиеся в промежутке между метаном и водой, могут кристаллизоваться, что и произошло в описанном выше случае. Замороженные гидраты могут поглощаться раствором и выделяться из него. Эта теория известна как теория айсбергов. Практически, как показывают исследования, все непроводящие вещества, которые подвергались испытанию, образуют устойчивые кристаллические гидраты. В то же время у электролитов такая тенденция выражена слабо. Все это ведет к совершенно новому пониманию растворимости.
Считалось, что растворение электролитов происходит в результате действия сил притяжения. Теперь же доказано, что растворение неэлектролитов происходит не благодаря силам притяжения между этими веществами и водой, а в результате недостаточного притяжения между ними. Вещества, не распадающиеся на ионы, соединяются с водой, так как они устраняют внутреннее давление и тем самым способствуют появлению кристаллических образований.
Чтобы лучше понять образование таких гидратов, целесообразно рассмотреть их молекулярную структуру.
Доказано, что образующиеся гидраты имеют кубическую структуру (решетку) в отличие от гексагональной структуры льда. Дальнейшие работы исследователей показали что гидрат может иметь две кубические решетки: в одной из них промежутки между молекулами равны 12, в другой — 17 А. В меньшей решетке 46 молекул воды, в большей 136. Дырки молекул газа в меньшей решетке имеют 12-14 граней, а в большей — 12-16, к тому же они разнятся по своим размерам и заполняются молекулами различной величины, причем могут быть заполнены не все дырки. Такая модель с большой степенью точности объясняет действительное строение гидратов.
Роль таких гидратов в жизненных процессах трудно переоценить. Эти процессы происходят в основном в промежутках между молекулами воды и протеина. Вода при этом имеет сильную тенденцию к кристаллизации, так как в протеиновой молекуле содержится много неионных, или неполярных, групп. Всякий такой гидрат образуется при меньшей плотности, чем лед, поэтому его образование может вести к значительному разрушительному расширению.
Итак, вода — это своеобразное и сложное вещество с определенными и разнообразными химическими свойствами. Она имеет стройную и в то же время меняющуюся физическую структуру.
Развитие всей живой и в значительной части неживой природы неразрывно связано с характерными особенностями воды.
www.comodity.ru
Растворение. Растворимость веществ в воде.Вода, столь широко распространенная в природе, всегда содержит растворенные вещества. В пресной воде рек и озер их мало, в то время как в морской воде содержится 3,5% растворенных солей. В первичном океане (во время появления жизни на Земле) массовая доля солей, по предположениям, была низка, около 1%. «Именно в этом растворе впервые развились живые организмы, и из этого раствора они получили ионы и молекулы, необходимые для их роста и жизни… С течением времени живые организмы развивались и изменялись, что позволило им покинуть водную среду и перейти на сушу и затем подняться в воздух. Они приобрели эту способность, сохранив в своих организмах водный раствор в виде жидкостей, содержащих необходимый запас ионов и молекул», — вот так оценивает роль растворов в возникновении и развитии жизни на Земле известный американский химик, лауреат Нобелевской премии Лайнус Полит. Внутри нас, в каждой нашей клеточке — воспоминание о первичном океане, в котором зародилась жизнь, — водные растворы, обеспечивающие саму жизнь. В каждом живом организме бесконечно течет по сосудам — артериям, венам и капиллярам — волшебный раствор, составляющий основу крови, массовая доля солей в нем такая же, как в первичном океане — 0,9%. Сложные физико-химические процессы, происходящие в организмах человека и животных, также протекают в растворах. Усвоение пищи связано с переводом питательных веществ в раствор. Природные водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами. Многие технологические процессы в химической и других отраслях промышленности, например получения соды, удобрений, кислот, металлов, бумаги, протекают в растворах. Изучение свойств растворов занимает очень важное место в современной науке. Отличие раствора от других смесей в том, что частицы составных частей распределяются в нем равномерно, и в любом микрообъеме такой смеси состав одинаков. Растворимость веществ в воде зависит от температуры. Как правило, растворимость твердых веществ в воде увеличивается с повышением температуры, а растворимость газов — уменьшается, поэтому воду можно почти полностью освободить от растворенных в ней газов кипячением? Сколько бы мы не перемешивали раствор с остатком нерастворившейся соли, больше соли не раствориться — раствор будет насыщен этой солью при данной температуре. И этот раствор будет называется насыщенным. Ненасыщенным называется раствор, в котором при данной температуре вещество больше не растворяется. Если же при этой температуре в воде растворить соли меньше, то раствор будет ненасыщенным. Ненасыщенным называется такой раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе. При охлаждении насыщенного раствора возникает избыток растворенного вещества, если оно де выпадает в осадок, то образуется пересыщенный раствор.Пересыщенным называется такой раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях. При работе с различными веществами важно знать их растворимость в воде. Вещество считается хорошо растворимым, если при комнатной температуре в 100 г воды растворяется больше 10 г этого вещества. Если при таких условиях растворяется меньше 1 г вещества в 100 г воды, то такое вещество считается малорастворимым. К веществам практически нерастворимым относятся такие, растворимость которых меньше 0,01 г в 100 г водыЛтабл. 9). Совершенно нерастворимых веществ в природе не существует. Например, даже серебро и золото чуть-чуть растворяются в воде. Как известно, растворы золота или серебра в воде убивают микробов. |
slavavode.ucoz.ru
