Самостоятельный расчет концентрации растворов | Все своими руками
Опубликовал admin | Дата 28 декабря, 2011Концентрация раствора характеризуется количеством того или иного вещества, растворенного в единице объема воды или другой жидкости. Концентрация раствора в подавляющем большинстве случаев должна быть строго определенной. Поэтому следует отказаться от составления растворов на глазок.
Концентрация растворов выражается:
1) в частях (например. 100 частей воды, 37 частей серной кислоты и 16 частей двухромовокислого калия) или
2) в процентах (например, 21%-ный водный раствор едкого калия). Иногда концентрация раствора выражается отношением (например, водный раствор серной кислоты 1:10; это означает, что нужно взять 1 часть серной кислоты и 10 частей воды). Во всех случаях (части и проценты) имеются в виду весовые соотношения веществ.
Перерасчет водных растворов с процентов по весу на части
Для определения весовых количеств воды можно пользоваться мензуркой, считая число кубических сантиметров соответствующим числу граммов, а для химикатов — аптекарскими весами (достаточна точность до 0,5 г).
При составлении растворов, концентрация которых дана в процентах в таблице, вес раствора принимается за 100%. Поэтому, например, для приготовления 21%-ного раствора едкого калия отмеряют 21 часть этого вещества и 79 частей воды. Такие взвешивания не всегда удобны, поскольку чаще всего приходится исходить из объема или веса необходимого раствора, чтобы не приготовлять его в излишке. Тогда делают арифметические перерасчеты. Однако их можно избежать, если воспользоваться приведенной таблицей, которая позволяет определить, какое количество по весу вещества нужно на 100 частей или 100 см³ воды, если известна концентрация в процентах. Например, на 100 см³ 21%-ного водного раствора едкого калия приходится 26.58 части едкого калия.
Обсудить эту статью на — форуме «Радиоэлектроника, вопросы и ответы».
Просмотров:1 411
www.kondratev-v.ru
Как рассчитать концентрацию вещества
Концентрация раствора – это величина, показывающая, какая масса того или иного вещества содержится в определенном объеме или массе раствора. Даже самый далекий от химии человек сталкивается с этим понятием буквально на каждом шагу: например, покупая в магазине 9% уксус для домашнего консервирования, или 20% сливки, чтобы добавлять их в кофе. Как же вычисляется концентрация раствора?
Спонсор размещения P&G Статьи по теме «Как рассчитать концентрацию вещества» Как записать рациональное выражение концентрации раствора Как найти коэффициент распределения Как вычислить концентрацию веществ1
Предположим, в количестве 200 или 300 миллилитрах воды растворили 58,5 граммов хлористого натрия, то есть хорошо знакомой всем поваренной соли. Потом, приливая воду, довели общую массу раствора до одного килограмма. Несложно догадаться, что раствор в этом случае будет содержать 58,5 граммов соли и 941,5 граммов воды. Какова будет массовая доля соли?
2
Вычислить это проще простого, для этого количество соли разделите на общую массу раствора и умножьте на 100%, это будет выглядеть следующим образом:
(58,5/1000) * 100% = 5,85%.
3
Сформулируйте задачу немного по-другому. Такое же количество соли растворили в воде, потом довели объем раствора до одного литра. Какова будет молярная концентрация раствора?
4
Вспомните само определение молярной концентрации. Это — количество молей растворенного вещества, содержащееся в одном литре раствора. А чему равен моль поваренной соли? Ее формула – NaCl, молярная масса – примерно 58,5. Иными словами, в одном литре раствора у вас содержится ровно один моль соли. Вы получите 1,0 молярный раствор.
5
Ну, а теперь вернитесь к первоначальным условиям задачи – там, где общий вес раствора составил ровно один килограмм. Как вам найти моляльность такого раствора?
6
И здесь тоже нет ничего сложного. Выше вы уже вычислили, что на 58,5 граммов поваренной соли приходится 941, 5 граммов воды. Подставляя известные величины в формулу m = v/M, где m – значение моляльности, v – количество молей вещества в растворе, а M — масса растворителя в килограммах, получите:
1,0/0,9415 = 1,062 моляльный раствор.
Как простоmasterotvetov.com
Процентное содержание — растворенное вещество
Процентное содержание — растворенное вещество
Cтраница 1
Процентное содержание растворенного вещества показывает количество единиц массы вещества, содержащееся в 100 единицах массы, раствора. Так, 12 % — ный раствор КОН должен содержать 12 единиц массы КОН в 100 единицах массы раствора и для его приготовления следует взять 12 единиц массы КОН и 88 единиц массы растворителя. [1]
Процентное содержание растворенного вещества вычисляют следующим образом. Например, 20 г поваренной соли были растворены в ПО г воды. [2]
Процентное содержание растворенного вещества показывает число единиц массы вещества, содержащееся в 100 единицах массы, раствора. Так, 12 % — ный раствор КОН должен содержать 12 ед. [3]
Она выражает 1 / 100 процентного содержания растворенного вещества и растворителя: а) в процентах массы, б) в мольных процентах. [4]
Процентная концентрация по массе выражается процентным содержанием растворенного вещества, отнесенного ко всему раствору. [5]
Зная плотность раствора, по справочнику можно найти процентное содержание растворенного вещества и, если нужно, вычислить концентрацию раствора в необходимых единицах. [6]
Первую производную удельного веса d по р ( процентное содержание растворенного вещества в водном растворе по весу) Менделеев обозначает через А, вторую производную — через В. [7]
Если в таблице нет цифры, точно отвечающей отсчету по шкале ареометра, то процентное содержание растворенного вещества вычисляют методом интерполяции по двум ближайшим величинам. Требуется определить процентное содержание NaOH в растворе. [8]
Если в таблице удельных весов нет величины, точно отвечающей отсчету на шкале ареометра, то процентное содержание растворенного вещества вычисляют из двух ближайших табличных значений. Считая, что в этом промежутке процентное содержание изменяется прямо пропорционально изменению удельного веса, можно сделать следующий расчет. [10]
Рефрактометрами называются приборы, в которых для определения концентрации прозрачных веществ используется зависимость коэффициента преломления раствора от процентного содержания растворенного вещества. Применяются они в химической, нефтеперерабатывающей и пищевой промышленности. На рис. 9 — 9 показана одна из возможных схем фотоэлектрического рефрактометра. [12]
Различают процентную, весовую, молярную и нормальную ( эквивалентную) концентрации. Первая выражает процентное содержание растворенного вещества в массе раствора. [13]
Поплавковые плотномеры основаны на использовании закона Архимеда. Предназначены для измерения плотности жидкости или процентного содержания растворенных веществ в двухкомпонентных растворах. [14]
Весовые ( или массовые) концентрации. Процентная концентрация по весу ( массе) выражается процентным содержанием растворенного вещества, отнесенного ко всему раствору. [15]
www.ngpedia.ru
Расчеты при приготовлении растворов процентной концентрации
При приготовлении растворов процентной концентрации вещество отвешивают на техно-химических весах, а жид- I кости отмеривают мерным цилиндром. Поэтому навеску! вещества рассчитывают с точностью до 0,1 г, а объем 1 жидкости с точностью до 1 мл.
Прежде чем приступить к приготовлению раствора, | необходимо произвести расчет, т. е. рассчитать количество растворяемого вещества и растворителя для приготовления определенного количества раствора заданной концентрации.
РАСЧЕТЫ ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ СОЛЕЙ
Пример 1. Надо приготовить 500 г 5% раствора нитЯ рата калия. 100 г такого раствора содержат 5 г KN03;1 Составляем пропорцию:
100 г раствора—5 г KN03
500 » 1 — х » KN03
5-500 „_ х= -jQg- = 25 г.
Воды нужно взять 500—25 = 475 мл.Пример 2. Надо приготовить 500 г 5% раствора СаСЬ из соли СаС12-6Н20. Вначале производим расчет для безводной соли.
100 г раствора—5 г СаС12 500 » » —х » СаС12 5-500 _ х= 100 =25г—
Мольная масса СаС12 = 111, мольная масса СаС12-•6Н20 = 219*. Следовательно, 219 г СаС12-6Н20 содержат 111 г СаС12. Составляем пропорцию:
219 г СаС12-6Н20-111 г СаС12
х » СаС12-6Н20— 26 » CaCI,
219-25 х = —jjj— = 49,3 г.
Количество воды равно 500—49,3=450,7 г, или 450,7 мл. Так как воду отмеривают мерным цилиндром, то десятые доли миллилитра в расчет не принимают. Следовательно, нужно отмерить 451 мл воды.
РАСЧЕТЫ ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ КИСЛОТ
При приготовлении растворов кислот необходимо учитывать, что концентрированные растворы кислот не являются 100% и содержат воду. Кроме того, нужное количество кислоты не отвешивают, а отмеривают мерным цилиндром.
Пример 1. Нужно приготовить 500 г 10% раствора соляной кислоты, исходя из имеющейся 58% кислоты, плотность которой d=l,19.
1. Находим количество чистого хлористого водорода, которое должно быть в приготовленном растворе кислоты:
100 г раствора —10 г НС1 500 » » — х » НС1 500-10 * = 100 = 50г—
* Для расчета растворов процентной концентрации мольную, массу округляют до целых чисел.
2. Находим количество граммов концентрированной }
кислоты, в котором будет находиться 50 г НС1:
100 г кислоты—38 г НС1 х » » —50 » НС1 100•50
X gg— » = 131 ,6 Г.
3. Находим объем, который занимает это количество 1
кислоты:
V — — — 131‘6 1106щ
4. Количество растворителя (воды) равно 500—;
—131,6 = 368,4 г, или 368,4 мл. Так как необходимое ко-
личество воды и кислоты отмеривают мерным цилинд-
ром, то десятые доли миллилитра в расчет не принима-
ют. Следовательно, для приготовления 500 г 10% раство-
ра соляной кислоты необходимо взять 111 мл соляной I
кислоты и 368 мл воды.
Пример 2. Обычно при расчетах для приготовления кислот пользуются стандартными таблицами, в которых указаны процент раствора кислоты, плотность данного раствора при определенной температуре и количество граммов этой кислоты, содержащееся в 1 л раствора данной концентрации (см. приложение V). В этом случае расчет упрощается. Количество приготовляемого раствора кислоты может быть рассчитано на определенный объем.
Например, нужно приготовить 500 мл 10% раствора соляной кислоты, исходя из концентрированного 38% j раствора. По таблицам находим, что 10% раствор соляной кислоты содержит 104,7 г НС1 в 1 л раствора. Нам I нужно приготовить 500 мл, следовательно, в растворе должно быть 104,7:2 = 52,35 г НО.
Вычислим, сколько нужно взять концентрированной I кислоты. По таблице 1 л концентрированной НС1 содержит 451,6 г НС1. Составляем пропорцию: 1000 мл—451,6 г НС1 х » —52,35 » НС1
1000-52,35 х= 451,6 =»5 мл.
Количество воды равно 500—115 = 385 мл.
Следовательно, для приготовления 500 мл 10% раствора соляной кислоты нужно взять 115 мл концентрированного раствора НС1 и 385 мл воды.
505days.com
концентрация, массовая доля. Определение, расчет и рекомендации
Массовая концентрация раствора является одним из распространенных понятий в современной химии. В статье мы выявим особенности растворов, их виды, применение. Отметим некоторые примеры расчета разных видов концентраций.
Особенности растворов
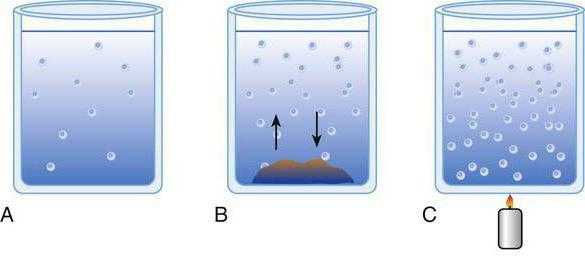
Раствор — это однородная система, имеющая переменный состав. Из двух компонентов раствора один всегда выступает в качестве среды. Именно в ней будут растворяться структурные фрагменты других веществ. Ее называют растворителем, внутри которого и располагаются молекулы растворенного вещества.
Если смешивается два газообразных вещества, то в таком случае не выделяют растворителя. Для каждой конкретной ситуации всегда проводятся специальные расчеты.
Получение однородных систем
Для получения однородных растворов необходимо дробление растворенных веществ до структурных единиц. Только в таком случае системы будут истинными. При раздроблении до небольших капелек, песчинок, которые будут распределяться в среде, получают коллоидные растворы, эмульсии, суспензии.
Применение растворов
Кстати, в строительстве смесь песка, цемента, воды тоже называют раствором, но с химической точки зрения он представляет собой суспензию. Практическое значение растворов можно объяснить по разным причинам.
Химические реакции в жидких растворах происходят в объеме растворителя. Это делает их доступными для реакции без любого дополнительного действия на систему. В смеси, содержащей твердые частицы, невозможно провести реакцию в полном объеме. Чтобы ускорить процесс, потребуется соприкосновение частиц в некоторых точках. Для повышения скорости реакции перетирают кристаллы в ступке, затем их прессуют. Но не сразу можно достигнуть полноты протекания процесса.
В растворе же протекает процесс иначе. Молекулы движутся свободно, при их столкновениях происходят химические превращения. Энергия, которая начинает выделяться в таком взаимодействии, аккумулируется растворителем, система практически не разогревается.

Физические свойства и концентрация растворов
Массовая доля вещества позволяет определять количественное соотношение растворенного вещества и растворителя, взятое для их приготовления. Металлические сплавы, кстати, тоже являются растворами, но твердыми, характеризующимися определенными физическими параметрами.
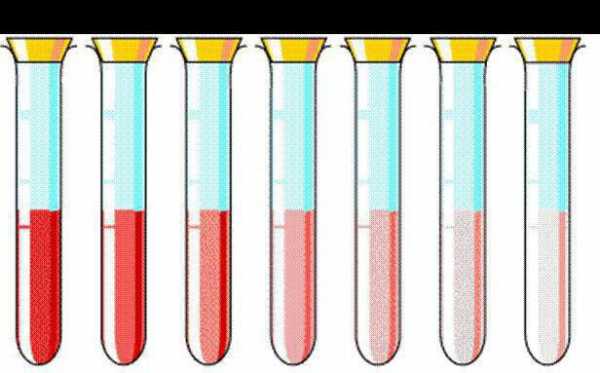
Растворы обладают способностью менять силы действия растворенного компонента. Это делает их востребованными в сельском хозяйстве, медицине. Например, раствор марганцовки (перманганата калия) используют для обработки ссадин и ран в средней концентрации. Но практическое значение имеет и его незначительная концентрация. Так, массовая доля вещества 2-3% придает раствору слабо-розовый цвет, востребованный для промывания желудка.
Темные фиолетовые кристаллы перманганата калия не применяют в медицинских целях, поскольку они обладают сильными окислительными свойствами. Вообще, интенсивность окраски напрямую связана с тем, какова его концентрация. Массовая доля вещества позволяет регулировать токсичность готового раствора.

Массовая доля
Как вычисляется подобная концентрация? Массовая доля вещества характеризуется отношением массы вещества к массе раствора, взятого в процентах. На их органолептические свойства оказывает влияние не только то, что будет растворяться, но и количественный показатель. Например, для слабого раствора поваренной соли почти не характерен привкус, а при больших концентрациях он проявляется в разной степени.
Как на практике определяется концентрация? Массовая доля вещества в растворе рассматривается в школьном курсе неорганической химии. Задачи на ее определение включены в тестовые задания для выпускников 9 класса.
Приведем пример задания, в котором используется концентрация.
Массовая доля поваренной соли 25%. Масса раствора 250 граммов. Определите массу воды, содержащейся в нем. Для проведения вычислений сначала нужно выяснить массу вещества. Исходя из пропорции, получаем, что вещества в растворе 62,5 грамма. Для определения массы воды нужно вычесть из 250 граммов массу самого вещества, в результате получаем 187,5 г.

Виды концентраций
Что такое концентрация? Массовых долей в растворе может содержаться не более ста процентов. В химии термин «концентрация» предполагает некое содержание растворенного вещества. Существует несколько ее вариантов: молярная, массовая концентрация.
Например, если необходимо приготовить раствор из 80 граммов воды и 20 граммов поваренной соли и определить массовые доли вещества в растворе, сначала нужно определить массу раствора. Она составит сто граммов. Процентное содержание вещества получается 20 процентов.
Мы проанализировали, что представляет собой массовая доля. Молярная концентрация предполагает отношение количества вещества к объему взятого раствора. Чтобы приготовить раствор с заданной молярной концентрацией, сначала определяют массу вещества. Затем взвешивают его нужное количество и растворяют в литре растворителя.
Расчет молярной концентрации
Так, для приготовления 2 литров раствора с концентрацией 0,15 моль/л сначала рассчитывают массу соли, которая содержится в растворе. Для этого нужно разделить 0,15 моль на 2 литра, получаем 0,075 моль. Теперь вычисляем массу: 0,075 моль умножаем на 58,5 г/моль. Результат — 4,39 г.
Задачи аналитической химии
В качестве прикладной химической задачи рассматривают анализ. С его помощью выявляют состав смеси, проводят диагностические пробы, анализируют горные породы. Для этого нужно определять качественный и количественный состав раствора.
Среди тех задач, которые чаще всего встречаются в неорганической химии, выделим определение концентрации одного вещества по заданной величине у другого вещества. С помощью опытов можно осуществить постепенное добавление к раствору, у которого известна молярная концентрация, искомого раствора. Данный процесс называется титрованием.
Растворимость и растворители
Самым распространенным растворителем является вода. В ней отлично растворяются основания, кислоты, соли, некоторые органические соединения. Именно водные растворы являются самыми распространенными в природе системами. Вода выполняет функцию биологического растворителя. Она считается основой для протекания многих сред: крови, цитозолей, межклеточных жидкостей. Многие типы животных и растений живут именно в водной среде.
Растворимостью называют свойство вещества растворяться в выбранном растворителе. Это сложное явление, которое требует учета определенных нюансов и особенностей строения растворителя.
В качестве хороших органических веществ можно отметить спирты. Они в свой состав включают гидрокисльные группы, поэтому имеют высокую растворимость.

Заключение
Любая жидкость может рассматриваться в качестве растворителя. Именно поэтому часто ведут речь о взаимной растворимости разных жидких веществ. К примеру, среди органических веществ можно упомянуть о растворимости в воде сложных эфиров.
Различные виды концентраций, используемые в неорганической и органической химии, помогают проводить качественные и количественные определения веществ. Теория растворов востребована в аналитической химии, фармацевтике и современной медицине.
fb.ru
Примеры расчета концентрации растворов
1. Сколько граммов гидроксида натрия потребуется для приготовления 2 л 20%-ного раствора?
Решение. Согласно таблице относительных плотностей, плотность 20%-ного раствора гидроксида натрия – 1,225. Масса 2 л раствора равна:
m = V ·ρ = 2000 · 1,225 = 2450 г.
В 100 г 20%-ного р-ра – 20 г NaOH.
В 2450 г 20%-ного р-ра – x NaOH.
x = 490 г NaOH.
2. Сколько воды необходимо прибавить к 200 мл 68%-ного раствора азотной кислоты (относительная плотность 1,4), чтобы получить 10%-ный раствор кислоты?
Решение. Согласно таблице относительных плотностей 68%-ная азотная кислота имеет плотность 1,4. Масса HNO3 в 200 мл 68%-ного раствора:
В 100 г р-ра – 68 г HNO3.
В 200 · 1,4 г р-ра – x HNO3
x = 190,4 г.
Эта же масса HNO3составит 10% массы разбавленного раствора. Масса 10%-ного раствора HNO3:
В 100 г 10%-ного р-ра – 10 г HNO3.
В x г 10%-ного р-ра – 190,4 г HNO3
x = 1904 г.
Для разбавления исходного раствора кислоты необходимо 1624 г или 1624 мл воды (1904 – 280).
3. Сколько миллилитров 96%-ной серной кислоты (относительная плотность 1,84) необходимо взять для приготовления 2 л 0,5 н раствора?
Решение. Эквивалентная масса серной кислоты равна 49 г. В 1 л 0,5 н раствора содержится 24,5 г, а в 2 л раствора – 49 г серной кислоты.
Масса 96%-ного раствора серной кислоты, в котором содержится 49 г сульфата водорода:
В 100 г р-ра – 96 г H2SO4.
В x г р-ра – 49 г H2SO4.
x = 51,04 г.
Объем 51,04 г 96%-ного раствора H2SO4:
4. Рассчитайте объем 40%-ной фосфорной кислоты (ρ = 1,25 г/см3), который потребуется для приготовления 300 мл раствора с массовой долей кислоты 5% (ρ = 1,03 г/см3)?
Решение. Вычислим массу 300 мл раствора с массовой долей фосфорной кислоты 0,05 (5%): m = V · ρ:
mр-ра= 1,03 · 300 = 309 г.
Определим массу фосфорной кислоты, необходимую для приготовления 300 мл такого раствора: W = m в –ва / m p -ра
m в — ва= ω (H3PO4) · mp -ра,
m в — ва = 0,05 · 309 = 15,45 г.
Находим, какая масса раствора 40%-ной фосфорной кислоты (m в — ва = 0,4) содержит 15,45 г Н3РО4: m = m в — ва / ω:
m р—ра= 15,45 / 0,4 = 38,63 г.
Рассчитаем V1, занимаемый 38,63 г 40%-ной фосфорной кислоты:
V = mр / ρ,
V((H3PO4) = 38,63 / 1,25 = 30,9 мл.
5. К 250 г 18%-ного раствора LiCl добавили 6 г этой же соли. Какова стала массовая доля соли в растворе?
Решение. Вычислим массу LiCl, содержащуюся в исходном растворе:
ω = m в—ва / mp-ра,
mp = 250 · 0,18 = 45 г.
После добавления 6 г масса LiCl стала:
m(LiCl) = 45 + 6 = 51 г.
Масса раствора тоже изменилась:
m = 250 + 6 = 256 г.
Находим массовую долю LiCl в полученном растворе:
ω = m(LiCl) / mp-ра,
ω = 51 / 256 ·100%= 20%.
6. Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42,6 г в воде массой 300 г, если плотность раствора равна 1,12 г/мл.
Решение. Определим массу полученного раствора:
mp-ра = m(Na2SO4) + m(H2O) = 42,6 + 300 = 342,6 г.
Рассчитаем объем раствора:
V = m/ ρ
V = 342,6 / 1,12 = 306 мл = 0,306 л.
Количество вещества Na2SO4 равно:
v(Na2SO4) = m(Na2SO4) / M(Na2SO4).
v(Na2SO4) = 42,6 / 142 = 0,3 моль.
Определяем молярную концентрацию раствора:
См = v(Na2SO4) / Vр—ра.
См = 0,3 / 0,306 = 0,98 моль / литр.
studfiles.net
Способы выражения содержания растворенного вещества в растворе. Растворимость
Содержание растворенного вещества в растворе может быть выражено либо безразмерными величинами-долями или процентами, либо величинами размерными — концентрациями. Далее приведены употребляемые в химии способы выражения содержания растворенного вещества в растворе:
| Способ выражения содержания растворенного вешества в растворе | Определение |
| Массовая доля (С) | Процентное отношение массы растворенного вещества к общей массе раствора ( С= 9,2 %) |
| Мольная доля (N ) | Отношение количества растворенного вещества (или растворителя) к сумме количеств всех веществ, находящихся в растворе. Например, в системе, состоящей из растворителя и единственного растворенного вещества, мольная доля последнего (N2) равна N = n /(n + n ), а мольная доля растворителя N = 1 — N , где n и n — соответственно количество растворителя и количество растворенного вещества. |
| Молярная концентрация или молярность (С или М) | Отношение количества растворенного вещества к объему раствора; например, 1,5 М раствор или С =1,5 моль/ л. |
| Моляльная концентрация или моляльность (m) | Отношение количества растворенного вещества к массе растворителя; например, m = 2 моль/кг (Н О). |
| Эквивалентная концентрация или нормальность (СН или н.) | Отношение числа эквивалентов растворенного вещества к объему раствора; например: 0,75 н. раствор или СН = 0,75 моль/ л. |
ПРИМЕР 1. Найти массы воды и медного купороса CuSO4× 5Н2О, необходимые для приготовления одного литра раствора, содержащего 8% (масс.) безводной соли. Плотность 8% раствора СuSO4 равна 1,084 г/ мл.
Решение. Масса 1 л полученного раствора будет составлять
1,084 × 1000 = 1084 г. В этом растворе должно содержаться 8% безводной соли, т. е. 1084 × 0,08 = 86,7 г. Массу CuSO × 5 Н О (мольная масса 249,7 г/ моль), содержащую 86,7 г безводной соли (мольная масса 159,6 г/ моль), найдем из пропорции:
249,7 : 159,6 = Х : 86,7 ; Х = 249, 7 × 86,7 / 159,6 = 135,6 г.
Необходимая для приготовления масса воды составит:
1084 — 135,6 = 948,4 г.
ПРИМЕР 2. Найти моляльность, нормальность и молярность
15%-ного (по массе ) раствора Н SO (r=1,10 г/ мл).
Решение. Для вычисления моляльности найдем сначала массу серной кислоты, приходящуюся на 100 г воды:
1000: 85 = Х : 15 ; X = 15 × 1000/ 85 = 176,5 г.
Мольная масса серной кислоты равна 98г/ моль; следовательно:
m = 176,5 / 98 = 1,80 моль/ кг.
Для расчета нормальности и молярности раствора найдем массу серной кислоты, содержащуюся в 1000 мл (т.е. в 1000 × 1,1 = 1100 г) раствора:
1100 : 100 = У : 15 ; У = 1100 × 15/ 100 = 165 г
Эквивалентная масса серной кислоты равна 49 г./ моль. Следовательно:
С = 165/ 49 = 3,37 н. и См = 165/ 98 = 1,68 моль/ л.
Растворимость вещества измеряется содержанием вещества в его насыщенном растворе. Обычно растворимость твердых веществ и жидкостей выражают значением коэффициента растворимости, т.е. массой вещества, растворяющегося при данных условиях в 100 г растворителя с образованием насыщенного раствора.
Растворимость газов часто характеризуют коэффициентом абсорбции, который выражает объем газа, растворяющегося в одном объеме растворителя с образованием насыщенного раствора. Согласно закону Генри, объем растворяющегося газа (а, значит, и коэффициент абсорбции) не зависит при данной температуре от парциального давления газа.
ПРИМЕР 3. Коэффициенты абсорбции кислорода и азота при 273 К равны соответственно 0,049 и 0,023. Газовую смесь, содержащую 20% (об.) кислорода и 80% (об.) азота, взболтали с водой при 273 К до получения раствора. Найти процентное соотношение по объему растворенных в воде газов.
Решение. По условию задачи в 1 л воды растворяется 49 мл кислорода и 23 мл азота. Однако непосредственно сравнивать эти объемы нельзя, так как парциальные давления растворенных газов различны и составляют соответственно 0,2 и 0,8 от общего давления газовой смеси. Если принять последнее за единицу, то объемы растворенных кислорода и азота, приведенные к этому давлению, будут равны :
49 × 0,2= 9,8 мл О и 23 × 0,8 = 18,4 мл N ;
тогда общий объем растворенных газов составит:
9,8 + 18,4 = 28,2 мл.
Находим процентное содержание каждого газа:
9,8 × 100 / 28,2 = 35 % (об.) O и 18,4 × 100/ 28,2 = 65 % (об.) азота.
ЗАДАЧИ 37-42
37. Сколько граммов Na SO потребуется для приготовления 5 л 8%-ного (по массе) раствора (плотность r= 1,075 г/ мл)?
38. Сколько граммов 30%-ного (по массе) раствора NaCl нужно добавить к 300 г воды, чтобы получить 10%-ный раствор соли?
39.Плотность 26%-ного (по массе) раствора КОН равна 24 г/ мл. Сколько молей КОН находится в 5 л раствора?
40. Растворимость хлорида кадмия при 293 К равна 114,1 г в 100 г воды. Вычислить массовую долю и моляльность CdCl в насыщенном растворе.
41. Сколько граммов Na CO содержится в 500 мл 0,25 н. раствора?
42. Газовую смесь, содержащую 40% (об.) N О и 60% (об.) NO, растворяли при 290 К и постоянном давлении в воде до полного насыщения ее. Рассчитать процентный состав (по объему) газовой смеси после выделения ее из воды, если при 290 К коэффициенты абсорбции N O и NO составляют соответственно 0,690 и 0,050.
infopedia.su
