1 Простые и сложные вещества, хим элементы
По элементному составу различают простые вещества, состоящие из атомов одного элемента (H2, O2,Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O,NH3, OF2, H2SO4, MgCl2,K2SO4). Простыми называют такие вещества, которые состоят из атомов одного химического элемента. Сложными называют такие вещества, которые состоят из атомов разных химических элементов.
химический элемент-это определённый вид атома. Все химические элементы представлены в периодической системе химических элементов Д.И.Менделеева. Каждый из них имеет определённый химический знак, или символ и определённое название и произношение, которым вы будете пользоваться при названии формул веществ.
2 Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
ОКСИДЫ И ГИДРОКСИДЫ
К этому классу относятся минералы, представляющие собой соединения различных элементов с кислородом, а в гидроксидах присутствует также и вода. По количеству входящих в него минералов он стоит на одном из первых мест, на его долю приходится около 17% массы всей земной коры (из них на долю оксидов кремния – около 12,5 % и оксидов железа – 3,9%). Минералы этого класса образуются как в эндогенных, так и в экзогенных условиях.Для минералов этой группы преобладает ионный тип химической связи. Кристаллохимические структуры характеризуются обычно тетраэдрической или октаэдрической группировкой кислорода и гидроксильных групп.
3
КИСЛОТЫ И СОЛИ
Кислоты — сложные вещества, состоящие из атомов водорода и кислотного остатка. (С точки зрения теории электролитической диссоциации: кислоты — электролиты, которые при диссоциации в качестве катионов образуют только H+).
Классификация:
1. По составу : бескислородные и кислородсодержащие.
2. По числу атомов водорода, способных замещаться на металл : одно-, двух-, трёхосновные…
Соли — сложные вещества, которые состоят из атомов металла и кислотных остатков. Это наиболее многочисленный класс неорганических соединений.
Классификация: средние, кислые, основные, двойные, смешанные, комплексные.
-
4 Закон сохранения массы веществ. Закон постоянства состава
Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции. С законом сохранения массы веществ тесно связан закон сохранения энергии: энергия не возникает из ничего и не исчезает бесследно, но одни ее виды могут превращаться в другие в строго эквивалентных количествах. Так при разложении воды, кислот, щелочей или солей посредством электрического тока электрическая энергия превращается в химическую. То же наблюдается при зарядке аккумулятора. Обратный процесс — превращение химической энергии в электрическую — происходит при разрядке аккумулятора. Тепловые эффекты химических реакций таковы по своей величине, что изменение массы веществ в их результате не могут быть измерены. Поэтому закон сохранения массы веществ соблюдается практически при всех химических реакциях.
Закон сохранения массы послужил основой для изучения количественного состава различных химических соединений. Многочисленные опыты показали, что качественный и количественный состав сложных различных веществ постоянны и не зависят от способа их получения.
studfiles.net
Основные понятия и законы химии
16
1 Основные понятия химии.
Химия относится к естественным наукам. Она изучает состав, строение, свойства и превращения веществ, а также явления, сопровождающие эти превращения.
Вещество является одной из основных форм существования материи. Вещество как форма материи состоит из отдельных частиц различной степени сложности и обладает собственной массой, так н а з ы в а е м о й
массой покоя.
-
Простые и сложные вещества. Аллотропия.
Все вещества можно
разделить на
Простые вещества состоят из атомов одного химического элемента, сложные — из атомов нескольких химических элементов.
Химический элемент — это определенный вид атомов с одинаковым зарядом ядра. Следовательно, атом — это мельчайшая частица химического элемента.
Понятие простое вещество нельзя отождествлять с понятием
химический элемент. Химический элемент характеризуется определенным положительным зарядом ядра атома, изотопным составом, химическими свойствами. Свойства элементов относятся к его отдельным атомам. Простое вещество характеризуется определенной плотностью, растворимостью, температурами плавления и кипения и т.п. Эти свойства относятся к совокупности атомов и для разных простых веществ они различны.
Простое вещество — это форма существования химического элемента в свободном состоянии. Многие химические элементы образуют несколько простых веществ, различных по строению и свойствам. Это явление называется аллотропией, а образующие вещества — аллотропными видоизменениями. Так, элемент кислород образует две аллотропные модификации — кислород и озон, элемент углерод — алмаз, графит, карбин, фуллерен.
Явление аллотропии вызывается двумя причинами: различным числом атомов в молекуле (например, кислород О2 и азон О3) либо образованием различных кристаллических форм (например, углерод образует следующие аллотропные модификации: алмаз, графит, карбин, фуллерен), карбин был открыт в 1968г (А.Сладков, Россия), а фуллерен в 1973 г теоретически (Д.Бочвар, Россия), а в 1985г — экспериментально (Г.Крото и Р.Смолли, США).
Сложные вещества состоят не из простых веществ, а из химических элементов. Так водород и кислород, входящие в состав воды, содержатся в воде не в виде газообразных водорода и кислорода с их характерными свойствами, а в виде элементов — водорода и кислорода.
Мельчайшей частицей веществ, имеющих молекулярную структуру, является молекула, которая сохраняет химические свойства данного вещества. Согласно современным представлениям из молекул состоят в основном вещества, находящиеся в жидком и газообразном состоянии. Большинство же твердых веществ (в основном неорганических) состоит не из молекул, а из других частиц (ионов, атомов). Не имеют молекулярной структуры соли, оксиды металлов, алмаз, металлы и пр.
-
Относительная атомная масса
Современные методы исследования позволяют определить чрезвычайно малые массы атомов с большей точностью. Так, например, масса атома водорода составляет 1,674 10-27 кг, углерода – 1,993 10-26 кг.
В химии традиционно используются не абсолютные значения атомных масс, а относительные. В 1961г за единицу атомной массы принята атомная единица массы (сокращенно а.е.м.), которая представляет собой 1/12 часть массы атома изотопа углерода 12С.
Большинство химических элементов имеют атомы с различной массой (изотопы). Поэтому относительной атомной массой (или просто атомной массой) Аr химического элемента называется величина, равная отношению средней массы атома элемента к 1/12 массы атома углерода 12С.
Атомные массы элементов обозначают Аr, где индекс r – начальная буква английского слова
Относительная атомная масса – одна из основных характеристик химического элемента.
studfiles.net
Простые и сложные вещества
1. Простыми называются вещества, которые состоят из атомов одного химического элемента (О2, Н2, Na, Al)
2. Сложными называются вещества, которые состоят из нескольких химических элементов (H2O, CuSO4)
3. Оксиды — сложные вещества, которые состоят из атомов двух химических элементов, один из которых кислород со степенью окисления -2.
4. Основные оксиды — оксиды, которым соответствуют основания (CaO — Ca(OH)2)5. Кислотные оксиды — оксиды, которым соответствуют кислоты (P2O5 — H3PO4, Mn2O7 — HMnO4)
6. Амфотерные оксиды — оксиды, проявляющие основные и кислотные свойства (Al2O3, BeO, ZnO, Cr2O3)
7. Несолеобразующие оксиды — не проявляют ни основных ни кислотных свойств (N2O, NO, CO)
8. Кислоты — сложные вещества, которые состоят из атомов водорода и кислотных остатков
HCl — соляная кислота (хлороводородная) (хлориды)
HNO3 — азотная (нитраты)
H2SO4 — серная (сульфаты)
H3PO4 — фосфорная (фосфаты)
H2CO3 — угольная (карбонаты)
H2S — сероводородная (сульфиды)
H2SO3 — сернистая (сульфиты)
H2SiO3 — кремниевая (силикаты)
HF — фтороводородная (плавиковая) (фториды)
HBr — бромоводородная (бромиды)
HNO2 — азотистая (нитриты)
9. Основания — сложные вещества, которые состоят из катиона металла и гидроксид-ионов (NaOH, Fe(OH)3). Растворимые в воде основания называют щелочами.
10. Соли — сложные вещества, которые состоят из катионов металлов и анионов кислотных остатков (NaCl, CuSO4)
Давайте порассуждаем вместе
1. Сульфат алюминия относят к классу:
1) оксидов
2) оснований
3) солей
4) кислот
Ответ: сульфат алюминия Al2(SO4)3 относят к классу солей, т.к. это сложное вещество, которое состоит из катионов металла алюминия и кислотных остатков сульфат-анионов.
2. Кислотой и щелочью соответственно являются вещества, формулы которых:
1) HCl, Cu(OH)2
2) HNO3, Ba(OH)2
3) NaCl, NaOH
4) H2SiO3, Fe(OH)2
Ответ: правильный ответ №2, т.к. HNO3 — это азотная кислота, а Ва(OH)2 — основание, которое хорошо растворяется в воде, значит является щелочью
3. Основному оксиду соответствует формула:
1) SO3
2) NO2
3) MgO
4) P2O5
Ответ: MgO — основный оксид, т.к. ему соответствует основание Mg(OH)2
4. Амфотерным оксидом и кислотным оксидом соответственно явлются вещества:
1) Al2O3, SO2
2) NaOH, P2O5
3) ZnO, HCl
4) Zn(OH)2, H2SO4
Ответ: правильный ответ №1, т.к. Al2O3 — амфотерный оксид, а SO2 — кислотный оксид, ему соответствует сернистая кислота H2SO3
5. Нерастворимым основанием и солью соответственно являются вещества:
1) KOH, Ca(NO3)2
2) CaO, Na2CO3
3) Mg(OH)2, H2SO4
4) Fe(OH)3, AgBr
Ответ: правильный ответ №4, т.к. Fe(OH)3 — нерастворимое основание, а AgBr — бромид серебра — соль
dx-dy.ru
| 1. В каком ряду перечислены два сложных вещества и одно простое: | |
| а) кислород, азот, вода | б) хлор, аммиак, углекислый газ |
| в) водород, бром, углерод | г) алмаз, оксид кремния (IV), медь |
| 2. Аллотропные видоизменения кислорода – озон и кислород – различаются между собой: | |
| а) все ответы верны | б) физическими свойствами |
| в) химическими свойствами | г) количественным составом молекул |
| 3. В каких выражениях речь идет о простом веществе кислород, а не о химическом элементе: | |
| а) кислород входит в состав воды | б) кислород плохо растворяется в воде |
| в) в оксиде меди (II) массовая доля кислорода составляет 20 % | г) все ответы верны |
| 4. Какие утверждения справедливы для понятия «простое вещество»: | |
| а) форма существования химического элемента в природе | б) все ответы верны |
| в) состоит из атомов одного вида | г) простых веществ больше, чем химических элементов |
| 5. Найдите вариант ответа, где указано простое вещество: | |
| 6. К простым веществам относится каждое из двух веществ: | |
| а) натрий и вода | б) хлор и углерод |
| в) кислород и сульфат натрия | г) серная кислота и аммиак |
| 7. В перечне азотная кислота, калий, нитрат кальция, железо, оксид натрия, сульфид бария, фосфора — число формул простых веществ равно: | |
| 8. К сложным веществам относятся: | |
| 9. Аллотропные модификации углерода: | |
| г) все ответы верны | |
| 10. Благородные газы: | |
| г) все ответы верны | |
himiy88.blogspot.com
§ 1.5. Простые и сложные вещества. Аллотропы. Вещества и смеси.
В предыдущей главе было сказано, что образовывать связи друг с другом могут не только атомы одного химического элемента, но также атомы разных элементов. Вещества, образованные атомами одного химического элемента, называют простыми веществами, а вещества, образованные атомами разных химических элементов, — сложными. Некоторые простые вещества имеют молекулярное строение, т.е. состоят из молекул. Например, молекулярное строение имеют такие вещества, как кислород, азот, водород, фтор, хлор, бром, йод. Каждое из этих веществ образовано двухатомными молекулами, поэтому их формулы можно записать как O2, N2, H2, F2, Cl2, Br2 и I2 соответственно. Как можно заметить, простые вещества могут иметь одинаковое название с элементами, их образующими. Поэтому следует четко различать ситуации, когда речь идет о химическом элементе, а когда о простом веществе.
Нередко простые вещества имеют не молекулярное, а атомное строение. В таких веществах атомы могут образовывать друг с другом связи различных типов, которые подробно будут рассмотрены чуть позже. Веществами подобного строения являются все металлы, например, железо, медь, никель, а также некоторые неметаллы — алмаз, кремний, графит и т.д. Для данных веществ обычно характерно не только совпадение названия химического элемента с названием им образованного вещества, но также идентичны запись формулы вещества и обозначения химического элемента. Например, химические элементы железо, медь и кремний, имеющие обозначения Fe, Cu и Si, образуют простые вещества, формулы которых Fe, Cu и Si соответственно. Существует также небольшая группа простых веществ, состоящих из разрозненных атомов, никак не связанных между собой. Такие вещества являются газами, которые называют, ввиду их крайне низкой химической активности, благородными. К ним относятся гелий (Не), неон (Ne), аргон (Аr), криптон (Кr), ксенон (Хе), радон (Rn).
Поскольку только известных простых веществ насчитывается около 500, то логично вытекает вывод о том, что для многих химических элементов характерно явление, называемое аллотропией.
Аллотропия – явление, когда один химический элемент может образовывать несколько простых веществ. Разные химические вещества, образованные одним химическим элементом, называют аллотропными модификациями или аллотропами.
Так, например, химический элемент кислород может образовывать два простых вещества, одно и которых имеет название химического элемента – кислород. Кислород как вещество состоит из двухатомных молекул, т.е. формула его O2. Именно данное соединение входит в состав жизненно необходимого нам воздуха. Другой аллотропной модификацией кислорода является трехатомный газ озон, формула которого O3. Несмотря на то что и озон, и кислород образованы одним химическим элементом, их химическое поведение весьма различно: озон отличается намного большей активностью по сравнению с кислородом в реакциях с теми же веществами. Кроме того, данные вещества отличаются друг от друга по физическим свойствам уже как минимум из-за того, что молекулярная масса озона больше, чем у кислорода в 1,5 раза. Это приводит к тому, что его плотность в газообразном состоянии также больше в 1,5 раза.
Многие химические элементы склонны образовывать аллотропные модификации, отличающиеся друг от друга особенностями строения кристаллической решетки. Так, например, на рисунке 5, вы можете видеть схематичные изображения фрагментов кристаллических решеток алмаза и графита, которые являются аллотропными модификациями углерода.
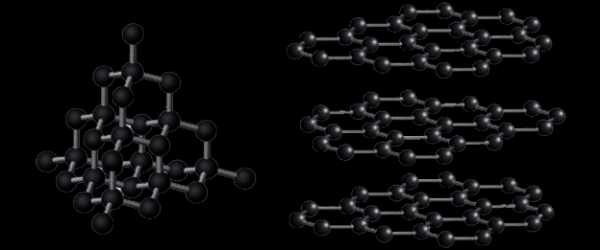
Рисунок 5. Фрагменты кристаллических решеток алмаза (а) и графита (б)
Кроме того, углерод может иметь и молекулярное строение: такая структура наблюдается у такого типа веществ, как фуллерены. Вещества данного типа образованы молекулами углерода сферической формы. На рисунке 6 представлены 3D модели молекулы фуллерена с60 и футбольного мяча для сравнения. Обратите внимание на их интересное сходство.
Рисунок 6. Молекула фуллерена С60 (а) и футбольный мяч (б)
Сложные вещества — это вещества, которые состоят из атомов разных элементов. Они так же, как и простые вещества, могут иметь молекулярное и немолекулярное строение. Немолекулярный тип строения сложных веществ может быть более разнообразен, нежели у простых. Любые сложные химические вещества могут быть получены либо прямым взаимодействием простых веществ, либо последовательностью их взаимодействий друг с другом. Важно осознавать один факт, который заключается в том, что свойства сложных вещества как физические, так и химические сильно отличаются от свойств простых веществ, из которых они получены. Например, поваренная соль, имеющая форуму NaCl и представляющая собой бесцветные прозрачные кристаллы, может быть получена взаимодействием натрия, являющегося металлом с характерными для металлов свойствами (блеск и электропроводность), с хлором Cl2 — газом желто-зеленого цвета.
Серная кислота H2SO4 может быть образована серией последовательных превращений из простых веществ — водорода H2, серы S и кислорода O2. Водород — газ легче воздуха, образующий с воздухом взрывчатые смеси, сера — твердое вещество желтого цвета, способное гореть, и кислород — газ чуть тяжелее воздуха, в котором могут гореть многие вещества. Серная кислота, которая может быть получена из данных простых веществ, представляет собой тяжелую маслянистую жидкость, обладающая сильными водоотнимающими свойствами, из-за которых обугливает многие вещества органического происхождения.
Очевидно, что помимо индивидуальных химических веществ, бывают также и их смеси. Преимущественно именно смесями различных веществ образован мир вокруг нас: сплавы металлов, продукты питания, напитки, различные материалы, из которых состоят окружающие нас предметы.
Например, воздух, которым мы дышим, состоит в основном из азота N2 (78%), жизненно необходимого нам кислорода (21%), оставшийся же 1% приходится на примеси других газов (углекислый газ, благородные газы и др.).
Смеси веществ разделяют на гомогенные и гетерогенные. Гомогенными смесями называют такие смеси, у которых нет границ раздела фаз. Гомогенными смесями являются смесь спирта и воды, сплавы металлов, раствор соли и сахара в воде, смеси газов и т.д. Гетерогенными смесями называют такие смеси, у которых имеется граница раздела фаз. К смесям такого типа можно отнести смесь песка и воды, сахара и соли, смесь масла и воды и др.
Вещества, из которых состоят смеси, называют компонентами.
Смеси простых веществ в отличие от химических соединений, которые могут быть получены из этих простых веществ, сохраняют свойства каждого компонента.
scienceforyou.ru
Урок 4. Сложные вещества – HIMI4KA
В уроке 4 «Сложные вещества» из курса «Химия для чайников» дадим определение химическим соединениям, рассмотрим различия органических и неорганических соединений, а также выясним, что означает качественный и количественный состав. Напоминаю, что в прошлом уроке «Молекулы и простые вещества» мы рассмотрели, что такое молекулы, простые вещества, а также металлы и неметаллы.

Химические элементы существуют не только в виде свободных атомов и простых веществ. Они также могут входить в состав самых различных химических соединений.
Вещества, состоящие из атомов разных химических элементов, называются сложными веществами или химическими соединениями.
Органические и неорганические вещества
Подавляющее большинство химических веществ — это сложные вещества. Вы уже знаете некоторые из них. Вода, метан, сахар, поваренная соль — сложные вещества. Сложные вещества делятся на две группы — неорганические и органические.
Органические вещества
Все органические вещества объединяет главный признак: в их состав обязательно входят атомы углерода. Кроме углерода, в состав органических веществ чаще всего входят атомы водорода, кислорода, а также азота, фосфора, серы. Почти все органические вещества горючи и легко разлагаются при нагревании. Практически все они имеют молекулярное строение (рис. 41).

Простейшим органическим веществом является природный газ метан. Но вам, наверное, знакомы и такие органические вещества, как сахар (сахароза), уксусная и лимонная кислоты, спирт, крахмал, белки, жиры, пластмассы и т. д. Органических веществ миллионы. Они содержатся во всех животных и растительных организмах (откуда и произошло их название), входят в состав пищи, топлива, лекарств, красителей, самых разнообразных материалов.
Неорганические вещества
Неорганические вещества являются соединениями всех остальных элементов. К неорганическим традиционно относят также несколько веществ, содержащих углерод: углекислый и угарный газы, мел, соду и некоторые другие. Неорганических веществ около 700 тыс., но их общая масса многократно превышает массу органических веществ. Почти все они — твердые вещества немолекулярного строения (рис. 42), входят в состав минералов, почв, горных пород.
Качественный и количественный состав веществ
Каждое вещество характеризуется определенным качественным и количественным составом.
Качественный состав вещества показывает, из атомов каких элементов оно состоит. Например, вода состоит из атомов водорода и кислорода, а метан— из атомов углерода и водорода. Число атомов каждого элемента в составе мельчайшей частицы вещества характеризует его количественный состав. Например, молекула воды состоит из двух атомов водорода и одного атома кислорода, а молекула метана — из одного атома углерода и четырех атомов водорода.
Сложное вещество можно с помощью различных химических методов разложить на несколько новых веществ, и так до тех пор, пока не получатся вещества, каждое из которых будет являться простым. Например, сахар при нагревании разлагается на воду и уголь (углерод):
а воду можно разложить с помощью электрического тока на водород и кислород:
Свойства простых веществ, которые при этом получаются (углерода, кислорода и водорода), совершенно не похожи на свойства сложных веществ — сахара и воды. Это разные вещества с разными свойствами. Свойства сложного вещества не являются суммой свойств простых веществ, которые образуются при его разложении.
Сложные вещества, как и простые, имеют либо молекулярное, либо немолекулярное строение. При этом вещества молекулярного строения могут существовать при обычных условиях в различных агрегатных состояниях. Например, метан — газ, вода — жидкость, сахар — твердое вещество.
Вещества немолекулярного строения при обычных условиях — твердые кристаллы, например поваренная соль, мел. Конечно, при нагревании (иногда до нескольких тысяч градусов) такие вещества плавятся, а затем переходят и в парообразное состояние.
Отличия между сложными веществами и смесями веществ
Необходимо различать сложные вещества и смеси веществ:
| Сложное вещество (химическое соединение) | Смесь веществ |
| Образуется в результате соединения атомов различных элементов между собой (химический процесс) | Образуется в результате смешивания различных веществ (физический процесс) |
| Свойства сложного вещества отличаются от свойств простых веществ, из которых оно получено | Свойства веществ, из которых составлена смесь, не изменяются |
| Имеет определенный качественный и количественный состав | Состав произвольный |
| Разлагается на составные части только в результате химических процессов | Разделяется на составные части с помощью различных физических методов |
Краткие выводы урока:
- Сложными называются вещества, состоящие из атомов разных химических элементов.
- Каждое чистое вещество имеет определенный качественный и количественный состав.
- Свойства сложного вещества отличаются от свойств простых веществ, из которых оно получено.
- Сложные вещества имеют молекулярное или немолекулярное строение.
- Все сложные вещества делятся на органические и неорганические.
Надеюсь урок 4 «Сложные вещества» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Многообразие веществ. Простые и сложные вещества
Многообразие веществ. Простые и сложные вещества. Металлы и неметаллы
Сейчас известно более 20 миллионов веществ. Химики ежедневно синтезируют новые соединения. Вещества могут быть простыми и сложными. В состав простых веществ входят атомы только одного элемента. Вещества, молекулы которых состоят из атомов различных элементов, связанных между собой постоянными соотношениями, называют сложными веществами. Сложные вещества также называют химическими соединениями. Например, в состав кислорода O2 входят атомы только элемента кислорода. Кислород относится к простым веществам. В состав углекислого газа CO2 входят атомы различных элементов: один атом углерода и два атома кислорода. Углекислый газ относится к числу сложных веществ.
Очень важно различать понятия «химический элемент» и «простое вещество». Например, Углерод как химический элемент — это просто вид атомов, имеет заряд ядра плюс шесть, он может входить в состав простых веществ (графит, алмаз и др.). Или сложных веществ (пищевая сода NaHCO3, мел CaCO3 . Кроме того, необходимо различать понятие «смесь» и «сложное вещество». Вещества, входящие в состав смеси, сохраняют свои индивидуальные свойства, тогда как свойства сложного вещества существенно отличаются от свойств простых веществ, образованных теми же химическими элементами.
По своим свойствам простые вещества делятся на металлы и неметаллы. Четкой границы между металлами и неметаллами не существует. Металлы — это ковки, пластические вещества, имеющие металлический блеск, способны проводить тепло и электричество. Общие свойства металлов объясняются их подобным внутренним строением. Их атомы образуют особый тип атомных кристаллов, называемых металлическими кристаллами. Неметаллы — это химические элементы, образующие в свободном состоянии простые вещества, не проявляют физических свойств металлов. Неметаллы не имеют такого сходства в свойствах, как металлы. Например, такие металлы как алюминий, железо, серебро должны серебристо-белый или серый цвет, металлический блеск. Сравним некоторые неметаллы: водород — газ, сера — твердое вещество, алмаз — очень прочный, но хрупкий.
Для всех металлов характерно немолекулярного строение. Для неметаллов наиболее характерна молекулярное строение, но встречаются неметаллы и атомного строения (алмаз и кремний). В периодической системе металлических элементов значительно больше, чем неметаллических. Неметаллические элементы в основном расположены в правой части периодической системы.
xn—-7sbfhivhrke5c.xn--p1ai
