Синтез АТФ в клетке
Аденозинтрифосфорная кислота-АТФ — обязательный энергетический компонент любой живой клетки. АТФ также нуклеотид, состоящий из азотистого основания аденина, сахара рибозы и трех остатков молекулы фосфорной кислоты. Это неустойчивая структура. В обменных процессах от нее последовательно отщепляются остатки фосфорной кислоты путем разрыва богатой энергией, но непрочной связи между вторым и третьим остатками фосфорной кислоты. Отрыв одной молекулы фосфорной кислоты сопровождается выделением около 40 кДж энергии. В этом случае АТФ переходит в аденозиндифосфорную кислоту (АДФ), а при дальнейшем отщеплении остатка фосфорной кислоты от АДФ образуется аденозинмонофосфорная кислота (АМФ).
Схема строения АТФ и превращения ее в АДФ (Т.А. Козлова, В.С. Кучменко. Биология в таблицах. М.,2000)
АДФ
Следовательно, АТФ — своеобразный
аккумулятор энергии в клетке, который «разряжается» при ее расщеплении.
Распад АТФ происходит в процессе реакций синтеза белков, жиров,
углеводов и любых других жизненных функций клеток. Эти реакции идут с
поглощением энергии, которая извлекается в ходе расщепления веществ.
АТФ синтезируется в митохондриях в несколько этапов. Первый из них — подготовительный — протекает ступенчато, с вовлечением на каждой ступени специфических ферментов. При этом сложные органические соединения расщепляются до мономеров: белки — до аминокислот, углеводы — до глюкозы, нуклеиновые кислоты — до нуклеотидов и т. д. Разрыв связей в этих веществах сопровождается выделением небольшого количества энергии. Образовавшиеся мономеры под действием других ферментов могут претерпеть дальнейший распад с образованием более простых веществ вплоть до диоксида углерода и воды.
Схема
Синтез АТФ в мвтохондрии клетки
ПОЯСНЕНИЯ К СХЕМЕ ПРЕВРАЩЕНИЕ ВЕЩЕСТВ И ЭНЕРГИИ В ПРОЦЕССЕ ДИССИМИЛЯЦИИ
I этап — подготовительный:
сложные органические вещества под действием пищеварительных ферментов
распадаются на простые, при этом выделяется только тепловая энергия.
Белки ->аминокислоты
Жиры-> глицерин и жирные кислоты
Крахмал ->глюкоза
II этап-гликолиз (бескислородный):
осуществляется в гиалоплазме, с мембранами не связан; в нем участвуют
ферменты; расщеплению подвергается глюкоза:
У дрожжевых грибов молекула глюкозы без
участия кислорода превращается в этиловый спирт и диоксид углерода
(спиртовое брожение):
У других микроорганизмов гликолиз
может завершаться образованием ацетона, уксусной кислоты и т, д. Во
всех случаях распад одной молекулы глюкозы сопровождается образованием
двух молекул АТФ. В ходе бескислородного расщепления глюкозы в виде
химической связи в молекуле АТФ сохраняется 40% анергии, а остальная
рассеивается в виде теплоты.
III этап-гидролиз (кислородный): осуществляется в митохондриях, связан с матриксом митохондрий и внутренней мембраной, в нем участвуют ферменты, расщеплению подвергается молочная кислота: СзН6Оз+ЗН20 —>3СО2+ 12Н. С02 (диоксид углерода) выделяется из митохондрий в окружающую среду. Атом водорода включается в цепь реакций, конечный результат которых — синтез АТФ. Эти реакции идут в такой последовательности:
1. Атом водорода Н с помощью
ферментов-переносчиков поступает во внутреннюю мембрану митохондрий,
образующую кристы, где он окисляется: Н-е—>H+
2. Протон водорода H+
(катион) выносится переносчиками на наружную поверхность мембраны
крист. Для протонов эта мембрана непроницаема, поэтому они
накапливаются в межмембранном пространстве, образуя протонный резервуар.
3. Электроны водорода e переносятся на внутреннюю поверхность мембраны крист и тут же присоединяются к кислороду с помощью фермента оксидазы, образуя отрицательно заряженный активный кислород (анион): O2 + е—>O2-
4. Катионы и анионы по обе стороны мембраны создают разноименно заряженное электрическое поле, и когда разность потенциалов достигнет 200 мВ, начинает действовать протонный канал. Он возникает в молекулах ферментов АТФ-синтетаз, которые встроены во внутреннюю мембрану, образующую кристы.
5. Через протонный канал протоны водорода H+ устремляются
внутрь митохондрий, создавая высокий уровень энергии, большая часть
которой идет на синтез АТФ из АДФ и Ф (АДФ+Ф—>АТФ), а протоны H+ взаимодействуют с активным кислородом, образуя воду и молекулярный 02:
( 4Н++202- —>2Н20+02)
Таким образом, О2,
поступающий в митохондрии в процессе дыхания организма, необходим для
присоединения протонов водорода Н. При его отсутствии весь процесс в
митохондриях прекращается, так как электронно-транспортная цепь
перестает функционировать. Общая реакция III этапа:
(2СзНбОз + 6Oз + 36АДФ + 36Ф —> 6С02 + 36АТФ + +42Н20)
В результате расщепления одной молекулы глюкозы образуются 38 молекул АТФ: на II этапе — 2 АТФ и на III этапе - 36 АТФ. Образовавшиеся молекулы АТФ выходят за пределы митохондрии и участвуют во всех процессах клетки, где необходима энергия. Расщепляясь, АТФ отдает энергию (одна фосфатная связь заключает 40 кДж) и в виде АДФ и Ф (фосфата) возвращается в митохондрии.
www.examen.ru
Синтез АТФ: особенности данного процесса
Энергетический обмен, который проходит во всех клетках живого организма, называют диссимиляцией. Он представляет собой совокупность реакций разложения органических соединений, при которых выделяется определенное количество энергии.
 Диссимиляция проходит в два или три этапа, что зависит от вида живых организмов. Так, у аэробов энергетический обмен состоит из подготовительного, бескислородного и кислородного этапов. У анаэробов (организмы, которые способны функционировать в бескислородной среде) диссимиляция не требует последнего этапа.
Диссимиляция проходит в два или три этапа, что зависит от вида живых организмов. Так, у аэробов энергетический обмен состоит из подготовительного, бескислородного и кислородного этапов. У анаэробов (организмы, которые способны функционировать в бескислородной среде) диссимиляция не требует последнего этапа.
Конечная стадия энергетического обмена у аэробов заканчивается полным окислением. При этом происходит расщепление молекул глюкозы с образованием энергии, которая частично идет на образование АТФ.
Стоит отметить, что синтез АТФ происходит в процессе фосфорилирования, когда к АДФ присоединяется неорганический фосфат. При этом аденозинтрифосфорная кислота синтезируется в митохондриях при участии АТФ-синтазы.
Какая реакция происходит при образовании данного энергетического соединения?
Аденозиндифосфат и фосфат соединяются с образованием АТФ и макроэргической связи, на образование которой затрачивается около 30,6 кДж / моль. Аденозинтрифосфат обеспечивает клетки энергией, поскольку значительное его количество высвобождается при гидролизе именно макроэргических связей АТФ.
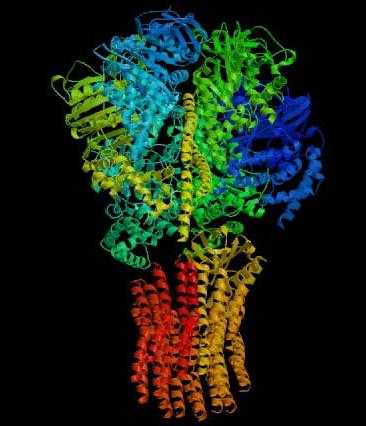
 Молекулярной машиной, которая отвечает за синтез АТФ, является специфическая синтаза. Она состоит из двух частей. Одна из них находится в мембране и представляет собой канал, по которому протоны попадают внутрь митохондрии. При этом высвобождается энергия, которая улавливается другой структурной частью АТФ под названием F1. Она содержит статор и ротор. Статор в мембране размещается неподвижно и состоит из дельта-области, а также альфа- и бета-субъединиц, которые отвечают за химический синтез АТФ. Ротор содержит гамма-, а также эпсилон-субъединицы. Эта часть крутится, используя энергию протонов. Данная синтаза обеспечивает синтез АТФ, если протоны с внешней мембраны направлены к середине митохондрий.
Молекулярной машиной, которая отвечает за синтез АТФ, является специфическая синтаза. Она состоит из двух частей. Одна из них находится в мембране и представляет собой канал, по которому протоны попадают внутрь митохондрии. При этом высвобождается энергия, которая улавливается другой структурной частью АТФ под названием F1. Она содержит статор и ротор. Статор в мембране размещается неподвижно и состоит из дельта-области, а также альфа- и бета-субъединиц, которые отвечают за химический синтез АТФ. Ротор содержит гамма-, а также эпсилон-субъединицы. Эта часть крутится, используя энергию протонов. Данная синтаза обеспечивает синтез АТФ, если протоны с внешней мембраны направлены к середине митохондрий.
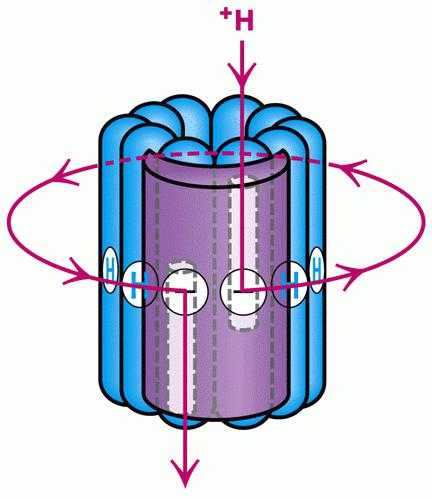 Необходимо отметить, что химическим реакциям в клетке свойственна пространственная упорядоченность. Продукты химических взаимодействий веществ распределяются асимметрично (положительно заряженные ионы идут в одну сторону, а отрицательно заряженные частицы направляются в другую сторону), создавая на мембране электрохимический потенциал. Он состоит из химической и электрической компоненты. Следует сказать, что именно этот потенциал на поверхности митохондрий становится универсальной формой запасания энергии.
Необходимо отметить, что химическим реакциям в клетке свойственна пространственная упорядоченность. Продукты химических взаимодействий веществ распределяются асимметрично (положительно заряженные ионы идут в одну сторону, а отрицательно заряженные частицы направляются в другую сторону), создавая на мембране электрохимический потенциал. Он состоит из химической и электрической компоненты. Следует сказать, что именно этот потенциал на поверхности митохондрий становится универсальной формой запасания энергии.
Данная закономерность была обнаружена английским ученым П. Митчеллом. Он предположил, что вещества после окисления имеют вид не молекул, а положительно и отрицательно заряженных ионов, которые размещаются на противоположных сторонах мембраны митохондрий. Данное предположение позволило выяснить природу образования макроэргических связей между фосфатами в процессе синтеза аденозинтрифосфата, а также сформулировать хемиосмотическую гипотезу этой реакции.
fb.ru
синтез атф — помогите. В каких структурах клетки идёт синтез атф? — 22 ответа
Где происходит синтез атф
В разделе Домашние задания на вопрос помогите. В каких структурах клетки идёт синтез атф? заданный автором
скорость лучший ответ это Синтез АТФ происходит главным образом в митохондриях и обеспечивается в основном энергией, выделяющейся при расщеплении глюкозы, но могут использоваться и другие простые органические соединения — сахара, жирные кислоты и пр.
Митохондрии способны использовать для синтеза АТФ не только расщепление глюкозы. В их матриксе содержатся также ферменты, расщепляющие жирные кислоты. Особенностью этого цикла является большой энергетический выход — 51 молекула АТФ на каждую молекулу жирной кислоты. Не случайно медведи и другие животные, впадая в спячку, запасают именно жиры. Любопытно, что часть запасаемого жира имеет у них бурый цвет. Такие жировые клетки содержат множество митохондрий необычного строения: их внутренние мембраны пронизаны порами. Ионы водорода свободно проходят через эти поры, и синтез АТФ в клетках бурого жира не происходит. Вся энергия, освобождающаяся в процессе кислородного расщепления жирных кислот, выделяется в виде большого количества тепла, согревающего животных во время долгой зимней спячки.
Привет! Вот подборка тем с ответами на Ваш вопрос: помогите. В каких структурах клетки идёт синтез атф?
Ответ от Ольга ламберти[гуру]
кажется в рибосомах, насколько я помню
Ответ от трудоспособный[активный]
на шерховатой ЭПС
Ответ от Евровидение[новичек]
Синтез АТФ происходит главным образом в митохондриях и обеспечивается в основном энергией, выделяющейся при расщеплении глюкозы, но могут использоваться и другие простые органические соединения — сахара, жирные кислоты и пр.
Ответ от 2 ответа[гуру]
Привет! Вот еще темы с нужными ответами:
Аденозинтрифосфат на Википедии
Посмотрите статью на википедии про Аденозинтрифосфат
Ответить на вопрос:
22oa.ru
Ответы@Mail.Ru: Содержание АТФ (где содержится)
АТФ и ее роль в клеткеВ цитоплазме каждой клетки, а также в митохондриях, хлоро-пластах и ядрах содержится аденозинтрифосфорная кислота (Л ТФ) . Она поставляет энергию для большинства реакций, происходящих в клетке. С помощью АТФ клетка синтезирует новые молекулы белков, углеводов, жиров, избавляется от отходов, осуществляет активный транспорт веществ, биение жгутиков и ресничек и т. д.
Молекула АТФ представляет собой нуклеотид, образованный азотистым основанием аденином, пятиуглеродным сахаром рибо-зой и тремя остатками фосфорной кислоты. Фосфатные группы в молекуле АТф соединены между собой высокоэнергетическими (макроэргическими) связями (в формуле обозначены символом ~):
Связи между фосфатными группами не очень прочные, и при их разрыве выделяется большое количество энергии. В результате гидролитического отщепления от АТФ фосфатной группы образуется аденозиндифосфорная кислота (АДФ) н высвобождается порция энергии:
АДФ также может подвергаться дальнейшему гидролизу с отщеплением еще одной фосфатной группы и выделением второй порции энергии; при этом АДФ преобразуется в аденозин-монофосфат (АМФ) , который далее не гидролизуется:
АТФ образуется из АДФ и неорганического фосфата за счет энергии, освобождающейся при окислении органических веществ и в процессе фотосинтеза. Этот процесс называется фосфорили-рованием. При этом должно быть затрачено не менее 40 кДж/моль энергии, которая аккумулируется в макроэргических связях:
Следовательно, основное значение процессов дыхания и фотосинтеза определяется тем, что они поставляют энергию для синтеза АТФ, с участием которой в клетке выполняется большая часть работы.
Таким образом, АТФ — это главный универсальный поставщик энергии в клетках всех живых организмов.
АТФ чрезвычайно быстро обновляется. У человека, например, каждая молекула АТФ расщепляется и вновь восстанавливается 2 400 раз в сутки, так что ее средняя продолжительность жизни менее 1 мин. Синтез АТФ осуществляется главным образом в митохондриях и хлоропластах (частично в цитоплазме) . Образовавшаяся здесь АТФ направляется в те участки клетки, где возникает потребность в энергии.
Источник : Н. А. Лемеза Л. В. Камлюк Н. Д. Лисов «Пособие по биологии для поступающих в ВУЗы»
otvet.mail.ru
Синтез АТФ — SportWiki энциклопедия
Анаэробный синтез АТФ: субстратное фосфорилирование, синтез АТФ из фосфокреатина, аденилаткиназная реакция[править]
АТФ (аденозинтрифосфат): молекула, обеспечивающая энергией живые клетки[править]
Рис. 10.1. Строение аденозинтрифосфата (АТФ)Молекулы АТФ жизненно необходимы. АТФ служит источником энергии, необходимой для сокращения мышц, проведения нервного импульса, протекания многих биохимических реакций и т.п. В покое расходуется 28 г (1 унция) АТФ в минуту, что эквивалентно 1,4 кг (3 фунта) в час, а при физической нагрузке расход АТФ достигает 0,5 кг в минуту! АТФ состоит из аденина, рибозы и трех фосфатных групп, которые называются а-, β- и у-фосфатными группами (рис. 10.1). Гидролиз высокоэнергетических фосфоангидридных связей между β- и у-атомами фосфора или между а- и β-атомами фосфора высвобождает энергию, необходимую для проведения биохимических реакций, т.е. для поддержания жизни организма.
Самый энергетически выгодный метод синтеза АТФ — это аэробное окислительное фосфорилирование. Однако АТФ может также образоваться в анаэробных условиях, хотя и с меньшей эффективностью. Существует три способа анаэробного синтеза АТФ: субстратное фосфорилирование, образование АТФ из фосфокреатина и в результате аденилаткиназной реакции. Хотя анаэробный синтез АТФ и не так энергетически выгоден, способность синтезировать АТФ в бескислородной среде может иметь жизненно важное значение.
Синтез АТФ путем субстратного фосфорилирования[править]
На рис. 10.2 показано, что АТФ образуется в процессе гликолиза в ходе фосфоглицераткиназной и пируваткиназной реакций, а также в цикле Кребса в ходе реакции, катализируемой ферментом сукцинил-КоА-синтетазой с участием нуклеозидцифосфаткиназы (рис. 10.3). Примечание: для этих реакций кислород не требуется.
-
Рис. 10.2. Образование АТФ в ходе гликолиза путем субстратного фосфорилирования
-
Рис. 10.3. В цикле Кребса путем субстратного фосфорилирования образуется ГТФ, который затем под действием нуклеозиддифосфаткиназы превращается в АТФ
Получение АТФ из фосфокреатина[править]
Фосфокреатин — это «аварийный запас» высокоэнергетического фосфата, который можно использовать для быстрого образования АТФ, необходимого для сокращения мышц в анаэробных условиях. Этот интенсивный механизм синтеза АТФ может в экстренных ситуациях спасти жизнь; однако запасы фосфокреатина расходуются очень быстро, всего за несколько секунд.
В периоды покоя, когда молекул АТФ много, креатинкиназа фосфорилирует креатин с образованием фосфокреатина. Особенно важна роль этой реакции в мышцах. Если вдруг требуется сделать резкий рывок, фосфокреатин фосфорилирует АДФ до АТФ, необходимого для сокращения мышц (рис. 10.4) По этой причине фосфокреатин еще называют «фосфаген».
Рис. 10.4. Образование АТФ из фосфокреатина при физической нагрузке и синтез фосфокреатина из креатина в период покояКреатин выводится в форме креатинина[править]
Креатин — это аминокислота, не входящая в состав белков. Креатин синтезируется из аргинина и выводится с мочой в форме креатинина. Уровень креатинина в крови и клиренс креатинина используются для оценки скорости клубочковой фильтрации при нарушении работы почек. Примечание: не путайте креатин, креатинин и карнитин.
Прием креатина повышает работоспособность[править]
Эргогенные средства — это вещества, которые повышают скорость, силу или выносливость спортсмена. Многие из них опасны и запрещены к использованию. Мнения противоречивы, тем не менее многие ученые сходятся на том, что креатин — единственное эргогенное средство, для которого научно доказано его свойство повышать работоспособность как при спринтерских, так и при продолжительных нагрузках.
Образование АТФ из АДФ под действием аденилаткиназы[править]
После того как АТФ гидролизуется для высвобождения энергии, необходимой для сокращения мышц, в клетках образуется и накапливается АДФ. Но АДФ тоже содержит энергоемкую а-фосфоангидридную связь (рис. 10.1). Природа изобретательна: эта энергия становится доступной после того, как в анаэробных условиях две молекулы АДФ под действием аденилаткиназы образуют АТФ (рис. 10.5) (раньше фермент аденилаткиназу называли миокиназой).
Рис. 10.5. Образование АТФ из двух молекул АДФ в процессе аденилаткиназной реакцииАэробный синтез АТФ[править]
Синтез АТФ в дыхательной цепи путем окислительного фосфорилирования[править]
Митохондрия[править]
Рис. 11.1. Схема строения митохондрииМитохондрия — это органелла, по размеру сопоставимая с бактериальной клеткой. Примечательно, что у митохондрии есть две мембраны. Наружная мембрана пронизана молекулами порина. Порины образуют каналы, по которым через мембрану могут проходить молекулы с массой менее 10 кДа. Внутренняя мембрана ПРАКТИЧЕСКИ непроницаема; она образует впячивания — кристы. Через внутреннюю мембрану свободно проходят только небольшие молекулы — вроде Н20 и NH3. Лишь немногие другие молекулы с помощью белков-переносчиков и челночных систем способны преодолеть этот барьер.
Считается, что митохондрия — пример эндосимбиоза. Внутренняя мембрана митохондрии с заключенным в ней содержимым когда-то была древней анаэробной бактерией, которая проникла в примитивную клетку на ранних этапах эволюции. Сохранились и следы прошлого: так, митохондрия имеет свою собственную ДНК (мтДНК), кодирующую 37 генов. 24 из них участвуют в трансляции мтДНК, остальные кодируют белки дыхательной цепи. Примечательно, что только 13 из всех белков митохондриальной дыхательной цепи (а всего их более 85) закодированы в мтДНК. Остальные кодирует ядерная ДНК, и они транспортируются в митохондрию из цитоплазмы.
Дыхательная цепь[править]
Рис. 11.2. Транспорт электронов в дыхательной цепи. На схеме показан поток электронов от промежуточных метаболитов цикла Кребса (малата и сукцината) к кислороду по цепи переноса электронов, через комплексы I, II, III, IVДыхательная цепь — эффективный путь получения АТФ с использованием НАДН и ФАДН2, которые образуются в процессе окисления метаболического «топлива» [прежде всего углеводов и жирных кислот]. Дыхательная цепь состоит из пяти комплексов — I, II, III, IV и сложного комплекса грибовидной формы (комплекс V). Грибовидный «мультикомплекс» состоит из субъединиц F1 (субъединица «один») и F0 (субъединица «О», связывает олигомицин). Некоторые из комплексов дыхательной цепи содержат цитохромы, которые транспортируют электроны по цепи: комплекс III содержит цитохром b, а комплекс IV — цитохром а/аЗ. Кроме того, в транспорте электронов принимают участие убихинон (кофермент Q10) и цитохром С. Все комплексы дыхательной цепи расположены во внутренней мембране митохондрий. Комплексы I, III и IV не только переносят электроны, но также выполняют функцию молекулярных протонных насосов: они «выкачивают» протоны из матрикса в межмембранное пространство. Внутренняя мембрана непроницаема, в частности, она непроницаема для протонов, поэтому они возвращаются в матрикс только одним путем — через протонный канал комплекса F1/F0, который в этот момент синтезирует АТФ.
Поток электронов упрощенно показан на рис.
Патологии митохондрий[править]
Существуют различные нарушения дыхательной цепи. Многие из них наследственно передаются по материнской линии, поскольку все митохондрии зиготы происходят из митохондрий яйцеклетки. При делении клетки тысячи молекул мтДНК случайным образом распределяются между дочерними клетками, поэтому разные ткани могут содержать как нормальные, так и мутантные молекулы мтДНК (это состояние называется гетероплазмией). Вследствие этого клиническая картина при таких патологиях очень изменчива. Мутации в ядерных генах, кодирующих белки дыхательной цепи, передаются по аутосомному типу и обычно вызывают более тяжелые нарушения.
Атрофия зрительного нерва Лебера[править]
Атрофия зрительного нерва Лебера вызывается мутацией участка митохондриальной ДНК, который кодирует одну из субъединиц комплекса I. От этого нарушения дыхательной цепи митохондрий сильнее всего страдает, по-видимому, зрительный нерв. Болезнь проявляется во взрослом возрасте и приводит к потере зрения.
Митохондриальная энцефаломиопатия, лактацидоз и инсультоподобные эпизоды (синдром MELAS)[править]
Причина синдрома MELAS — мутация гена мтДНК, кодирующего лейциновую транспортную РНК митохондрий. Эта мутация влияет на трансляцию мтДНК, и поэтому при синдроме MELAS нарушена структура всех комплексов дыхательной цепи, кроме комплекса II, который полностью кодируется ядерным геномом.
Болезнь Ли[править]
Болезнь Ли — дегенеративное заболевание центральной нервной системы с характерными патологическими изменениями. Обычно развивается в раннем возрасте. Заболевание генетически гетерогенно: чаще всего причиной болезни являются мутации участков ядерных геномов, кодирующих компоненты дыхательной цепи, однако в некоторых случаях болезнь Ли развивается из-за мутаций митохондриальных генов. При болезни Ли может быть нарушена активность АТФ-синтетазы (комплекса V) или комплексов I, II, III, IV. При некоторых формах болезни Ли имеют место нарушения активности пируватдегидрогеназного комплекса.
Недостаточность пируватдегидрогеназного комплекса приводит к повышению в крови концентраций пирувата, лактата и аланина. У некоторых больных наблюдается улучшение состояния при приеме липоевой кислоты или тиамина (коферментов пируватдегидрогеназного комплекса). С ограниченным успехом применяется лечение кетогенной низкоуглеводной диетой. (Кетоновые тела легко проходят гематоэнцефалический барьер, и при их катаболизме образуется ацетил-КоА независимо от пируватдегирогеназного комплекса.)
Биосинтез АТФ путем окислительного фосфорилирования (часть I)[править]
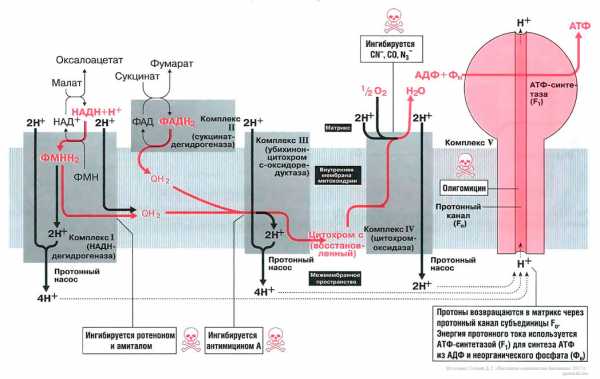
Биосинтез АТФ в дыхательной цепи, в котором принимает участие как поток электронов (е-), так и поток протонов (Н+), происходит путем окислительного фосфорилирования. Дыхательная цепь состоит из четырех комплексов (I, II, III, IV) и структуры грибовидной формы — АТФ-синтаза с субъединицами F0/F1 или комплекса V, который синтезирует АТФ из АДФ и неорганического фосфата (Фн). Ниже будет рассмотрено, как создается поток электронов и протонов в дыхательной цепи: первый начинается от комплекса I, второй — от комплекса II.
Комплекс I[править]
Поток электронов начинается от НАДН. Энергия для синтеза АТФ возникает благодаря разделению зарядов в комплексе I, которое вызывает движение электронов (электрический ток) и протонов (протонный ток). Молекулярный насос комплекса I выкачивает четыре протона в межмембранное пространство. Другие комплексы (III и VI) тоже выкачивают протоны в межмембранное пространство, и образуется электрохимический градиент протонов; в конечном итоге все эти протоны возвращаются обратно через протонный канал АТФ-синтазы (см. ниже). В комплексе I электроны переносятся с НАДН на убихинон (кофермент Q). Два электрона и два протона восстанавливают убихинон до убихинола (Qh3), и убихинол движется в толще мембраны к комплексу III.
Комплекс II[править]
Поток протонов начинается от ФАДН2. Комплекс II содержит ФАД в виде простетических групп нескольких дегидрогеназ (например, сукцинатдегидрогеназы). Этот ФАД восстанавливается до ФАДН2. Далее комплекс II передает электроны убихинону (Q) для последующего переноса электронов к комплексу III. Примечание, комплекс II не выкачивает протоны.
Комплекс III[править]
В роли донора электронов выступает убихинол Qh3, который при этом окисляется до убихинона Q и в этом виде может возвращаться обратно и принимать следующую пару электронов и протонов. Убихинол передает электроны на цитохром, который транспортирует их в комплекс IV. Протонный насос комплекса III выбрасывает 4 протона в межмембранное пространство.
Комплекс IV[править]
Электроны, поступившие от цитохрома с, передаются кислороду, и кислород полностью восстанавливается с образованием воды. Комплекс IV выбрасывает в межмембранное пространство только 2 протона.
АТФ-синтаза (комплекс V)[править]
Этот комплекс состоит из «ножки гриба» — субъединицы F0, содержащей протонный канал, и из «выпуклой части» — АТФ-синтазы (или F1). Субъединица F0 получила свое название благодаря тому, что она ингибируется олигомицином, а субъединица F1 была первой открытой и выделенной «фракцией» среди всех элементов дыхательной цепи. Поток протонов проходит через протонный канал и запускает молекулярный двигатель, который заставляет АДФ и Фн реагировать друг с другом, образуя молекулы АТФ.
Чтобы синтезировать одну молекулу АТФ и транспортировать ее в цитозоль, требуется 4 протона. При окислении 1 молекулы НАДН+ высвобождается 10 протонов, энергия которых достаточно для образования 2,5 молекул АТФ. При окислении 1 молекулы ФАДН2 высвобождается 6 протонов, энергии которых достаточно для синтеза 1,5 молекул АТФ[1].
Утечка электронов приводит к образованию активных форм кислорода[править]
Примерно 2% электронов высвобождаются из дыхательной цепи и связываются непосредственно с кислородом, образуя активные формы кислорода (АФК). Если работа дыхательной цепи нарушена, АФК образуются в большем количестве. Эти вещества повреждают митохондрии, вызывая все большие нарушения дыхательной цепи. Возникает порочный круг, и в результате из-за накопления различных повреждений под действием АФК происходит старение клетки.
Дыхательные яды[править]
Вещества, которые ингибируют образование АТФ, потенциально токсичны для организма.
Амитал и ротенон блокируют транспорт электронов в комплексе I. Ротенон выделяют из корней растения деррис (Derris scandens) и нередко используют в качестве природного пестицида. Он малотоксичен для человека, поскольку плохо всасывается в желудочно-кишечном тракте. Однако ротенон ядовит для рыб, так как быстро всасывается через жабры. К тому же при долговременном воздействии ротенон опасен и для человека, так как вызывает развитие болезни Паркинсона.
Антимицин блокирует транспорт электронов в комплексе III.
Цианиды(CN-), угарный газ (СО) и азиды (N3-) ингибируют комплекс IV. Поэтому при отравлении цианидом блокируются аэробные метаболические процессы, несмотря на то что кровь достаточно насыщена кислородом. Из-за остановки аэробного метаболизма венозная кровь принимает цвет артериальной крови. Кроме того, наблюдается гипервентиляция, поскольку из-за накопления молочной кислоты стимулируется дыхательный центр.
Олигомицин блокирует протонный канал (F0 в комплексе V) и не дает протонам возвращаться в матрикс. Поэтому АТФ-синтаза (F1) теряет способность синтезировать АТФ.
Биосинтез АТФ путем окислительного фосфорилирования (часть II)[править]
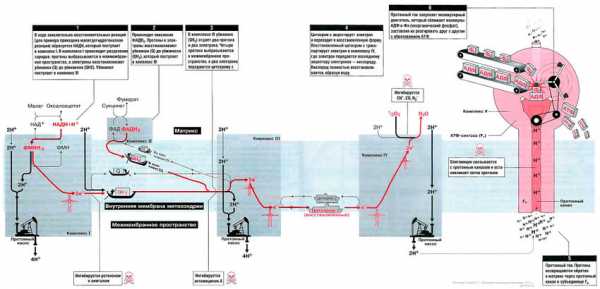
На рис. 13.1 показан поток электронов и протонов в дыхательной цепи. Электроны и протоны от НАДН+ через комплекс I и от ФАДН2 через комплекс II передаются комплексу III. Затем электроны транспортируются в комплекс IV, где они присоединяются к кислороду. В это время протоны выкачиваются протонными насосами из матрикса в межмембранное пространство и возвращаются обратно в матрикс через протонный канал F0-субъединицы АТФ-синтазы (комплекс V). Поток протонов (протонный ток) включает молекулярным двигатель — F1-субъединицу АТФ-синтазного комплекса, и она располагает молекулы АДФ и Фн таким образом, что они объединяются в молекулы АТФ.
- ↑ В отечественных учебниках биохимии принято считать эти значения равными «3» и «2» соответственно, т.е. при окислении 1 молекулы НАДН образуется 3 молекулы АТФ, а при окислении ФАДН2 — 2 молекулы АТФ, что отражает теоретический максимум синтеза АТФ.
sportwiki.to
Откуда в клетке АТФ? — Биохимия
Способы получения энергии в клетке
В клетке существуют четыре основных процесса, обеспечивающих высвобождение энергии из химических связей при окислении веществ и ее запасание:
1. Гликолиз (2 этап биологического окисления) – окисление молекулы глюкозы до двух молекул пировиноградной кислоты, при этом образуется 2 молекулы АТФ и НАДН. Далее пировиноградная кислота в аэробных условиях превращается в ацетил-SКоА, в анаэробных условиях – в молочную кислоту.
2. β-Окисление жирных кислот (2 этап биологического окисления) – окисление жирных кислот до ацетил-SКоА, здесь образуются молекулы НАДН и ФАДН2. Молекулы АТФ «в чистом виде» не появляются.
3. Цикл трикарбоновых кислот (ЦТК, 3 этап биологического окисления) – окисление ацетильной группы (в составе ацетил-SКоА) или иных кетокислот до углекислого газа. Реакции полного цикла сопровождаются образованием 1 молекулы ГТФ (что эквивалентно одной АТФ), 3 молекул НАДН и 1 молекулы ФАДН2.
4. Окислительное фосфорилирование (3 этап биологического окисления) – окисляются НАДН и ФАДН2, полученные в реакциях катаболизма глюкозы, аминокислот и жирных кислот. При этом ферменты дыхательной цепи на внутренней мембране митохондрий обеспечивают образование большей части клеточного АТФ.
Два способа синтеза АТФ
В клетке постоянно происходит использование всех нуклеозидтрифосфатов (АТФ, ГТФ, ЦТФ, УТФ, ТТФ) как донора энергии. При этом АТФ является универсальным макроэргом, участвующим практически во всех сторонах метаболизма и деятельности клетки. И именно за счет АТФ обеспечивается фосфорилирование нуклеотидов ГДФ, ЦДФ, УДФ, ТДФ до нуклеозидтрифосфатов.
У других нуклеозидтрифосфатов существует некая специализация. Так, УТФ участвует в обмене углеводов, в частности в синтезе гликогена. ГТФ задействован в рибосомах, участвует в образовании пептидной связи в белках. ЦТФ используется в синтезе фосфолипидов.
Основным способом получения АТФ в клетке является окислительное фосфорилирование, протекающее в структурах внутренней мембраны митохондрий. При этом энергия атомов водорода молекул НАДН и ФАДН2, образованных в гликолизе, ЦТК, окислении жирных кислот, преобразуется в энергию связей АТФ.
Однако также есть другой способ фосфорилирования АДФ до АТФ – субстратное фосфорилирование. Этот способ связан с передачей макроэргического фосфата или энергии макроэргической связи какого-либо вещества (субстрата) на АДФ. К таким веществам относятся метаболиты гликолиза (1,3-дифосфоглицериновая кислота, фосфоенолпируват), цикла трикарбоновых кислот (сукцинил-SКоА) и резервный макроэрг креатинфосфат. Энергия гидролиза их макроэргической связи выше, чем 7,3 ккал/моль в АТФ, и роль указанных веществ сводится к использованию этой энергии для фосфорилирования молекулы АДФ до АТФ.
Классификация макроэргов
Макроэргические соединения классифицируются по типу связи, несущей дополнительную энергию:
1. Фосфоангидридная связь. Такую связь имеют все нуклеотиды: нуклеозидтрифосфаты (АТФ, ГТФ, ЦТФ, УТФ, ТТФ) и нуклеозиддифосфаты (АДФ, ГДФ, ЦДФ, УДФ, ТДФ).
2. Тиоэфирная связь. Примером являются ацил-производные коэнзима А: ацетил-SКоА, сукцинил-SКоА, и другие соединения любой жирной кислоты и HS-КоА.
3. Гуанидинфосфатная связь – присутствует в креатинфосфате, запасном макроэрге мышечной и нервной ткани.
4. Ацилфосфатная связь. К таким макроэргам относится метаболит гликолиза 1,3-дифосфоглицериновая кислота (1,3-дифосфоглицерат). Она обеспечивает синтез АТФ в реакции субстратного фосфорилирования.
5. Енолфосфатная связь. Представитель – фосфоенолпируват, метаболит гликолиза. Он также обеспечивает синтез АТФ в реакции субстратного фосфорилирования в гликолизе..
.
Вы можете спросить или оставить свое мнение.
biokhimija.ru
АТФ и ее роль в клетке
В цитоплазме каждой клетки, а также в митохондриях, хлоропластах и ядрах содержится аденозинтрифосфорная кислота (АТФ). Она поставляет энергию для большинства реакций, происходящих в клетке. С помощью АТФ клетка синтезирует новые молекулы белков, углеводов, жиров, избавляется от отходов, осуществляет активный транспорт веществ, биение жгутиков и ресничек и т. д.
Молекула АТФ представляет собой нуклеотид, образованный азотистым основанием аденином, пятиуглеродным сахаром рибозой и тремя остатками фосфорной кислоты. Фосфатные группы в молекуле АТФ соединены между собой высокоэнергетическими (макроэргическими) связями :
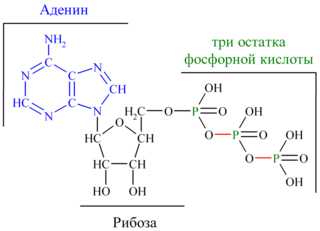
Связи между фосфатными группами не очень прочные, и при их разрыве выделяется большое количество энергии. В результате гидролитического отщепления от АТФ фосфатной группы образуется аденозиндифосфорная кислота (АДФ) н высвобождается порция энергии:
АДФ также может подвергаться дальнейшему гидролизу с отщеплением еще одной фосфатной группы и выделением второй порции энергии; при этом АДФ преобразуется в аденозин-монофосфат (АМФ), который далее не гидролизуется:
АТФ образуется из АДФ и неорганического фосфата за счет энергии, освобождающейся при окислении органических веществ и в процессе фотосинтеза. Этот процесс называется фосфорилированием. При этом должно быть затрачено не менее 40 кДж/моль энергии, которая аккумулируется в макроэргических связях:
Следовательно, основное значение процессов дыхания и фотосинтеза определяется тем, что они поставляют энергию для синтеза АТФ, с участием которой в клетке выполняется большая часть работы.
Таким образом, АТФ — это главный универсальный поставщик энергии в клетках всех живых организмов.
АТФ чрезвычайно быстро обновляется. У человека, например, каждая молекула АТФ расщепляется и вновь восстанавливается 2 400 раз в сутки, так что ее средняя продолжительность жизни менее 1 мин. Синтез АТФ осуществляется главным образом в митохондриях и хлоропластах (частично в цитоплазме). Образовавшаяся здесь АТФ направляется в те участки клетки, где возникает потребность в энергии.
Источник : Н.А. Лемеза Л.В.Камлюк Н.Д. Лисов «Пособие по биологии для поступающих в ВУЗы»
sbio.info
