Размеры и масса атомов и молекул
Относительная атомная и молекулярная масса
В таблице химических элементов Д.И.Менделеева приведены относительные атомные массы элементов.
Относительную молекулярную массу можно найти как сумму относительных атомных масс элементов, входящих в химическую формулу вещества.
Относительная атомная масса и относительная молекулярная масса – величины безразмерные.
Размеры и масса атомов и молекул
Можно говорить и просто о массе атома или молекулы. Массу микрочастиц часто измеряют в атомных единицах массы:
Масса любого атома в кг равна:
а масса любой молекулы в кг:
Линейные размеры атомов и молекул представляют собою величины порядка .
Чтобы нагляднее представить себе размеры атомов молекул и их количество в определенном объеме вещества, приведем один интересный пример: если все атомы, находящиеся в 1 см3 меди, расположить в одну линию плотно друг к другу, то длина такой цепочки будет примерно 14 миллиардов километров. Это примерно в 90 раз больше, чем расстояние от Земли до Солнца.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Размеры атомов и молекул
Туннельные микроскопы обеспечивают увеличение в 100 млн раз. Это позволяет измерять размеры атомов с очень большой точностью. Так, диаметр атома углерода оказался равным 1,4·10 -8 см. Такой же порядок имеют и размеры других атомов.
Размеры атомов и молекул, найденные другими методами, оказываются примерно такими же.
Эти размеры так малы, что их невозможно себе представить. Что вам может сказать, например, число 2,3·10-8см — размер молекулы водорода? В таких случаях прибегают к помощи сравнений. Если, например, вашу голову увеличить до размеров средней звезды типа Солнца, то молекула при этом увеличится до размеров головы.
А вот еще сравнение. Если представить себе, что все размеры в мире возросли в 108 раз, то молекула водорода будет выглядеть как шарик диаметром всего в 2,3 см (средних размеров слива), а рост человека стал бы равным 170 000 км, размер мухи — 10 000 км, толщина волоса — 10км, размер красного кровяного тельца (эритроцита) — 700 м.
Число молекул
При
столь малых размерах молекул число их
в любом макроскопическом теле чрезвычайно
велико. Подсчитаем приблизительное
число молекул в капле воды массой 1 г и,
следовательно, объемом 1 см
Представьте себе, что поверхность земного шара твердая и гладкая. На всей поверхности вплотную друг к другу стоят люди. Число людей при этом будет чуть меньше числа молекул в 1 см3 воздуха при нормальном атмосферном давлении и температуре 0 °С.
Надо помнить основные положения молекулярно-кинетической теории. Атомы имеют размеры порядка 10-8см. Изображения атомов, полученные с помощью туннельного микроскопа, не оставляют никаких сомнений в их существовании,
§ 2.2. Масса молекул. Постоянная Авогадро
Массы молекул очень малы, если выражать их в граммах или килограммах, а число молекул в макроскопических телах огромно. С очень маленькими и очень большими числами иметь дело неудобно. Ученые нашли довольно простой способ избежать этого неудобства и характеризовать массы молекул и их число вполне обозримыми числами, не выходящими далеко за пределы сотни. Сейчас вы познакомитесь с тем, как это делается.
Масса молекулы воды
В предыдущем параграфе мы выяснили, что в 1 г воды содержится 3,7·1022 молекул. Следовательно, масса одной молекулы равна:
Массы такого же порядка имеют и молекулы других веществ, исключая огромные молекулы органических соединений. Например, масса молекулы гемоглобина превышает массу молекулы воды в несколько десятков тысяч раз.
Относительная молекулярная масса
Так
как массы молекул очень малы, удобно
использовать не абсолютные значения
масс, а относительные. По международному
соглашению, принятому в 1961 г., массы всех
молекул сравнивают с
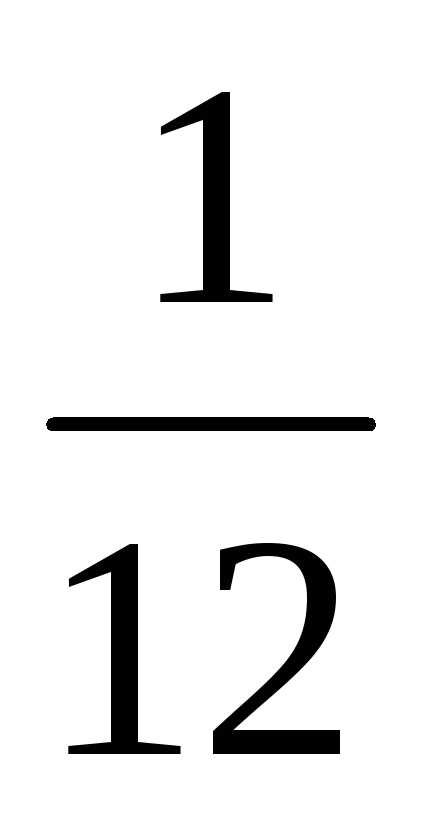
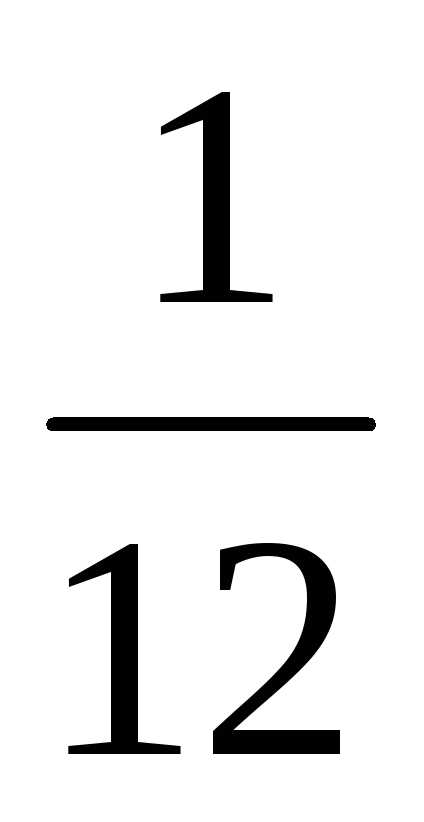 введен для того, чтобы относительные
массы атомов были близки к целым числам.
Относительная масса атома углерода
точно равна 12, а атома водорода примерно
равна единице.
введен для того, чтобы относительные
массы атомов были близки к целым числам.
Относительная масса атома углерода
точно равна 12, а атома водорода примерно
равна единице.
*
Точнее, с
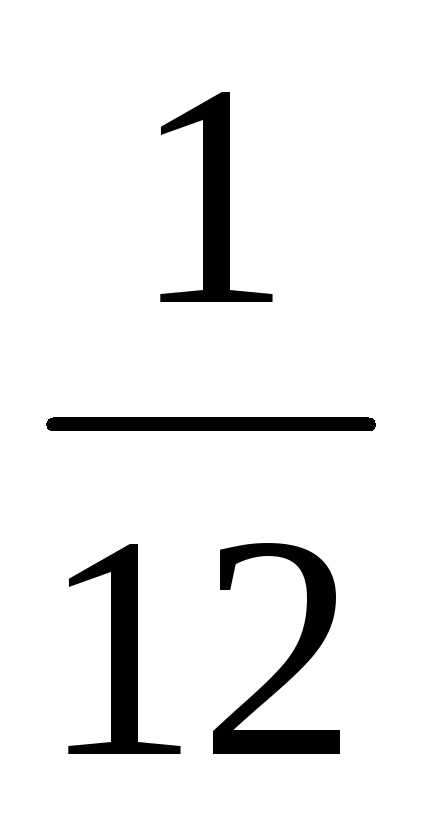 массы атома наиболее
распространенного изотопа углерода-12.
массы атома наиболее
распространенного изотопа углерода-12.
Относительной
молекулярной (или атомной) массой
вещества М
r
называют
отношение массы молекулы (или атома)
данного вещества к
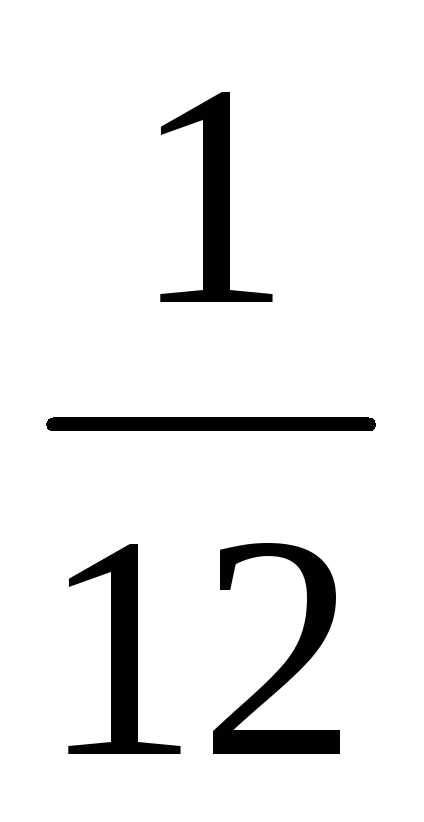 массы
атома углерода т0С:
массы
атома углерода т0С:
(2.2.1)
Относительные атомные массы всех химических элементов точно измерены. Складывая относительные атомные массы, можно вычислить относительную молекулярную массу. Например, относительная молекулярная масса воды Н2О приближенно равна 18, так как относительные атомные массы водорода и кислорода примерно равны 1 и 16:2-1 + 16=18.
studfiles.net
Масса и размер молекул | Физика для всех
Многие опыты показывают, что размер молекулы очень мал. Линейный размер молекулы или атома можно найти различными способами. Например, с помощью электронного микроскопа, получены фотографии некоторых крупных молекул, а с помощью ионного проектора (ионного микроскопа) можно не только изучить строение кристаллов, но определить расстояние между отдельными атомами в молекуле.
Используя достижения современной экспериментальной техники, удалось определить линейные размеры простых атомов и молекул, которые составляют около 10-8 см. Линейные размеры сложных атомов и молекул намного больше. Например, размер молекулы белка составляет 43*10-8 см.
Для характеристики атомов используют представление об атомных радиусах, которые дают возможность приближённо оценить межатомные расстояния в молекулах, жидкостях или твёрдых телах, так как атомы по своим размерам не имеют чётких границ. То есть атомный радиус – это сфера, в которой заключена основная часть электронной плотности атома (не менее 90…95%).
Размер молекулы настолько мал, что представить его можно только с помощью сравнений. Например, молекула воды во столько раз меньше крупного яблока, во сколько раз яблоко меньше земного шара.
Моль вещества
Массы отдельных молекул и атомов очень малы, поэтому в расчётах удобнее использовать не абсолютные значения масс, а относительные.
Относительная молекулярная масса (или относительная атомная масса) вещества Мr – это отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода.
Мr = (m0) : (m0C / 12)
где m0 – масса молекулы (или атома) данного вещества, m0C – масса атома углерода.
Относительная молекулярная (или атомная) масса вещества показывает, во сколько раз масса молекулы вещества больше 1/12 массы изотопа углерода С12. Относительная молекулярная (атомная) масса выражается в атомных единицах массы.
Атомная единица массы – это 1/12 массы изотопа углерода С12. Точные измерения показали, что атомная единица массы составляет 1,660*10
1 а.е.м. = 1,660 * 10-27 кг
Относительная молекулярная масса вещества может быть вычислена путём сложения относительных атомных масс элементов, входящих в состав молекулы вещества. Относительная атомная масса химических элементов указана в периодической системе химических элементов Д.И. Менделеева.
В периодической системе Д.И. Менделеева для каждого элемента указана атомная масса, которая измеряется в атомных единицах массы (а.е.м.). Например, атомная масса магния равна 24,305 а.е.м., то есть магний в два раза тяжелее углерода, так как атомная масса углерода равна 12 а.е.м. (это следует из того, что 1 а.е.м. = 1/12 массы изотопа углерода, который составляет большую часть атома углерода).
Зачем измерять массу молекул и атомов в а.е.м., если есть граммы и килограммы? Конечно, можно использовать и эти единицы измерения, но это будет очень неудобно для записи (слишком много чисел придётся использовать для того, чтобы записать массу). Чтобы найти массу элемента в килограммах, нужно атомную массу элемента умножить на 1 а.е.м. Атомная масса находится по таблице Менделеева (записана справа от буквенного обозначения элемента). Например, вес атома магния в килограммах будет:
m0Mg = 24,305 * 1 a.e.м. = 24,305 * 1,660 * 10-27 = 40,3463 * 10-27 кг
Массу молекулы можно вычислить путём сложения масс элементов, которые входят в состав молекулы. Например, масса молекулы воды (Н2О) будет равна:
m0Н2О = 2 * m0H + m0O = 2 * 1,00794 + 15,9994 = 18,0153 a.e.м. = 29,905 * 10-27 кг
Количество вещества принято считать пропорциональным числу частиц. Количество вещества – это физическая величина, характеризующая относительное число молекул и атомов в теле. Единица количества вещества называется молем (моль).
Моль равен количеству вещества системы, в которой содержится столько же молекул, сколько содержится атомов в 0,012 кг углерода С
Постоянная Авогадро
Количество вещества ν равно отношению числа молекул в данном теле к числу атомов в 0,012 кг углерода, то есть количеству молекул в 1 моле вещества.
ν = N / NA
где N – количество молекул в данном теле, NA – количество молекул в 1 моле вещества, из которого состоит тело.
NA – это постоянная Авогадро. Количество вещества измеряется в молях.
Постоянная Авогадро – это количество молекул или атомов в 1 моле вещества. Эта постоянная получила своё название в честь итальянского химика и физика Амедео Авогадро (1776 – 1856).
В 1 моле любого вещества содержится одинаковое количество частиц.
NA = 6,02 * 1023 моль-1
Молярная масса – это масса вещества, взятого в количестве одного моля:
μ = m0 * NA
где m0 – масса молекулы.
Молярная масса выражается в килограммах на моль (кг/моль = кг*моль-1).
Молярная масса связана с относительной молекулярной массой соотношением:
μ = 10-3 * Mr [кг*моль-1]
Масса любого количества вещества m равна произведению массы одной молекулы m0 на количество молекул:
m = m0N = m0NAν = μν
Количество вещества равно отношению массы вещества к его молярной массе:
ν = m / μ
Массу одной молекулы вещества можно найти, если известны молярная масса и постоянная Авогадро:
m0 = m / N = m / νNA = μ / NA
Более точное определение массы атомов и молекул достигается при использовании масс-спректрометра – прибора, в котором происходит разделение пучком заряженных частиц в пространстве в зависимости от их массы заряда при помощи электрических и магнитных полей.
Для примера найдём молярную массу атома магния. Как мы выяснили выше, масса атома магния равна m0Mg = 40,3463 * 10-27кг. Тогда молярная масса будет:
μ = m0Mg * NA = 40,3463 * 10-27 * 6,02 * 1023 = 2,4288 * 10-2 кг/моль
То есть в одном моле «помещается» 2,4288 * 10-2 кг магния. Ну или примерно 24,28 грамм.
Как видим, молярная масса (в граммах) практически равна атомной массе, указанной для элемента в таблице Менделеева. Поэтому когда указывают атомную массу, то обычно делают так:
Атомная масса магния равна 24,305 а.е.м. (г/моль).
Можете посчитать молярную массу для различных элементов и убедиться в правоте этого утверждения. Для расчёта молярной массы можно использовать простой калькулятор, который находится внизу страницы:
av-mag.ru
Размеры и массы молекул и атомов – HomeWork.net.ua
В физике и химии имеется много методов, позволяющих точно определить размеры молекул, атомов химических элементов и входящих в них частиц. Некоторые из этих методов будут рассмотрены дальше. Если условно представлять себе молекулы в виде шариков, то их диаметры в большинстве случаев меньше нанометра (1 нм=10-9 м). Например, диаметр молекулы воды (Н20) равен 0,26 нм.
Молекулы так малы, что представить себе их размеры можно только с помощью сравнений. Приведем одно из них: молекула воды во столько раз меньше крупного яблока, во сколько раз яблоко меньше земного шара. Заметим, что молекулы органических веществ, и особенно полимеров, могут содержать тысячи атомов и имеют значительно большие размеры.
Массы молекул оказались по привычным для нас масштабам тоже весьма малыми. Например, масса молекулы кислорода (О2) равна 53,5*10-27 кг, а масса молекулы водорода (Н2) — 3,34*10-27 кг. Масса самого легкого в природе атома водорода (Н) равна 1,672*10-27 кг. На практике измерять массы молекул и атомов в килограммах или граммах оказалось неудобным. Для этого была введена новая, дополнительная единица измерения — атомная единица массы. Атомной единицей массы называют 1/12 массы изотопа углерода С12; краткое наименование — а. е. м.
Масса молекулы, (атома), выраженная в атомных единицах массы, называется относительной молекулярной (атомной) массой. Она показывает, во сколько раз масса молекулы вещества больше 1/12 массы изотопа углерода С12. Например, относительная масса молекулы водорода равна 2,01594, а молекулы азота — 28,0134. Точные измерения показали, что 1 а. е. м. = 1,660*10-27 кг. Таким образом, зная массу молекулы mотн в атомных единицах, ее массу m в кг можно найти по следующей формуле:
m=mотн*1,660*10-27 кг.
homework.net.ua
Масса атомов и молекул | Учеба-Легко.РФ
Масса атомов и молекул



Для измерения масс атомов и молекул в физике и химии принята единая система измерения. Эти величины измеряются в относительных единицах.
Атомная единица массы (а.е.м.) равна 1/12 массы m атома углерода 12С (m одного атома 12С равна 1,993Ч10-26кг).
Относительная атомная масса элемента (Ar) – это безразмерная величина, равная отношению средней массы атома элемента к 1/12 массы атома 12С. При расчете относительной атомной массы учитывается изотопный состав элемента. Величины Ar определяют по таблице Д.И. Менделеева.
Абсолютная масса атома (m) равна относительной атомной массе, умноженной на 1 а.е.м. Например, для атома водорода абсолютная масса определяется следующим образом:
m (H) = 1,008Ч1,661Ч10-27 кг = 1,674Ч10-27 кг
Относительная молекулярная масса соединения (M r) – это безразмерная величина, равная отношению массы m молекулы вещества к 1/12 массы атома 12С:
Относительная молекулярная масса равна сумме относительных масс атомов, входящих в состав молекулы. Например:
М r (C2H6) = 2Ч A r (C) + 6ЧA r (H) = 2Ч12 + 6 = 30.Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на 1 а.е.м.
Лекция добавлена 15.11.2012 в 12:46:01
uclg.ru
Атомные и молекулярные массы
ОСНОВНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ И ЗАКОНЫ. АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВ
Химия – наука о веществах и их превращениях
Вещество– вид материи, состоящий из дискретных частиц, обладающих массой покоя (атомы, молекулы, ионы). Способ существования материи – движение.
Фундаментальный закон природы – закон неуничтожимости материи и движения имеет следствием закон сохранения массы, открытый М.В. Ломоносовым в 1748 году и опубликованный в 1760 году: масса веществ, вступивших в реакцию, равна массе веществ, образующихся в результате реакции.
Атомно-молекулярное учение
М.В. Ломоносов является также создателем атомно-молекулярного учения, которое он сформулировал в 1741 году.
Основные положения атомно-молекулярного учения:
1) Все вещества состоят из молекул, между которыми имеются промежутки. Молекула– мельчайшая частица вещества, обладающая его химическими свойствами.
2) Молекулы состоят из атомов, которые соединяются друг с другом в определенных соотношениях.
Атом – наименьшая частица химического элемента в составе простых и сложных веществ, химически неделимая.
3) Молекулы и атомы находятся в непрерывном движении.
4) Атомы характеризуются определенной массой и размерами.
5) Разным элементам соответствуют разные атомы (элемент – вид атомов).
6) Молекулы простых веществ состоят из одинаковых атомов, а молекулы сложных – из разных.
Закон постоянства состава
Открытие закона сохранения массы ознаменовало переход химии к количественным методам исследования. Был изучен состав многих веществ и установлен закон постоянства состава в 1799-1807 гг. Ж. Прустом: всякое чистое вещество, независимо от способов его получения и нахождения в природе, имеет постоянный качественный и количественный состав.
Закон простых кратных отношений
Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных весовых соотношениях. Многие элементы могут соединяться друг с другом в нескольких различных весовых соотношениях и при этом образуются разные вещества (СО, СО2). В молекулах СО и СО2, N2O, NO и NO2 состав меняется скачками, а не постепенно, что свидетельствует о дискретном строении вещества. Этот закон, подтвержденный на опыте, был первым доказательством реальности существования атомов.
Атомные и молекулярные массы
Атомы и молекулы имеют абсолютные массы порядка 10–24–10–21 г, неудобные для сравнения, поэтому химики пользуются относительными значениями масс атомов. Представление об относительной атомной массе было введено Дж. Дальтоном в 1803 г. За единицу массы он принял массу самого легкого атома – водорода. В настоящее время в качестве эталона принята масса 1/12 массы атома углерода изотопа 12С, равная 1,66043×10–24 г.
Относительная атомная (Аr) масса показывает во сколько раз данный атом тяжелее 1/12 массы атома изотопа углерода 12С.
| , | (1.2) |
где mа – масса атома, mа(С) – масса атома изотопа углерода 12С.
Для определения атомной массы элементов в 19 веке использовался метод, основанный на законе теплоемкости П.Л. Дюлонга и А.Т. Пти (1819 г.): молярная теплоемкость (СМ) для различных простых веществ в кристаллическом состоянии одинакова и равна приблизительно 26,4 Дж. Она равна произведению удельной теплоемкости (Суд) на молярную массу элемента:
| Смолярная=Суд×М =26,4 Дж | (1.3) |
Используя величину удельной теплоемкости, которая легко определяется экспериментально (отношение количества теплоты полученного или отданного 1 г вещества к соответствующему изменению температуры) можно найти приближенное значение атомной массы. Исключения составляют легкие элементы, особенно неметаллы, имеющие теплоемкость значительно меньше (бериллий, бор, кремний, алмаз).
В настоящее время атомные массы элементов определяют методом масс-спектроскопии. Массы атомов определяют по отклонению траектории их ионов, двигающихся в магнитном поле, поскольку величина отклонение зависит от отношения массы иона к его заряду.
Относительная молекулярная масса (Mr)показывает во сколько раз данная молекула тяжелее 1/12 массы атома 12С.
| , | (1.4) |
где mм – масса молекулы.
Похожие статьи:
poznayka.org
Основные положения МКТ. Масса и размер молекул. Количество вещества. Молекулярная физика
Основные положения МКТ. Масса и размер молекул. Количество вещества. Молекулярная физика
МКТ — это просто!
«Ничто не существует, кроме атомов и пустого пространства …» — Демокрит
«Любое тело может делиться до бесконечности» — Аристотель
Основные положения молекулярно-кинетической теории (МКТ)
Цель МКТ — это объяснение строения и свойств различных макроскопических тел и тепловых явлений, в них протекающих, движением и взаимодействием частиц, из которых состоят тела.
Макроскопические тела — это большие тела, состоящие из огромного числа молекул.
Тепловые явления — явления, связанные с нагреванием и охлаждением тел.
Основные утверждения МКТ
1. Вещество состоит из частиц (молекул и атомов).
2. Между частицами есть промежутки.
3. Частицы беспорядочно и непрерывно движутся.
4. Частицы взаимодействуют друг с другом (притягиваются и отталкиваются).
Подтверждение МКТ:
1. экспериментальное
— механическое дробление вещества; растворение вещества в воде; сжатие и расширение газов; испарение; деформация тел; диффузия; опыт Бригмана: в сосуд заливается масло, сверху на масло давит поршень, при давлении 10 000 атм масло начинает просачиваться сквозь стенки стального сосуда;
— диффузия; броуновское движение частиц в жидкости под ударами молекул;
— плохая сжимаемость твердых и жидких тел; значительные усилия для разрыва твердых тел; слияние капель жидкости;
2. прямое
— фотографирование, определение размеров частиц.
Броуновское движение
Броуновское движение — это тепловое движение взвешенных частиц в жидкости (или газе).
Броуновское движение стало доказательством непрерывного и хаотичного (теплового) движения молекул вещества.
— открыто английским ботаником Р. Броуном в 1827 г.
— дано теоретическое объяснение на основе МКТ А. Эйнштейном в 1905 г.
— экспериментально подтверждено французским физиком Ж. Перреном.
Масса и размеры молекул
Размеры частиц
Диаметр любого атома составляет около см.
Число молекул в веществе
где V — объем вещества, Vo — объем одной молекулы
Масса одной молекулы
где m — масса вещества,
N — число молекул в веществе
Единица измерения массы в СИ: [m]= 1 кг
В атомной физике массу обычно измеряют в атомных единицах массы (а.е.м.).
Условно принято считать за 1 а.е.м. :
Относительная молекулярная масса вещества
Для удобства расчетов вводится величина — относительная молекулярная масса вещества.
Массу молекулы любого вещества можно сравнить с 1/12 массы молекулы углерода.
где числитель — это масса молекулы, а знаменатель — 1/12 массы атома углерода
— это величина безразмерная, т.е. не имеет единиц измерения
Относительная атомная масса химического элемента
где числитель — это масса атома, а знаменатель — 1/12 массы атома углерода
— величина безразмерная, т.е. не имеет единиц измерения
Относительная атомная масса каждого химического элемента дана в таблице Менделеева.
Другой способ определения относительной молекулярной массы вещества
Относительная молекулярная масса вещества равна сумме относительных атомных масс химических элементов, входящих в состав молекулы вещества.
Относительную атомную массу любого химического элемента берем из таблицы Менделеева!)
Количество вещества
Количество вещества (ν) определяет относительное число молекул в теле.
где N — число молекул в теле, а Na — постоянная Авогадро
Единица измерения количества вещества в системе СИ: [ν]= 1 моль
1 моль — это количество вещества, в котором содержится столько молекул (или атомов), сколько атомов содержится в углероде массой 0,012 кг.
Запомни!
В 1 моле любого вещества содержится одинаковое число атомов или молекул!
Но!
Одинаковые количества вещества для разных веществ имеют разную массу!
Постоянная Авогадро
Число атомов в 1 моле любого вещества называют числом Авогадро или постоянной Авогадро:
Молярная масса
Молярная масса (M) — это масса вещества, взятого в одном моле, или иначе — это масса одного моля вещества.
где
— масса молекулы
— постоянная Авогадро
Единица измерения молярной массы: [M]=1 кг/моль.
Формулы для решения задач
Эти формулы получаются в результате подстановки вышерассмотренных формул.
Масса любого количества вещества
и формула для 7 класса
(плотность х объем)
Количество вещества
Число молекул в веществе
Молярная масса
Масса одной молекулы
Связь между относительной молекулярной массой и молярной массой
Молекулярная физика. Термодинамика — Класс!ная физика
Основные положения МКТ. Масса и размер молекул. Количество вещества. — Взаимодействие молекул. Строение твердых тел, жидкостей и газов. — Идеальный газ. Основное уравнение МКТ. — Температура. Тепловое равновесие. Абсолютная шкала температур. — Уравнение состояния идеального газа. — Изопроцессы. Газовые законы. — Взаимные превращения жидкостей и газов. Влажность воздуха. — Твердые тела. Кристаллические тела. Аморфные тела.
class-fizika.ru
