Азот и его характеристики
Общая характеристика азота
Большая часть азота находится в свободном состоянии. Свободный азот является главной составной частью воздуха, который содержит 78,2% (об.) азота. Неорганические соединения азота не встречаются в природе в больших количествах, если не считать натриевую селитру NaNO3, образующую мощные пласты на побережье Тихого океана в Чили. Почва содержит незначительные количества азота, преимущественно в виде солей азотной кислоты. Но в виде сложных органических соединений – белков – азот входит в состав всех живых организмов.
Общее содержание азота в земной коре (включая гидросферу и атмосферу) составляет 0,04% (масс.).
В виде простого вещества азот – это бесцветный газ, не имеющий запаха и весьма мало растворимый в воде. Он немного легче воздуха: масса 1 л азота равна 1,25 г.
Атомная и молекулярная масса азота
Относительной атомной массой элемента называют отношение массы атома данного элемента к 1/12 массы атома углерода. Относительная атомная масса безразмерна и обозначается A
Массы молекул, также как массы атомов выражаются в атомных единицах массы. Молекулярной массой вещества называется масса молекулы, выраженная в атомных единицах массы. Относительной молекулярной массой вещества называют отношение массы молекулы данного вещества к 1/12 массы атома углерода, масса которого равна 12 а.е.м. Известно, что молекула азота двухатомна – N2. Относительная молекулярная масса молекулы азота будет равна:
Mr(N2) = 14,0064× 2 ≈ 28.
Изотопы азота
В природе азот существует в виде двух стабильных изотопов 14N (99,635%) и 15N (0,365%). Их массовые числа равны 14 и 15 соответственно. Ядро атома изотопа азота 14N содержит семь протонов и семь нейтронов, а изотопа 15N – такое же количество протонов и шесть нейтронов.
Существует четырнадцать искусственных изотопов азота с массовыми числами от 10-ти до 13-ти и от 16-ти до 25-ти, из которых наиболее стабильным является изотоп 13Nс периодом полураспада равным 10 минут.
Ионы азота
На внешнем энергетическом уровне атома азота имеется пять электронов, которые являются валентными:
1s22s22p3.
Схема строения атома азота представлена ниже:
В результате химического взаимодействия азот может терять свои валентные электроны, т.е. являться их донором, и превращаться в положительно заряженные ионы или принимать электроны другого атома, т.е. являться их акцептором, и превращаться в отрицательно заряженные ионы:
N0 –5e → N2+;
N0-4e → N4+;
N0-3e → N3+;
N
N0-1e → N1+;
N0+1e → N1-;
N0+2e → N2-;
N0+3e → N3-.
Молекула и атом азота
Молекула азота состоит из двух атомов – N2. Приведем некоторые свойства, характеризующие атом и молекулу азота:
|
Энергия ионизации атома, эВ |
14,53 |
|
Сродство атома к электрону, эВ |
0,27 |
|
Относительная электроотрицательность |
3,07 |
|
Радиус атома, нм |
0,071 |
|
Стандартная энтальпия диссоциации молекул при 25 oС, кДж/моль |
945 |
Примеры решения задач
ru.solverbook.com
Вещество азот
Азот – это элемент, который активно использует природа в построении веществ. Вещество азот присутствует в человеческом организме, и практически во всех объектах флоры и фауны. Флора и фауна играют различные роли в круговороте азота. Фауна перерабатывает и поглощает вещества, производимые флорой из частиц неживой природы. Эти частицы называются воздухом и водными растворами различных веществ. Такие процессы в природе позволяют создать условия для более сложных и динамичных организмов.
Вещество азот применяется в различных областях. Это производство нашатырного спирта, используемого в медицине, взрывчатых веществ, производство удобрений. Удобрения, содержащие
Основное потребление азота приходится на химическую промышленность, а также нефтехимические предприятия. Его используют как самостоятельный компонент – участник технологических процессов (обработка поверхностей металла азотом) и химических реакций (синтез аммиака), так и вспомогательный второстепенный элемент в основных технологиях. Что касается последнего, то здесь вещество азот используют не в качестве сырья, а как средство.
Большинство случаев, когда вещество азот применяют, используя его инертные свойства. Таким образом, инертную защитную среду газ создает в процессе выплавки специальных сплавов и сталей, нефтяной переработки, стекольная промышленность также использует его инертные свойства.
Пищевая промышленность широко использует вещество азот при упаковке продуктов, с высоким содержанием пищевых жиров. За счет замещения кислорода азотом замедляются процессы окисления и гниения. А значит, увеличивается срок хранения продукта. Поскольку азот мало растворим в воде, вкус, запах и цвет продукта в упаковке не изменяется.
В современном производстве распространены генераторы азота и азотные установки, производящие азот из сжатого воздуха. Используя такие генераторы, исчезает необходимость в покупке баллонов с азотом, что может занять больше времени, стоимости, проблем перевозки и других факторов, несущих очевидные неудобства.
Воздух, окружающий нас, содержит объем азота 78%, кислорода – 21% и необходим для поддержания жизнедеятельности в атмосфере Земли. Также некоторый объем азота входит в состав белков, по массе это примерно 16 – 18%.
Азот, как экологически чистый газ, используют в установках пожаротушения. Безусловный плюс – азотная установка пожаротушения на окружающую среду не имеет никакого вредного воздействия. Затраты на эксплуатацию совсем незначительны, поскольку
Объем азота в газообразном состоянии взрыво- и пожаробезопасен, останавливает окисление, гниение. Нефтехимия применяет газ в качестве продувки трубопроводов и резервуаров, проверяет работу трубопровода, находящегося под давлением. Горнодобывающее дело использует объем азота при создании взрывобезопасной среды шахт. Производство электроники применяет как продувку области, где нельзя допустить возможность окислением кислорода. Объем азота всегда успешно замещает воздух в случаях окисления.
Азотный газ всегда используют при дальнейшем синтезе самых разных соединений (это азотные удобрения, аммиак, красители, взрывчатые вещества и т. п.).
Пищевая промышленность зарегистрировала азот как пищевую добавку Е 941. Широкое и очень значимое применение газовой среды для упаковки, хранения продуктов. Используя объем азота в процессе упаковки, осуществляется возможность замедления роста анаэробных микроорганизмов, тем самым увеличивая срок хранения пищевых продуктов. Упакованные с добавлением газовой среды макаронные изделия, картофельные чипсы, сухие молочные продукты и др. не изменяют вкуса и запаха из-за низкой растворимости азота в воде.
Компания «Азотная станция» предлагает генераторы азота MAXIGAS, производящие азот из сжатого воздуха.
В природе азот в основной своей части находится в свободном положении и является важной составной частью воздуха, содержащего азота 78,2%. В воздухе над одним километром в квадрате находится 8 миллионов тонн азота. Земная кора содержит около 0,03 молярной доли. Азот относят к составу сложных органических соединений. Эти соединения называют белками, входящими в состав всех живых организмов. В процессе исчезновения и разложения их остатков образовываются новые простые азотные соединения, которые при подходящих им условиях (это может быть отсутствие влаги) накапливаются. Известный советский микробиолог сказал: «азот более драгоценен с общебиологической точки зрения, чем самые редкие из благородных металлов».
Главное свойство азота – это его инертность. В воде растворяется 15,4 мл/л при температуре 20С. Создание инертной среды, увеличивающее сроки хранения скоропортящейся продукции при перевозке и хранении. Это продукты, с высоким масло-жировым содержанием (сухие молочные продукты, картофельные чипсы, экструдированные кукурузные снеки, смеси орехов и т. д.) Упаковка при помощи газовой смеси, в основе которой 100% азота, предотвращает сплющивание упаковки, чем намного больше привлекает потребителя.
Следующее свойство – отсутствие запаха, вкуса и цвета.Помимо этого, газ участвует в синтезе аммиака. Из аммиака производится азотная кислота, взрывчатые вещества, различные минеральные удобрения. А за счет возможности создания инертной среды проводятся процессы перекачивания горючих жидкостей, проходит процесс обработки металлов (если они не вступают в контакт с азотом), разные химические процессы. При помощи азота протравливают принадлежности, используемые в медицинской сфере.
Такое свойство азота, как очень низкая температура кипения, позволяет использование жидкого азота в охладительных установках. В этом состоянии он не токсичное вещество, невзрывоопасен и инертен. Азот применяют и в косметологии, что показывает отличные результаты, его также используют для улучшения характеристик стали. Она может выдерживать нагрев до 500С и не терять своей твердости. Это происходит в случае, когда поверхность стали азотирована.
Невозможно выделить какое-то одно свойство, потому что все вышеперечисленные предполагают его использование во многих сферах.Популярная библиотека химических элементов. Раритетные издания. Наука и техника
Азот
| 7 | |
N |
5 2 |
| АЗОТ | |
| 14,0067 | |
| 2s22p3 | |
Всем известно: азот инертен. Часто мы сетуем за это на элемент №7, что естественно: слишком дорогой ценой приходится расплачиваться за его относительную инертность, слишком много энергии, сил и средств приходится тратить на его превращение в жизненно необходимые соединения.
Но, с другой стороны, не будь азот так инертен, в атмосфере произошли бы реакции азота с кислородом, и жизнь на пашей планете в тех формах, в которых она существует, стала бы невозможной. Растения, животные, мы с вами буквально захлебывались бы в потоках неприемлемых жизнью окислов и кислот. И «при всем при том» именно в окислы и азотную кислоту мы стремимся превратить возможно большую часть атмосферного азота. Это один из парадоксов элемента №7. (Здесь автор рискует быть обвиненным в тривиальности, ибо парадоксальность азота, вернее его свойств, стала притчей во языцех. И все же…)
Азот – элемент необыкновенный. Порою кажется, что чем больше мы о нем узнаем, тем непонятнее он становится. Противоречивость свойств элемента №7 отразилась даже в его названии, ибо ввела в заблуждение даже такого блистательного химика, как Антуан Лоран Лавуазье. Это Лавуазье предложил назвать азот азотом после того, как не первым и не последним получил и исследовал не поддерживающую дыхания и горения часть воздуха. Согласно Лавуазье, «азот» означает «безжизненный», и слово это произведено от греческого «а» – отрицание и «зоэ» – жизнь.
Термин «азот» бытовал еще в лексиконе алхимиков, откуда и заимствовал его французский ученый. Означал он некое «философское начало», своего рода кабалистическое заклинание. Знатоки утверждают, что ключом к расшифровке слова «азот» служит заключительная фраза из Апокалипсиса: «Я есть альфа и омега, начало и конец, первый и последний…» В средние века особо почитались три языка: латинский, греческий и древнееврейский. И слово «азот» алхимики составили из первой буквы «а» (а, альфа, алеф) и последних букв: «зет», «омега» и «тов» этих трех алфавитов. Таким образом, это таинственное синтетическое слово означало «начало и конец всех начал».
Современник и соотечественник Лавуазье Ж. Шапталь, не мудрствуя лукаво, предложил назвать элемент №7 гибридным латино-греческим именем «нитрогениум», что значит «селитру рождающий». Селитры – азотнокислые соли, вещества, известные с древнейших времен. (О них речь впереди.) Надо сказать, что термин «азот» укоренился только в русском и французском языках. По-английски элемент №7 – «Nitrogen», по-немецки – «Stockton» (удушающее вещество). Химический же символ N – дань шапталевскому нитрогениуму.
Кем открыт азот
Открытие азота приписывают ученику замечательного шотландского ученого Джозефа Блэка Даниелю Резерфорду, который в 1772 г. опубликовал диссертацию «О так называемом фиксируемом и мефитическом воздухе». Блэк прославился своими опытами с «фиксируемым воздухом» – углекислым газом. Он обнаружил, что после фиксирования углекислоты (связывания ее щелочью) остается еще какой-то «не фиксируемый воздух», который был назван «мефитическим» – испорченным – за то, что не поддерживал горения и дыхания. Исследование этого «воздуха» Блэк и предложил Резерфорду в качестве диссертационной работы.
Примерно в то же время азот был получен К. Шееле, Дж. Пристли, Г. Кавендишем, причем последний, как следовало из его лабораторных записей, изучал этот газ раньше Резерфорда, но, как всегда, не спешил с публикацией результатов своих трудов. Однако все эти выдающиеся ученые имели весьма смутное представление о природе открытого ими вещества. Они были убежденными сторонниками теории флогистона и связывали свойства «мефитического воздуха» с этой мнимой субстанцией. Только Лавуазье, ведя наступление на флогистон, убедился сам и убедил других, что газ, который он назвал «безжизненным», – простое вещество, как и кислород…
Вселенский катализатор?
Можно лишь догадываться, что означает «начало и конец всех начал» в алхимическом «азоте». Но об одном из «начал», связанных с элементом №7, можно говорить всерьез. Азот и жизнь – понятия неотделимые. По крайней мере, всякий раз, когда биологи, химики, астрофизики пытаются постичь «начало начал» жизни, то непременно сталкиваются с азотом.
Атомы земных химических элементов рождены в недрах звезд. Именно оттуда, от ночных светил и дневного светила, начинаются истоки нашей земной жизни. Это обстоятельство и имел в виду английский астрофизик У. Фаулер, говоря, что «все мы… являемся частичкой звездного праха»…
Звездный «прах» азота возникает в сложнейшей цепи термоядерных процессов, начальная стадия которых – превращение водорода в гелий. Это многостадийная реакция, идущая, как предполагают, двумя путями. Один из них, получивший название углеродно-азотного цикла, имеет самое непосредственное отношение к элементу №7. Этот цикл начинается, когда в звездном веществе, помимо ядер водорода – протонов, уже есть и углерод. Ядро углерода-12, присоединив еще один протон, превращается в ядро нестабильного азота-13:
126C + 11H → 137N + γ.
Но, испустив позитрон, азот снова становится углеродом – образуется более тяжелый изотоп 13С:
137N → 136C + е+ + γ.
Такое ядро, приняв лишний протон, превращается в ядро самого распространенного в земной атмосфере изотопа —14N.
136C + 11H → 147N + γ.
Увы, лишь часть этого азота отправляется в путешествие по Вселенной. Под действием протонов азот-14 превращается в кислород-15, а тот, в свою очередь, испустив позитрон и гамма-квант, превращается в другой земной изотоп азота – 15N:
147N + 11H → 158O + γ;
158O → 157N + е+ + γ.
Земной азот-15 стабилен, но и он в недрах звезды подвержен ядерному распаду; после того, как ядро 15N примет еще один протон, произойдет не только образование кислорода 16О, но и другая ядерная реакция:
157N + 11H → 126С + 42He.
В этой цепи превращений азот – один из промежуточных продуктов. Известный английский астрофизик Р.Дж. Тейлер пишет: «14N – изотоп, который нелегко построить. В углеродно-азотном цикле образуется азот, и, хотя впоследствии он снова превращается в углерод, все же если процесс протекает стационарно, то азота в веществе оказывается больше, чем углерода. Это, по-видимому, основной источник 14N»…
В умеренно сложном углеродно-азотном цикле прослеживаются любопытные закономерности. Углерод 12С играет в нем роль своеобразного катализатора. Судите сами, в конечном счете не происходит изменения количества ядер 12С. Азот же, появляясь в начале процесса, исчезает в конце… И если углерод в этом цикле – катализатор, то азот явно – аутокатализатор, т.е. продукт реакции, катализирующий ее дальнейшие промежуточные стадии.
Мы не случайно завели здесь речь о каталитических свойствах элемента №7. Но сохранил ли эту особенность звездный азот и в живом веществе? Катализаторы жизненных процессов – ферменты, и все они, равно как и большинство гормонов и витаминов, содержат азот.
Азот в атмосфере Земли
Жизнь многим обязана азоту, но и азот, по крайней мере атмосферный, своим происхождением обязан не столько Солнцу, сколько жизненным процессам. Поразительно несоответствие между содержанием элемента №7 в литосфере (0,01%) и в атмосфере (75,6% по массе или 78,09% по объему). В общем-то, мы обитаем в азотной атмосфере, умеренно обогащенной кислородом.
Между тем ни на других планетах солнечной системы, ни в составе комет или каких-либо других холодных космических объектов свободный азот не обнаружен. Есть его соединения и радикалы – CN*, NH*, NH*2, NH*3, а вот азота нет. Правда, в атмосфере Венеры зафиксировано около 2% азота, но эта цифра еще требует подтверждения. Полагают, что и в первичной атмосфере Земли элемента №7 не было. Откуда же тогда он в воздухе?
По-видимому, атмосфера нашей планеты состояла вначале из летучих веществ, образовавшихся в земных недрах: Н2, Н2О, СО2, СН4, NH3. Свободный азот если и выходил наружу как продукт вулканической деятельности, то превращался в аммиак. Условия для этого были самые подходящие: избыток водорода, повышенные температуры – поверхность Земли еще не остыла. Так что же, значит, сначала азот присутствовал в атмосфере в виде аммиака? Видимо, так. Запомним это обстоятельство.
Но вот возникла жизнь… Владимир Иванович Вернадский утверждал, что «земная газовая оболочка, наш воздух, есть создание жизни». Именно жизнь запустила удивительнейший механизм фотосинтеза. Один из конечных продуктов этого процесса – свободный кислород стал активно соединяться с аммиаком, высвобождая молекулярный азот:
CO2 + 2Н2О → фотосинтез → НСОН + Н2О + О2;
4NH3 + 3O2 → 2N2 + 6Н2О.
Кислород и азот, как известно, в обычных условиях между собой не реагируют, что и позволило земному воздуху сохранить «статус кво» состава. Заметим, что значительная часть аммиака могла раствориться в воде при образовании гидросферы.
В наше время основной источник поступления N2 в атмосферу – вулканические газы.
Если разорвать тройную связь…
Разрушив неисчерпаемые запасы связанного активного азота, живая природа поставила себя перед проблемой: как связать азот. В свободном, молекулярном состоянии он, как мы знаем, оказался весьма инертным. Виной тому – тройная химическая связь его молекулы: N≡N.
Обычно связи такой кратности малоустойчивы. Вспомним классический пример ацетилена: НС = СН. Тройная связь его молекулы очень непрочна, чем и объясняется невероятная химическая активность этого газа. А вот у азота здесь явная аномалия: его тройная связь образует самую стабильную из всех известных двухатомных молекул. Нужно приложить колоссальные усилия, чтобы разрушить эту связь. К примеру, промышленный синтез аммиака требует давления более 200 атм. и температуры свыше 500°C, да еще обязательного присутствия катализаторов… Решая проблему связывания азота, природе пришлось наладить непрерывное производство соединений азота методом гроз.
Статистика утверждает, что в атмосфере нашей планеты ежегодно вспыхивают три с лишним миллиарда молний. Мощность отдельных разрядов достигает 200 млн киловатт, а воздух при этом разогревается (локально, разумеется) до 20 тыс. градусов. При такой чудовищной температуре молекулы кислорода и азота распадаются на атомы, которые, легко реагируя друг с другом, образуют непрочную окись азота:
N2 + O2 → 2NО.
Благодаря быстрому охлаждению (разряд молнии длится десятитысячную долю секунды) окись азота не распадается и беспрепятственно окисляется кислородом воздуха до более стабильной двуокиси:
2NO + О2 → 2NO2.
В присутствии атмосферной влаги и капель дождя двуокись азота превращается в азотную кислоту:
3NO2 + H2O → 2HNO3 + NO.
Так, попав под свежий грозовой дождик, мы получаем возможность искупаться в слабом растворе азотной кислоты. Проникая в почву, атмосферная азотная кислота образует с ее веществами разнообразные естественные удобрения. Азот фиксируется в атмосфере и фотохимическим путем: поглотив квант света, молекула N2 переходит в возбужденное, активированное состояние и становится способной соединяться с кислородом…
Бактерии и азот
Из почвы соединения азота попадают в растения. Далее: «лошади кушают овес», а хищники – травоядных животных. По пищевой цепи идет круговорот вещества, в том числе и элемента №7. При этом форма существования азота меняется, он входит в состав все более сложных и нередко весьма активных соединений. Но не только «грозорожденный» азот путешествует по пищевым цепям..
Еще в древности было замечено, что некоторые растения, в частности бобовые, способны повышать плодородие почвы.
«…Или, как сменится год, золотые засеивай злаки
Там, где с поля собрал урожай, стручками шумящий,
Или где вика росла мелкоплодная с горьким лупином…»
Вчитайтесь: это же травопольная система земледелия! Строки эти взяты из поэмы Вергилия, написанной около двух тысяч лет назад.
Пожалуй, первым, кто задумался над тем, почему бобовые дают прибавки урожая зерновых, был французский агрохимик Ж. Буссенго. В 1838 г. он установил, что бобовые обогащают почву азотом. Зерновые же (и еще многие другие растения) истощают землю, забирая, в частности, все тот же азот. Буссенго предположил, что листья бобовых усваивают азот из воздуха, но это было заблуждением. В то время немыслимо было предположить, что дело не в самих растениях, а в особых микроорганизмах, вызывающих образование клубеньков на их корнях. В симбиозе с бобовыми эти организмы и фиксируют азот атмосферы. Сейчас это прописная истина…
В наше время известно довольно много различных азотфиксаторов: бактерии, актиномицеты, дрожжевые и плесневые грибки, сине-зеленые водоросли. И все они поставляют азот растениям. Но вот вопрос: каким образом без особых энергетических затрат расщепляют инертную молекулу N2 микроорганизмы? И почему одни из них обладают этой полезнейшей для всего живого способностью, а другие нет? Долгое время это оставалось загадкой. Тихий, без громов и молний механизм биологической фиксации элемента №7 был раскрыт лишь недавно. Доказано, что путь элементарного азота в живое вещество стал возможен благодаря восстановительным процессам, в ходе которых азот превращается в аммиак. Решающую роль при этом играет фермент нитрогеназа. Его центры, содержащие соединения железа и молибдена, активируют азот для «стыковки» с водородом, который предварительно активируется другим ферментом. Так из инертного азота получается весьма активный аммиак – первый стабильный продукт биологической азотфиксации.
Вот ведь как получается! Сначала процессы жизнедеятельности перевели аммиак первичной атмосферы в азот, а затем жизнь снова превратила азот в аммиак. Стоило ли природе на этом «ломать копья»? Безусловно, потому что именно так и возник круговорот элемента №7.
Залежи селитры и рост народонаселения
Природная фиксация азота молниями и почвенными бактериями ежегодно дает около 150 млн т. соединений этого элемента. Однако не весь связанный азот участвует в круговороте. Часть его выводится из процесса и отлагается в виде залежей селитры. Богатейшей такой кладовой оказалась чилийская пустыня Атакама в предгорьях Кордильер. Здесь годами не бывает дождей. Но изредка на склоны гор обрушиваются сильные ливни, вымывающие почвенные соединения. Потоки воды в течение тысячелетий выносили вниз растворенные соли, среди которых больше всего было селитры. Вода испарялась, соли оставались… Так возникло крупнейшее в мире месторождение азотных соединений.
Еще знаменитый немецкий химик Иоганн Рудольф Глаубер, живший в XVII в., отметил исключительную важность азотных солей для развития растений. В своих сочинениях, размышляя о круговороте азотистых веществ в природе, он употреблял такие выражения, как «нитрозные соки почвы» и «селитра – соль плодородия».
Но природную селитру в качестве удобрения стали применять лишь в начале прошлого века, когда стали разрабатывать чилийские залежи. В то время это был единственный значительный источник связанного азота, от которого, казалось, зависит благополучие человечества. Об азотной же промышленности тогда не могло быть и речи.
В 1824 г. английский священник Томас Мальтус провозгласил свою печально известную доктрину о том, что народонаселение растет гораздо быстрее, чем производство продуктов питания. В это время вывоз чилийской селитры составлял всего около 1000 т в год. В 1887 г. соотечественник Мальтуса, известный ученый Томас Гексли предсказал скорый конец цивилизации из-за «азотного голода», который должен наступить после выработки месторождений чилийской селитры (ее добыча к этому времени составляла уже более 500 тыс. т в год).
Через 11 лет еще один знаменитый ученый сэр Уильям Крукс заявил в Британском обществе содействия наукам, что не пройдет и полувека, как наступит продовольственный крах, если численность народонаселения не сократится. Он также аргументировал свой печальный прогноз тем, что «в скором времени предстоит полное истощение залежей чилийской селитры» со всеми отсюда вытекающими последствиями.
Пророчества эти не оправдались – человечество не погибло, а освоило искусственную фиксацию элемента №7. Более того, сегодня доля природной селитры – лишь 1,5% от мирового производства азотсодержащих веществ.
Как связывали азот
Соединения азота люди умели получать давно. Ту же селитру приготовляли в особых сараях – селитряницах, но очень уж примитивным был этот способ. «Выделывают селитру из куч навоза, золы, помета, оскребков кож, крови, картофельной ботвы. Кучи эти два года поливают мочою и переворачивают, после чего на них образуется налет селитры», – такое описание селитряного производства есть в одной старинной книге.
Источником соединений азота может служить и каменный уголь, в котором до 3% азота. Связанного азота! Этот азот стали выделять при коксовании углей, улавливая аммиачную фракцию и пропуская ее через серную кислоту.
Конечный продукт – сульфат аммония. Но и это, в общем-то, крохи. Трудно даже представить, какими путями развивалась бы наша цивилизация, не реши она вовремя проблему промышленно приемлемой фиксации атмосферного азота.
Впервые атмосферный азот связал еще Шееле. В 1775 г. он получил цианистый натрий, нагревая в атмосфере азота соду с углем:
Na2CO3 + 4С + N2 → 2NaCN + 3СО.
В 1780 г. Пристли установил, что объем воздуха, заключенный в сосуде, перевернутом над водой, уменьшается, если через него пропускать электрическую искру, а вода приобретает свойства слабой кислоты. Этот эксперимент был, как мы знаем (Пристли этого не знал), моделью природного механизма фиксации азота. Четыре года спустя Кавендиш, пропуская электрический разряд через воздух, заключенный в стеклянной трубке со щелочью, обнаружил там селитру.
И хотя все эти эксперименты не могли в то время выйти за пределы лабораторий, в них виден прообраз промышленных способов фиксации азота – цианамидного и дугового, появившихся на рубеже XIX…XX вв.
Цианамидный способ был запатентован в 1895 г. немецкими исследователями А. Франком и Н. Каро. По этому способу азот при нагревании с карбидом кальция связывался в цианамид кальция:
CaC2 + N2 → Ca(CN)2.
В 1901 г. сын Франка, подав идею о том, что цианамид кальция может служить хорошим удобрением, по существу, положил начало производству этого вещества. Росту индустрии связанного азота способствовало появление дешевой электроэнергии. Наиболее перспективным способом фиксации атмосферного азота в конце XIX в. считался дуговой, при помощи электрического разряда. Вскоре после строительства Ниагарской электростанции американцы неподалеку пустили (в 1902 г.) первый дуговой завод. Через три года в Норвегии вступила в строй дуговая установка, разработанная теоретиком и специалистом по изучению северного сияния X. Биркеландом и инженером-практиком С. Эйде. Заводы подобного типа получили широкое распространение; селитру, которую они выпускали, называли норвежской. Однако расход электроэнергии при этом процессе был чрезвычайно велик и составлял до 70 тыс. киловатт/час на тонну связанного азота, причем только 3% этой энергии использовалось непосредственно на фиксацию.
Через аммиак
Перечисленные выше способы фиксации азота были лишь подходами к методу, появившемуся незадолго до первой мировой войны. Это о нем американский популяризатор науки Э. Слоссон весьма остроумно заметил: «Всегда говорилось, что англичане господствуют на море, а французы – на суше, немцам же остается только воздух. К этой шутке немцы отнеслись как будто бы серьезно и принялись использовать воздушное царство для нападения на англичан и французов… Кайзер… обладал целым флотом цеппелинов и таким способом фиксации азота, который не был известен никакой другой нации. Цеппелины разрывались, как мешки с воздухом, но заводы, фиксирующие азот, продолжали работать и сделали Германию независимой от Чили не только в годы войны, но и в мирное время»… Речь идет о синтезе аммиака – основном процессе современной индустрии связанного азота.
Слоссон был не совсем прав, говоря о том, что способ фиксации азота в аммиак не был известен нигде, кроме Германии. Теоретические основы этого процесса были заложены французскими и английскими учеными. Еще в 1784 г. знаменитый К. Бертолле установил состав аммиака и высказал мысль о химическом равновесии реакций синтеза и разложения этого вещества. Через пять лет англичанином У. Остином была предпринята первая попытка синтеза NH3 из азота и водорода. И, наконец, французский химик А. Ле Шателье, отчетливо сформулировав принцип подвижного равновесия, первым синтезировал аммиак. При этом он применил высокое давление и катализаторы – губчатую платину и железо. В 1901 г. Ле Шателье запатентовал этот способ.
Исследования по синтезу аммиака в начале века проводили также Э. Перман и Г. Аткинс в Англии. В своих экспериментах эти исследователи в качестве катализаторов применяли различные металлы, в частности медь, никель и кобальт…
Но наладить синтез аммиака из водорода и азота в промышленных масштабах впервые удалось, действительно, в Германии. В этом заслуга известного химика Фрица Габера. В 1918 г. он был удостоен Нобелевской премии по химии.
Технология производства NH3, разработанная немецким ученым, очень сильно отличалась от других производств того времени. Здесь впервые был применен принцип замкнутого цикла с непрерывно действующей аппаратурой и утилизацией энергии. Окончательную разработку технологии синтеза аммиака завершил коллега и друг Габера К. Бош, который в 1931 г. также был удостоен Нобелевской премии – за развитие методов химического синтеза при высоких давлениях.
По пути природы
Синтез аммиака стал еще одной моделью природной фиксации элемента №7. Напомним, что микроорганизмы связывают азот именно в NH3. При всех достоинствах процесса Габера – Боша он выглядит несовершенным и громоздким по сравнению с природным!
«Биологическая фиксация атмосферного азота… была неким парадоксом, постоянным вызовом для химиков, своего рода демонстрацией недостаточности наших знаний». Эти слова принадлежат советским химикам М.Е. Вольпину и А.Е. Шилову, которые предприняли попытку фиксации молекулярного азота в мягких условиях.
Сначала были неудачи. Но в 1964 г. в Институте элементоорганических соединении АН СССР, в лаборатории Вольпина, было сделано открытие: в присутствии соединений переходных металлов – титана, ванадия, хрома, молибдена и железа – элемент №7 активируется и при обычных условиях образует комплексные соединения, разлагаемые водой до аммиака. Именно эти металлы служат и центрами фиксации азота в ферментах азотфиксаторов, и прекрасными катализаторами в производстве аммиака.
Вскоре после этого канадские ученые А. Аллен и К. Зеноф, исследуя реакцию гидразина N2H2 с треххлористым рутением, получили химический комплекс, в котором, опять же в мягких условиях, азот оказался связанным. Этот результат настолько противоречил обычным представлениям, что редакция журнала, куда исследователи послали свою статью с сенсационным сообщением, отказалась ее печатать. В дальнейшем советским ученым удалось в мягких условиях получить и азотсодержащие органические вещества. Пока еще рано говорить о промышленных способах мягкой химической фиксации атмосферного азота, однако, достигнутые успехи позволяют предвидеть надвигающуюся революцию в технологии связывания элемента №7.
Современной наукой не забыты и старые способы получения азотных соединений через окислы. Здесь главные усилия направлены на разработку технологических процессов, ускоряющих расщепление молекулы N2 на атомы. Наиболее перспективными направлениями окисления азота считают сжигание воздуха в специальных печах, применение плазмотронов, использование для этих целей пучка ускоренных электронов.
Чего бояться?
Сегодня нет оснований опасаться, что человечество когда-либо будет испытывать недостаток в соединениях азота. Промышленная фиксация элемента №7 прогрессирует невероятными темпами. Если в конце 60-х годов мировое производство связанного азота составляло 30 млн т., то к началу будущего века оно, по всей вероятности, достигнет миллиарда тонн!
Такие успехи не только радуют, но и вызывают опасения. Дело в том, что искусственная фиксация N2 и внесение в почву огромного количества азотсодержащих веществ – самое грубое и значительное вмешательство человека в естественный круговорот веществ. В наше время азотные удобрения не только вещества плодородия, но и загрязнители окружающей среды. Они вымываются из почвы в реки и озера, вызывают вредное цветение водоемов, разносятся воздушными потоками на дальние расстояния…
В подземные воды уходит до 13% азота, содержащегося в минеральных удобрениях. Азотные соединения, особенно нитраты, вредны для людей и могут быть причиной отравлений. Вот вам и кормилец-азот!
Всемирная организация здравоохранения (ВОЗ) приняла предельно допустимую концентрацию нитратов в питьевой воде: 22 мг/л для умеренных широт и 10 мг/л для тропиков. В СССР санитарные нормы регламентируют содержание нитратов в воде водоемов по «тропическим» меркам – не более 10 мг/л. Выходит, что нитраты средство «обоюдоострое»…
4 октября 1957 г. человечество еще раз вмешалось в круговорот элемента №7, запустив в космос «шарик», заполненный азотом, – первый искусственный спутник…
Менделеев об азоте
«Хотя деятельнейшую, т.е. наиболее легко и часто химически действующую часть окружающего нас воздуха, составляет кислород, но наибольшую массу его, судя как по объему, так и по весу, образует азот; а именно газообразный азот составляет более 3/4, хотя и менее 4/5 объема воздуха. А так как азот лишь немногим легче кислорода, то весовое содержание азота в воздухе составляет около 3/4 всей его массы. Входя в таком значительном количестве в состав воздуха, азот, по-видимому, не играет особо видной роли в атмосфере, химическое действие которой определяется преимущественно содержанием в ней кислорода. Но правильное представление об азоте получается только тогда, когда узнаем, что в чистом кислороде животные не могут долго жить, даже умирают, и что азот воздуха, хотя лишь медленно и мало-помалу, образует разнообразные соединения, часть которых играет важнейшую роль в природе, особенно в жизни организмов».
Где применяют азот
Азот – самый дешевый из всех газов, химически инертных в обычных условиях. Его широко применяют в химической технологии для создания неокислительных сред. В лабораториях в атмосфере азота хранят легко окисляющиеся соединения. Выдающиеся произведения живописи иногда (в хранилищах или при транспортировке) помещают в герметические футляры, заполненные азотом, – чтобы предохранить краски от влаги и химически активных компонентов воздуха.
Значительной бывает роль азота в металлургии и при металлообработке. Различные металлы в расплавленном состоянии реагируют на присутствие азота по-разному. Медь, например, абсолютно инертна по отношению к азоту, поэтому изделия из меди часто сваривают в струе этого газа. Магний, напротив, при горении на воздухе дает соединения не только с кислородом, но и с азотом. Так что для работы с изделиями из магния при высоких температурах азотная среда неприменима. Насыщение азотом поверхности титана придает металлу большую прочность и износостойкость – на ней образуется очень прочный и химически инертный нитрид титана. Эта реакция идет лишь при высоких температурах.
При обыкновенной температуре азот активно реагирует только с одним металлом – литием.
Наибольшее количество азота идет на производство аммиака.
Азотный наркоз
Распространенное мнение о физиологической инертности азота не совсем правильно. Азот физиологически инертен при обычных условиях.
При повышенном давлении, например при погружении водолазов, растет концентрация растворенного азота в белковых и особенно жировых тканях организма. Это приводит к так называемому азотному наркозу. Водолаз словно пьянеет: нарушается координация движений, мутится сознание. В том, что причина этого – азот, ученые окончательно убедились после проведения экспериментов, в которых вместо обычного воздуха в скафандр водолаза подавалась гелио-кислородная смесь. При этом симптомы наркоза исчезли.
Космический аммиак
Большие планеты солнечной системы Сатурн и Юпитер состоят, как полагают астрономы, частично из твердого аммиака. Аммиак замерзает при –78°C, а на поверхности Юпитера, например, средняя температура – 138°C.
Аммиак и аммоний
В большой семье азота есть странное соединение – аммоний NH4. В свободном виде он нигде не встречается, а в солях играет роль щелочного металла. Название «аммоний» предложил в 1808 г. знаменитый английский химик Хэмфри Дэви. Латинское слово ammonium когда-то означало: соль из Аммонии. Аммония – область в Ливии. Там находился храм египетского бога Аммона, по имени которого и называли всю область. В Аммонии издавна получали аммонийные соли (в первую очередь нашатырь), сжигая верблюжий навоз. При распаде солей получался газ, который сейчас называют аммиаком.
С 1787 г. (в том самом году, когда был принят термин «азот») комиссия по химической номенклатуре дала этому газу имя ammoniaque (аммониак). Русскому химику Я.Д. Захарову это название показалось слишком длинным, и в 1801 г. он исключил из него две буквы. Так получился аммиак.
Веселящий газ
Из пяти окислов азота два – окись (NO) и двуокись (NO2) – нашли широкое промышленное применение. Два других – азотистый ангидрид (N2O3) и азотный ангидрид (N2O5) – не часто встретишь и в лабораториях. Пятый – закись азота (N2O). Она обладает весьма своеобразным физиологическим действием, за которое ее часто называют веселящим газом.
Выдающийся английский химик Хэмфри Дэви с помощью этого газа устраивал специальные сеансы. Вот как описывал действие закиси азота один из современников Дэви: «Одни джентльмены прыгали по столам и стульям, у других развязались языки, третьи обнаружили чрезвычайную склонность к потасовке».
Свифт смеялся напрасно
Выдающийся писатель-сатирик Джонатан Свифт охотно издевался над бесплодием современной ему науки. В «Путешествиях Гулливера», в описании академии Лагадо, есть такое место: «В его распоряжении были две большие комнаты, загроможденные самыми удивительными диковинами; пятьдесят помощников работали под его руководством. Одни сгущали воздух в сухое плотное вещество, извлекая из него селитру…»
Сейчас селитра из воздуха – вещь абсолютно реальная. Аммиачную селитру NH4NO3 действительно делают из воздуха и воды.
Бактерии связывают азот
Идею о том, что некоторые микроорганизмы могут связывать азот воздуха, первым высказал русский физик П. Коссович. Русскому биохимику С.Н. Виноградскому первому удалось выделить из почвы один вид бактерий, связывающих азот.
Растения разборчивы
Дмитрий Николаевич Прянишников установил, что растение, если ему предоставлена возможность выбора, предпочитает аммиачный азот нитратному. (Нитраты – соли азотной кислоты).
Важный окислитель
Азотная кислота HNO3 – один из самых важных окислителей, применяемых в химической промышленности. Первым ее приготовил, действуя серной кислотой на селитру, один из крупнейших химиков XVII в. Иоганн Рудольф Глаубер.
Среди соединений, получаемых сейчас с помощью азотной кислоты, многие совершенно необходимые вещества: удобрения, красители, полимерные материалы, взрывчатые вещества.
Двойная роль
Некоторые азотсодержащие соединения, применяемые в агрохимии, выполняют двоякие функции. Например, цианамид кальция хлопкоробы применяют как дефолиант – вещество, вызывающее опадение листьев перед уборкой урожая. Но это соединение одновременно служит и удобрением.
Азот в ядохимикатах
Далеко не все вещества, в состав которых входит азот, способствуют развитию любых растений. Аминные соли феноксиуксусной и трихлорфеноксиуксусной кислот – гербициды. Первая подавляет рост сорняков на полях злаковых культур, вторая применяется для очистки земель под пашни – уничтожает мелкие деревья и кустарники.
Полимеры: от биологических до неорганических
Атомы азота входят в состав многих природных и синтетических полимеров – от белка до капрона. Кроме того, азот – важнейший элемент безуглеродных, неорганических полимеров. Молекулы неорганического каучука – полифосфонитрилхлорида – это замкнутые циклы, составленные из чередующихся атомов азота и фосфора, в окружении ионов хлора. К неорганическим полимерам относятся и нитриды некоторых металлов, в том числе и самое твердое из всех веществ – боразон.
• Кислород
• Оглавление
Дата публикации:
17 февраля 2002 года
n-t.ru
Азот
Азот (лат. Nitrogenum) химический элемент V группы периодической системы Менделеева, атомный номер 7, атомная масса — 14,0067. Бесцветный газ, без вкуса и запаха. Один из самых распространенных элементов, главная составляющая часть атмосферы Земли (4*10^15 т). Слово «азот», предложенное французским химиком А. Лавуазье в конце XVIII в., греческого происхождения. «Азот» означает «безжизненный» (приставка «а» — отрицание. «зоэ» — жизнь). Именно так считал Лавуазье. Именно так считали его современники, в том числе шотландский химик и врач Д. Резерфорд, выделивший азот из воздуха чуть раньше своих известных коллег — шведа К. Шееле, англичан Д. Пристли и Г. Кавендиша. Резерфорд в 1772г. опубликовал диссертацию о так называемом «мафическом», т.е. неполноценном, воздухе, не поддерживающем горения и дыхания.
Название « азот » для нового газа казалось достаточно точным. Но так ли это? Азот действительно, в отличие от кислорода, не поддерживает дыхания и горения. Однако дышать чистым кислородом постоянно человек не может. Даже больным дают чистый кислород лишь непродолжительное время. На всех орбитальных станциях, на космических кораблях «Союз» и «Восток» космонавты дышали привычным атмосферным воздухом, почти на 4/5 состоящим из азота. Очевидно, он не просто нейтральный разбавитель кислорода. Именно смесь азота с кислородом наиболее приемлема для дыхания большинства обитателей нашей планеты.
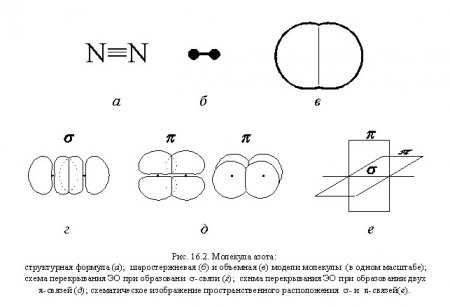
А разве справедливо называть безжизненным этот элемент? Чем подкармливают растения, внося минеральные удобрения? Прежде всего, соединениями азота, калия и фосфора. Азот входит в состав бесчисленного множества органических соединений, в том числе, таких жизненно важных, как белки и аминокислоты.
Для человечества чрезвычайно полезна относительная инертность этого газа. Будь он более склонен к химическим реакциям, атмосфера Земли не могла бы существовать в том виде, в каком она существует. Сильный окислитель кислород вступил бы с азотом в реакцию, и образовались бы ядовитые оксиды азота. Но если бы азот был действительно инертным газом, таким, например, как гелий, то тогда ни химические производства, ни всемогущие микроорганизмы не смогли бы связать азот атмосферы и удовлетворить потребность всего живого в связанном азоте. Не было бы аммиака, азотной кислоты, необходимой для производства множества веществ, не было бы важнейших удобрений. Не было бы и жизни на Земле, ведь азот входит в состав всех организмов. На долю азота приходится немалая часть от массы человеческого организма.
Элементарный, не связанный азот применяется достаточно широко. Это самый дешевый из газов, химически инертных в обычных условиях, поэтому в тех процессах металлургии и большой химии, где надо защищать активное соединение или расплавленный металл от взаимодействия с кислородом воздуха, создают чисто азотные защитные атмосферы. Под защитой азота хранят в лабораториях легко окисляющиеся вещества. В металлургии азотом насыщают поверхности некоторых металлов и сплавов, чтобы придать им большую твердость и износоустойчивость. Широко известно, например, азотирование стали и титановых сплавов.

Жидкий азот (температуры плавления и кипения азота: — 210°С и — 196°С) используют в холодильных установках. Малая химическая активность азота объясняется, прежде всего, строением его молекулы. Как и у большинства газов (кроме инертных), молекула азота состоит из двух атомов. В образовании связи между ними участвуют по 3 валентных электрона внешней оболочки каждого атома. Чтобы разрушить молекулу азота, необходимо затратить очень большую энергию — 954,6 кДж/моль. Без разрушения молекулы азот в химическую связь не вступит. При обычных условиях с ним способен вступить в реакцию только литий, давая нитрид Li3N. Намного активнее атомарный азот. При обычной температуре он вступает в реакции с серой, фосфором, мышьяком и некоторыми металлами, например с ртутью. Но получить азот в виде отдельных атомов сложно. Даже при 3000 С не наблюдается заметного разложения молекул азота на атомы.
Соединения азота имеют громадное значение и для науки, и для многих отраслей промышленности. Ради получения связанного азота человечество идет на огромные энергетические затраты.
Основным способом связывания азота в промышленных условиях остается синтез аммиака Nh4 (см. Синтез химический). Аммиак один из самых массовых продуктов химической промышленности, мировое производство его — более 70 млн. т. в год. Процесс идет при температуре 400-600° С и давлении в миллионы паскалей (сотни ат) в присутствии катализаторов, например губчатого железа с добавками оксида калия, оксида алюминия. Сам аммиак используется ограниченно и обычно в виде водных растворов (аммиачная вода как жидкое удобрение, нашатырный спирт — в медицине). Но аммиак, в отличие от атмосферного азота, довольно легко вступает в реакции присоединения и замещения. Да и окисляется он легче, чем азот. Поэтому аммиак и стал исходным продуктом для получения большинства азотсодержащих веществ.
Прямое окисление азота кислородом требует очень высоких температур (4000С°) или других очень активных методов воздействия на прочные молекулы азота электрического разряда, ионизирующего излучения. Известны пять оксидов азота (II) N3O оксид азота (III), N2O3 оксид азота (III), N2O3 оксид азота (III), NО2 оксид азота (IV), N2O5, оксид азота (V).
В промышленности широко применяется азотная кислота HNO3, которая одновременно является и сильной кислотой, и активным окислителем. Она способна растворять все металлы, кроме золота и платины. Химикам азотная кислота известна, по крайней мере, с XIII в., ею пользовались древние алхимики. Азотная кислота чрезвычайно широко используется для получения нитросоединений. Это главный нитрующий агент, с помощью которого в состав органических соединений вводят нитргруппы NO2. А когда три таких группы появятся, к примеру, в молекуле толуола С6Н5СН3, то обычный органический растворитель превращается во взрывчатое вещество тринитротолуол, тротил, или тол. Глицерин после нитрования превращается в опасное взрывчатое вещество нитроглицерин.
Не менее важна азотная кислота в производстве минеральных удобрений. Соли азотной кислоты-нитраты, прежде всего нитрат натрия, калия и аммония, используются главным образом как азотные удобрения. Но, как установил академик Д. Н. Прянишников, растение, если ему предоставлена возможность выбора, предпочитает аммиачный азот нитратному.
Соли другой кислоты азота — слабой азотистой HNO2 — называются нитритами и также довольно широко используются в химической и других отраслях промышленности. Нитрит натрия, например, в небольших дозах добавляют в колбасы и ветчину, чтобы сохранить присущий мясу розово-красный цвет.
Получать соединения азота с минимальными энергетическими затратами при небольших температурах и давлениях ученые стремятся уже давно. Идею о том, что некоторые микроорганизмы могут связывать азот воздуха, первым высказал русский физик П. Коссович в конце XIX в. А выделил из почвы первую азотфиксирующую бактерию другой наш соотечественник биохимик С. Н, Виноградский в 1890-е гг. Но лишь в последнее время стал более или менее ясен механизм связывания азота бактериями. Бактерии усваивают азот, превращая его в аммиак, который затем очень быстро превращается в аминокислоты и белки. Процесс идет при участии ферментов.
В лабораториях нескольких стран получены комплексные соединения, способные связывать атмосферный азот. Главная роль при этом отводится комплексам, содержащим молибден, железо и магний. В основном уже изучен и разработан механизм этого процесса.
nanolife.info
Азот — Циклопедия
Азот
Химический элемент
| Символ, номер | N, 7 |
| Атомная масса | 14,00643 а.е.м. |
| Электронная конфигурация | [He] 2s2 2p3 |
| Электроотрицательность | 3,04 по шкале Поллинга |
| Степени окисления | 5; 4; 3; 2; 1; 0; −1; −2; −3 |
| Плотность | 0,001251 г/см³ (при н.у.) |
| Температура плавления | -209,86 °C |
| Температура кипения | -195,75 °C |
| Структура кристаллической решетки | кубическая |
| Теплопроводность | (300 K) 0,026 Вт/(м·К) |
Азот — весьма инертный химический элемент.
[править] История открытия
В работе «Химический трактат о воздухе и огне» шведский химик К. Шееле описал получение и свойства «огненного воздуха» и отметил, что атмосферный воздух состоит из двух «видов воздуха»: «огненного» — кислорода и «флогистованого» — азота. Однако приоритет открытия кислорода принадлежит Джозефу Пристли, потому что труд Шееле был опубликован только в 1777 году.
В 1772 году азот (под названием «испорченного воздуха») как простое вещество описал Даниэль Резерфорд, он опубликовал магистерскую диссертацию, где указал основные свойства азота (не реагирует со щелочами, не поддерживает горения, непригоден для дыхания). Именно Даниэль Резерфорд и считается первооткрывателем азота.
[править] Происхождение названия
Название «азот» (от греч. ἀζωτος — безжизненный, (на других языках: лат. Nitrogenium — то, что порождает селитру) предложено в 1787 Антуан Лавуазье, который в то время в составе группы других французских ученых разрабатывал принципы химической номенклатуры.
[править] Распространение в природе
Круговорот азота в природеОбщее содержание азота в земной коре составляет 1 · 10−2 % по массе. Основная его масса находится в воздухе. Сухой воздух содержит в среднем 78,09 % по объему (или 75,6 % по массе) свободного азота, соответствует общей массе 4 • 1015 т.[1] В отношении малых количествах свободный азот находится в растворенном состоянии в водах океанов. В виде соединений с другими элементами (связанный азот) входит в состав всех растительных и животных организмов. Мощные месторождения азота в виде так называемой чилийской селитры известны лишь в Чили (Южная Америка). Кроме того, небольшие количества азота содержатся в почве, главным образом в виде органических соединений и солей азотной кислоты.
Азот имеет два стабильных изотопа: 14N (99,63 %) и 15N (0,37 %). Искусственно получено 4 радиоактивных изотопа азота с массовыми числами 12, 13, 16, 17.
[править] Химические свойства
Азот входит в главной подгруппы пятой группы периодической системы Менделеева. Порядковый номер его 7. Атомы азота имеют во внешней электронной оболочке пять электронов. Поэтому они могут присоединять три электрона, которых им не хватает для образования полностью заполненной восемью электронами оболочки, и восстанавливаться до ионов N 3 или терять пять валентных электронов, превращаясь в положительно заряженные ионы и проявляя при этом свою максимальную положительную валентность. Атомы азота также могут терять и меньшее количество электронов, проявляя при этом положительную валентность 1+, 2+, 3+ и 4+.
Молекулы азота двухатомные, оба атома прочно связаны между собой тремя общими электронными парами.
Чтобы разложить молекулу азота на атомы, надо потратить значительное количество энергии. Поэтому азот при обычных условиях химически довольно пассивный.
При высоких температурах, когда молекулы азота разлагаются и он переходит в атомарное состояние, он сравнительно легко вступает в реакции с металлами (особенно с активными), образуя так называемые нитриды. При высокой температуре, высоком давлении и наличии катализатора оксид соединяется с водородом с образованием аммиака. При температуре электрической искры (свыше 3000 °C) азот реагирует с кислородом, образуя неустойчивый при высокой температуре монооксид азота NO по реакции:
В природе эта реакция происходит при грозовых разрядах.
[править] Другие свойства
В обычных условиях азот физиологически инертен, но при вдыхании сжатого воздуха наступает состояние, называемое азотным наркозом, подобное алкогольному опьянению. Эти случаи могут быть при условии водолазных работ на глубине нескольких десятков метров. Для предупреждения возникновения данного состояния порой пользуются искусственными газовыми смесями, в которых азот заменен гелием или иным инертным газом. При резком и значительном снижении парциального давления азота, растворимость его в крови и тканях настолько уменьшается, что часть его выделяется в виде пузырьков, является одной из причин возникновения кессонной болезни, которая наблюдается у водолазов при быстром их поднятии на поверхность и у пилотов при больших скоростях взлета самолета, а также при входе в верхние слои атмосферы.
В смеси с кислородом азот используется как слабый наркотик, вызывающий состояние опьянения, эйфории, притупление болевой чувствительности. Используется для ингаляционного наркоза.
Получение азота разложением нитрита аммонияВ лабораторных условиях чистый азот обычно получают путем разложения при нагревании раствора нитрита аммония по реакции:
Еще один из лабораторных способов — пропускание аммиака над оксидом меди (II) при температуре 700 °C:
- 2NH3 + 3CuO → N2↑ + 3H2O + 3Cu.
Аммиак берут из насыщенного раствора при нагревании, количество CuO в 2 раза больше расчетного. Непосредственно перед применением азот очищают от примесей кислорода и аммиака пропусканием над медью и ее оксидом (II), затем сушат концентрированной серной кислотой и сухой щелочью. Процесс достаточно медленный, но газ получается довольно чистый.
В промышленности азот в больших количествах добывают из воздуха с помощью азотных станций.
Жидкий азотЖидкий азот применяется как хладагент и для криотерапии.
Промышленное применение газообразного азота обусловлены его инертными свойствами. Газообразный азот пожаро- и взрывобезопасный, препятствует окислению, гниению. В нефтехимии азот применяется для продувки резервуаров и трубопроводов, проверки работы трубопроводов под давлением, увеличение выработки месторождений. В горном деле азот может использоваться для создания в шахтах взрывобезопасной среды, для распирания пластов породы. В производстве электроники азот применяется для продувки областей, не допускающих наличия кислорода. Если в процессе, традиционно проходит с использованием воздуха, окисления или гниения являются негативными факторами — азот может успешно заменить воздух.
Большая часть получаемого в технике азота используется для производства аммиака.
В последнее время значительное распространение получило использование азота для создания инертной среды при проведении некоторых химических реакций, при перекачке горючих жидкостей и т. д.
Поскольку азот имеет низкую температуру кипения (77,4 К), то сжиженный азот является одним из главных криогенных жидостей.
Азот присутствует во многих взрывчатых веществах. Их свойства объясняются тем, что образование молекулы азота приводит к установлению очень прочной тройной связи, при этом высвобождается большое количество энергии.
- ↑ Кравчук П. А. Рекорды природы. — Любешов: Эрудит, 1993, 216 с.
- Глоссарий терминов по химии // Й.Опейда, О.Швайка. Ин-т физико-органической химии и углехимии им. Л. М. Литвиненко НАН Украины, Донецкий национальный университет — Донецк: «Вебер», 2008. — 758 с. ISBN 978-966-335-206-0
- Украинская советская энциклопедия. В 12-ти томах / Под ред. М. Желаемая. — 2-е изд. — К. : Гол. редакция УРЕ, 1974—1985.
- Ф. А. Деркач «Химия» Л. 1968
- Малая горная энциклопедия . В 3-х т. / Под ред. В. С. Белецкого. — Донецк: Донбасс, 2004.
cyclowiki.org
Азот — характеристика элемента, физические и химические свойства простого вещества. Аммиак, соли аммония.
 Азот (N) находится во втором периоде, пятой группе главной подгруппы. Порядковый номер – 7, Ar – 14,008.
Азот (N) находится во втором периоде, пятой группе главной подгруппы. Порядковый номер – 7, Ar – 14,008.
Молекула N2 – самая прочная из всех двухатомных за счет наличия тройной связи малой длины (энергия связи – 946 кДж). Связь в молекуле ковалентная неполярная.
Физические свойства: бесцветный газ, без запаха и вкуса; малорастворим в воде: в 1 л h3O растворяется 15,4 мл N2 при t° = 20 °C и p = 1 атм; t кипения =-196 °C; t плавления =-210 °C. Природный азот состоит из двух изотопов с атомными массами: 14 и 15.
Химические свойства азота: Атом азота имеет 7 электронов, из них 5 на внешнем уровне (5 валентных электронов). Он является одним из самых электроотрицательных элементов (3,04 по шкале Полинга), уступая лишь хлору (3.16), кислороду (3,44) и фтору (3,98).
Характерная валентность – 3 и 4.
Наиболее характерные степени окисления: -3, -2, -1, +2, +3, +4, +5, 0. В обычных условиях азот подобен инертному газу.
В обычных условиях азот непосредственно взаимодействует лишь с литием с образованием Li3N. При нагревании (то есть активации молекул N2) или воздействии электрического разряда вступает в реакцию со многими веществами, обычно выступает как окислитель (азот по электроотрицательности на 3 месте после кислорода и фтора) и лишь при взаимодействии со фтором и кислородом – как восстановитель.
N2 + 3H2 ↔ 2NH3
N2 + 2B → 2BN
3Si + 2N2 → Si3N4
3Ca + N2 → Ca3N2
N2 + O2 → 2NO.
Получение азота. В промышленности азот получают путем сжижения воздуха с последующим испарением и отделением азота от других газовых фракций воздуха (перегонка). Полученный азот содержит примеси благородных газов (аргона).
В лабораториях обычно используется азот, доставляемый с производства в стальных баллонах под повышенным давлением или жидкий азот в сосудах Дьюара. Можно получать азот разложением некоторых его соединений:
NH4NO2 → N2 + 2H2O (при to)
(NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O (при to)
2N2O → 2N2 + O2 (при to)
Особо чистый азот получают термическим разложением азида натрия:
2NaN3 → 2Na + 3N2 (при to)
Нахождение в природе: в природе азот встречается в основном в свободном состоянии. Содержание азота в воздухе — его объемная доля 78,09 %. В небольшом количество соединения азота находится в почве; азот входит в состав аминокислот, образующих через посредство пептидных связей белки; содержится в молекулах нуклеиновых кислот – ДНК и РНК – в составе азотистых оснований (нуклеотидов): гуанина, аденила, тимидила, цитизила и уридила. Общее содержание азота в земной коре – 0,01 %. Из минералов промышленное значение имеют чилийская селитра NaNO3 и индийская селитра KNO3.
himege.ru
Оксид азота (I, II, III, IV, V): свойства, получение, применение
Введение
Если внимательно взглянуть на азот в периодической системе химических элементов Д. И. Менделеева, то можно заметить, что он имеет переменную валентность. Это значит, что азот образует сразу несколько бинарных соединений с кислородом. Некоторые из них были открыты недавно, а некоторые — изучены вдоль и поперек. Существуют малостабильные и устойчивые оксиды азота. Химические свойства каждого из этих веществ совершенно разные, поэтому при их изучении нужно рассматривать как минимум пять оксидов азота. Вот о них и пойдет речь в сегодняшней статье.
Оксид азота (I)
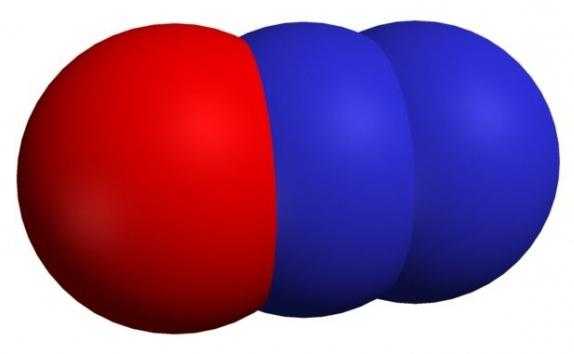 Формула — N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом.
Формула — N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом.
Свойства
В обычных условиях представлен бесцветным газом, имеющим сладковатый запах. Его могут растворять вода, этанол, эфир и серная кислота. Если газобразный оксид одновалентного азота нагреть до комнатной температуры под давлением 40 атмосфер, то он сгущается до бесцветной жидкости. Это несолеобразующий оксид, разлагающийся во время нагревания и показывающий себя в реакциях как восстановитель.
Получение
Этот оксид образуется, когда нагревают сухой нитрат аммония. Другой способ его получения — термическое разложение смеси «сульфаминовая + азотная кислота».
Применение
Используется в качестве средства для ингаляционного наркоза, пищевая промышленность знает этот оксид как добавку E942. С его помощью также улучшают технические характеристики двигателей внутреннего сгорания.
Оксид азота (II)
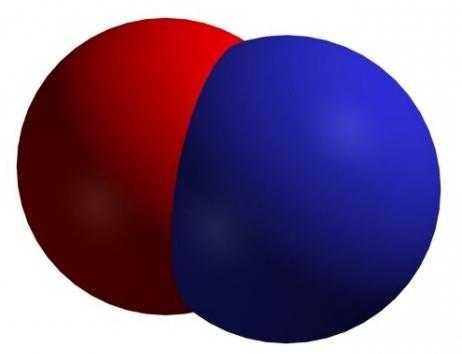 Формула — NO. Встречается под названиями монооксида азота, окиси азота и нитрозил-радикала
Формула — NO. Встречается под названиями монооксида азота, окиси азота и нитрозил-радикала
Свойства
При нормальных условиях имеет вид бесцветного газа, который плохо растворяется в воде. Его трудно сжижить, однако в твердом и жидком состояниях это вещество имеет голубой цвет. Данный оксид может окисляться кислородом воздуха
Получение
Его довольно просто получить, для этого нужно нагреть до 1200-1300оС смесь азота и кислорода. В лабораторных условиях он образуется сразу при нескольким опытах:
- Реакция меди и 30%-ного раствора азотной кислоты.
- Взаимодействие хлорида железа, нитрита натрия и соляной кислоты.
- Реакция азотистой и иодоводородной кислот.
Применение
Это одно из веществ, из которых получают азотную кислоту.
Оксид азота (III)
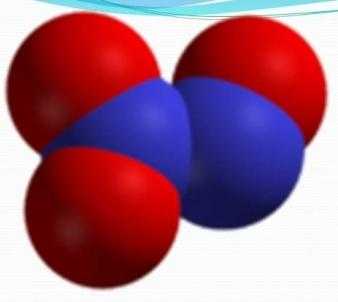 Формула — N2O3. Также его могут называть азотистым ангидридом и сесквиоксидом азота.
Формула — N2O3. Также его могут называть азотистым ангидридом и сесквиоксидом азота.
Свойства
В нормальных условиях является жидкостью, которая имеет синий цвет, а в стандартных — бесцветным газом. Чистый оксид существует только в твердом агрегатном состоянии.
Получение
Образуется при взаимодействии 50%-ной азотной кислоты и твердого оксида трехвалентного мышьяка (его также можно заменить крахмалом).
Применение
С помощью этого вещества в лабораториях получают азотистую кислоту и ее соли.
Оксид азота (IV)
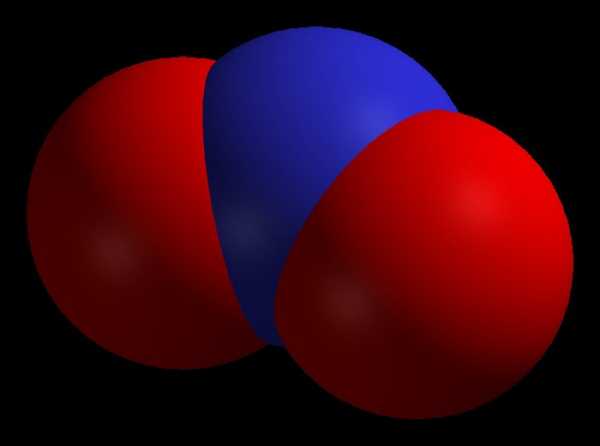 Формула — NO2. Также его могут называть диоксидом азота или бурым газом.
Формула — NO2. Также его могут называть диоксидом азота или бурым газом.
Свойства
Последнее название соответствует одному из его свойств. Ведь этот оксид имеет вид или красно-бурого газа или желтоватой жидкости. Ему присуща высокая химическая активность.
Получение
Данный оксид получают при взаимодействии азотной кислоты и меди, а также во время термического разложения нитрата свинца.
Применение
С помощью него производят серную и азотную кислоты, окисляют жидкое ракетное топливо и смесевые взрывчатые вещества.
Оксид азота (V)
Формула — N2O5. Может встречаться под названиями пентаоксида диазота, нитрата нитроила или азотного ангидрида.
Свойства
Имеет вид бецветных и очень летучих кристаллов. Они могут плавиться при температуре 32,3оС.
Получение
Этот оксид образуется при нескольких реакциях:
- Дегидрация азотной кислоты оксидом пятивалентного фосфора.
- Пропускание сухого хлора над нитратом серебра.
- Взаимодействие озона с оксидом четырехвалентного азота.
Применение
Из-за своей крайней неустойчивости в чистом виде нигде не используется.
Заключение
В химии существует девять оксидов азота, приведенные выше являются только классическими соединениями этого элемента. Остальные четыре — это, как уже было сказано, нестабильные вещества. Однако их все объединяет одно свойство — высокая токсичность. Выбросы оксидов азота в атмосферу приводят к ухудшению состояния здоровья живущих поблизости от промышленных химических предприятий людей. Симптомы отравления каким-либо из этих веществ — токсический отек легких, нарушение работы центральной нервной системы и поражение крови, причина которого — связывание гемоглобина. Поэтому с оксидами азота необходимо осторожно обращаться и в большинстве случаев использовать средства защиты.
fb.ru
