Факторы, ослабляющие степень гидролиза
ГИДРОЛИЗ СОЛЕЙ
Гидролиз-разложение солей водой, но не всякая соль подвергается гидролизу.
Разберем несколько реакций:
KOH +HCl = KCl + H2O
Или в ионном виде:
K++ OH— = K++ OH—+ H2O
Из этой реакции видно, что реакция идет только в сторону образования продуктов реакции, обратная реакция невозможна. Теперь другой пример:
NaOH + HCN = NaCN +H2O
Na++ OH— + HCN = Na++ CN—+ H2O
В этом примере реакция обратима,т.к. слабый электролит присутствует и в исходных веществах и в продуктах реакции. Возможность протекания обратной реакции указывает на взаимодействие соли с водой. Значит, с водой может взаимодействовать соль,которая образована одним (кислотой или основанием) или двумя слабыми электролитами.
Гидролиз – это взаимодействие соли с водой с образованием слабого электролита.
1 тип гидролиза
Соди, образованные сильным основанием и сильной кислотой.
Такие соли гидролизу не подвергаются (см. NaCl, аналогично KNO3 BaCl2, Na2SO4 ) и в растворах таких солей среда нейтральная.
2 тип гидролиза
Соли, образованные слабым основанием и сильной кислотой.
Например, хлорид аммония – NH4Cl образован слабым основанием и сильной кислотой.
NH4Cl =NH4++ Cl—
NH4++ Cl—+ H+OH—= NH4OH +Cl—+ H+
Или в сокращенном виде
NH4++ H+OH— = NH4OH + H+Таким образом, соли, образованные слабым основанием и сильной кислотой, гидролизуются по катиону и реакция среды в растворе такой соли — кислая
NH4Cl + H2O = NH4OH + HCl
Соли,образованные многокислотными основаниями, гидролизуются ступенчато.
Например, гидролиз нитрата алюминия.
Al(NO3)3= Al3++ 3NO3—
Гидролизу будет подвергаться катион алюминия, т.к гидроксид алюминия — слабый электролит.
Al3+ + H+OH—= AlOH2++ H+
AlOH2++ H+OH—= Al(OH)2++ H+
Т.к. катион алюминия трехзарядный катион, то для него возможны три стадии гидролиза ( см.ионные уравнения). В действительности соли полностью не разлагаются и в молекулярном виде будем писать реакции только по первой стадии:
Al(NO3)3+ H2O = AlOH(NO3)2 + HNO3
Попытайтесь самостоятельно написать гидролиз следующих солей
ZnCL2 FeSO4 Fe2(SO4)3
3 тип гидролиза
Соли, образованные сильным основанием и слабой кислотой.
Например, гипохлорит натрия –NaClO образован слабой кислотой и сильным основанием
NaClO= Na++ ClO—
Гидролизоваться будет остаток слабого электролита,т.е. анион
Na++ClO—+ H+OH—= Na++ HClO + OH—
Или в сокращенном виде
ClO—+HOH=HClO+OH—
При таком типе гидролиза среда будет щелочная
NaClO +H2O = HClO + NaOH
Анионы слабых многоосновных кислот гидролизуются ступенчато
Разбирем на примере фосфата калия
K3PO4= 3K++ PO43-
PO43-+ HOH = HPO42-+ OH—
HPO42-+ HOH = H2PO4—+ OH—
H2PO4—+HOH = H3PO4+OH—
В молекулярном виде пишем гидролиз только по первой стадии
K3PO4 + H2O = K2HPO4+ KOH
Испольэуя разобранные примеры, попытайтесь самостоятельнл написать гидролиз силиката натрия,
Нитрита бария, ацетата калия
4 тип гидролиза
Соли, образованные слабым основанием и слабой кислотой.
Такие соли гидролизуются по кати ону и аниону. Если соль образована слабым и нерастворимым основанием и слабой и летучей кислотой, то такая соль в растворе не существует, т.к. полностью гидролизуется яяяяя9 см. таблицу растворимости солей)
Т.к. фармацевту приходится в своей профессиональной деятельности готовить или отпускать жидкие лекарственные формы (содержат растворы солей) фармацевт должен знать способы ослабления или подавления гидролиза.
Факторы, ослабляющие степень гидролиза
1 Т.к. реакция гидролиза – реакция эндотермрическая, т.е. для ее протекания требуется тепло, повышение температуры. Значит, чтобы реакция протекала медленнее, слабее – температуру надо понижать, т.е. раствор надо охлаждать ( поэтому лекарства рекомендуют хранить в прохладном месте)
2 Для ослабления гидролиза растворы солей долны быть более концентрированными( представте, что в растворе преобладают молекулы соли, значит на всех воды не хватит и соль разлагаться будет меньше)
3 Самый важный фактор, т. к.. при приготовлении лекарственной формы концентрация заданы и изменить нельзя. При приготовлении инъекционных растворов их подвергают стерилизации, т.е. нагреванию , значит два первых фактора не могут влиять и ослаблять разложение соли. Применяют химическую стабилизацию и прибавляют сильный электролит(кислоту или щелочь) в зависимости от реакции среды раствора. Если среда кислая -0джобавляют кислоту, если среда щелочная – джобавляют щелочь ( т.е. вводят одноименный сильный электролит)
В некоторых случаях необходимо гидролиз усилить ( например, при нанесении рисунка на хлопчатобумажную ткань ее необходим о пропитать гидроксидом алюминая, чтобы лучше нанести рисунок. Но гидроксид алюминия – нерастворимое соединениен и равномерное нанесение на ткань невозможно. Поэтому ткань обрабатывают солью алюминия, а затем создают условия,усиливающие гидролиз соли. В результате ткань равномерно пропитана гидроксидом алюминия)
studopedya.ru
гидролиз солей — Стр 5
на рН буферного раствора. Наблюдается ли изменение рН буферного раствора при разбавлении в n1 раз и в n2 раз?
Таблица 3.4 Экспериментальные данные исследования свойств буферного
раствора в связи с разбавлением
исходногобуферного раствора |
|
Объем, |
| рН по универсальному | |||||
|
| мл |
| ||||||
|
|
|
| индикатору |
| ||||
|
|
|
|
|
|
| |||
|
|
|
|
|
|
| |||
|
|
|
|
|
|
|
| ||
буфер- |
|
|
|
|
| После разбавления в n | |||
|
|
|
|
| раз |
| |||
ного |
| воды |
| воды |
|
| |||
|
| до раз- |
|
|
| ||||
первое |
| второе | |||||||
рас- |
| (V1) |
| (V2) |
| ||||
|
| бавления | разбавле- |
| разбавле- | ||||
твора |
|
|
|
|
| ||||
рН |
|
|
|
|
|
| ние |
| ние |
|
|
|
|
|
| в n1 раз |
| в n2 раз | |
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
|
|
|
Контрольные вопросы и задачи
1.Что называется буферным раствором? Для каких целей готовят буферные растворы в лаборатории?
2.Приведите примеры наличия и функционирования буферных систем в природе.
3.Объясните принцип действия ацетатного и аммиачного буферных рас-
творов.
4.В каком интервале рН наблюдается действие буферного раствора?
5.Как изменяется рН буферного раствора при разбавлении?
6.Объясните механизм поддержания постоянства рН при добавлении в приготовленный вами буферный раствор: а) кислоты; б) щелочи.
7.Что называется буферной емкостью? От каких факторов она зависит? При каком значении рН буферная емкость раствора максимальна?
8. | Буферная система содержит 0,1 моль/л муравьиной кислоты и |
0,1 моль/л формиата калия. Определить рН. | |
9. | Как изменится рН буферного раствора, содержащего 0,1 М нитрата ам- |
мония и 0,01 М гидроксида аммония, если его разбавить в 4 раза?
10.Определить рН буферного раствора, содержащего 1,1 моль/л NН4ОН и
1,1 моль/л NН4Сl.
11.Определить рН и рОН раствора, если к 1 л воды прибавить 11,5 г муравьиной кислоты и 10,5 г формиата калия.
12.Смешали 20 мл 0,2 М раствора ацетата натрия с 20 мл 0,3 н. раствора уксусной кислоты. Определить рН раствора.
13.100 мл 23 н. раствора муравьиной кислоты смешали с 30 мл 15 н. раствора формиата натрия. Определить рН раствора.
14.Рассчитать рН раствора, содержащего в 0,5 л 30 г уксусной кислоты и 41 г ацетата натрия.
15.Вычислить концентрацию Н+, ОН– и рН раствора, полученного при смешивании 50 мл 0,2 М раствора уксусной кислоты и 3 мл 0,1 М раствора ацетата натрия.
16.Рассчитать концентрацию ионов водорода и рН раствора, который получился при сливании 10 мл 0,1 М раствора карбоната натрия Nа2СО3 и 8 мл 0,1
Мраствора гидрокарбоната натрия NаНСО3.
17. | K 25 мл | 0,2 | M раствора гидрофосфата натрия добавили 15 мл | ||
0,2 M раствора дигидрофосфата натрия. Полученную смесь разбавили до 50 мл. | |||||
Вычислите рН полученного раствора. |
| ||||
18. | К 100 мл | 0,1 | M | раствора | фтороводородной кислоты прибавлено |
5 г фторида натрия. Вычислите рН полученного раствора. | |||||
19. | Смешали | 21 | мл | раствора | 0,1 М раствора бензоната натрия |
и 9 мл 0,1 М раствора бензойной кислоты. Вычислить рН, если константа ионизации равна 6,3·10–5.
20. Сколько миллилитров 0,5 М раствора хлорида аммония следует прибавить к 100 мл 0,5 н. раствора гидроксида аммония, чтобы получить буферную систему с рН = 9,25?
21. Каково соотношение концентраций СН3СООН и СН3СООNа
вацетатном буферном растворе, если его рН = 4,74?
22.Сколько граммов формиата калия следует взять, чтобы при растворении в 25 мл 0,03 М раствора муравьиной кислоты получить смесь с рН = 4,0.
23. | Сколько граммов формиата натрия следует добавить | к 100 мл |
0,2 М | раствора муравьиной кислоты, чтобы получить | буферный |
раствор с рН = 3,32? |
| |
24. | Сколько мл 0,5 M раствора нитрата аммония надо | добавить |
к 10 мл 0,12 M раствора аммиака, чтобы получить раствор с рН = 9,2?
Лабораторная работа № 4. ГИДРОЛИЗ СОЛЕЙ
Цель работы. Установить взаимосвязь между составом соли и ее способностью подвергаться гидролизу. Научиться составлять молекулярные и ионные уравнения реакций гидролиза солей. С помощью индикаторов экспериментально определить характер среды в растворах солей. Сопоставить результаты эксперимента с теоретическими данными.
Гидролиз – разложение веществ водой. Гидролизом соли называется обменное взаимодействие ионов соли с молекулами воды, в результате, которого изменяется характер среды (соотношение между ионами водо-
рода и гидроксила в растворе).
Реакция гидролиза – это реакция обратная реакции нейтрализации.
гидролиз
СОЛЬ + h3Oкислота + основание
нейтрализация
Nh5Cl + h3O Nh5OH + HCl
Nh5+ + h3O Nh5OH + H+.
Гидролиз соли происходит лишь в тех случаях, если ионы соли с ионами Н+ или ОН– молекул воды образуют новые слабые электролиты. Процесс гидролиза – это обратный процесс диссоциации слабого электролита. Возможность и характер протекания реакции гидролиза определяется природой кислоты и основания, которые образовали данную соль.
Гидролизу подвергаются соли, образованные:
–сильным основанием и слабой кислотой;
–слабым основанием и сильной кислотой;
–слабым основанием и слабой кислотой.
Гидролизу не подвергаются соли, образованные сильным основанием и сильной кислотой.
Гидролиз протекает обратимо, ступенчато, продукты гидролиза солей, как правило, определяются первой ступенью.
Рассмотрим возможные случаи гидролиза солей.
1. Гидролиз солей, образованных сильным основанием и слабой кислотой (КСN, NaClO, Na2CO3, K3PO4 и т. д.).
А) Гидролиз соли, образованной слабой одноосновной кислотой:
NaClO + h3O НClO + NaОН
Na+ + ClOˉ + h3O Na+ + ОНˉ + НClO или
ClOˉ + h3O НClO + ОНˉ ().
В обеих частях уравнения имеются малодиссоциированные вещества (h3O, НClO), но вода является более слабым электролитом, чем хлорноватистая кислота, поэтому равновесие реакции смещено в сторону обратной реакции. Из уравнения видно, что в результате гидролиза в растворе увеличивается концентрация ионов ОНˉ, т. е. реакция среды щелочная (рН > 7).
Б) Гидролиз соли, образованной слабой многоосновной кислотой:
Na3РО4 + h3O Na2HРO4 + NaОН.
Гидролиз протекает за счет взаимодействия ионов РО43– с молекулами h3O. Запишем сокращенное ионное уравнение реакции гидролиза, помня, что гидролиз протекает обратимо (при этом равновесие смещено в сторону обратной реакции) и ступенчато (к исходному иону присоединяется только один ион водорода):
РО43– + h3O HРO42– + ОНˉ (рН > 7).
По полученному ионному уравнению дописываем молекулярное уравнение реакции гидролиза.
Таким образом, в результате гидролиза соли, образованной сильным основанием и слабой многоосновной кислотой, образуется кислая соль и основание. В растворе соли среда – щелочная, так в растворе появляется избыток ионов ОН–.
2. Гидролиз солей, образованных слабыми основаниями и силь-
ными кислотами (Nh5Cl, ZnSO4, FeCl3, Al2(SO4)3 и др.).
Рассмотрим гидролиз сульфата цинка, соли образованной слабым афотерным основанием и сильной кислотой:
2ZnSO4 + 2h3O (ZnOH)2SO4 + h3SO4.
Гидролиз этой соли протекает по катиону, запишем сокрашенное ионное уравнение гидролиза, помня, что гидролиз протекает обратимо (равновесие смещено в сторону обратной реакции) и ступенчато (к исходному иону присоединяется только один гидроксильный ион):
Zn2+ + h3O ZnOH+ + H+ (pH < 7).
Врастворе появляется избыток ионов водорода, следовательно, в растворе соли среда – кислая (рН < 7).
По полученному ионному уравнению записываем молекулярное уравнение и расставляем коэффициенты.
При гидролизе соли, образованной слабым многокислотным основанием и сильной кислотой, образуется основная соль и кислота.
Вхолодных и умеренно концентрированных растворах солей гидролиз протекает по первой ступени. При повышении температуры и разбавлении растворов гидролиз усиливается, равновесие смещается в сторону прямой реакции, и тогда могут протекать и вторые ступени гидролиза.
3. Гидролиз солей, образованных слабым основанием и слабой кислотой.
Соли, образованные катионом слабого основания и анионом слабой кислоты, гидролизуются одновременно и по катиону, и по аниону с образованием слабого основания и слабой кислоты. Характер среды в таких растворах будет зависеть от свойств образующихся слабых электролитов, т. е. среда может быть слабокислой, слабощелочной или даже нейтральной.
Nh5CN + h3O Nh5OH + HCN
Nh5+ + CN– + h3O Nh5OH + HCN.
Для того чтобы определить характер среды, необходимо сопоставить константы диссоциации слабой кислоты (Кд =7,9·10-10)и слабого основания (Кд =1,76· 10-5).Из сравнения констант диссоциации кислоты и основания [Кд(Nh5ОН) > Кд(HCN)] следует, что раствор цианида аммония должен иметь слабощелочную среду.
(Nh5)2CО3 + h3O Nh5OH + Nh5HCО3
Nh5+ + CО32– + h3O Nh5OH + HCО3ˉ.

Особый случай гидролиза солей, образованных слабым многокислотным основанием и слабой многоосновной кислотой (Al2S3, Cr2S3, Fe2(CO3)2, Al2(CO3)2 и др.), когда разложение солей под действием воды происходит полностью.
Al2S3 + 6 h3O → 2 Al(OH)3↓ + 3 h3S↑.
В присутствии воды гидролиз идет и по катиону, и по аниону.
Al3+ + h3O AlOh3+ + H+
h3O S2– + h3O HS– + ОН–
Из образовавшихся ионов H+ и ОН– образуется вода – слабый электролит, концентрация ионов уменьшается, и равновесие смещается в сторону прямой реакции, т. е. гидролиз усиливается, идут вторые ступени гидролиза:
AlOh3+ | + h3O Al(OH)2+ + H+ |
| |
h3O | |||
– | – | ||
HS | + h3O h3S + ОН |
| |
|
В итоге равновесие реакции полностью смещается в сторону прямой реакции, и гидролиз идет до конца. В итоге образуется слабое и малорастворимое основание, которое выпадает в осадок. Кроме того, образуется второй слабый электролит, который является летучей кислотой. Поэтому соли такого типа не могут существовать в водном растворе. В таблице растворимости таких солей стоит прочерк.
При сливании растворов сульфата алюминия и сульфида натрия тоже образуется осадок и выделяется газ с неприятным запахом:
Аl2(SO4)3 + 3 Na2S + 6 h3O → 2 Al(OH)3 ↓ + 3 h3S↑ + 3 Na2SO4 Al3+ + h3O AlOh3+ + H+ h3O
S2– + h3O HS– + ОН–
При сливании водных растворов хлорида железа и карбоната натрия реакция гидролиза протекает до конца с образованием коричневого осадка Fe(OH)3 и с выделением газа CO2:
2 FeCl3 + 3 Na2CO3 + 3 h3O → 2 Fe(OH)3↓ + 3 CO2 ↑ + 6 NaCl
Fe 3+ + h3O FeOh3+ | + H+ |
| |
h3O | |||
CО32- + h3O HCO3- | + ОН– | ||
|

Эти соли взаимно усиливают гидролиз друг друга. Поскольку гидроксид алюминия амфотерное соединение, то для его получения чаще используют раствор соды, а не щелочь.
Степень гидролиза и константа гидролиза
Количественными характеристиками процесса гидролиза являются степень гидролиза и константа гидролиза.
Любое химическое равновесие можно охарактеризовать величиной константы равновесия. Для реакции гидролиза ацетата натрия
Ch4COONa + h3O Ch4COOH + NaОН
Ch4COO– + h3O Ch4COOH + ОН–
константа равновесия имеет вид:
В этом выражении концентрация воды преобладает в системе и остается величиной постоянной [h3O] = const. Перемножив две постоянные, получают тоже постоянную величину (Кг):
Кравн.· [h3O] = const = Кг
Преобразуем выражение константы гидролиза в вид удобный для расчетов, умножив числитель и знаменатель на одну и ту же величину
[H+], или заменим, получим:
Подобным образом находим константу гидролиза для соли, образованной слабой многоосновной кислотой. Например, для соли К3РО4 константа гидролиза будет рассчитываться по формуле
Для соли, образованной слабым основанием и сильной кислотой, константа гидролиза будет равна:

Для соли, образованной слабым основанием и слабой кислотой, константа гидролиза будет равна:
Из выражений констант гидролиза следует, что чем слабее кислота или основание, образовавшее данную соль, тем больше константа гидролиза, тем в большей степени соль подвергается гидролизу.
Степень гидролиза (αг или β) – отношение числа молекул соли, подвергшихся гидролизу, к общему числу молекул.
Степень гидролиза соли можно вычислить, зная константу гидролиза соли:
Концентрацию ионов H+ или ОНˉ, образующихся при гидролизе соли, вычисляют используя константу гидролиза или степень гидролиза:
или
Пример 1. Вычислите рН и степень гидролиза соли в растворе карбоната натрия с молярной концентрацией 0,1 моль/л.
Решение. Запишем уравнение реакции гидролиза карбоната натрия. Na2СО3 + h3O NaHСO3 + NaОН
CО32– + h3O HCO3ˉ + ОНˉ.
При гидролизе образуется избыток ионов ОНˉ, следовательно, в растворе соли среда – щелочная. Вычислим концентрацию гидроксильных ионов, предварительно вычислив константу гидролиза:
Вычисление рН и степени гидролиза можно выполнить двумя способами.
48
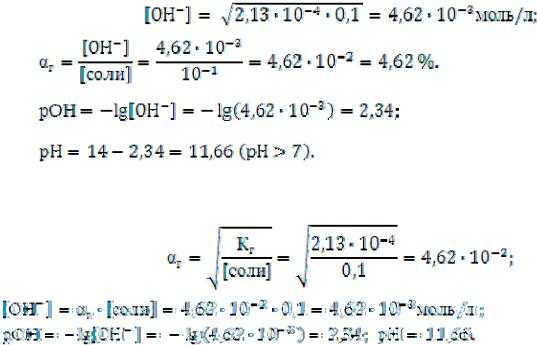
А) Вычислим сначала концентрацию гидроксильных ионов, а затем степень гидролиза и рН.
Б) Вычислим сначала степень гидролиза, а затем концентрацию гидроксильных ионов и рН.
Техника безопасности
1.Перед выполнением работы следует ознакомиться с методикой проведения эксперимента, понять цель исследования.
2.К работе приступать только после разрешения преподавателя.
3.Помните о токсичности многих солей (особенно солей «тяжелых» металлов – меди, цинка, кадмия, ртути, свинца, олова). Работайте аккуратно. При попадании на руки растворов солей и в конце работы тщательно вымойте руки.
4.Пролитые реактивы необходимо сразу же удалить влажной тряпкой, не допуская их контакта с незащищенной кожей рук.
5.Опыты, в которых выделяются ядовитые газы, проводите в вытяжном шкафу при включенной вентиляции.
6.Правильно проводите нагревание пробирок с растворами, направляя открытую часть пробирки внутрь вытяжного шкафа. Равномерно нагревайте содержимое пробирки.
7.Растворы солей и индикаторов используйте в количествах, указанных в описании эксперимента. Не используйте растворы, в названиях которых не уверены.
Экспериментальная часть
Реактивы. Соли (растворы или кристаллы): NaCl, NaNO3, Na2SO4, Na2CO3, Na2SiO3, Na2В4O7, NaHСO3, Ch4COONa, Na2S, Na3PO4, KCl,
KNO3, K2SO4, Nh5Cl, Nh5NO3, Nh5Ch4COO, ZnSO4, Аl2(SO4)3, Cr2(SO4)3, AlCl3, FeCl3, ВаCl2, СаCl2, MgCl2.
Растворы индикаторов: фенолфталеин, метиловый оранжевый, лакмус, индикаторная бумага.
Оборудование. Посуда: штатив с пробирками, пробиркодержатель, спиртовка.
Получите у преподавателя вариант задания для проведения эксперимента (варианты заданий смотрите в таблице 4.1).
Таблица 4.1
Варианты индивидуальных заданий
№ | Формула соли для опыта |
| Номера опытов | ||||
вари- |
| ||||||
|
|
|
|
|
|
| |
анта | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|
|
|
|
|
|
|
|
1 | Ch4COONa | Аl2(SO4)3 | (Nh5)2CО3 | NaNO3 | 5а | 6е | 7б |
2 | NaHСO3 | FeCl3 | Nh5Ch4COO | КС1 | 5б | 6г | 7а |
3 | Na2CO3, | Cr2(SO4)3 | (Nh5)2CО3 | КI | 5в | 6а | 7в |
4 | Na2SiO3, | ZnSO4 | Nh5Ch4COO | NaC1 | 5г | 6д | 7а |
5 | Na2S | Nh5Cl | (Nh5)2CО3 | Na2SO4 | 5а | 6б | 7б |
6 | NaNO2 | Nh5NO3 | Nh5Ch4COO | K2SO4 | 5б | 6в | 7в |
7 | Na2В4O7, | Аl2(SO4)3 | (Nh5)2CО3 | KNO3 | 5в | 6а | 7б |
8 | Na3PO4 | FeCl3 | Nh5Ch4COO | CaCl2 | 5г | 6б | 7в |
9 | Ch4COONa | Cr2(SO4)3 | (Nh5)2CО3 | BaCl2 | 5а | 6в | 7а |
10 | Na2SiO3 | Nh5С1 | Nh5Ch4COO | Ca(NO3)2 | 5б | 6е | 7б |
11 | Na2S | ZnSO4 | (Nh5)2CО3 | KNO3 | 5в | 6г | 7в |
12 | Na2CO3 | Nh5NO3 | Nh5Ch4COO | Na2SO4 | 5г | 6д | 7а |
13 | NаНCO3 | CuSO4 | Nh5Ch4COO | NaNO3 | 5б | 6е | 7б |
14 | Na2SiO3 | FeCl3 | (Nh5)2CО3 | K2SO4 | 5в | 6д | 7в |
studfiles.net
Ответы@Mail.Ru: Гидролиз солей, помогите, срочно!
http://hob-inf.narod.ru/chem/hydr.htmlhttp://himege.ru/gidroliz-solej/
Решение:
Степень гидролиза соли тем больше, чем слабее кислота или основание, образовавшие эту соль. Приведем ряд анионов и катионов, соответствующие уменьшению силы кислот и оснований их образующих.
Анионы:
F- > NO2− > Ch4COO− > SO32− > ClO− > CN− > CO32− > PO43− > S2− > SiO44−
Катионы:
Cd2+ > Mg2+ > Mn2+ > Fe2+ > Co2+ > Ni2+ > Nh5+ > Cu2+ > Pb2+ > Zn2+ > Al2+ > Cr 2+> Fe2+
Чем правее в этих рядах расположен ион, тем с большей силой идет гидролиз образованной им соли, т. е. его основание или кислота слабее, чем у стоящих слева от него.
NaCN и NaClO – это соли, образованные сильным основанием и слабой кислотой. В ряду анионов CN− стоит правее ClO−, таким образом, NaCN в большей степени подвергается гидролизу, чем NaClO.
Составим ионно-молекулярное и молекулярное уравнения гидролиза цианида натрия NaCN.
Цианид натрия NaCN – соль слабой кислотой HCN и сильного основания NaOH. При растворении в воде молекулы NaCN диссоциируют на катионы Na+ и анионы CN−. Катионы Na+ не могут связывать ионы OH- воды, так как NaOH – это сильный электролит. Анионы CN− связывают ионы H+ воды, образуя молекулы слабого электролита HCN. Соль гидролизируется по аниону. Ионно-молекулярное уравнение гидролиза следующее:
CN- + H+OH- = HCN + OH-
В молекулярной форме уравнение гидролиза следующее: NaCN+ h3O = HCN + NaOH
В результате гидролиза в растворе появляется некоторый избыток ионов OH-, поэтому раствор NaCN имеет щелочную реакцию (pH >7).
Составьте молекулярное и ионно-молекулярное уравнение реакции гидролиза соли CuCl2 .Решение: Хлорид меди – соль слабого многокислотного основания Cu(OH)2 и сильной кислоты HCl . В данном случае катионы Cu2+ связывают гидроксильные ионы воды, образуя катионы основной соли CuOH+. Образование молекул Сu(OH)2 не происходит, так как ионы CuOH+ диссоциируют гораздо треднее, чем молекулы Cu(OH)2.В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза: Cu2+ + h3O ⇄ CuOH+ + H+или в молекулярной форме: CuCl2 + h3O ⇄CuOHCl + HCl
otvet.mail.ru
