§48. Особенности наследственности и изменчивости человека
1. Какой метод не применяется в генетике человека: цитогенетический, генеалогический, близнецовый, гибридологический, дерматоглифический?
В генетике человека не применяется гибридологический метод.
2. Какие особенности человека как объекта генетики осложняют изучение его наследственности и изменчивости?
Для людей невозможно экспериментально получать мутации, не применим гибридологический метод. Кроме того, генетический анализ усложняется рядом факторов: большим числом хромосом (2n = 46), малым количеством потомков в семье, медленной сменой поколений (одно поколение – в среднем 30 лет), широким генотипическим и фенотипическим полиморфизмом (разнообразием) и т.д.
3. Каковы основные методы изучения наследственности и изменчивости человека?
Основными методами изучения наследственности и изменчивости человека являются:

● Близнецовый метод, суть которого заключается в сравнительном изучении развития признаков у близнецов.
● Цитогенетический метод, основанный на микроскопическом изучении хромосом.
● Популяционно-статистический метод, связанный с изучением наследственных признаков в больших группах населения (популяциях).
● Дерматоглифический метод, предполагающий изучение рельефа кожи на пальцах, ладонях и подошвах стоп.
● Биохимические методы, связанные с качественным и количественным анализом определённых веществ, прежде всего ферментов и продуктов катализируемых ими реакций.
● Метод соматической гибридизации, суть которого состоит в получении и последующем изучении гибридных клеток, получаемых путём слияния соматических клеток человека с клетками других биологических видов.
● Молекулярно-генетические методы, связанные с анализом фрагментов нуклеиновых кислот, поиском и выделением генов и т.д.
4. Каким образом сравнительное изучение близнецов позволяет выявить роль генотипа и условий среды в формировании конкретных признаков организма?
Каким образом сравнительное изучение близнецов позволяет выявить роль генотипа и условий среды в формировании конкретных признаков организма?
В большинстве случаев близнецы, будучи одного и того же возраста и воспитываясь в одной семье, фактически развиваются в одинаковых условиях. Следовательно, влияние окружающей среды на них примерно одинаковое. Поэтому выявление сходства и различий близнецов (прежде всего – монозиготных) позволяет определить вклад генотипа и условий среды в формирование определённых признаков.
Монозиготные близнецы имеют одинаковый генотип. Следовательно, признаки, по которым однояйцевые близнецы сходны, в большей степени предопределены генотипом, а на признаки, по которым данные близнецы различаются, существенное влияние оказывают условия окружающей среды.
5. Какие методы генетики человека можно использовать для выявления генных мутаций? Хромосомных и геномных мутаций?
Для выявления генных мутаций применяют, прежде всего, биохимические методы, а также секвенирование.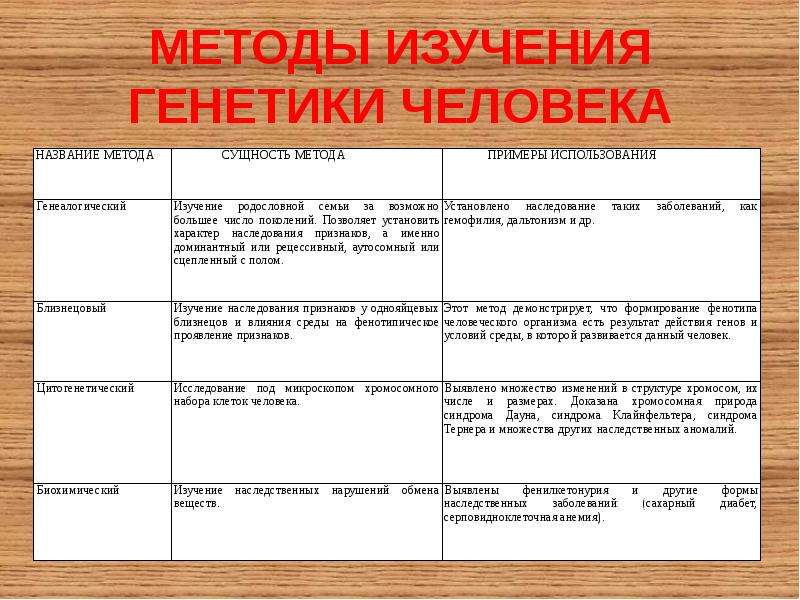 Для выявления хромосомных и геномных мутаций широко используется цитогенетический метод. Кроме того, мутации, при которых происходит изменение папиллярных узоров кожи, например, трисомию по 21 хромосоме (причина развития синдрома Дауна), можно выявлять с помощью дерматоглифического метода.
Для выявления хромосомных и геномных мутаций широко используется цитогенетический метод. Кроме того, мутации, при которых происходит изменение папиллярных узоров кожи, например, трисомию по 21 хромосоме (причина развития синдрома Дауна), можно выявлять с помощью дерматоглифического метода.
6. Охарактеризуйте основные молекулярно-генетические методы, которые используются для изучения наследственности и изменчивости человека.
● С помощью метода гибридизации ДНК можно осуществлять поиск определённых генов или их фрагментов. Для этого к образцам исследуемой ДНК добавляют специальные зонды – искусственно синтезированные цепочки ДНК с известной последовательностью нуклеотидов. ДНК-зонд создают таким образом, чтобы он мог комплементарно связаться с искомым геном, а также содержал радиоактивную или светящуюся метку, необходимую для последующего обнаружения зонда.
● Полимеразная цепная реакция (ПЦР) – метод, позволяющий многократно воспроизвести (т. е. «размножить») определённый фрагмент ДНК. ПЦР широко используется в биологии и медицине, например, для диагностики заболеваний (наследственных, инфекционных), установления отцовства, клонирования генов и др.
е. «размножить») определённый фрагмент ДНК. ПЦР широко используется в биологии и медицине, например, для диагностики заболеваний (наследственных, инфекционных), установления отцовства, клонирования генов и др.
● Секвенирование представляет собой определение последовательности нуклеотидов молекул нуклеиновых кислот. Секвенирование ДНК используется для «расшифровки» генов и выявления любых типов генных мутаций.
● Метод генной дактилоскопии связан с исследованием особых повторяющихся последовательностей нуклеотидов (так называемых минисателлитных ДНК). Их структура и расположение в хромосомах уникально для каждого человека (как отпечатки пальцев) и совпадает только у монозиготных близнецов. Анализ таких последовательностей используется для идентификации личности или установления родства.
7. Наследственная форма сахарного диабета обусловлена рецессивным аутосомным геном. Обследование населения крупного изолированного острова показало, что 1% людей, проживающих на этом острове, страдают врождённым сахарным диабетом.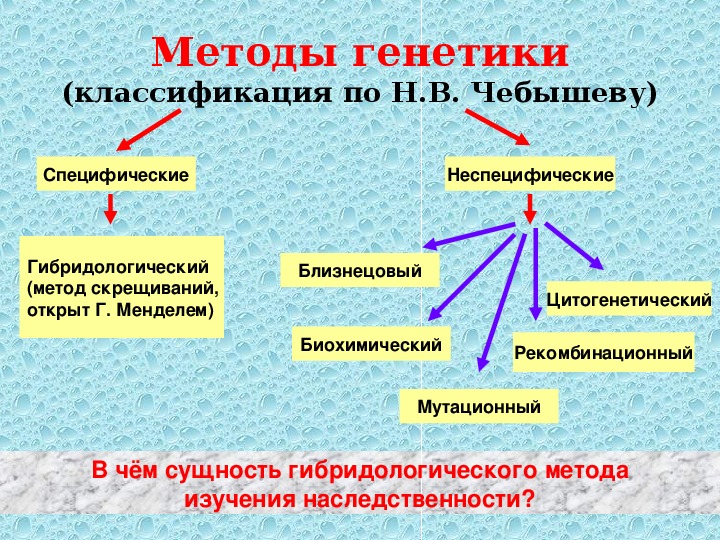 Какую долю (%) среди здорового населения острова составляют гетерозиготные носители этого заболевания?
Какую долю (%) среди здорового населения острова составляют гетерозиготные носители этого заболевания?
● Введём обозначения генов:
А – нормальный углеводный обмен;
а – врождённый сахарный диабет.
● Пусть р – частота доминантного аллеля в данной популяции, а q – частота рецессивного аллеля.
Тогда р + q = 1 (или 100%).
Исследуемый признак является аутосомным, т.е. мужские и женские гаметы, несущие аллель А, формируются у людей, населяющих остров, с одинаковой частотой (вероятностью) – р. Сперматозоиды и яйцеклетки, несущие аллель а, образуются с частотой (вероятностью) q. Случайное слияние гамет приводит к появлению потомков трёх генотипических классов: АА, Аа и аа.
● Для наглядности построим решётку Пеннета:
Поскольку гаметы А образуются с частотой р, гаметы а – с частотой q, то доля людей, имеющих генотип АА, равна p2, генотип Аа – 2pq, генотип аа – q2.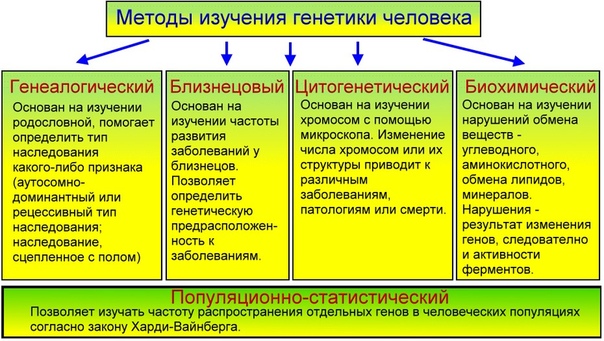
● В условии сказано, что доля людей, страдающих врождённой формой сахарного диабета, составляет 0,01 (или 1%), т.е. q2 = 0,01. Следовательно, q = √¯0,01 = 0,1 (или 10%). Тогда p = 1 – 0,1 = 0,9 (или 90%).
Здоровое население острова составляет 0,99 (или 99%).
При этом носителями заболевания (Аа) являются: 2pq = 2 × 0,9 × 0,1 = 0,18 (или 18%).
Значит, доля носителей среди здорового населения составляет 0,18 : 0,99 × 100% ≈ 18,2%.
Ответ: доля носителей врождённой формы сахарного диабета среди здорового населения острова составляет 18,2%.
Дашков М.Л.
Сайт: dashkov.by
Вернуться к оглавлению
| < Предыдущая | Следующая > |
|---|
Трудные вопросы ЕГЭ по биологии
|
Методы Некоторые методы, встречающиеся в ЕГЭ по биологии, отличаются от методов, описанных в школьных учебниках. |
1. Выберите два верных ответа. Вклад биотехнологии в медицину состоит в
1) использовании химического синтеза для получения лекарственных препаратов
2) создании лечебных сывороток на основе плазмы крови иммунизированных животных
3) синтезе гормонов человека в бактериальных клетках
4) изучении родословных человека для выявления наследственных заболеваний
5) культивировании штаммов бактерий и грибков для производства антибиотиков в промышленных масштабах
2. Выберите два верных ответа. Какие методы исследования позволили установить пространственную структуру молекулы ДНК?
1) цитогенетический метод
2) рентгеноструктурный анализ
3) метод культуры клеток
4) метод моделирования
5) центрифугирование
3. Выберите два верных ответа. Какие методы исследования помогают изучить процесс фотосинтеза в клетках?
1) экспериментальный метод
2) метод микроскопирования
3) метод меченых атомов
4) метод клеточных культур
5) метод центрифугирования
4. Выберите два верных ответа. Популяционно-статистический метод исследования генетики человека используется для
Выберите два верных ответа. Популяционно-статистический метод исследования генетики человека используется для
1) расчета частоты встречаемости нормальных и патологических генов
2) изучения биохимических реакций и обмена веществ
3) предсказания вероятности генетических аномалий
4) определения степени влияния среды на развитие признаков
5) изучения структуры генов, их количества и расположения в молекуле ДНК
5. Выберите два верных ответа. Близнецовый метод исследования генетики человека используется для
1) изучения характера наследования признака
2) определения степени влияния среды на развитие признаков
3) предсказания вероятности рождения близнецов
4) оценки генетической предрасположенности к различным заболеваниям
5) расчета частоты встречаемости нормальных и патологических генов
6. Выберите два верных ответа. Цитогенетический метод исследования генетики человека
1) основан на составлении родословных человека
2) используется для изучения характера наследования признака
3) заключается в микроскопическом исследовании структуры хромосом и их количества
4) используется для выявления хромосомных и геномных мутаций
5) помогает установить степень влияния среды на развитие признаков
7. Выберите два верных ответа. Метод меченых атомов используют для определения
Выберите два верных ответа. Метод меченых атомов используют для определения
1) наличия исследуемого белка в клетке
2) наследования сцепленных с полом признаков
3) концентрации ядовитых веществ в воде
4) положения генов на хромосомах
5) возможности проявления признаков у потомков
8. Выберите два верных ответа. Кариотипирование – это метод, позволяющий определить
1) наличие предковых генов в геноме человека
2) наличие хромосомных перестроек
3) возможность проявления генных мутаций
4) пол человека на стадии эмбриона
5) внешний вид человека
9. Выберите два верных ответа. Культивирование клеток животных используеют для
1) выращивания неплодовитых организмов
2) создания химерных животных
3) изучения влияния препаратов на клетки
4) выведения новых гибридных видов
5) создания антител к определенным вирусам
10. Выберите два верных ответа. Полиплоидизацию используют в селекции растений для
1) преодоления стерильности гибридов растений
2) создания новых сочетаний аллелей в чистых линиях
3) выведения устойчивых к засухе растений
4) повышения урожайности культурных растений
5) получений гетерозисных гибридов
Методы изучения генетики человека
Цели:
- Образовательные:
- объяснить причины невозможности применения к человеку экспериментальных методов генетики растений и животных;
- изучить сущность и значение основных методов антропогенетики: генеалогического, близнецового, цитогенетического;
- познакомить учащихся с новыми достижениями в области пренатальной и постнатальной диагностики наследственных болезней человека;
- Воспитательные:
- показать значение материальных основ наследственности и окружающей среды в формировании биологических особенностей и социальных черт личности человека;
- определить единство биологических закономерностей для всей живой природы от микроорганизма до человека;
- показать, как знание генетики помогает выяснить причины многих тяжелых заболеваний человека, своевременно ставить диагноз, находить меры профилактики и лечения;
- Развивающие:
- обеспечить развитие познавательных процессов учащихся в ходе решения проблемных вопросов и исследовательских задач;
- продолжить развитие общеучебных умений и навыков: работать с дополнительной литературой, составлять доклады;
- научить анализировать родословные, решать
задачи с использованием формулы Хольцингера.

Оборудование: плакаты «Родословная с аутосомно-доминантным типом наследования», «Родословная с аутосомно-рецессивным типом наследования», «Родословная сцепленного с полом рецессивного типа наследования», «Родословная сцепленного с полом доминантного типа наследования», «Родословная голандрического типа наследования»; таблицы «Близнецовый метод», «Кариотип человека»; фотографии «Наследственные заболевания человека»; выставка книг по генетике человека; презентация.
Предварительная работа:
- деление учащихся на группы;
- подготовка каждой группой доклада по одной из тем: «Метод анализа родословных в генетических исследованиях человека», «Близнецовый метод изучения генетики человека. Близнецы», «Цитогенетический метод антропогенетики», «Экспресс-методы и методы пренатальной диагностики»;
- подготовка каждой группой вопросов по
предложенным темам.

ХОД УРОКА
I. Организационный момент
II. Актуализация (слайды 2, 3, 4)
– Изучением наследственности отдельных видов организмов занимается частная генетика. Частную генетику человека называют антропогенетикой. Установлено, что основные генетические закономерности являются общими для всех органических форм. Человек не является исключением. Социальная жизнь человека не свела на нет роль биологических факторов в его жизни, а, напротив, еще более их усложнила и разнообразила. Поэтому исследования в области антропогенетики встречают большие трудности.
– Какие методы изучения генетики растений и животных вы знаете? (Основным методом является гибридологический, который заключается в скрещивании организмов в ряду поколений с последующим изучением потомства. Также используются цитологический, биохимический и др.)
– Применимы ли к человеку методы
экспериментальной генетики? (Нет, т. к.
невозможно произвольное скрещивание, малое
число потомков в каждой семье, поздняя половая
зрелость, невозможность жизни потомков в
контролируемых условиях)
к.
невозможно произвольное скрещивание, малое
число потомков в каждой семье, поздняя половая
зрелость, невозможность жизни потомков в
контролируемых условиях)
– Таким образом, применимость к человеку
классического генетического анализа как
основного метода изучения наследственности и
изменчивости исключена из-за невозможности
экспериментальных скрещиваний, длительности
времени достижения половой зрелости и малого
количества потомства на пару. Не смотря на
перечисленные трудности, генетика человека
изучена на сегодня лучше, чем генетика многих
других организмов, благодаря развитию медицины и
разнообразным методам исследования.
Тема нашего урока «Методы изучения генетики
человека».
Сегодня мы познакомимся с основными методами
антропогенетики, их сущностью и значением в
выявлении причин многих тяжелых заболеваний и
определении мер их профилактики и лечения.
III. Изучение нового материала
Изучение нового материала
1) Исторические данные
Накопление и систематизирование данных о
закономерностях наследования некоторых
признаков человека началось в XVIII-XIX веках,
задолго до открытия Г. Менделем главных законов
наследования и становления генетики как науки.
Впервые хромосомы человека на цитологических
препаратах были описаны в самом конце XIX века, еще
до существования хромосомной теории. Тем не
менее, многие данные были слишком противоречивы.
Так, например, вплоть до середины XIX века
по-разному оценивалось количество хромосом
человека в кариотипе – от 47 до 49. Именно сейчас мы
стоим на пороге познания тайн наследственности
человека, единственного вида, обладающего
разумом и способного целенаправленно изменять
окружающий мир, т.к. новые достижения в области
молекулярной генетики и генной инженерии
позволяют изучать не только хромосомы, но и даже
отдельные гены.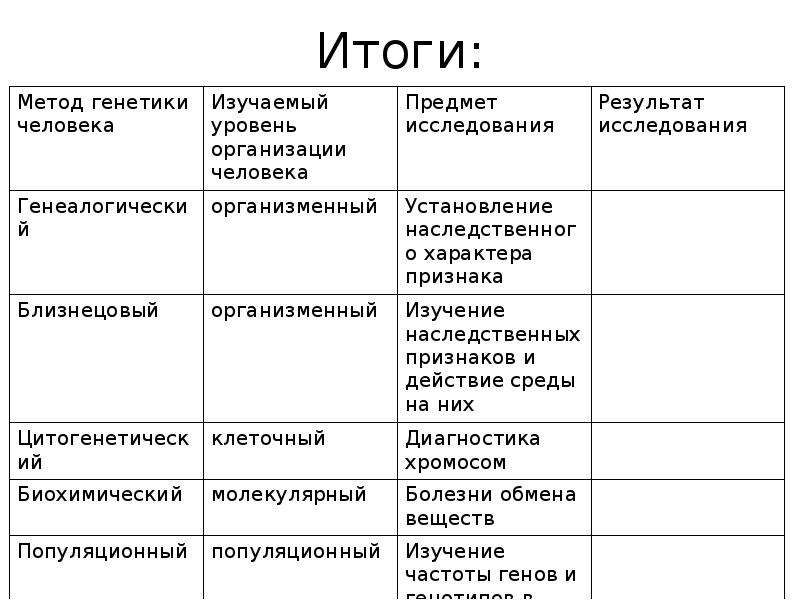 Поэтому мы рассмотри методы,
которые существуют достаточно давно:
Поэтому мы рассмотри методы,
которые существуют достаточно давно:
- генеалогический;
- близнецовый;
- цитогенетический.
И новые современные экспрес-методы и методы пренатальной диагностики.
2) Генеалогический метод (слайды 5, 6, 7, 8)
Первым исторически сложившимся методом
изучения генетики человека является
генеалогический метод, сущность которого
заключается в анализе распределения каких-либо
признаков среди представителей одной семьи в
родословной. Еще в XVIII веке впервые была
опубликована работа, посвященная анализу
наследования полидактилии (шестипалости) в
родословной одной семьи, включающей шесть
поколений.
– Определим особенности генеалогического
метода, его значение и возможности применения.
Доклад «Метод анализа родословных в
генетических исследованиях человека»
(дополнение «Архивы», «Анализ собственной
родословной»). [Приложение 1]
[Приложение 1]
Вопросы: (слайд 11)
– Как составить родословную?
– Кто готов проанализировать свою родословную?
– Почему при аутосомно-рецессивном типе
наследования признак появляется в IV поколении?
– Почему при голандрическом типе наследования
болеют только мужчины?
Вывод: Таким образом, самый древний из методов генетики человека – генеалогический – не исчерпал своих возможностей и в наше время. Он является основным в практике медико-генетического консультирования. С его помощью уточняется риск развития заболевания, вероятность носительства аномального гена. Зачастую при определении прогноза потомства другие сложные лабораторные методы дают значительно меньше информации. (Cлайд 12)
3) Близнецовый метод (слайды 13, 14, 15, 16)
Для решения многих теоретических проблем и
практических медицинских задач, связанных с
заболеваниями, требуется определить меру
участия наследственности и среды в
возникновении патологии. Особое значение в
изучении сложно исследуемых признаков и
заболеваний имеют генетически идентичные
индивиды, которые встречаются в человеческих
популяциях – близнецы.
Особое значение в
изучении сложно исследуемых признаков и
заболеваний имеют генетически идентичные
индивиды, которые встречаются в человеческих
популяциях – близнецы.
– Определим значение близнецового метода в
изучении величины наследуемости.
Доклад «Близнецовый метод изучения генетики человека» (дополнение «Близнецы»). [Приложение 2]
Вопросы: (слайд 17)
– Одинаков ли состав белков у двух
монозиготных близнецов, если в их клетках не было
мутаций?
– Почему у детей иногда появляются признаки
несвойственные родителям?
– Почему монозиготные близнецы всегда одного
пола, а дизиготные могут быть разного пола?
– Кто такой Гальтон? Почему он стал изучать
генетику человека?
– Одинакова ли вероятность рождения близнецов у
представителей разных рас?
Вывод: Итак, близнецовый метод позволяет
дать первоначальную оценку генетической
составляющей в фенотипической изменчивости
какого-либо признака. Он применяется для
изучения многих широко распространенных
заболеваний (сердечно-сосудистых,
желудочно-кишечных, психических,
злокачественных опухолей и др.). Однако
результаты близнецовых исследований являются
достаточно неспецифичными и не позволяют
определять точные механизмы влияния факторов
внешней среды на формирование каких-либо
признаков. Поэтому популярность этого метода в
последнее время снизилась. (Cлайд 18)
Он применяется для
изучения многих широко распространенных
заболеваний (сердечно-сосудистых,
желудочно-кишечных, психических,
злокачественных опухолей и др.). Однако
результаты близнецовых исследований являются
достаточно неспецифичными и не позволяют
определять точные механизмы влияния факторов
внешней среды на формирование каких-либо
признаков. Поэтому популярность этого метода в
последнее время снизилась. (Cлайд 18)
4) Цитогенетический метод (слайды 19, 20, 21, 22)
На данный момент чаще используют
цитогенетический метод. Это стало возможным
благодаря применению методики культуры
различных тканей и метода дифференциальной
окраски хромосом. Использование этих методов
позволяет точно учитывать аномалии хромосом.
– Определим основные этапы цитогенетического
метода и условия его применения.
Доклад «Цитогенетический метод
антропогенетики» (демонстрация фотографий
наследственной патологии человека). [Приложение
3]
[Приложение
3]
Вопросы: (слайд 23)
– Какие биологические материалы можно
использовать для получения препаратов хромосом?
– Как изучают хромосомы лимфоцитов, если они не
делятся митозом?
– Что такое мутации?
– Какие мутации ведут к возникновению
наследственной патологии?
– Какое заболевание у ребенка с представленным
кариотипом? Каков его пол?
Вывод: Итак, цитогенетический метод основан на микроскопическом исследовании кариотипа. Позволяет выявить геномные и хромосомные мутации. (слайд 24)
5) Экспресс-методы и методы пренатальной диагностики (слайды 25, 26)
На пороге третьего тысячелетия произошел
переход на генный уровень изучения болезней
человека. Всего известно пять тысяч
наследственных болезней, из них две тысячи –
тяжелейшие расстройства. Значительные успехи
достигнуты в изучении молекулярных причин
наследственных болезней. Теперь стоит задача
ранней диагностики заболеваний, чтобы провести
своевременную профилактику или прервать
беременность в случае тяжелой патологии
будущего ребенка.
Теперь стоит задача
ранней диагностики заболеваний, чтобы провести
своевременную профилактику или прервать
беременность в случае тяжелой патологии
будущего ребенка.
– Рассмотрим новые экспресс – методы и методы
пренатальной диагностики.
Доклад «Экспресс-методы и методы пренатальной диагностики» [Приложение 4]
Вопросы: (слайд 27)
– Какие методы пренатальной диагностики
наследственных заболеваний показаны всем
беременным женщинам?
– Почему степень риска рождения детей с
отклонениями от нормы значительно больше у
алкоголиков, чем у непьющих родителей?
– Где расположено тельце Барра и как оно
выглядит?
– Каковы показания для пренатальной
диагностики?
Вывод: Информация о генетических
особенностях каждого человека дает возможность
еще до рождения ребенка предсказать, к каким
наследственным заболеваниям будет
предрасположен человек, какие меры профилактики
и лечения могут быть приняты. (Cлайд 28)
(Cлайд 28)
IV. Закрепление
1) Беседа: (слайд 29)
– Каковы особенности человека как объекта
генетических исследований?
– Какие методы применяются для изучения
генетики человека?
– В чем суть и каковы возможности
генеалогического метода?
– Чем прямые цитогенетические методы отличаются
от непрямых?
– Почему внимательное наблюдение за проявлением
признаков в ряду поколений может помочь изучать
закономерности наследственности и изменчивости?
– Какое значение имеют генетические методы
исследования наследственности человека для
медицины и здравоохранения?
– Какие важнейшие проблемы решает в настоящее
время медицинская генетика?
2) Решение задач:
А) Определите тип наследования по предложенным родословным. (Слайд 30)
Б) Конкордантность монозиготных
близнецов по массе тела составляет 80%, а
дизиготных – 30%. Каково соотношение
наследственных и средовых факторов в
формировании признака? (Слайд 31)
Каково соотношение
наследственных и средовых факторов в
формировании признака? (Слайд 31)
Вывод: Таким образом, невозможность
применения гибридологического метода на фоне
большого интереса к наследственности человека
привело к разработке специальных методов
изучения генетики человека. Это генеалогический,
близнецовый, цитогенетический методы,
экспресс-методы и методы пренатальной
диагностики.
Они позволяют понять природу наследственных
заболеваний, характер их наследования и выяснить
вероятность появления в будущих поколениях
наследственной патологии, а также быстрее
диагностировать и раньше начать лечение больных.
Сейчас диагностируется более трехсот
наследственных болезней и их число постоянно
растет. В ряде стран, в том числе и в России, уже
проводятся исследования, благодаря которым
появляется возможность получить генетический
паспорт – документ, в котором будут указаны
существенные для здоровья и выбора профессии
наследственные особенности.
V. Домашнее задание (слайд 32)
Конспект. Задачи:
Конкордантность монозиготных близнецов по росту составляет 65%, а дизиготных – 34%. Каково соотношение наследственных и средовых факторов в формировании признака?
Женщина имеет светлые волосы, ее ребенок также со светлыми волосами. Мать женщины светловолосая, две сестры и два брата – темноволосые. В семье брата – ребенок темноволосый. Составьте родословную. Определите, где возможно, гетерозиготность организмов.
Литература:
1. Биология для поступающих в вузы (способы
решения задач по генетике)./ Составитель Н.М.
Киреева. – Волгоград: «Учитель», 2000.
2. Заяц Р.Г., Бутиловский В.Э. Общая и
медицинская генетика. Лекции и задачи. –
Ростов-н/Д: Феникс, 2002.
3. Каменский А.А., Криксунов Е.А., Пасечник В.В.
Общая биология 10-11 класс. – М.: Дрофа, 2009.
4. Лобашев М.Е., Ватти К.В. Генетика с основами
селекции. – М.: Просвещение, 1979.
5. Медицинская генетика: Учебник / Н.П. Бочкова. М.:
Высшая школа, 2001.
6. Тимолянова Е.К. Медицинская генетика. –
Ростов-н/Д: Феникс, 2003.
Методы исследования генетики 10 класс
Урок биологии в 10 классе
с использованием современных электронных образовательных технологий
Тема: «Генетика человека» урок № 63« Методы исследования генетики человека»
Учитель биологии Солодкова Елена Дмитриевна. Глядянская СОШ
ЦельСпособствовать усвоению знаний о у учащихся об основных методах изучения наследственности человека, а также с методами лечения и предупреждения некоторых наследственных болезней человека .
Задачи
Тип урока:
Методы и приемы:
Образовательная: сформировать знания о наследовании признаков у человека , о его генетическом разнообразии и особенностях методики изучения генетики человека Развивающая: способствовать развитию у учащихся умений выражать мысли в словесной форме; развивать умение учащихся работать с текстом учебника и интернет ресурсами ( флеш- анимациями» при выполнении заданий;
Воспитывающая: способствовать выработке умения осознанно трудиться над поставленной целью; бережно относиться к ИКТ и оборудованию; формировать аккуратность при
оформлении заданий в тетради
Урок открытия нового знания
Словесные: беседа, рассказ сообщения учащихся; технические- работа с интернет ресурсами – решение генетических задач ;
Наглядные: демонстрация изобразительных средств –таблиц по генетике, рисунков учебника и презентации, инте6рнет ресурсов- флеш- анимаций
Практические: Распознавание роли различных методов генетики человека при изучении тех или иных наследственных признаков , решение генетических задач»
Основное содержание темы, термины и понятия
Генетические закономерности являются универсальными для всех живых организмов , в том числе и для человека. Однако в силу целого ряда особенностей исследование наследственности человека затруднено. Поэтому для изучения наследственности человека используются особые методы изучения его наследственности и изменчивости.
Однако в силу целого ряда особенностей исследование наследственности человека затруднено. Поэтому для изучения наследственности человека используются особые методы изучения его наследственности и изменчивости.
Термины и понятия: метод составления родословных- генеалогический , популяционный , близнецовый, цитогенетический и биохимический методы.
Планируемые результаты
Личностные
— сформировать познавательный интересы и мотивы, направленные на изучение методов генетики человека ;
—уметь анализировать, делать выводы
— воспитывать культуру общения , потребность в здоровом образе жизни
Уметь применять полученные знания при решении генетических задач.
Метапредметные
Познавательные:
— развивать умение работать с текстом учебника; преобразовывать информацию из одной формы в другую- из текстовой в табличную
-выполнять задания учителя и слушая сообщения обучающихся о различных методах изучения генетики человека, сопровождающиеся презентациями, флеш- анимациями
Регулятивные:
— умение ставить учебную задачу на основе соотнесения того, что уже известно из курса 9класса о методах изучения генетики человека и значении этих знаний для медицины;
— составление плана и последовательности действий при изучении материала урока.
— оценка результатов работы;
Коммуникативные:
— планировать учебное сотрудничество со сверстниками и учителем в процессе выполнения работы с текстом учебника и в процессе прослушивания презентаций , при решении задач с использованием флеш анимации ;
— уметь с достаточной полнотой и точностью выражать свои мысли в соответствии с задачами и условиями коммуникации, владеть монологической и диалогической формами речи.
Предметные
— выделять существенные признаки и особенности различных методов в изучения генетики человека;
— различать на рисунках таблицах и во время просмотра презентаций особенности методов изучения наследственности человека
— сравнивать биологических объектов, овладеть методом наблюдения
Организация образовательного пространства
Межпредметные связи
Ресурсы
Формы работы
Информатика: Работа с использованием презентации составленной учителем и презентаций учащихся (заполнение таблицы « Особенности методов изучения генетики человека»)
Решение задач с использованием интернет ресурсов.
Технические: таблицы по генетике и рисунки в учебнике , компьютер; проектор; экран;
Программные: презентации по проектам учащихся « Методы изучения генетики человека», Флеш анимация «Решение генетических задач и составление родословных» «учебник «Общая биология « 10- 11 класс В.В.Пасечника и др.
фронтальная —
индивидуальная
в паре —
ТЕХНОЛОГИЯ ИЗУЧЕНИЯ ТЕМЫ
I этап. Самоопределение к деятельности (целеполагание)
Цели деятельности
Актуализация темы. Вызов с использованием метода «кластер»
и постановка проблемного вопроса
Учитель: Сегодня мы познакомимся с особенностями изучения генетики человека. С чем как вы думаете связаны особенности изучения генетики человека? и какие методы используются для изучения наследственности человека ? Это проблемный вопрос, на который мы должны ответить на сегодняшнем уроке.
Обучающиеся: Эти особенности скорее всего связаны с тем, что человек не только биологический вид, отличающийся от других биологических видов своим строением, но и особенностями психической деятельности – высокоразвитым сознанием и развитой речью и сложной социальной деятельностью.
Учитель: Запишите в тетрадях тему сегодняшнего урока. (слайд№ 1)
Планируемый предметный результат
Мотивация учащихся к изучению темы, направив эмоции обучающихся на более глубокое восприятие материала.
Учитель: Определим круг вопросов, которые мы сегодня рассмотрим, что вы уже знаете о особенностях генетики человека и методах изучения наследовености и изменчивости признаков у человека , что бы хотели узнать нового? ( Слайд №2)
Обучающиеся пишут на доске : что они знают об особенностях изучения генетики человека как биологического так и социального существа
Учитель: запишем план урока в тетрадях ( слайд 3)
На основе анализа имеющихся знаний выявить «область незнания», поставить перед собой цель работы.
Поставить проблемный вопрос.
II этап Учебно-познавательная деятельность (изучение нового содержания)
Цели деятельности
Учебные задания и методы работы с информацией.
Планируемый предметный результат
Деятельностная цель:
Формирование способности учащихся к новым способам действия в процессе целеполагания и выполнения заданий учителя в процессе изучения нового материала.
Учитель: Прочитать текст учебника на стр. 176 и выделить особенности изучения генетики человека.
Ответ: В силу целого ряда особенностей человека исследование его наследственности затруднено:
1.Это невозможность направленного скрещивания именно тех пар, которые нужны для исследования ;
2.Позднее половое созревание ;
3.Малое потомство;
4. Невозможность содержания всех исследуемых людей в одинаковых условиях;
5. Относительно большое число хромосом. (23 пары).
Относительно большое число хромосом. (23 пары).
Учитель: Тем не менее изучение генетики человека необходимо хотя бы потому, что это нужно медицине. Заболевания, в основе которых лежат генетические нарушения, распространены гораздо шире, чем кажется на первый взгляд. Из-за этих нарушений около 15% эмбрионов погибают еще до рождения, 3% детей – при рождении, 3% детей умирают не достигнув взрослого возраста, 20% людей не вступают в брак и 10% браков – бездетны. Известно более 2000 болезней человека, вызываемых генетическими отклонениями.
Как же современная наука исследует генетику человека? Какие методы используются при этом.
Учащиеся: Это прежде всего метод изучения родословных некоторых семейств на протяжении длительного времени.
сообщение учащегося о генеалогическом методе )Слайд
Следующий метод – Популяционный.
Учитель: прочитать текст статьи на стр. 176-177. И ответить в чем заключается особенность этого метода изучения наследственности человека.
176-177. И ответить в чем заключается особенность этого метода изучения наследственности человека.
Следующий Близнецовый метод. ( сообщение учащегося)
Цитогенетический метод- (сообщение учащегося)
Биохимические методы ( сообщение учащегося)
В ходе прослушивания особенностей каждого метода в тетрадях ведется краткая запись .
http://interneturok.ru/ru/school/biology/10-klass/undefined-1/metody-issledovanija-genetiki-cheloveka Характерные особенности методов изучения генетики человека. Выберите самостоятельно вид краткой записи характерных особенностей каждого метода изучения генетики человека: таблица, тезисы, схема.
Примеры, использования методаПроверяем заполнение таблицы. Слайд №7
Личностный:
— выделять и находить в тексте термины и понятия,
— воспитать культуру общения и потребность в здоровом образе жизни;
— осознать социальную, практическую и личностную значимость
Изучаемого материала;
Предметный:
— расширение понятийной базы за счет включения в нее новых элементов.
-Изучить характерные особенности методики изучения генетики человека, выявить; специфические особенности цитогенетического, генеалогического популяционного и биохимического методов изучения генетики человека.
-умение правильно вести записи в тетради, выделяя главное;
— структурирование знаний в процессе заполнения таблицы.
III этап Диагностика качества освоения темы
Цели деятельности
Установить степень усвоения темы « Методы исследования генетики человека»
Учитель: Мы познакомились сегодня на уроке с основными методами изучения генетики человека.
Проверьте свои знания решив следующие задачи и ответив на вопросы в конце параграфа.
http://www.virtulab.net/images/stories/Inetractive_Biology/10_5.swf
(Слайд№8)
Почему трудно исследовать наследственность человека?
Слайд № 9 Эти особенности скорее всего связаны с тем, что человек не только биологический вид, отличающийся от других биологических видов своим строением, но и особенностями психической деятельности – высокоразвитым сознанием и развитой речью и сложной социальной деятельностью
Ответ: . : В силу целого ряда особенностей особенностей человека исследование его наследственности затруднено:
: В силу целого ряда особенностей особенностей человека исследование его наследственности затруднено:
1.Это невозможность направленного скрещивания именно тех пар, которые нужны для исследования ;
2.Позднее половое созревание ;
3.Малое потомство;
4. Невозможность содержания всех исследуемых людей в одинаковых условиях;
5. Относительно большое число хромосом. (23 пары).
Планируемый предметный результат
Личностный:
— творческое отношение
к процессу выбора и выполнения заданий;
Познавательный:
-Умение использовать методы наблюдения и сравнения биологических объектов.
Регулятивный:
-саморегуляция как способность к мобилизации сил и энергии,к волевому усилию и к преодолению препятствий ;
Коммуникативный:
— разрешение конфликтов в процессе обсуждения правильных ответов, культура поведения и речи.
IV этап. Рефлексивная деятельность
Цели деятельности
Самоанализ и самооценка
ученика
Планируемый предметный результат
-соотносить полученный результат с поставленной целью;
-оценить результат своей деятельности;
— оценить свое эмоциональное состояние
Самоанализ
I. Задание на самоанализ
Самооценка
II. Задание на самооценку. Закончите предложения:
Я доволен(льна) тем, что сегодня самостоятельно смог(ла) ………………..
Я не доволен(льна) тем, что сегодня …………………
Учащиеся усвоили изучаемый материал в полной мере, как это было запланировано.
Лаборатория генетики нарушений репродукции
I. Закономерности гаметогенеза и гонадогенеза млекопитающих животных и человека
Закономерности гаметогенеза и гонадогенеза млекопитающих животных и человека
- Изучены фундаментальные вопросы хронологии, динамики и закономерности развития мужских и женских половых желез и половых клеток человека и нескольких видов млекопитающих животных (коровы, зеленой мартышки, свиньи, крысы, мыши).
- Созданы оригинальные схемы оогенеза и сперматогенеза (Л.Ф. Курило,1983,1985,1989, 1996, которые включены в соответствующие учебники и монографии).
- Впервые в мире количественным методом доказано, что формирование примордиальных фолликулов (на примере человека, коровы, мыши, крысы) происходит после завершения конъюгации (в зиготене) и кроссинговера (в пахитене): вокруг ооцитов на стадии диплотены профазы 1 мейоза (Курило, 1980;1985; Kurilo,1981; Теплякова, Курило и др.,1984).
- Впервые в мире количественным методом прослежено развитие стадий: прелептотенной конденсации и деконденсации хромосом в ооцитах у человека, коровы, мыши и крысы и в мужских половых клетках эмбриона и плода человека; конденсации хромосом и локализации их вокруг ядрышка (стадия кариосферы) в ооцитах перед диакинезом из созревающих фолликулов у человека, коровы, зеленой мартышки (Курило, 1981; 1982, 1984, 1985; Курило и др.
 , 1983; 1986).
, 1983; 1986).
II. Разработка системы тестирования гаметотоксического эффекта, схемы и количественные критерии его оценки (для оогенеза и сперматогенеза)
Л.Ф. Курило разработано новое направление в гаметологии — количественное тестирование состояния гамет по стадиям их развития (гаметогенеза). Для этого направления исследований разработаны авторские методы, система и критерии количественной оценки гамето- и гонадотоксических воздействий (физических, химических и биологических факторов) на мужские и женские половые клетки и половые железы человека и животных. Эти методы находят применение при диагностике причин бесплодия и гаметопатий, при тестировании повреждающего гонады и гаметы фактора, при анализе эффективности лечения нарушений гаметогенеза, а также при профилактике названных состояний. Показано поражение оогенеза и сперматогенеза у потомства 1 поколения мышей и крыс после введения беременным самкам определенных соединений (ТиоТЭФ, алкоголь, никотин, окситетрациклин), выявлено пролонгированное для оо- и сперматогенеза F1 действие изученных соединений. На три метода получены патенты:1) Курило Л.Ф. «Способ цитологической диагностики нарушения сперматогенеза», патент на изобретение №2328736 от 1/2-2007; 2) Курило Л.Ф. «Способ диагностики генеративной потенции яичников», патент на изобретение №2367949 от 03/4-2008; 3) Королев Ю.Н., Курило Л.Ф., Никулина Л.А., Панова Л.Н., Гениатулина М.С., Шилейко Л.В. «Способ вторичной профилактики нарушений сперматогенеза при воздействии радиации» патент на изобретение №2169571.
На три метода получены патенты:1) Курило Л.Ф. «Способ цитологической диагностики нарушения сперматогенеза», патент на изобретение №2328736 от 1/2-2007; 2) Курило Л.Ф. «Способ диагностики генеративной потенции яичников», патент на изобретение №2367949 от 03/4-2008; 3) Королев Ю.Н., Курило Л.Ф., Никулина Л.А., Панова Л.Н., Гениатулина М.С., Шилейко Л.В. «Способ вторичной профилактики нарушений сперматогенеза при воздействии радиации» патент на изобретение №2169571.
III. Анализ структуры и механизмов развития наследственной патологии репродуктивной системы человека
- Установлены частота и типы хромосомных аберраций (ХА) (по лимфоцитам периферической крови и половым клеткам) при бесплодии у мужчин, женщин, при нарушении полового развития у детей обоего пола.
- Исследовано влияние хромосомных аберраций (ХА) в половых клетках из эякулята на гаметогенез и фертильность.
- Изучается частота нерасхождения хромосом в сперматидах и сперматозоидах (из эякулята) у лиц с ХА и при нормальном кариотипе.

- Отрабатываются подходы к выявлению мейотических мутаций у человека.
- Выявлены особенности патологии некоторых ультраструктур сперматозоидов при определенных случаях бесплодия: отсутствие динеиновых ручек или центрального дуплета микротрубочек аксонемы при синдроме Картагенера; нарушение конденсации хроматина при синдроме «незрелого» хроматина и др. (Брагина и др., 2001, 2005, 2009).
- Изучается корреляция между генными мутациями и фенотипом (на уровне клеток, органа – ткани, организма) при развитии заболеваний половой системы.
- Исследуется влияние половых инфекций (вирусных, бактериальных, протозойных) на гаметогенез и репродукцию (в т.ч. – на невынашивание беременности). Одними из первых выявили внутригаметную вирусную инфекцию.
- Формируется банк данных (электронный ресурс) по генетически обусловленным нарушениям репродуктивной системы.
IV. Исследование морально-этических и правовых проблем в репродуктологии и при использовании методов биомедицинских технологий.
- Степень информированности населения, специалистов репродуктологов и пациентов (с проблемами репродукции) в этико-правовых вопросах репродуктологии (методом опроса с помощью анкетирования).
- Этико-правовые проблемы при использовании репродуктивных и других биомедицинских технологий.
- «Статус эмбриона человека» – международное и внутреннее (российское) законодательство.
- По данному направлению Л.Ф. Курило являлась в 1997-2003 гг. экспертом рабочей группы по защите эмбриона и плода человека (CDBI-CO-GT3) при Руководящем Комитете по Биоэтике Совета Европы. Издан соответствующий Доклад (название приведено в библиографии).
- Л.Ф. Курило является одним из соавторов Федерального закона о временном запрете клонирования человека (2002). С 2011 г данный закон продлен бессрочно.
По названным направлениям осуществляется научно-методическое консультирование специалистов Москвы и других городов страны, проводится чтение лекций для студентов ВУЗов, медицинских училищ, врачей-курсантов РМАПО, МГМСУ, РУДН.
Инновационные методы молекулярной диагностики — генетический полиморфизм, моногенные заболевания Киев
Введение
Революционные достижения генетики человека, связанные с расшифровкой его генома, определяют переход современной медицины на молекулярный (геномный) уровень, способствуя тому, что проблемы классической медицины: диагностика, профилактика и лечение решаются на уровне нуклеиновых кислот и продуктов их экспрессии – РНК и белков. Диагностика моногенных заболеваний (заболеваний, обусловленных мутациями отдельного гена, проявление таких заболеваний не зависит от внешних факторов, но болезнь может развиться как в течение первых дней жизни, так и через несколько лет) помогает установить точный диагноз/носительство, позволяя оценить риски передачи наследственных заболеваний от родителей к ребенку. В то время как профилактическим направлением молекулярной медицины стала предиктивная (предсказательная) медицина, основной особенностью которой является индивидуальный подход к каждому пациенту, поскольку геном каждого человека индивидуален, а также профилактическая направленность, которая позволяет выявить заболевание, заложенное в генах, задолго до его проявления, позволяя предупредить болезнь. Данное направление применяется к мультифакториальным заболеваниям – то есть к таким, которые возникают при неблагоприятном сочетании генетических факторов (генетической предрасположенности) и неблагоприятного влияния внешней среды — вредных привычек, образа жизни, профессиональной деятельности и т.д. Полученные знания о геноме помогут человеку оставаться молодым, здоровым и сохранять хорошую физическую форму долгие годы. Методологическую основу предиктивной медицины составляют представления о генетическом полиморфизме, генах «предрасположенности».
Данное направление применяется к мультифакториальным заболеваниям – то есть к таким, которые возникают при неблагоприятном сочетании генетических факторов (генетической предрасположенности) и неблагоприятного влияния внешней среды — вредных привычек, образа жизни, профессиональной деятельности и т.д. Полученные знания о геноме помогут человеку оставаться молодым, здоровым и сохранять хорошую физическую форму долгие годы. Методологическую основу предиктивной медицины составляют представления о генетическом полиморфизме, генах «предрасположенности».
В человеческом организме около 30 тыс. генов. Гены в строго определенной последовательности расположены в хромосомах — гораздо более крупных образованиях, имеющихся в ядре каждой клетки (Рис. 1) и видимых под микроскопом. Хромосомный набор человека состоит из 46 хромосом (23 пары, в каждой паре одна получена от отца, другая — от матери). Одна из хромосомных пар определяет пол (эти хромосомы и называют половыми): у женщин имеется две хромосомы «Х», у мужчин — «Х» и «Y».
По числу хромосом и генов, по местоположению генов в хромосомах люди одинаковы (если речь не идет о хромосомных болезнях), но различные варианты одних и тех же генов и их сочетаний чрезвычайно разнообразны, отсюда генетическое разнообразие людей — от индивидуального до расового.
Уже сегодня расшифрованы все гены человека, и часть из них ученые научились использовать для «превентивной диагностики». Чтобы понимать, для чего необходима превентивная (то есть упреждающая) диагностика, надо понимать, что большинство болезней развиваются на почве «наследственной предрасположенности». Существуют некоторые заболевания, развитие которых на 100% предопределено наследственностью – они называются моногенными (то есть обусловленными одним единственным геном) и их не так уж много. В качестве примера можно привести гемофилию, фенилкетонурию, муковисцидоз. Большинство же болезней передаются по наследству в виде предрасположенности – то есть определенных особенностей обмена веществ, строения тела, силы иммунного ответа. Эти заболевания называются полигенными или мультифакториальными (то есть на их развитие влияют сразу несколько генов). К ним относятся большинство злокачественных опухолей, сахарный диабет 2 типа, системный атеросклероз и его осложнения – инфаркты, инсульты, гангрены; сердечная недостаточность; тромбозы и тромбоэмболии; остеопороз и связанные с ним переломы, и многие другие заболевания. Эти заболевания проявляются только при воздействии определенных условий внешней среды, поведения человека, набора привычек. То есть болезнь не передается по наследству со 100-процентной неотвратимостью, и при грамотном подходе ее развитие можно предотвратить.
Эти заболевания называются полигенными или мультифакториальными (то есть на их развитие влияют сразу несколько генов). К ним относятся большинство злокачественных опухолей, сахарный диабет 2 типа, системный атеросклероз и его осложнения – инфаркты, инсульты, гангрены; сердечная недостаточность; тромбозы и тромбоэмболии; остеопороз и связанные с ним переломы, и многие другие заболевания. Эти заболевания проявляются только при воздействии определенных условий внешней среды, поведения человека, набора привычек. То есть болезнь не передается по наследству со 100-процентной неотвратимостью, и при грамотном подходе ее развитие можно предотвратить.
Но для того, чтобы понимать, какие индивидуальные превентивные (то есть предупреждающие развитие болезни) программы помогут именно Вам, необходимо исследовать индивидуальные генетические особенности. Эти особенности можно исследовать при помощи методов предиктивной медицины, которые позволяют анализировать самые незначительные, так называемые полиморфные изменения, тот самый важнейший механизм, объясняющий нашу генетическую непохожесть. Таким образом, персонализированные исследования методами предиктивной медицины (поиск генетических полиморфизмов) могут выявить, почему каждый из нас по-своему переносит болезни, реагирует на стресс, лекарства, продукты питания. В настоящее время это самый мощный инструмент, который позволяет предупредить болезнь.
Таким образом, персонализированные исследования методами предиктивной медицины (поиск генетических полиморфизмов) могут выявить, почему каждый из нас по-своему переносит болезни, реагирует на стресс, лекарства, продукты питания. В настоящее время это самый мощный инструмент, который позволяет предупредить болезнь.
Генетический полиморфизм
Предиктивную медицину уместно рассматривать как первый и наиболее ранний этап активного воздействия человека на свой организм с целью своевременной коррекции потенциально возможной патологии или патологического процесса. Концептуальную основу предиктивной медицины составляют представления о генетическом полиморфизме.
ДНК выявляется более чем у 1 % людей в популяции и не приводит к развитию заболевания, это называется полиморфизмом, если же менее 1 % или с высокой вероятностью приводит к болезни — мутацией.
Рисунок 2. Пример генетического полиморфизма.
Полиморфными принято называть гены, которые представлены в популяции несколькими разновидностями — аллелями, что обусловливает разнообразие признаков внутри вида. Большинство известных полиморфизмов выражаются либо в заменах одного нуклеотида, либо в изменении числа повторяющихся фрагментов ДНК. Генетические полиморфизмы могут быть полезными, нейтральными, однако значительно чаще они приводят к появлению белковых продуктов с несколько измененными физико-химическими свойствами и параметрами функциональной активности. При этом функциональный спектр таких белков может сильно меняться от практически нейтрального эффекта генетического полиморфизма до полного нарушения функции соответствующего белкового продукта. Следует заметить, что отличие между полиморфизмом и мутацией довольно условно: когда один из вариантов нуклеотидных последовательностей участка ДНК выявляется более чем у 1 % людей в популяции и не приводит к развитию заболевания, это называется полиморфизмом, если же менее 1 % или с высокой вероятностью приводит к болезни — мутацией.
Большинство известных полиморфизмов выражаются либо в заменах одного нуклеотида, либо в изменении числа повторяющихся фрагментов ДНК. Генетические полиморфизмы могут быть полезными, нейтральными, однако значительно чаще они приводят к появлению белковых продуктов с несколько измененными физико-химическими свойствами и параметрами функциональной активности. При этом функциональный спектр таких белков может сильно меняться от практически нейтрального эффекта генетического полиморфизма до полного нарушения функции соответствующего белкового продукта. Следует заметить, что отличие между полиморфизмом и мутацией довольно условно: когда один из вариантов нуклеотидных последовательностей участка ДНК выявляется более чем у 1 % людей в популяции и не приводит к развитию заболевания, это называется полиморфизмом, если же менее 1 % или с высокой вероятностью приводит к болезни — мутацией.
Масштабы полиморфизма ДНК таковы, что между последовательностями ДНК двух людей, если только они не однояйцевые близнецы, существуют миллионы различий.
Пренатальная диагностика моногенных заболеваний
Хотя лишь немногие болезни полностью обусловлены мутацией одного гена, концепция моногенных болезней по-прежнему важна. Для таких болезней обычно характерен один из трех типов наследования: аутосомно-доминантный, аутосомно-рецессивный или Х-сцепленный. Общая распространенность моногенных болезней составляет 10 на 1000 новорожденных. Одна и та же моногенная болезнь может быть обусловлена разными мутациями в одном гене. Например, в гене муковисцидоза описано свыше 1700 вызывающих болезнь мутаций.
Генодиагностика применяется для выбора лечения и медико-генетического консультирования при многих моногенных болезнях, таких как нейрофиброматоз, синдром Марфана, семейная гиперхолестеринемия, поликистоз почек, муковисцидоз, гемоглобинопатии и других. При этих заболеваниях генодиагностика позволяет поставить или подтвердить диагноз даже в отсутствие симптомов, выявить заболевание у родственников больного, иногда предсказать тяжесть заболевания. На основе результатов генодиагностики проводят медико-генетическое консультирование.
На основе результатов генодиагностики проводят медико-генетическое консультирование.
Существует несколько типов генетического тестирования:
- Диагностическое тестирование — помогает поставить или подтвердить диагноз у человека с симптомами.
- Прогностическое тестирование — относится к бессимптомному тестированию, когда члену семьи был поставлен диагноз и существует необходимость выявления мутации в семье.
- Тестирование на носительство — используется для рецессивных или Х-сцепленных заболеваний, когда есть случаи заболевания в семейном анамнезе или высокий уровень заболеваемости в популяции, помогает оценить риск определенных заболеваний у будущего потомства и спланировать рождение здорового потомства.
- Пренатальное тестирование — тестирование плода, о котором известно, что он подвержен высокому риску.
- Преимплантационное тестирование — тестирование эмбрионов на очень ранних сроках, полученных в результате экстракорпорального оплодотворения, альтернатива пренатальному тестированию и прерыванию беременности.

- Скрининг новорожденных — тестирование заболеваний у новорожденных.
Превентивное генетическое тестирование мультифакториальных заболеваний
В отличие от моногенных заболеваний, мультифакториальные заболевания обусловлены взаимодействием большого числа генов и внешних факторов. При мультифакториальных заболеваниях наследуются не сами заболевания, а только предрасположенность к ним, и только при сочетании полиморфных генов с неблагоприятными внешними факторами (лекарства, продукты питания, вредные привычки, загрязнения окружающей среды) возможно проявление заболевания. Такие гены, аллельные варианты которых при наличии определенных условий предрасполагают к определенным заболеваниям, и получили название генов предрасположенности. Сочетания аллельных вариантов различных генов, вовлеченных в развитие каждой конкретной патологии, получили название «генных сетей». Идентификация всех генов человека, открытие новых генных сетей неизмеримо увеличивают возможности генетического тестирования наследственной предрасположенности и значение медико-генетического консультирования.
Генетическое тестирование наследственной предрасположенности уже достаточно широко практикуется во многих частных лабораториях и диагностических центрах мира.
В лабораториях проведены исследования ассоциации множества генов-кандидатов с рядом болезней, таких как ишемическая болезнь сердца, сахарный диабет, гипертоническая болезнь, различные виды опухолей и некоторые другие. Генетическое тестирование в досимптоматический период дает возможность выявить существующие пока только в геноме наследственные тенденции к развитию будущих болезней и, исходя из современного врачебного опыта, наметить пути их ранней профилактики. Внедрение результатов этих исследований в клиническую практику позволит получить пациенту информацию о возможном риске развития у него указанных заболеваний, а врач, принимая во внимание результаты молекулярно-генетического анализа, — разработать тактику упреждающей терапии предполагаемого заболевания, что позволит снизить заболеваемость, инвалидность и смертность населения. По данным английских ученых, ослабление неблагоприятного эффекта функционально неполноценных аллелей генов предрасположенности с помощью диеты, коррекции образа жизни, лекарственных и пищевых добавок позволяет человеку “выиграть” 14 лет активной полноценной жизни. По данным Института Медицины США, превентивное генетическое тестирование в США помогает предотвратить возникновение более 2 млн побочных реакций на медикаменты, 3 млн врачебных ошибок, 2.2 млн хирургических вмешательств, 200 тысяч сердечных приступов и 100 тысяч летальных исходов в год.
По данным английских ученых, ослабление неблагоприятного эффекта функционально неполноценных аллелей генов предрасположенности с помощью диеты, коррекции образа жизни, лекарственных и пищевых добавок позволяет человеку “выиграть” 14 лет активной полноценной жизни. По данным Института Медицины США, превентивное генетическое тестирование в США помогает предотвратить возникновение более 2 млн побочных реакций на медикаменты, 3 млн врачебных ошибок, 2.2 млн хирургических вмешательств, 200 тысяч сердечных приступов и 100 тысяч летальных исходов в год.
Приведенные выше факты свидетельствуют о большом медицинском и социальном значении тестирования аллелей «генов предрасположенности» и генов наследственных заболеваний. При достаточно высоком уровне медицинского обслуживания выявление лиц с наследственной предрасположенностью к той или иной патологии чрезвычайно важно для профилактики, лечения и прогноза течения заболеваний.
Среди них наиболее известных генов предрасположенности – гены предрасположенности к раку легких (CYP1A1, GSTP1, GSTM1, GSTT1), ишемической болезни сердца (NOS3), нарушению метаболизма фолиевой кислоты (MTHFR), инфаркту миокарда, гипертонии (АСЕ, AGT), болезни Альцгеймера (АPOЕ), тромбозу (F2, F5), воспалению (IL6, IL10), неприживаемости зубных имплантов (TNF, IL1A), мужского бесплодия (AZF, CFTR, SRY), гестоза (F5, FGB, APOE, MTHFR), истощения яичников (INHA, FSHR, ESR1) и др. Установлено, что у курильщков с мутациями в генах GSTM1 и GSTT1 риск заболеть раком легких примерно в 3 раза выше по сравнению с курильщиками без этих мутаций. Еще выше (почти в 20 раз) риск рака молочной железы у курящих женщин с мутациями в генах GSTM1 и NAT2. Тестирование генов метаболизма лекарств позволяет не только идентифицировать индивидуумов с «быстрым» и «медленным» типами метаболизма лекарственных препаратов, но и определять индивидуальную чувствительность к ним. Более того, именно таким образом можно подобрать индивидуальную дозировку различных лекарств и таким путем приблизиться к идеальной схеме индивидуального лечения, то есть к решению основной задачи фармакогенетики.
Установлено, что у курильщков с мутациями в генах GSTM1 и GSTT1 риск заболеть раком легких примерно в 3 раза выше по сравнению с курильщиками без этих мутаций. Еще выше (почти в 20 раз) риск рака молочной железы у курящих женщин с мутациями в генах GSTM1 и NAT2. Тестирование генов метаболизма лекарств позволяет не только идентифицировать индивидуумов с «быстрым» и «медленным» типами метаболизма лекарственных препаратов, но и определять индивидуальную чувствительность к ним. Более того, именно таким образом можно подобрать индивидуальную дозировку различных лекарств и таким путем приблизиться к идеальной схеме индивидуального лечения, то есть к решению основной задачи фармакогенетики.
Гены человека остаются неизменными в течение всей жизни. Достаточно однократного проведения диагностики, чтобы стало ясно, какие основные заболевания нашего времени угрожают вам, а какие нет. Генетическое тестирование в любом возрасте, задолго до начала самого заболевания, позволяет не только выявить уникальные особенности генотипа каждого человека, его генетическую индивидуальность, но и заранее начать профилактические мероприятия, предупреждающие развитие болезни. Своевременная коррекция питания, профориентации и пр. позволили бы избежать многих катастроф, способствовали профилактике многих недугов, обеспечили творческое долголетие.
Своевременная коррекция питания, профориентации и пр. позволили бы избежать многих катастроф, способствовали профилактике многих недугов, обеспечили творческое долголетие.
Врач-генетик МЦ «ИГР» Надежда Казачкова.
Список использованной литературы
- Баранов В.С., Асеев М.В., Баранова Е.В. Гены предрасположенности и генетический паспорт. Природа.1999. №3. 17-27
- Баранова Е.В. Код ДНК, или Как продлить молодость. Издательство АСТ, М. 2007. 223 с.
- Боринская С.А.. Геномика и биотехнология: наука начала третьего тысячелетия. Энергия. 2005, № 10. 28-34.
- Бочков Н.П. Клиническая генетика. Издательство: Медицина. 1997. 287 с.
- Клаг У., Каммингс М. Основы генетики. Издательство: Техносфера. 2007. 896 с.
- Тюняев А.А. Синдром гомеологическо-хромосомного иммунодефицита (СГХИД). Преамбула. Апрель – август 2008 года.
- Сингер М., Берг П. Гены и геномы. В 2-х томах. Издательство: Мир.
 1998. 764 с.
1998. 764 с. - Gibson G. & Muse S. V. A Primer of Genome Science. 2005. 350 pp.
- Motulsky A. If I had a gene test; What would I have and who would I tell? Lancet.1999. № 1.35-37.
- Nebert D.W., Carvan M.J. Ecogenetics: from Biology to Health. Toxicol.Industr.Health.1997.V.13.163-192.
- Schmutz J., Wheeler J. et al. Quality assessment of the human genome sequence. Nature. 2008. 453, 56-64.
- Venter J.C. et al. The sequence of the human genome. Science. 2001, 291, 1304-1351.
«Биохимический метод исследования генетики человека»
Биохимический метод изучения генетики человека основан на изучении характера биохимических реакций в организме и обмена веществ для установления носительства аномального гена или уточнения диагноза.
В отличие от цитогенетического метода, который позволяет изучать структуру хромосом и кариотипа в норме и диагностировать наследственные болезни, связанные с изменением их числа и нарушением организации, наследственные заболевания, обусловленные генными мутациями, а также полиморфизм по нормальным первичным продуктам генов изучают с помощью биохимических методов.
Эти методы позволяют определить место и характер мутации по изменениям в составе затронутых мутацией белков. Например, при мутации, ведущей к замене всего одной аминокислоты в огромной молекуле переносчика кислорода — гемоглобина, возникает наследственное заболевание, получившее название серповидной анемии, при котором эритроциты принимают форму полумесяца. Исследовав аминокислотный состав гемоглобина и обнаружив замену, можно сразу поставить диагноз.
Впервые эти методы стали применять для диагностики генных болезней еще в начале XX в. В последние 30 лет их широко используют в поиске новых форм мутантных аллелей. С их помощью описано более 1000 врожденных болезней обмена веществ. Для многих из них выявлен дефект первичного генного продукта. Наиболее распространенными среди таких заболеваний являются болезни, связанные с дефектностью ферментов, структурных, транспортных или иных белков. Установлено большое разнообразие гемоглобинов у человека, связанное с изменением структуры его пептидных цепей, что нередко является причиной развития заболеваний. Дефекты ферментов устанавливают путем определения содержания в крови и моче продуктов метаболизма, являющихся результатом функционирования данного белка. Дефицит конечного продукта, сопровождающийся накоплением промежуточных и побочных продуктов нарушенного метаболизма, свидетельствует о дефекте фермента или его дефиците в организме.
Дефекты ферментов устанавливают путем определения содержания в крови и моче продуктов метаболизма, являющихся результатом функционирования данного белка. Дефицит конечного продукта, сопровождающийся накоплением промежуточных и побочных продуктов нарушенного метаболизма, свидетельствует о дефекте фермента или его дефиците в организме.
Предметами современной биохимической диагностики являются специфические метаболиты, энзимопатии, различные белки. Объектами биохимического анализа могут служить моча, пот, плазма и сыворотка крови, форменные элементы крови, культуры клеток (фибробласты, лимфоциты). Для биохимической диагностики используются как простые качественные реакции (например, хлорид железа для выявления фенилкетонурии), так и более точные методы.
Биохимическую диагностику наследственных нарушений обмена проводят в два этапа. На первом этапе отбирают предположительные случаи заболеваний, на втором — более точными и сложными методами уточняют диагноз заболевания. Применение биохимических исследований для диагностики заболеваний в пренатальном периоде или непосредственно после рождения позволяет своевременно выявить патологию и начать специфические медицинские мероприятия, как, например, в случае фенилкетонурии. Для определения содержания в крови, моче или амниотической жидкости промежуточных, побочных и конечных продуктов обмена кроме качественных реакций со специфическими реактивами на определенные вещества используют хроматографические методы исследования аминокислот и других соединений.
Для определения содержания в крови, моче или амниотической жидкости промежуточных, побочных и конечных продуктов обмена кроме качественных реакций со специфическими реактивами на определенные вещества используют хроматографические методы исследования аминокислот и других соединений.
Биохимические методы изучения наследственности человека помогают обнаружить ряд заболеваний обмена веществ (углеводного, аминокислотного, липидного и др.) при помощи, например, исследования биологических жидкостей путем качественного или количественного анализа.
С помощью биохимических методов открыто около 500 молекулярных болезней, являющихся следствием проявления мутантных генов. При различных типах заболеваний удается либо определить сам аномальный белок-фермент, либо установить промежуточные продукты обмена. По результатам биохимических анализов возможно поставить диагноз болезни и определить методы лечения. Ранняя диагностика и применение различных диет на первых этапах постэмбрионального развития позволяют излечить некоторые заболевания или хотя бы облегчить состояние больных с неполноценными ферментными системами.
Методы исследования генетики человека: родословная и популяционная генетика — видео и стенограмма урока
Как мы изучаем генетику человека
Итак, что же остается изучать генетикам человека? По сути, они должны изучать геном человека в его естественном контексте без каких-либо манипуляций. Вместо скрининга мутантов генетики должны изучать встречающиеся в природе мутации. Вместо того, чтобы проводить контролируемые скрещивания, генетики должны изучать, как гены и фенотипы передаются людям в рамках существующих семей, анализируя родословных , которые представляют собой диаграммы семейных историй, которые показывают фенотипы и семейные отношения людей.Просто собирая семейные истории и создавая родословные, мы часто можем многое определить о генетическом заболевании, например, является ли оно доминантным или рецессивным. Мы также можем определить, вызвано ли заболевание геном на Х-хромосоме или аутосомой.
Если заболевание вызвано геном на аутосоме, что у человека означает любую из пронумерованных хромосом от одной до двадцати двух, состояние считается аутосомным . Однако, если заболевание вызвано геном на Х-хромосоме, говорят, что он сцеплен с полом .Большинство связанных с полом состояний, таких как дальтонизм на красный / зеленый цвет, являются рецессивными. Таким образом, если у человека, у которого есть копия аллеля дальтонизма, есть другая Х-хромосома с доминантным аллелем дикого типа, то этот человек не будет дальтоником.
Однако, если заболевание вызвано геном на Х-хромосоме, говорят, что он сцеплен с полом .Большинство связанных с полом состояний, таких как дальтонизм на красный / зеленый цвет, являются рецессивными. Таким образом, если у человека, у которого есть копия аллеля дальтонизма, есть другая Х-хромосома с доминантным аллелем дикого типа, то этот человек не будет дальтоником.
Вместо этого этот человек будет носителем только дальтоника. Это происходит очень часто у женщин, потому что у них две Х-хромосомы. Лишь в очень редких случаях женщина может иметь два рецессивных аллеля дальтонизма и подвергаться им. Однако, поскольку у мужчин есть только одна Х-хромосома, не существует второй Х-хромосомы, обеспечивающей доминантный аллель.Из-за этого, когда человек мужского пола получает единственную копию дальтоника аллеля, эта единственная копия определит его фенотип и сделает его дальтоником.
Многофакторные черты
До сих пор в этом уроке мы говорили только о чертах и условиях, которые контролируются генами в одном локусе в геноме человека. Однако все мы знаем, что не каждый признак определяется генами в одном локусе. Фактически, многие черты определяются комбинацией генов более чем в одном месте в геноме человека, а также негенетическими факторами.
Однако все мы знаем, что не каждый признак определяется генами в одном локусе. Фактически, многие черты определяются комбинацией генов более чем в одном месте в геноме человека, а также негенетическими факторами.
Многофакторные черты — это черты, которые вызваны множеством факторов. В большинстве случаев многофакторные признаки имеют как генетические, так и негенетические факторы, которые вносят вклад в фенотип. Рост у человека — это пример многофакторной черты. Однако большинство генетиков не особо озабочены ростом человека. Вместо этого человеческие генетики в основном озабочены человеческими расстройствами и болезнями.
Некоторые из наиболее распространенных и разрушительных заболеваний человека являются многофакторными, включая диабет, болезни сердца, болезнь Альцгеймера, ревматоидный артрит и рак, и это лишь некоторые из них.Считается, что на все эти заболевания влияют несколько локусов генов, а также множество негенетических факторов.
Генетик мог бы назвать их многофакторными; однако эти заболевания, вызванные множеством факторов, обычно называются комплексными заболеваниями . Общей чертой сложных заболеваний является то, что их тяжесть и возраст начала часто весьма различны. Эту сложность усугубляет тот факт, что некоторые из этих заболеваний действительно влияют друг на друга. Например, диабет сам по себе является фактором риска сердечных заболеваний.
Общей чертой сложных заболеваний является то, что их тяжесть и возраст начала часто весьма различны. Эту сложность усугубляет тот факт, что некоторые из этих заболеваний действительно влияют друг на друга. Например, диабет сам по себе является фактором риска сердечных заболеваний.
Human Population Genetics
Неудивительно, что генетику сложных заболеваний гораздо труднее понять, чем простое аутосомное заболевание, и методы, используемые для их изучения, также более сложны. Из-за многофакторности этих заболеваний каждый ген, который способствует развитию сложного заболевания, оказывает лишь частичное влияние на болезнь.
Поскольку ни один ген не может в одиночку вызвать сложное заболевание, мы не можем отслеживать аллель в семье вместе с заболеванием.Вместо этого генетики должны использовать популяционную генетику при изучении сложных заболеваний. Обычно для этого требуется сбор тысяч образцов ДНК и историй болезни как у затронутых, так и у здоровых людей из одной и той же популяции.
Кроме того, поскольку генетики пытаются выделить генетические факторы, они стараются минимизировать влияние негенетических факторов. Конечно, полностью исключить эти факторы из уравнения невозможно. Вместо этого генетики делают следующее лучшее и пытаются сопоставить негенетические факторы пораженных и незатронутых людей.
Если 50% пораженных лиц являются курильщиками, то около 50% незатронутых лиц также должны быть курильщиками. Если средний возраст пораженных людей составляет 65 лет, то средний возраст здоровых людей также должен быть около 65. Чем больше похожи эти две группы, тем более вероятно, что различия между ними связаны с их генетикой. .
Краткое содержание урока
Итак, вкратце, генетика человека — это уникальная область, требующая уникальных подходов для раскрытия генома человека.Генетические методы, такие как скрининг мутантов и контролируемые скрещивания, просто невозможны с людьми, поэтому вместо этого генетики должны полагаться на естественные мутации и существующие семейные истории. Родословные — это карты семейных историй, которые показывают фенотипы и семейные отношения людей.
Родословные — это карты семейных историй, которые показывают фенотипы и семейные отношения людей.
Просто собирая семейные истории и создавая родословные, мы часто можем многое определить о генетическом заболевании, например, является ли оно доминантным или рецессивным.Мы также можем определить, вызвано ли заболевание геном на Х-хромосоме или аутосомой. Аутосомное заболевание вызвано геном на аутосоме. Напротив, сцепленное с полом состояние вызвано геном на Х-хромосоме. Связанные с полом состояния, такие как красно-зеленая дальтонизм, обычно поражают мужчин, потому что у них есть только одна Х-хромосома, и, следовательно, этот признак контролируется только одним геном.
В то время как некоторые признаки определяются генами в одном локусе, многие другие определяются комбинацией нескольких генов и негенетических факторов. Многофакторные черты — это черты, которые вызваны множеством факторов. Некоторые из наиболее распространенных и разрушительных заболеваний человека имеют многофакторный характер. Эти заболевания, вызванные множеством факторов, обычно называют комплексными заболеваниями . Общей чертой сложных заболеваний является то, что их тяжесть и возраст начала часто весьма различны. Для изучения этих сложных заболеваний генетики человека часто используют популяционную генетику.
Эти заболевания, вызванные множеством факторов, обычно называют комплексными заболеваниями . Общей чертой сложных заболеваний является то, что их тяжесть и возраст начала часто весьма различны. Для изучения этих сложных заболеваний генетики человека часто используют популяционную генетику.
Результат обучения
Когда вы закончите этот урок, вы должны знать, что генетика человека — очень сложное исследование из-за долгого времени поколений.Это также жизненно важное исследование сложных заболеваний и семейных отношений.
Методология генетики человека
Am J Hum Genet. 1959 Jun; 11 (2 Pt 2): 315–334.
* Частично поддержано грантами A-1822, A-1831 и H-3708 от Национальных институтов здравоохранения.
Эта статья цитируется в других статьях в PMC.Полный текст
Полный текст доступен в виде отсканированной копии оригинальной печатной версии. Получите копию для печати (файл PDF) полной статьи (2. 3M) или щелкните изображение страницы ниже, чтобы просмотреть страницу за страницей. Ссылки на PubMed также доступны для Избранные ссылки .
3M) или щелкните изображение страницы ниже, чтобы просмотреть страницу за страницей. Ссылки на PubMed также доступны для Избранные ссылки .
Избранные ссылки
Эти ссылки находятся в PubMed. Это может быть не полный список ссылок из этой статьи.
- ОЛДРИХ Р.А., ШТАЙНБЕРГ АГ, КЭМПБЕЛЛ, округ Колумбия. Родословная, демонстрирующая рецессивное состояние, связанное с полом, характеризующееся истощением ушей, экзематоидным дерматитом и кровавым поносом. Педиатрия. 1954 Февраль; 13 (2): 133–139.[PubMed] [Google Scholar]
- ALLISON AC. Аспекты полиморфизма у человека. Колд Спринг Харб Symp Quant Biol. 1955; 20: 239–255. [PubMed] [Google Scholar]
- BAILEY NTJ. Оценка частот рецессивов при неполном множественном выборе. Энн Ойген. 1951 декабрь; 16 (3): 215–222. [PubMed] [Google Scholar]
- BOOK JA. Генетические исследования в северной шведской популяции; отпрыск от браков двоюродных братьев и сестер. Энн Хам Жене. 1957 Март; 21 (3): 191–221.
 [PubMed] [Google Scholar]
[PubMed] [Google Scholar] - NEEL СП.Проблемы с оценкой частоты необычных наследственных признаков. Am J Hum Genet. 1954 Март; 6 (1): 51–60. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- FALLS HF, NEEL JV. Генетика ретинобластомы. AMA Arch Ophthalmol. 1951 Октябрь; 46 (4): 367–389. [PubMed] [Google Scholar]
- GRAHAM JB. Биохимическая генетика свертывания крови. Am J Hum Genet. 1956 июн; 8 (2): 63–79. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- HUNTLEY CC, DEES SC. Экзема, связанная с тромбоцитопенической пурпурой и гнойным средним отитом; отчет о пяти смертельных случаях.Педиатрия. 1957 Март; 19 (3): 351–361. [PubMed] [Google Scholar]
- KROOTH RS. Использование оплодотворения пораженных людей и их здоровых братьев и сестер при оценке приспособленности. Am J Hum Genet. 1955 декабрь; 7 (4): 325–360. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- LI CC. Разделение рецессивного потомства. Методы Med Res. 1954; 6: 3–16.
 [PubMed] [Google Scholar]
[PubMed] [Google Scholar] - MORTON NE. Анализ сегрегации в генетике человека. Наука. 1958, 10 января; 127 (3289): 79–80. [PubMed] [Google Scholar]
- Morton NE, Crow JF, Muller HJ.ОЦЕНКА ВЗАИМНОГО ПОВРЕЖДЕНИЯ ЧЕЛОВЕКА НА ОСНОВЕ ДАННЫХ О ВСПОМОГАТЕЛЬНЫХ БРАКАХ. Proc Natl Acad Sci U S. A. 1956, ноябрь; 42 (11): 855–863. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- MULLER HJ. Наш груз мутаций. Am J Hum Genet. 1950 июн; 2 (2): 111–176. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Neel JV, Kodani M, Brewer R, Anderson RC. Частота кровнородственных браков в Японии с замечаниями по оценке сравнительных частот генов и ожидаемой скорости появления индуцированных рецессивных мутаций.Am J Hum Genet. 1949 декабрь; 1 (2): 156–178. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- REED TE, NEEL JV. Генетическое исследование множественного полипоза толстой кишки с приложением метода оценки относительной приспособленности. Am J Hum Genet. 1955 Сен; 7 (3): 236–263.
 [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar] - REESE AB. Частота ретинобластомы у потомков родителей, переживших болезнь. AMA Arch Ophthalmol. 1954 декабрь; 52 (6): 815–818. [PubMed] [Google Scholar]
- SLATIS HM.Метод оценки частоты аномальных аутосомно-рецессивных генов у человека. Am J Hum Genet. 1954 декабрь; 6 (4): 412–418. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Stern C. ЗАКОН ХАРДИ-ВЕЙНБЕРГА. Наука. 1943, 5 февраля; 97 (2510): 137–138. [PubMed] [Google Scholar]
- ТАКЕР Д.П., STEINBERG AG, COGAN DG. Частота генетической передачи спорадической ретинобластомы. AMA Arch Ophthalmol. 1957, апрель; 57 (4): 532–535. [PubMed] [Google Scholar]
- WINTERS RW, GRAHAM JB, WILLIAMS TF, McFALLS VW, BURNETT CH.Генетическое исследование семейной гипофосфатемии и резистентного к витамину D рахита. Врачи Trans Assoc Am. 1957; 70: 234–242. [PubMed] [Google Scholar]
Здесь представлены статьи из Американского журнала генетики человека, любезно предоставленные Американским обществом генетики человека
Что такое редактирование генома и CRISPR-Cas9 ?: MedlinePlus Genetics
Редактирование генома ( также называется редактированием генов) — это группа технологий, которые дают ученым возможность изменять ДНК организма. Эти технологии позволяют добавлять, удалять или изменять генетический материал в определенных местах генома. Было разработано несколько подходов к редактированию генома. Недавняя из них известна как CRISPR-Cas9, что является сокращением от кластеризованных регулярно чередующихся коротких палиндромных повторов и CRISPR-ассоциированного белка 9. Система CRISPR-Cas9 вызвала большой интерес в научном сообществе, потому что она быстрее, дешевле и эффективнее. точный и более эффективный, чем другие существующие методы редактирования генома.
Эти технологии позволяют добавлять, удалять или изменять генетический материал в определенных местах генома. Было разработано несколько подходов к редактированию генома. Недавняя из них известна как CRISPR-Cas9, что является сокращением от кластеризованных регулярно чередующихся коротких палиндромных повторов и CRISPR-ассоциированного белка 9. Система CRISPR-Cas9 вызвала большой интерес в научном сообществе, потому что она быстрее, дешевле и эффективнее. точный и более эффективный, чем другие существующие методы редактирования генома.
CRISPR-Cas9 был адаптирован из естественной системы редактирования генома бактерий. Бактерии захватывают фрагменты ДНК вторгшихся вирусов и используют их для создания сегментов ДНК, известных как массивы CRISPR. Массивы CRISPR позволяют бактериям «запоминать» вирусы (или близкие к ним). Если вирусы атакуют снова, бактерии производят сегменты РНК из массивов CRISPR, чтобы атаковать ДНК вирусов. Затем бактерии используют Cas9 или аналогичный фермент, чтобы разрезать ДНК, что выводит из строя вирус.
Система CRISPR-Cas9 работает аналогично в лаборатории. Исследователи создают небольшой фрагмент РНК с короткой «направляющей» последовательностью, которая прикрепляется (связывается) с определенной целевой последовательностью ДНК в геноме. РНК также связывается с ферментом Cas9. Как и в случае с бактериями, модифицированная РНК используется для распознавания последовательности ДНК, а фермент Cas9 разрезает ДНК в заданном месте. Хотя Cas9 является наиболее часто используемым ферментом, можно также использовать другие ферменты (например, Cpf1). После того, как ДНК разрезана, исследователи используют собственный механизм восстановления ДНК клетки, чтобы добавить или удалить части генетического материала или внести изменения в ДНК, заменив существующий сегмент индивидуализированной последовательностью ДНК.
Редактирование генома представляет большой интерес для профилактики и лечения заболеваний человека. В настоящее время большая часть исследований по редактированию генома проводится для понимания болезней с использованием клеток и животных моделей. Ученые все еще работают над тем, чтобы определить, является ли этот подход безопасным и эффективным для использования на людях. Он изучается в исследованиях по широкому кругу заболеваний, включая одногенные расстройства, такие как муковисцидоз, гемофилия и серповидно-клеточная анемия. Он также является многообещающим для лечения и профилактики более сложных заболеваний, таких как рак, болезни сердца, психические заболевания и инфекция, вызванная вирусом иммунодефицита человека (ВИЧ).
Ученые все еще работают над тем, чтобы определить, является ли этот подход безопасным и эффективным для использования на людях. Он изучается в исследованиях по широкому кругу заболеваний, включая одногенные расстройства, такие как муковисцидоз, гемофилия и серповидно-клеточная анемия. Он также является многообещающим для лечения и профилактики более сложных заболеваний, таких как рак, болезни сердца, психические заболевания и инфекция, вызванная вирусом иммунодефицита человека (ВИЧ).
Этические проблемы возникают, когда редактирование генома с использованием таких технологий, как CRISPR-Cas9, используется для изменения генома человека. Большинство изменений, вносимых при редактировании генома, ограничиваются соматическими клетками, то есть клетками, отличными от яйцеклеток и сперматозоидов. Эти изменения затрагивают только определенные ткани и не передаются от поколения к поколению. Однако изменения, внесенные в гены в яйцеклетках или сперматозоидах (клетках зародышевой линии) или в генах эмбриона, могут быть переданы будущим поколениям. Редактирование зародышевых клеток и генома эмбриона поднимает ряд этических проблем, в том числе допустимо ли использовать эту технологию для улучшения нормальных человеческих качеств (таких как рост или интеллект).Из соображений этики и безопасности редактирование зародышевых клеток и генома эмбриона в настоящее время запрещено законом во многих странах.
Редактирование зародышевых клеток и генома эмбриона поднимает ряд этических проблем, в том числе допустимо ли использовать эту технологию для улучшения нормальных человеческих качеств (таких как рост или интеллект).Из соображений этики и безопасности редактирование зародышевых клеток и генома эмбриона в настоящее время запрещено законом во многих странах.
Статьи в научных журналах для дальнейшего чтения
Ormond KE (1), Mortlock DP (2), Scholes DT (3), Bombard Y (4), Brody LC (5), Faucett WA (6), Garrison NA (7), Hercher L (8), Isasi) Р. (9), Миддлтон А. (10), Мусунуру К. (11), Шрайнер Д. (12), Вирани А. (13), Янг CE (3). Редактирование генома зародышевой линии человека. Am J Hum Genet. 2017 3 августа; 101 (2): 167-176. PubMed: 28777929. Полный текст доступен бесплатно в центре PubMed: PMC5544380.
Гупта Р.М., Мусунуру К. Расширение набора инструментов генетического редактирования: ZFN, TALEN и CRISPR-Cas9. J Clin Invest. 2014 Октябрь; 124 (10): 4154-61. DOI: 10. 1172 / JCI72992. Epub 2014 1 октября. Обзор. PubMed: 25271723. Полный текст доступен бесплатно в центре PubMed: PMC41.
1172 / JCI72992. Epub 2014 1 октября. Обзор. PubMed: 25271723. Полный текст доступен бесплатно в центре PubMed: PMC41.
Hsu PD, Lander ES, Zhang F. Разработка и применение CRISPR-Cas9 для геномной инженерии. Клетка. 2014 5 июня; 157 (6): 1262-78. DOI: 10.1016 / j.cell.2014.05.010. Обзор. PubMed: 24
Komor AC, Badran AH, Liu DR. Технологии на основе CRISPR для манипулирования геномами эукариот. Клетка. 2017 20 апреля; 169 (3): 559. DOI: 10.1016 / j.cell.2017.04.005. PubMed: 28431253.
Lander ES. Герои CRISPR. Клетка. 2016 14 января; 164 (1-2): 18-28. DOI: 10.1016 / j.cell.2015.12.041. Обзор. PubMed: 26771483.
Генетика человека | Междисциплинарная программа аспирантуры
Генетика — это изучение изменчивости и передачи наследственного материала от поколения к поколению, а также того, как эта информация преобразуется в биологические функции.Генетика использует несколько методов, чтобы понять изменчивость, передачу и функцию наследственного материала от молекулярного уровня до уровня популяции. Из-за всепроникающего воздействия генетической изменчивости на биологическую функцию генетика стала объединяющей темой для многих исследований в биологических и биомедицинских науках и может служить центром изучения практически всех биологических процессов и систем. Генетика играет все возрастающую роль в выяснении клеточных и молекулярных механизмов заболеваний и врожденных дефектов человека, а также в их профилактике, диагностике и лечении.В дополнение к использованию генетики для изучения биомедицинских вопросов, возникающих в других областях, генетика включает в себя важный набор вопросов о том, как информационное содержание набора относительно простых молекул может быть преобразовано в сложные организмы, как вариации на молекулярном уровне могут вызывают различия между людьми с точки зрения нормальных вариаций и процессов болезни, а также то, как эти вариации внутри и между популяциями могут быть использованы для объяснения различий в распространенности болезни.
Из-за всепроникающего воздействия генетической изменчивости на биологическую функцию генетика стала объединяющей темой для многих исследований в биологических и биомедицинских науках и может служить центром изучения практически всех биологических процессов и систем. Генетика играет все возрастающую роль в выяснении клеточных и молекулярных механизмов заболеваний и врожденных дефектов человека, а также в их профилактике, диагностике и лечении.В дополнение к использованию генетики для изучения биомедицинских вопросов, возникающих в других областях, генетика включает в себя важный набор вопросов о том, как информационное содержание набора относительно простых молекул может быть преобразовано в сложные организмы, как вариации на молекулярном уровне могут вызывают различия между людьми с точки зрения нормальных вариаций и процессов болезни, а также то, как эти вариации внутри и между популяциями могут быть использованы для объяснения различий в распространенности болезни.
| НАПРАВЛЕНИЯ ИССЛЕДОВАНИЙ ГЕНЕТИКИ ЧЕЛОВЕКА |
Исследователи из Центра генетических исследований человека имени Вандербильта изучают человеческие черты, используя несколько подходов. Примеры включают: Примеры включают: |
| МОДЕЛЬНЫЕ СИСТЕМЫ Мышь, рыба-зебра, мухи, культура клеток |
| ОБНАРУЖЕНИЕ ГЕНА ЗАБОЛЕВАНИЯ Рак груди, толстой кишки и предстательной железы, болезнь Альцгеймера, аутизм, рассеянный склероз, сердечная аритмия, сердечно-сосудистые заболевания, гипертония, тромбоз, диабет, ожирение, СПИД, малярия, туберкулез Митохондриальная болезнь, преждевременные роды |
| ГЕНЕТИКА НАСЕЛЕНИЯ Различия в состоянии здоровья среди европейского, афроамериканского, латиноамериканского и азиатского населения |
| ВЫЧИСЛИТЕЛЬНЫЕ МЕТОДЫ Взаимодействия ген-ген, взаимодействия ген-среда, системная геномика, высокопроизводительное секвенирование |
| Аналитическая химия | 2 | Химия аналитическая | 83 | 10. 745 745 |
7,1 | 2.476 |
| Аналитическая химия | 2 | Спектроскопия | 43 | 10,745 | 7,1 | 2,476 |
| Биологические науки о животных | 1 | Зоология | 175 | 8,923 | 4,7 | 3,588 |
| Биологические науки о животных | 14 | Биотехнология и прикладная микробиология | 159 | 8.923 | 4,7 | 3,588 |
| Биологические науки о животных | 1 | Сельское хозяйство, молочные продукты и зоотехники | 63 | 8,923 | 4,7 | 3,588 |
| Биологические науки о животных | 2 | Ветеринария | 146 | 8,923 | 4,7 | 3,588 |
| Антропология | 5 | Антропология | 88 | 3.448 | 15,8 | 0,682 |
| Астрономия и астрофизика | 1 | Астрономия и астрофизика | 68 | 30,065 | 11,4 | 4,625 |
| Биохимия | 4 | Биохимия и молекулярная биология | 298 | 23,643 | 12,3 | 4,969 |
| Биомедицинская инженерия | 9 | Биомедицинская инженерия | 90 | 9. 590 590 | 8,9 | 1,813 |
| Биофизика | 2 | Биофизика | 72 | 12,981 | 7,1 | 5,667 |
| Биология рака | 31 | Онкология | 242 | 9,391 | 2,1 | 2,667 |
| Клеточная биология и биология развития | 18 | Клеточная биология | 195 | 13,827 | 10.1 | 0,818 |
| Клетка и биология развития | 1 | Биология развития | 41 | 13,827 | 10,1 | 0,818 |
| Химическая и биомолекулярная инженерия | 1 | Прикладная химия | 74 | 11,059 | 5,9 | 1,304 |
| Химическая и биомолекулярная инженерия | 5 | Химическая инженерия | 143 | 11.059 | 5,9 | 1,304 |
| Клиническая психология | 1 | Психология, клинические (социальные науки) | 131 | 18,561 | 8,1 | 4,222 |
| Клиническая психология | 2 | Психология (наука) | 77 | 18,561 | 8,1 | 4,222 |
| Физика конденсированного состояния | 6 | Физика конденсированного состояния | 69 | 16. 109 109 | 5,5 | 11,826 |
| Криминология | 2 | Криминология и пенология | 69 | 9,956 | 2,3 | 1,375 |
| Науки о Земле и планетах | 2 | Науки о Земле, междисциплинарные | 199 | 12,810 | 14,2 | 4,917 |
| Науки о Земле и планетах | 5 | Астрономия и астрофизика | 68 | 12.810 | 14,2 | 4,917 |
| Экология, эволюция и систематика | 5 | Эволюционная биология | 50 | 13,915 | 18,0 | 0,840 |
| Экология, эволюция и систематика | 3 | Экология | 166 | 13,915 | 18,0 | 0,840 |
| Экономика | 59 | Экономика | 377 | 4.193 | 6,9 | 0,548 |
| Энтомология | 1 | Энтомология | 102 | 19,686 | 14,7 | 13,652 |
| Окружающая среда и ресурсы | 3 | Исследования окружающей среды (социальные науки) | 125 | 11,108 | 9,9 | 1,235 |
| Окружающая среда и ресурсы | 8 | Науки об окружающей среде (наука) | 274 | 11. 108 108 | 9,9 | 1,235 |
| Финансовая экономика | 41 | Бизнес, финансы | 108 | 2,879 | 6,7 | 0,133 |
| Финансовая экономика | 100 | Экономика | 377 | 2,879 | 6,7 | 0,133 |
| Механика жидкости | 1 | Физика, жидкости и плазма | 34 | 18.511 | 15,9 | 12,650 |
| Механика жидкости | 1 | Механика | 136 | 18,511 | 15,9 | 12,650 |
| Пищевая наука и технологии | 1 | Пищевая наука и технологии | 144 | 13,635 | 5,5 | 4,438 |
| Генетика | 4 | Генетика и наследственность | 175 | 16.830 | 11,4 | 0,333 |
| Геномика и генетика человека | 14 | Генетика и наследственность | 175 | 8,929 | 8,4 | 2,040 |
| Иммунология | 3 | Иммунология | 162 | 28,527 | 11,2 | 8,200 |
| Право и социальные науки | 27 | Закон | 151 | 2. 444 444 | 8,3 | 0,111 |
| Право и социальные науки | 55 | Социология | 149 | 2,444 | 8,3 | 0,111 |
| Лингвистика | 5 | Язык и лингвистика (AHCI) | 205 | 3,512 | 3,5 | 0,864 |
| Лингвистика | 14 | Лингвистика (социальные науки) | 193 | 3.512 | 3,5 | 0,864 |
| Морские науки | 2 | Геохимия и геофизика | 88 | 13,850 | 7,3 | 7,571 |
| Морские науки | 1 | Морская и пресноводная биология | 110 | 13,850 | 7,3 | 7,571 |
| Морские науки | 1 | Океанография | 65 | 13.850 | 7,3 | 7,571 |
| Исследования материалов | 20 | Материаловедение, многопрофильное | 335 | 16,286 | 10,8 | 1. 000 000 |
| Медицина | 6 | Медицина, исследования и эксперименты | 140 | 13,739 | 8,7 | 4,704 |
| Микробиология | 7 | Микробиология | 137 | 15.500 | 13,5 | 1,308 |
| Неврология | 14 | Неврология | 273 | 12,449 | 13,8 | 2,833 |
| Ядерная наука и наука о частицах | 2 | Ядерная физика | 19 | 14,219 | 10,5 | 1,353 |
| Ядерная наука и наука о частицах | 3 | Физика, частицы и поля | 29 | 14.219 | 10,5 | 1,353 |
| Питание | 2 | Питание и диетология | 89 | 11,848 | 14,2 | 0,471 |
| Организационная психология и организационное поведение | 2 | Психология, прикладная | 83 | 18,333 | 4,7 | 3,150 |
| Организационная психология и организационное поведение | 1 | Менеджмент | 226 | 18. 333 333 | 4,7 | 3,150 |
| Патология: механизмы заболевания | 1 | Патология | 77 | 23,472 | 7,0 | 10,500 |
| Фармакология и токсикология | 1 | Токсикология | 93 | 13,820 | 11,0 | 6,938 |
| Фармакология и токсикология | 6 | Фармакология и фармация | 275 | 13.820 | 11,0 | 6,938 |
| Физическая химия | 19 | Физическая химия | 162 | 12,703 | 12,4 | 5,600 |
| Физиология | 2 | Физиология | 81 | 19,318 | 11,0 | 6,783 |
| Фитопатология | 5 | Науки о растениях | 235 | 13.078 | 12.5 | 1,059 |
| Биология растений | 1 | Науки о растениях | 235 | 26,379 | 12,9 | 5,862 |
| Политология | 2 | Политология | 182 | 8,091 | 11,6 | 1,750 |
| Психология | 1 | Психология (наука) | 77 | 24,137 | 12,9 | 7. 040 040 |
| Психология | 2 | Психология междисциплинарная (социальные науки) | 140 | 24,137 | 12,9 | 7,040 |
| Общественное здравоохранение | 2 | Общественное, экологическое и ок. Здравоохранение (социальные науки) | 176 | 21,981 | 9,5 | 4,621 |
| Общественное здравоохранение | 4 | Общественное, экологическое и ок.Здравоохранение (наука) | 203 | 21,981 | 9,5 | 4,621 |
| Экономика ресурсов | 31 | Экономика | 377 | 5,184 | 5,4 | 0,913 |
| Экономика ресурсов | 28 | Исследования окружающей среды (социальные науки) | 125 | 5,184 | 5,4 | 0,913 |
| Экономика ресурсов | 1 | Экономика и политика сельского хозяйства (наука) | 21 | 5. 184 184 | 5,4 | 0,913 |
| Социология | 3 | Социология | 149 | 8,055 | 18,3 | 1,545 |
| Статистика и ее применение | 7 | Математика, междисциплинарные приложения | 108 | 5,810 | 3,9 | 1,250 |
| Статистика и ее применение | 7 | Статистика и вероятность | 125 | 5.810 | 3,9 | 1,250 |
| Вирусология | 2 | Вирусология | 36 | 10,431 | 4,3 | 3,429 |
| Vision Science | 46 | Неврология | 273 | 6,422 | 3,8 | 0,750 |
| Vision Science | 4 | Офтальмология | 62 | 6,422 | 3,8 | 0.750 |
6 Методы изучения генетики человека
Некоторые из основных методов изучения генетики человека следующие:
В последние годы были разработаны новые методы. С помощью этих методов стало возможным многое понять о способе наследования ряда признаков у людей.
С помощью этих методов стало возможным многое понять о способе наследования ряда признаков у людей.
1. Записи о родословных хорошо записаны и содержатся в хорошем состоянии, поэтому стало легче отслеживать передачу определенного признака от поколения к поколению.
2. Популяционная генетика широко использовалась при изучении генетики человека. Таким образом, методы, с помощью которых можно анализировать судьбу персонажей в популяции, преодолели ограничение, связанное с небольшим количеством потомства у человека.
3. Биохимическая генетика , метод культивирования клеток и генетические методы соматических клеток помогли понять химические основы наследования большого количества признаков.
4. Технология слияния клеток помогает производить различные комбинации генетического материала человека в клонах потомства.Изучая эти клоны, генетики смогли по-новому взглянуть на генетику человека. С помощью этой технологии можно изолировать гибриды, образованные между клетками, полученными от мыши и человека.
С помощью этой технологии можно изолировать гибриды, образованные между клетками, полученными от мыши и человека.
5. Путем сравнения фенотипов однояйцевых и разнояйцевых близнецов (исследование близнецов) установлена наследственная основа ряда признаков. Наследственные и обусловленные окружающей средой черты могут быть выявлены путем сравнительного исследования однояйцевых и разнояйцевых близнецов.
6. В цитологии человека были разработаны новые методы окрашивания. С помощью таких передовых методов было обнаружено, что правильное число диплоидных хромосом человека, т. Е. 46, является правильным.
В отсутствие селекционных экспериментов информация о наследовании человека в основном была получена путем изучения родословной естественных черт. Такие черты могут быть несущественными или важными для здоровья и благополучия человека.
Это могут быть цвет глаз, альбинизм, дальтонизм, рост, способность ощущать вкус химического вещества, называемого PTC, способность вертеть языком, гемофилия, врожденные ошибки мета-холизма, умственные способности и так далее (рис.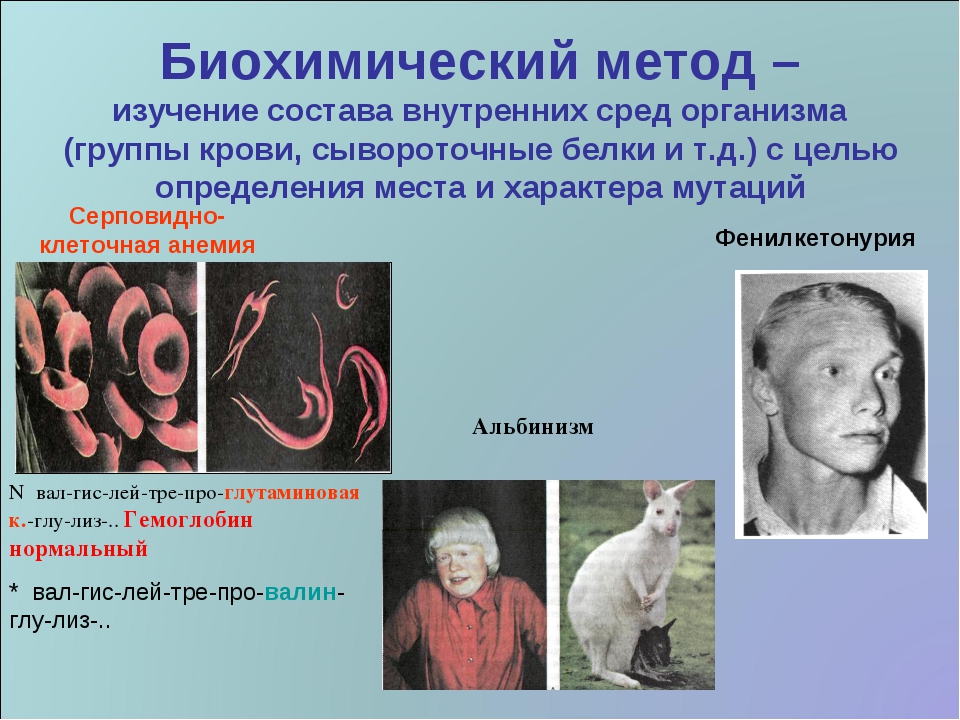 5.62).
5.62).
Возможность попробовать PTC:
Дегустаторы PTC (фенилтиокарбамида) считают его очень горьким на вкус. Не дегустаторы либо не пробуют его, либо узнают какой-то другой вкус, кроме горького. Большинство людей являются дегустаторами, предполагая, что это определяется доминантным аллелем T.
Три возможных генотипа — TT, Tt и tt. Не дегустаторы являются гомозиготными рецессивными tt. Дегустаторы с генотипом ТТ, Тт.Если у tt, не участвующего в дегустации, есть брат-дегустатор TT или Tt, то его родители гетерозиготны только по гену (Tt x tt) или (Tt x Tt)
.Точно так же способность катать язык в трубке, как в манере, контролируется доминантным аллелем R. Ролики имеют генотип RR или Rr, а не-ролики всегда гомозиготные рецессивные rr.
Корпус Barr (рис. 5.63) :
Мерри Барр (1949) обнаружил тело, сильно окрашенное нуклеиновыми кислотами в нервных клетках самок кошек.Позже было замечено, что почти все соматические клетки самок млекопитающих представляют собой наличие этого тела. Он был идентифицирован как половой хроматин или тельце Барра. У нормальных мужчин этого нет.
Он был идентифицирован как половой хроматин или тельце Барра. У нормальных мужчин этого нет.
Тело прилегает к ядерной мембране и выглядит как округлый диск. В 1954 году Дэвидсон и Смит наблюдали, что он принимает особую форму в полиморфно-ядерных лейкоцитах и называется барабанной палочкой, потому что его можно наблюдать как отросток к ядру. Он торчит из ядра.
Структура хромосом:
Разработаны специальные методы окрашивания хромосом человека флуоресцентными красителями после различных обработок. Рисунок полос служит для идентификации отдельных сегментов хромосомы (рис. 5.64).
В последние годы были разработаны методы группирования Q, G, R, O и C. Интересно отметить, что каждая хромосома демонстрирует уникальный паттерн полос при определенной обработке, и ее паттерн остается неизменным при той же обработке.
Исследование полос может быть использовано в качестве маркеров анализа родословных, популяционных исследований и локализации генов. Исследования группирования имеют более широкое применение при изучении клинических заболеваний, то есть роли хромосомных изменений в неправильном развитии, умственной отсталости и абортах.
Исследования группирования имеют более широкое применение при изучении клинических заболеваний, то есть роли хромосомных изменений в неправильном развитии, умственной отсталости и абортах.
границ | Размышления о генетике человека: призыв к развитию теории генетики болезней
Введение
Разработка теоретических моделей генетики человека и интеграция этих моделей с экспериментом и статистической оценкой имеют решающее значение для научного прогресса.Эта точка зрения утверждает, что усиление усилий в области теории генетики болезней, дополняющих экспериментальные и статистические усилия, приведет к эскалации раскрытия молекулярной этиологии сложных заболеваний. В частности, разработка новых реалистичных моделей генетики болезней поможет выяснить сложный патогенез заболевания, а предсказанные закономерности в генетических данных, полученные с помощью этих моделей, позволят проводить параллельные, более всесторонние статистические испытания различных аспектов прогнозов генетики болезней, тем самым лучше выявляя очаги болезни. Под теоретической генетикой человека я намерен охватить все исследования, посвященные моделированию наследуемой архитектуры, лежащей в основе признаков болезни, и исследования результирующих принципов и динамики таких моделей. Следовательно, объем теоретической работы по генетике болезней включает построение и анализ моделей, описывающих, как возникают предрасполагающие к заболеванию аллели (1), (2) передаются через семьи и популяции и (3) взаимодействуют с другими рисковыми и защитными аллелями как в факторы генома и окружающей среды, вызывающие болезненные состояния.Теоретическая работа улучшает понимание жизнеспособных генетических моделей болезней, согласующихся с эмпирическими результатами исследований сцепления, передачи и ассоциации, а также популяционной генетики. Кроме того, понимание закономерностей генетических данных, ожидаемых в реалистичных моделях болезней, позволит использовать более эффективные подходы к обнаружению предрасполагающих к болезням аллелей и дополнительных наследственных факторов, важных при распространенных заболеваниях.
Под теоретической генетикой человека я намерен охватить все исследования, посвященные моделированию наследуемой архитектуры, лежащей в основе признаков болезни, и исследования результирующих принципов и динамики таких моделей. Следовательно, объем теоретической работы по генетике болезней включает построение и анализ моделей, описывающих, как возникают предрасполагающие к заболеванию аллели (1), (2) передаются через семьи и популяции и (3) взаимодействуют с другими рисковыми и защитными аллелями как в факторы генома и окружающей среды, вызывающие болезненные состояния.Теоретическая работа улучшает понимание жизнеспособных генетических моделей болезней, согласующихся с эмпирическими результатами исследований сцепления, передачи и ассоциации, а также популяционной генетики. Кроме того, понимание закономерностей генетических данных, ожидаемых в реалистичных моделях болезней, позволит использовать более эффективные подходы к обнаружению предрасполагающих к болезням аллелей и дополнительных наследственных факторов, важных при распространенных заболеваниях. Несмотря на ключевую роль теории генетики болезней, такое исследование не особенно активно.В настоящее время деятельность в области генетики болезней человека в основном сосредоточена на крупномасштабных эмпирических исследованиях и, в меньшей степени, на статистических методах с ограниченным вкладом в теорию.
Несмотря на ключевую роль теории генетики болезней, такое исследование не особенно активно.В настоящее время деятельность в области генетики болезней человека в основном сосредоточена на крупномасштабных эмпирических исследованиях и, в меньшей степени, на статистических методах с ограниченным вкладом в теорию.
Фон и каркас
В общих чертах, научный прогресс основан на прочном взаимодействии между тремя видами деятельности: (1) эмпирическим экспериментированием и наблюдением, (2) разработкой теоретических моделей и извлечением их предсказанных закономерностей и (3) статистической оценкой вероятностного соответствия. между предсказанными закономерностями и эмпирическими данными.Очень важные открытия, безусловно, могут произойти без формализации этой деятельности, но эти три аспекта, тем не менее, имеют решающее значение. В качестве примера рассмотрим относительно недавнее замечательное открытие сложной низкоуровневой примеси между современными людьми и архаическими людьми (Green et al. , 2010; Reich et al., 2010; Gronau et al., 2011; Li and Durbin, 2011; Санкарараман и др., 2016). Это открытие было сделано благодаря героическим усилиям по выделению, секвенированию, сборке и выравниванию архаической ДНК останков неандертальцев и денисовцев.Параллельно с этим были разработаны прогнозы генетической архитектуры, моделей дивергенции и общих хромосомных регионов на основе моделей примесей с использованием как молекулярной филогенетики, так и теории популяционной генетики, включая мутации, генетический дрейф, миграцию и демографию. Наконец, соответствие между наблюдаемыми генетическими данными и теоретическими предсказаниями было достигнуто с помощью различных подходов, основанных на правдоподобии, байесовского и фишеровского подходов. Не будет преувеличением сказать, что этот прогресс наших научных знаний зависел от тщательных эмпирических наблюдений / экспериментов, развития теории популяционной генетики и формальной оценки богатых теоретических предсказаний на основе наблюдаемых данных с помощью строгих статистических методов.
, 2010; Reich et al., 2010; Gronau et al., 2011; Li and Durbin, 2011; Санкарараман и др., 2016). Это открытие было сделано благодаря героическим усилиям по выделению, секвенированию, сборке и выравниванию архаической ДНК останков неандертальцев и денисовцев.Параллельно с этим были разработаны прогнозы генетической архитектуры, моделей дивергенции и общих хромосомных регионов на основе моделей примесей с использованием как молекулярной филогенетики, так и теории популяционной генетики, включая мутации, генетический дрейф, миграцию и демографию. Наконец, соответствие между наблюдаемыми генетическими данными и теоретическими предсказаниями было достигнуто с помощью различных подходов, основанных на правдоподобии, байесовского и фишеровского подходов. Не будет преувеличением сказать, что этот прогресс наших научных знаний зависел от тщательных эмпирических наблюдений / экспериментов, развития теории популяционной генетики и формальной оценки богатых теоретических предсказаний на основе наблюдаемых данных с помощью строгих статистических методов. Самые случайные наблюдатели заметят множество дополнительных примеров этой парадигмы из различных областей науки, таких как физика элементарных частиц (Glashow, 1961; Higgs, 1964; Weinberg, 1967), механика (Einstein, 1916; Schrodinger, 1926), кинетика ферментов (Michaelis, Menten, 1913), полупроводники (Hall, 1879; Wilson, 1931; Mott, 1938; Schottky, 1938), атомная химия (Hund, 1926; Mulliken, 1932; Huckel, 1934), классическая генетика (Mendel, 1866; Fisher, 1918), наследственность и эволюция (Fisher, 1930; Wright, 1932; Price, 1970), популяционная генетика (Hardy, 1908; Weinberg, 1908; Hudson, 1982, 1983; Kingman, 1982a; Gillespie, 1993, 2000). ) и экология хищник-жертва (Лотка, 1925).Во всех этих и многих других областях теоретическая работа является динамическим компонентом научного процесса: необъяснимые эмпирические явления мотивируют новую теорию, часто относительно безупречно, и, наоборот, предсказанные закономерности, вытекающие из механистических моделей, перевариваются экспериментаторами и быстро проверяются.
Самые случайные наблюдатели заметят множество дополнительных примеров этой парадигмы из различных областей науки, таких как физика элементарных частиц (Glashow, 1961; Higgs, 1964; Weinberg, 1967), механика (Einstein, 1916; Schrodinger, 1926), кинетика ферментов (Michaelis, Menten, 1913), полупроводники (Hall, 1879; Wilson, 1931; Mott, 1938; Schottky, 1938), атомная химия (Hund, 1926; Mulliken, 1932; Huckel, 1934), классическая генетика (Mendel, 1866; Fisher, 1918), наследственность и эволюция (Fisher, 1930; Wright, 1932; Price, 1970), популяционная генетика (Hardy, 1908; Weinberg, 1908; Hudson, 1982, 1983; Kingman, 1982a; Gillespie, 1993, 2000). ) и экология хищник-жертва (Лотка, 1925).Во всех этих и многих других областях теоретическая работа является динамическим компонентом научного процесса: необъяснимые эмпирические явления мотивируют новую теорию, часто относительно безупречно, и, наоборот, предсказанные закономерности, вытекающие из механистических моделей, перевариваются экспериментаторами и быстро проверяются.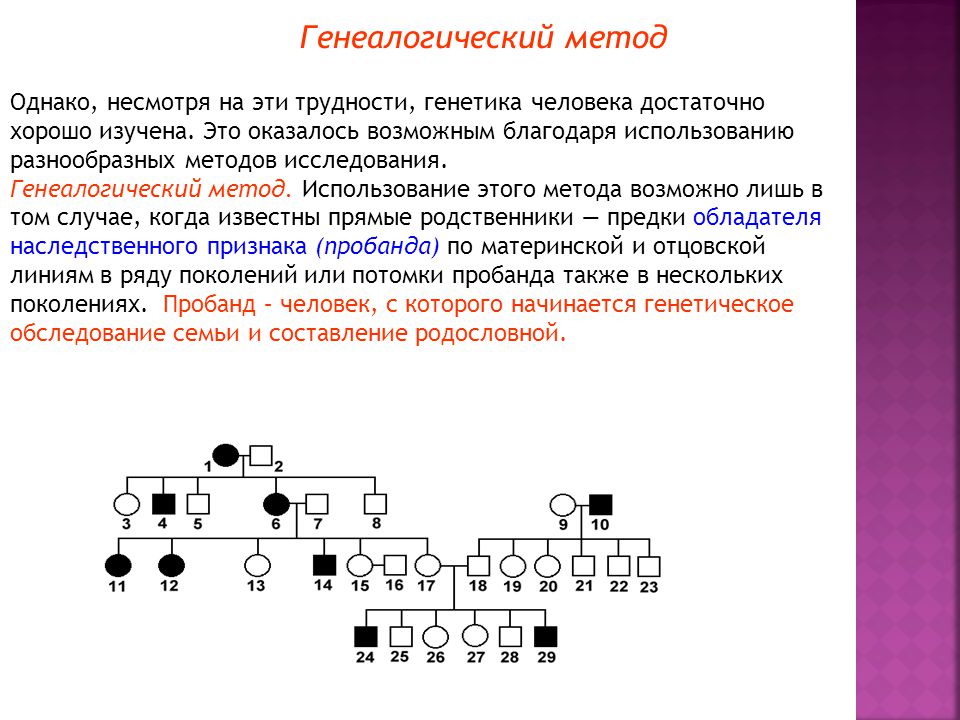 что привело к быстрому и эффективному расширению нашего понимания этих явлений.
что привело к быстрому и эффективному расширению нашего понимания этих явлений.
Для сравнения, картирование генов болезней создало относительно бесплодный ландшафт теории.В значительной степени мотивированная желанием повлиять на клиническую практику, генетика болезней человека исторически была очень прагматичной областью, где технологический прогресс в генотипировании и секвенировании стимулировал крупномасштабные исследования, а большая часть количественной работы была сосредоточена на статистических методах анализа, а не на анализе. более справедливое разделение статистики и теории. Это продолжается, несмотря на случаи, когда глубокие сдвиги в подходах были вызваны теоретическими выводами. Например, длительная стагнация в картировании общих, сложных заболеваний была нарушена теоретическими разработками в середине-конце 1990-х годов, показавшими, что высокоплотное генотипирование с использованием популяционных выборок значительно повысило бы способность обнаруживать высокочастотные предрасполагающие к болезням аллели умеренных размеры эффекта, мотивирующие парадигму GWAS из чрезмерно упрощенной модели генетики болезни (Kaplan et al. , 1995; Риш и Мерикангас, 1996; Long et al., 1997; Сюн и Го, 1998; Кругляк, 1999; Лонг и Лэнгли, 1999).
, 1995; Риш и Мерикангас, 1996; Long et al., 1997; Сюн и Го, 1998; Кругляк, 1999; Лонг и Лэнгли, 1999).
Хотя это и не является обычным явлением, существуют и другие исторические примеры теории генетики болезней, способствующие ускоренному прогрессу в генетике человека, включая теорию селективного преимущества гетерозигот при малярии и серповидно-клеточной анемии (Allison, 1954), согласно которой сложные заболевания действительно имеют наследственный компонент (Steinberg et al., 1951; Pickering, 1978; Debray et al., 1979; Kendler and Diehl, 1993; DeBraekeleer, 1991; Lynn et al., 1995; Stein et al., 2005), что большие мультиплексные семьи были идеальными для изучения взаимосвязей заболеваний в рамках моделей Менделирующих болезней (Thompson, 1978; Botstein et al., 1980), и более разрозненное влияние теоретических идей популяционной генетики, таких как аллель частотные спектры сильно смещены в сторону очень редких аллелей (Ewens, 1972; Watterson, 1975; Slatkin and Rannala, 1997; Long and Langley, 1999; Eyre-Walker, 2010; Hudson, 2015) — акцентируется в быстрорастущих популяциях, гаплотипы демонстрируют блокировку -подобная структура в паттернах LD (Hill, Robertson, 1968; Hudson, Kaplan, 1985; Nothnagel et al.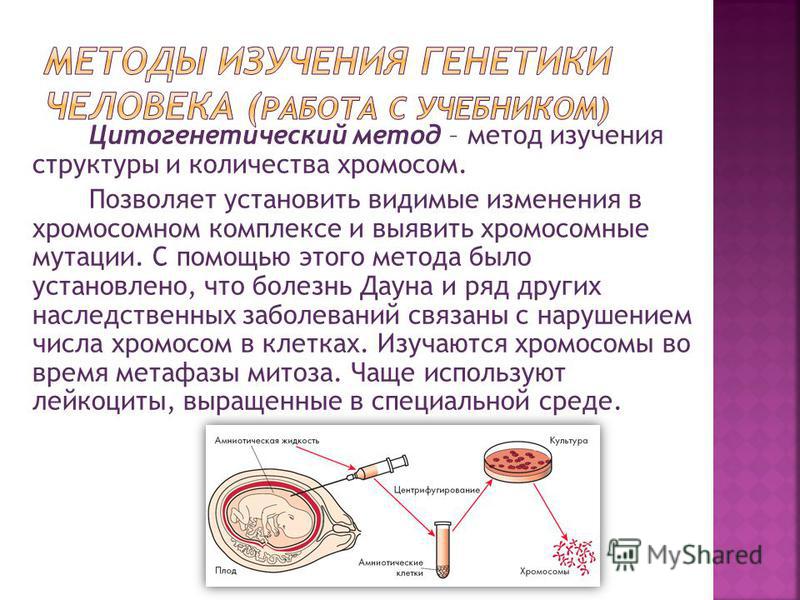 , 2002; Wiuf and Posada, 2003), узкие места в популяции с последующим расширением акцентируют влияние аллельного доминирования на приспособленность (Balick et al., 2015), а аллели с пагубным влиянием на приспособленность возникают позже, чем нейтральные в отношении приспособленности при той же частоте аллелей ( Маруяма, 1974; Ziezun et al., 2013). Теоретическая работа была проведена по применению высокополигенной аддитивной модели к распространенным заболеваниям, предлагая некоторые проверяемые прогнозы (Yang et al., 2010, 2011a; Vinkhuyzen et al., 2013; Loh et al., 2015). Дополнительные полезные усилия были сосредоточены на широко распространенных эпистатических взаимодействиях (Hodge, 1981; Neuman and Rice, 1992; Majewski et al., 2001; Zuk et al., 2012). Однако конкурирующие теоретические модели генетики общих болезней немногочисленны, хотя и история, и разум говорят в пользу более активного теоретического сообщества и усиления взаимодействия между теорией, экспериментом и статистическими методами.
, 2002; Wiuf and Posada, 2003), узкие места в популяции с последующим расширением акцентируют влияние аллельного доминирования на приспособленность (Balick et al., 2015), а аллели с пагубным влиянием на приспособленность возникают позже, чем нейтральные в отношении приспособленности при той же частоте аллелей ( Маруяма, 1974; Ziezun et al., 2013). Теоретическая работа была проведена по применению высокополигенной аддитивной модели к распространенным заболеваниям, предлагая некоторые проверяемые прогнозы (Yang et al., 2010, 2011a; Vinkhuyzen et al., 2013; Loh et al., 2015). Дополнительные полезные усилия были сосредоточены на широко распространенных эпистатических взаимодействиях (Hodge, 1981; Neuman and Rice, 1992; Majewski et al., 2001; Zuk et al., 2012). Однако конкурирующие теоретические модели генетики общих болезней немногочисленны, хотя и история, и разум говорят в пользу более активного теоретического сообщества и усиления взаимодействия между теорией, экспериментом и статистическими методами.
Что представляет собой полезную теорию генетики болезней?
Хотя многие области исследований справедливо подпадают под эту рубрику, основное внимание следует уделять разработке тестируемых моделей, которые описывают набор наследуемых факторов и взаимодействий, вызывающих болезненные состояния.Сюда входят частоты аллелей и генотипов, количество локусов восприимчивости, количество и типы аллелей восприимчивости, пенетрантность, эпистатические взаимодействия, свойства семейной передачи и изменение эффекта с помощью переменных окружающей среды. Важно проводить различие между генетикой, которая предрасполагает человека к заболеванию, и генетическим репертуаром, лежащим в основе предрасположенности к заболеванию в популяции затронутых людей, поскольку мы не знаем, в какой степени этиология болезни каждого человека уникальна. для сложных фенотипов заболеваний.То есть, хотя на основе анализа на уровне популяции четко установлено, что сложные заболевания являются полигенными, в настоящее время у нас мало доказательств, которые однозначно говорят об уровне гетерогенности аллелей и локусов при любом сложном заболевании. Какой набор генотипов в наборе локусов достаточен для возникновения болезни у человека? Каковы различия в этих предрасполагающих к заболеванию наборах генотипов и локусов у больных людей? Совместно ли аллели разделяются с болезненными состояниями по структурам родства? Последовательные и полезные теории генетики болезней должны отвечать на эти вопросы.
Какой набор генотипов в наборе локусов достаточен для возникновения болезни у человека? Каковы различия в этих предрасполагающих к заболеванию наборах генотипов и локусов у больных людей? Совместно ли аллели разделяются с болезненными состояниями по структурам родства? Последовательные и полезные теории генетики болезней должны отвечать на эти вопросы.
Теоретическая популяционная генетика, в которой многочисленные практики используют теорию объединения и аналогичные инструменты для изучения поддержания аллелей в популяциях и выяснения эволюционных сил, ответственных за генетические вариации, является относительно продвинутой (Kaplan et al., 1988; Hudson, 1991; Charlesworth et al. ., 1997; Calafell et al., 2001). Поскольку популяционная генетика занимается динамикой и распределением аллелей в популяциях (Ewens, 1972; Moran, 1975; Watterson, 1975; Kingman, 1982a, b; Charlesworth and Jain, 2014; Greenbaum, 2015), актуальность теории популяционной генетики к картированию генов заболевания — особенно для исследований ассоциации случай-контроль, мелкомасштабного картирования и стратификации населения — несомненно, с несколькими важными достижениями, демонстрирующими применимость (Pritchard et al. , 2000; Моррис и др., 2002; Молитор и др., 2003; Burkett et al., 2014). Однако теория популяционной генетики сама по себе недостаточна для того, чтобы служить полной теорией для моделирования генетики болезни: (1) объединенная теория в значительной степени связана с выборками случайных хромосом из популяции, а не от людей, пораженных болезнью; (2) обращению с родственными лицами уделяется ограниченное внимание; (3) в то время как популяционная генетика направлена на определение относительного воздействия естественного отбора, генетического дрейфа, мутаций и демографических эффектов, болезни имеют сложную, загадочную связь с приспособленностью — некоторые заболевания могут быть результатом баланса мутации и отбора, другие болезни могут нести гены восприимчивости. которые нейтральны по отношению к отбору, в то время как гены некоторых болезней могут подвергаться направленному отбору, а многие заболевания, такие как диабет 2 типа (Hu, 2011), могут возникать в результате перехода к современной среде; (4) теоретическая популяционная генетика концентрируется на динамике отдельных локусов в отдельности; и (5) соматические мутации и наследственные эпигенетические факторы, которые играют важную роль, по крайней мере, в некоторых распространенных заболеваниях, часто не являются предметом основной теории популяционной генетики.
, 2000; Моррис и др., 2002; Молитор и др., 2003; Burkett et al., 2014). Однако теория популяционной генетики сама по себе недостаточна для того, чтобы служить полной теорией для моделирования генетики болезни: (1) объединенная теория в значительной степени связана с выборками случайных хромосом из популяции, а не от людей, пораженных болезнью; (2) обращению с родственными лицами уделяется ограниченное внимание; (3) в то время как популяционная генетика направлена на определение относительного воздействия естественного отбора, генетического дрейфа, мутаций и демографических эффектов, болезни имеют сложную, загадочную связь с приспособленностью — некоторые заболевания могут быть результатом баланса мутации и отбора, другие болезни могут нести гены восприимчивости. которые нейтральны по отношению к отбору, в то время как гены некоторых болезней могут подвергаться направленному отбору, а многие заболевания, такие как диабет 2 типа (Hu, 2011), могут возникать в результате перехода к современной среде; (4) теоретическая популяционная генетика концентрируется на динамике отдельных локусов в отдельности; и (5) соматические мутации и наследственные эпигенетические факторы, которые играют важную роль, по крайней мере, в некоторых распространенных заболеваниях, часто не являются предметом основной теории популяционной генетики.
Точно так же теоретические модели из количественной генетики также проблематичны в их прямом применении к исследованиям архитектуры генетики болезней. Эти модели почти исключительно являются прямыми производными модели бесконечно полигенных, миниатюрных аддитивных эффектов (модель IPMAE) (Falconer and MacKay, 1996; Frank, 2011). Часто, когда применяется к дихотомическому исходу, на модель IPMAE накладывается пороговая величина (Райт, 1934) или функция ответственности (Falconer, 1965; Curnow and Smith, 1972).Исторически сложилось так, что работа над моделью IPMAE была разработана для изучения количественных признаков, таких как тощая масса домашнего скота и урожайность сельскохозяйственных животных, и специально разработанные родословные для оценки таких показателей, как племенная ценность (Falconer and MacKay, 1996; Lynch и Уолш, 1998). Хотя эта модель полезна для анализа количественных признаков в популяциях в целом, а ее применение к человеческим болезням сильно аргументировано некоторыми (Hill et al. , 2008; Plomin et al., 2009), действительно ли соединение функции ответственности с моделью IPMAE является подходящей моделью аллельной архитектуры для любого дихотомического сложного заболевания, в настоящее время неизвестно. Многие, если не большинство физиологии болезней фундаментально отличаются от естественных фенотипических вариаций, исследованных количественными генетиками, и разумно предположить, что их основная аллельная архитектура также отличается. В последнее время некоторые решительно выступили против продолжения использования модели IPMAE с целью вскрытия сложных заболеваний (Nelson et al., 2013; Женин и Клерже-Дарпу, 2015). Хотя я лично предпочитаю модели, отличные от модели IPMAE для сложных заболеваний, я не думаю, что ни теоретических, ни эмпирических данных в настоящее время достаточно, чтобы полностью отвергнуть модель IPMAE. Конечно, возможно, a priori , что десятки или сотни тысяч локусов в геноме несут аллели очень малых размеров эффекта, и все они незначительно способствуют аддитивному увеличению риска заболевания.
, 2008; Plomin et al., 2009), действительно ли соединение функции ответственности с моделью IPMAE является подходящей моделью аллельной архитектуры для любого дихотомического сложного заболевания, в настоящее время неизвестно. Многие, если не большинство физиологии болезней фундаментально отличаются от естественных фенотипических вариаций, исследованных количественными генетиками, и разумно предположить, что их основная аллельная архитектура также отличается. В последнее время некоторые решительно выступили против продолжения использования модели IPMAE с целью вскрытия сложных заболеваний (Nelson et al., 2013; Женин и Клерже-Дарпу, 2015). Хотя я лично предпочитаю модели, отличные от модели IPMAE для сложных заболеваний, я не думаю, что ни теоретических, ни эмпирических данных в настоящее время достаточно, чтобы полностью отвергнуть модель IPMAE. Конечно, возможно, a priori , что десятки или сотни тысяч локусов в геноме несут аллели очень малых размеров эффекта, и все они незначительно способствуют аддитивному увеличению риска заболевания. Более того, многие типы моделей могут иметь аддитивные и почти независимые эффекты, поскольку размеры этих эффектов становятся небольшими.Если сложные заболевания представляют собой совокупность различных физиологических образований с их собственной генетической этиологией, ошибочно объединенные врачами, представляется возможным, что модель IPMAE может быть разумной, по крайней мере, для интерпретации данных популяционных исследований. Если молекулярные сети сильно избыточны и необходимы многочисленные патогенные изменения, чтобы поставить под угрозу функцию этих сетей, то модель IPMAE может быть подходящей. Таким образом, вместо того, чтобы полностью отказываться от модели IPMAE, разумным направлением было бы поощрение разработки альтернативных теоретических моделей.Конкурентный рынок моделей генетики болезней является критически важным звеном в разгадывании генетической архитектуры всех болезней. Конечно, соответствие между предсказаниями IPMAE и экспериментальными данными будет решающим арбитром.
Более того, многие типы моделей могут иметь аддитивные и почти независимые эффекты, поскольку размеры этих эффектов становятся небольшими.Если сложные заболевания представляют собой совокупность различных физиологических образований с их собственной генетической этиологией, ошибочно объединенные врачами, представляется возможным, что модель IPMAE может быть разумной, по крайней мере, для интерпретации данных популяционных исследований. Если молекулярные сети сильно избыточны и необходимы многочисленные патогенные изменения, чтобы поставить под угрозу функцию этих сетей, то модель IPMAE может быть подходящей. Таким образом, вместо того, чтобы полностью отказываться от модели IPMAE, разумным направлением было бы поощрение разработки альтернативных теоретических моделей.Конкурентный рынок моделей генетики болезней является критически важным звеном в разгадывании генетической архитектуры всех болезней. Конечно, соответствие между предсказаниями IPMAE и экспериментальными данными будет решающим арбитром. Эмпирически жюри смешано с некоторыми исследованиями, предлагающими умеренные доказательства согласованности между данными генетической ассоциации и моделью IPMAE (Yang et al., 2010, 2011a; Vinkhuyzen et al., 2013; Bulik-Sullivan et al., 2015; Loh et al., 2015; Loh et al. al., 2015), а другие — нет (Ritchie et al., 2001; Кирино и др., 2013; Ридж и др., 2013; Fritsche et al., 2014), а семейные данные еще не окончательно подтверждают или опровергают эту модель. Следует отметить, что полезная глобальная мера степени полигенного наследования обсуждалась Yang et al. (2011b). Интересно отметить, что при тестировании моделей полигенетической архитектуры на данных GWAS для четырех сложных заболеваний — ревматоидного артрита, целиакии, инфаркта миокарда / ишемической болезни сердца и диабета 2 типа — с использованием приближенного вычисления Байеса, Шталь и его коллеги оценили общую плотность числа независимых заболеваний. -предрасполагающие SNP и объяснение дисперсии шкалы ответственности, демонстрирующее согласованность с моделями, использующими примерно 2000 SNP (Stahl et al.
Эмпирически жюри смешано с некоторыми исследованиями, предлагающими умеренные доказательства согласованности между данными генетической ассоциации и моделью IPMAE (Yang et al., 2010, 2011a; Vinkhuyzen et al., 2013; Bulik-Sullivan et al., 2015; Loh et al., 2015; Loh et al. al., 2015), а другие — нет (Ritchie et al., 2001; Кирино и др., 2013; Ридж и др., 2013; Fritsche et al., 2014), а семейные данные еще не окончательно подтверждают или опровергают эту модель. Следует отметить, что полезная глобальная мера степени полигенного наследования обсуждалась Yang et al. (2011b). Интересно отметить, что при тестировании моделей полигенетической архитектуры на данных GWAS для четырех сложных заболеваний — ревматоидного артрита, целиакии, инфаркта миокарда / ишемической болезни сердца и диабета 2 типа — с использованием приближенного вычисления Байеса, Шталь и его коллеги оценили общую плотность числа независимых заболеваний. -предрасполагающие SNP и объяснение дисперсии шкалы ответственности, демонстрирующее согласованность с моделями, использующими примерно 2000 SNP (Stahl et al. , 2012).
, 2012).
В генетике человека большинство моделей общей генетической архитектуры заболеваний, используемых на практике, делятся на два чрезмерно упрощенных лагеря: (1) моногенные и двухлокусные модели с двуаллельными маркерами и, как правило, с одним из четырех классических способов наследования (полностью доминантным). , полностью рецессивный, аддитивный или мультипликативный) и (2) прямые производные модели IPMAE. Достаточно зайти так далеко, чтобы взглянуть на широко используемые калькуляторы мощности для исследований генетической ассоциации или сцепления, чтобы увидеть это довольно повсеместное, давнее, но довольно бессильное положение вещей.Исследования параметрической связи с использованием моногенных моделей дали ложные результаты для сложных заболеваний (Génin and Clerget-Darpoux, 2015). Во многом их использование объясняется удобством — как модели моногенных / двух локусов, так и модель IPMAE математически поддаются обработке, а другие, более реалистичные модели могут потребовать сложной математической обработки или вычислительных подходов. Мало того, что эти два класса моделей представляют собой концы широкого спектра моделей, но и это ограниченное количество моделей генетики болезней является симптомом анемичных теоретических усилий.Тем не менее, то, что мы узнали о свойствах и динамике IPMAE (Blangero et al., 2013; Zhou et al., 2013) и моногенных / двухлокусных моделей (Li and Reich, 2000; Zaykin et al., 2006) ; Schrodi et al., 2007; Zaykin and Shibata, 2008) хорошо послужат нам для разработки следующего поколения теоретических моделей генетики болезней. Например, конечная аддитивная полигенная модель расслабляется из предположения IPMAE о чрезвычайно большом количестве локусов болезни (Cannings et al., 1978; Lange, 1997).Кроме того, начинают разрабатываться новые статистические подходы, явно использующие теоретические модели полигенного наследования для лучшего понимания генетической изменчивости сложных признаков (Zhou et al., 2013). На мой взгляд, заслуживают внимания модели конечных редких аллелей с умеренно высокими величинами эффекта, высокой аллельностью и высокой гетерогенностью локусов с модификацией эффекта генетическим фоном.
Мало того, что эти два класса моделей представляют собой концы широкого спектра моделей, но и это ограниченное количество моделей генетики болезней является симптомом анемичных теоретических усилий.Тем не менее, то, что мы узнали о свойствах и динамике IPMAE (Blangero et al., 2013; Zhou et al., 2013) и моногенных / двухлокусных моделей (Li and Reich, 2000; Zaykin et al., 2006) ; Schrodi et al., 2007; Zaykin and Shibata, 2008) хорошо послужат нам для разработки следующего поколения теоретических моделей генетики болезней. Например, конечная аддитивная полигенная модель расслабляется из предположения IPMAE о чрезвычайно большом количестве локусов болезни (Cannings et al., 1978; Lange, 1997).Кроме того, начинают разрабатываться новые статистические подходы, явно использующие теоретические модели полигенного наследования для лучшего понимания генетической изменчивости сложных признаков (Zhou et al., 2013). На мой взгляд, заслуживают внимания модели конечных редких аллелей с умеренно высокими величинами эффекта, высокой аллельностью и высокой гетерогенностью локусов с модификацией эффекта генетическим фоном. Важно отметить, что совсем недавние результаты моделирования, по-видимому, отдают предпочтение неполным моделям рецессивности для сложных этиологий признаков, демонстрируя согласованность как с реалистичными генетическими моделями популяций, так и с данными о наследственности и результатами GWAS (Sanjak et al., 2016). Такая работа предполагает определение приоритетности тестов рецессивных типов наследования и комплексного тестирования гетерозиготности для общего картирования болезней.
Важно отметить, что совсем недавние результаты моделирования, по-видимому, отдают предпочтение неполным моделям рецессивности для сложных этиологий признаков, демонстрируя согласованность как с реалистичными генетическими моделями популяций, так и с данными о наследственности и результатами GWAS (Sanjak et al., 2016). Такая работа предполагает определение приоритетности тестов рецессивных типов наследования и комплексного тестирования гетерозиготности для общего картирования болезней.
Хотя бесспорно, что существенные биологические открытия и клиническая полезность стали результатом выявления аллелей, действительно связанных / связанных со сложными заболеваниями (Sabbagh and Darlu, 2006; Roychowdhury and Chinnaiyan, 2013; Bottini and Peterson, 2014; Kavanaugh et al., 2014; Everett et al., 2015; Lueck et al., 2015), в настоящее время мы находимся в зачаточном состоянии понимания генетики болезни, когда прогнозирование какого-либо общего, сложного заболевания еще не является клинически осуществимым (Schrodi et al. , 2014), а эффективных, узконаправленных методов лечения мало. Одним из ярких моментов для прогнозирования заболеваний, заимствованным из количественной генетики и работы над высокополигенными аддитивными моделями, является использование наилучшего линейного несмещенного прогнозирования (BLUP) (Speed and Balding, 2014; Vilhjalmsson et al., 2015). Тем не менее, полное отсутствие реалистичных теоретических моделей резко препятствует нашему прогрессу, так как мощные экспериментальные конструкции и методы анализа могут быть оптимизированы для соответствия предсказаниям таких моделей.Тем не менее, инструменты доступны для значительного теоретического продвижения. Подходы к обработке данных (Fan et al., 2014) и машинное обучение стали частью разработки генетических моделей и их оценки (Libbrecht and Noble, 2015). Программное обеспечение для графического моделирования хорошо разработано (Hall et al., 2009). Кроме того, исследование и использование причинных моделей может также способствовать развитию теории генетики человека (Pearl, 2000; Madsen et al.
, 2014), а эффективных, узконаправленных методов лечения мало. Одним из ярких моментов для прогнозирования заболеваний, заимствованным из количественной генетики и работы над высокополигенными аддитивными моделями, является использование наилучшего линейного несмещенного прогнозирования (BLUP) (Speed and Balding, 2014; Vilhjalmsson et al., 2015). Тем не менее, полное отсутствие реалистичных теоретических моделей резко препятствует нашему прогрессу, так как мощные экспериментальные конструкции и методы анализа могут быть оптимизированы для соответствия предсказаниям таких моделей.Тем не менее, инструменты доступны для значительного теоретического продвижения. Подходы к обработке данных (Fan et al., 2014) и машинное обучение стали частью разработки генетических моделей и их оценки (Libbrecht and Noble, 2015). Программное обеспечение для графического моделирования хорошо разработано (Hall et al., 2009). Кроме того, исследование и использование причинных моделей может также способствовать развитию теории генетики человека (Pearl, 2000; Madsen et al. , 2011a, b). Доступны быстрые алгоритмы цепи Маркова-Монте-Карло для проверки сложных, обширных пространств параметров.И, что наиболее важно, накопленные результаты исследований мультиплексного сцепления, исследований затронутых пар братьев и сестер, исследований, оценивающих соответствие заболевания между относительными парами разной степени родства, исследований близнецов, исследований передачи / неравновесия в семье, GWAS, а также исследований семейного и популяционного секвенирования. доступны. Более того, высокопроизводительное генотипирование и секвенирование нарисовали подробную картину сырья, из которого берутся образцы генетики болезни: частотный спектр аллелей и паттерны LD.Модели генетики болезней должны соответствовать этим результатам. В идеале будет разработан обширный ассортимент жизнеспособных теоретических моделей генетики болезней, генерирующих информативные, отличительные прогнозы. Эти прогнозы затем могут быть проверены на основе накопленных шаблонов генетических данных, что дает апостериорные вероятности или правдоподобия для каждой модели.
, 2011a, b). Доступны быстрые алгоритмы цепи Маркова-Монте-Карло для проверки сложных, обширных пространств параметров.И, что наиболее важно, накопленные результаты исследований мультиплексного сцепления, исследований затронутых пар братьев и сестер, исследований, оценивающих соответствие заболевания между относительными парами разной степени родства, исследований близнецов, исследований передачи / неравновесия в семье, GWAS, а также исследований семейного и популяционного секвенирования. доступны. Более того, высокопроизводительное генотипирование и секвенирование нарисовали подробную картину сырья, из которого берутся образцы генетики болезни: частотный спектр аллелей и паттерны LD.Модели генетики болезней должны соответствовать этим результатам. В идеале будет разработан обширный ассортимент жизнеспособных теоретических моделей генетики болезней, генерирующих информативные, отличительные прогнозы. Эти прогнозы затем могут быть проверены на основе накопленных шаблонов генетических данных, что дает апостериорные вероятности или правдоподобия для каждой модели. По мере накопления эмпирических данных апостериорная плотность вероятности в пространстве параметров моделей будет указывать на те модели с достаточно высокими апостериорными вероятностями, при этом многие модели будут исключены.Такая работа не только осветит правдоподобные этиологические модели сложных заболеваний, но и предложит мощные экспериментальные конструкции и статистические методы. В частности, с определением вероятных моделей генетики заболевания можно использовать различные предсказанные закономерности для улучшения обнаружения и оценки случайных локусов.
По мере накопления эмпирических данных апостериорная плотность вероятности в пространстве параметров моделей будет указывать на те модели с достаточно высокими апостериорными вероятностями, при этом многие модели будут исключены.Такая работа не только осветит правдоподобные этиологические модели сложных заболеваний, но и предложит мощные экспериментальные конструкции и статистические методы. В частности, с определением вероятных моделей генетики заболевания можно использовать различные предсказанные закономерности для улучшения обнаружения и оценки случайных локусов.
Более подробный пример может придать дополнительный вес и ясность этому аргументу. Рассмотрим стандартное исследование GWAS для случая общего заболевания / контроля.За заметными исключениями таких вопросов, как кластеризация субъектов с использованием методов уменьшения размеров (Price et al., 2006), большинство таких исследований разработаны и проанализированы исключительно для проверки простой гипотезы о независимости между статусом заболевания и частотой генотипов в отдельных местах.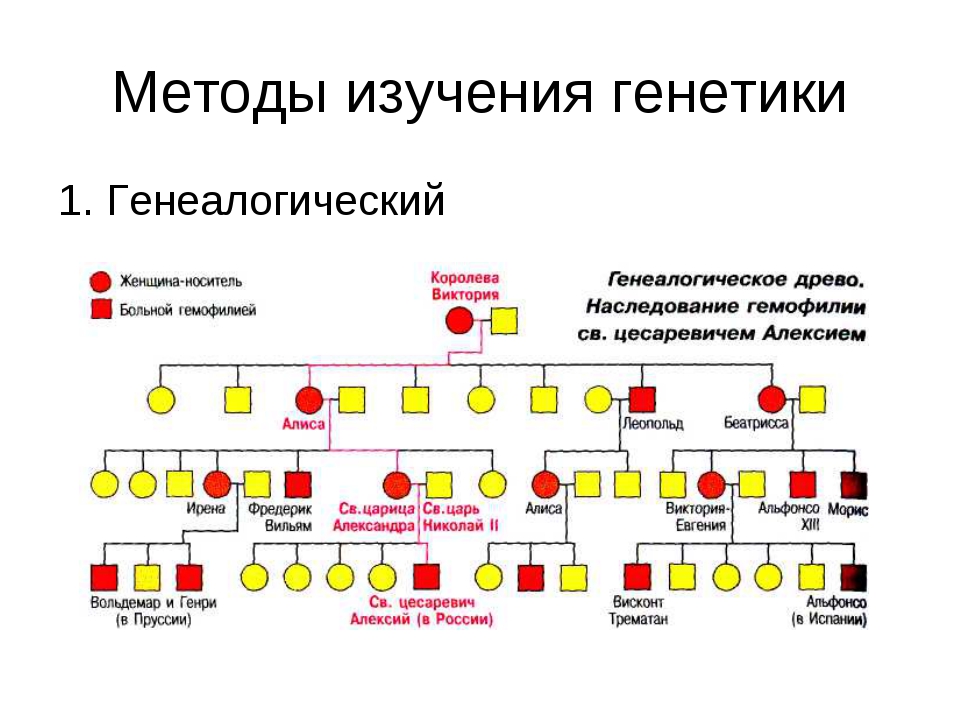 Однако формальные модели генетики болезней могут предложить множество предсказаний относительно паттернов генетической архитектуры в данных: (1) Заболевания с ранним началом и вероятными наследственными эффектами на приспособленность предсказывают отбор против предрасполагающих к заболеванию аллелей, которые будут вызывать отклонения от нейтральности, измеряемые метриками. например, Tajima (1989).(2) Отклонения от равновесия Харди-Вайнберга различаются в зависимости от случая и контроля в рамках нескольких моделей заболевания (Nielsen et al., 1999). (3) Ожидается, что паттерны неравновесия по сцеплению внутри случаев в локусе восприимчивости будут отличаться от паттернов, наблюдаемых в контроле (Zaykin et al., 2006; Schrodi et al., 2007; Pan, 2010). (4) Распад ассоциации заболевания с уменьшением неравновесия по сцеплению между причинным сайтом и тесно связанными маркерами следует определенной форме (Lai et al., 1994; Pritchard and Przeworski, 2001; Garcia et al., 2008; Schrodi et al., 2009; Maadooliat et al.
Однако формальные модели генетики болезней могут предложить множество предсказаний относительно паттернов генетической архитектуры в данных: (1) Заболевания с ранним началом и вероятными наследственными эффектами на приспособленность предсказывают отбор против предрасполагающих к заболеванию аллелей, которые будут вызывать отклонения от нейтральности, измеряемые метриками. например, Tajima (1989).(2) Отклонения от равновесия Харди-Вайнберга различаются в зависимости от случая и контроля в рамках нескольких моделей заболевания (Nielsen et al., 1999). (3) Ожидается, что паттерны неравновесия по сцеплению внутри случаев в локусе восприимчивости будут отличаться от паттернов, наблюдаемых в контроле (Zaykin et al., 2006; Schrodi et al., 2007; Pan, 2010). (4) Распад ассоциации заболевания с уменьшением неравновесия по сцеплению между причинным сайтом и тесно связанными маркерами следует определенной форме (Lai et al., 1994; Pritchard and Przeworski, 2001; Garcia et al., 2008; Schrodi et al., 2009; Maadooliat et al. , 2016). (5) Ожидается, что в случаях будет наблюдаться повышенное совместное использование хромосомных сегментов по сравнению с контрольной группой (Houwen et al., 1994; Te Meerman et al., 1995; Browning and Thompson, 2012). (6) Модели, генерирующие аллельную гетерогенность, такие как модель редкого аллеля / большого эффекта (RALE), предлагают исследовать множественные варианты предрасполагающей последовательности, сегрегационные по каждому гену / функциональному мотиву (личное общение с Рэем Уайтом, 2000-2010; Тервиллигер и Геринг, 2000; Притчард. , 2001; Thornton et al., 2013) и, возможно, тестирование на связывание. Требуется немного воображения, чтобы предположить, что в моделях генетики болезней существуют дополнительные, очень полезные предсказанные генетические паттерны, которые до сих пор используются недостаточно. Пока модель генетики болезни достаточно точна или прогнозы устойчивы по моделям, одновременное тестирование богатого набора теоретических прогнозов извлекает увеличенную информацию, позволяя более детально, достоверно и локализовать обнаружение патогенных аллелей.
, 2016). (5) Ожидается, что в случаях будет наблюдаться повышенное совместное использование хромосомных сегментов по сравнению с контрольной группой (Houwen et al., 1994; Te Meerman et al., 1995; Browning and Thompson, 2012). (6) Модели, генерирующие аллельную гетерогенность, такие как модель редкого аллеля / большого эффекта (RALE), предлагают исследовать множественные варианты предрасполагающей последовательности, сегрегационные по каждому гену / функциональному мотиву (личное общение с Рэем Уайтом, 2000-2010; Тервиллигер и Геринг, 2000; Притчард. , 2001; Thornton et al., 2013) и, возможно, тестирование на связывание. Требуется немного воображения, чтобы предположить, что в моделях генетики болезней существуют дополнительные, очень полезные предсказанные генетические паттерны, которые до сих пор используются недостаточно. Пока модель генетики болезни достаточно точна или прогнозы устойчивы по моделям, одновременное тестирование богатого набора теоретических прогнозов извлекает увеличенную информацию, позволяя более детально, достоверно и локализовать обнаружение патогенных аллелей. Примечательно, что Агарвала и его коллеги проделали отличную работу в этой области для диабета 2 типа (Agarwala et al., 2013). Они использовали комбинацию результатов моделирования и результатов исследований взаимосвязи затронутых братьев и сестер, GWAS, логистической регрессии полигенных оценок и исследований последовательности, чтобы уменьшить пространство моделей возможных архитектурных моделей. Они предполагают дальнейшее сокращение пространства возможных моделей в зависимости от результатов очень крупномасштабных исследований секвенирования. Я приветствую эти значительные усилия и надеюсь, что дальнейшая работа в этой области будет решительно поддержана.
Примечательно, что Агарвала и его коллеги проделали отличную работу в этой области для диабета 2 типа (Agarwala et al., 2013). Они использовали комбинацию результатов моделирования и результатов исследований взаимосвязи затронутых братьев и сестер, GWAS, логистической регрессии полигенных оценок и исследований последовательности, чтобы уменьшить пространство моделей возможных архитектурных моделей. Они предполагают дальнейшее сокращение пространства возможных моделей в зависимости от результатов очень крупномасштабных исследований секвенирования. Я приветствую эти значительные усилия и надеюсь, что дальнейшая работа в этой области будет решительно поддержана.
Есть аналогичные последствия для такой теоретической генетики болезней в применении к семейным исследованиям.Прогнозы, основанные на реалистичных моделях генетики болезней, позволяют согласованно исследовать такие важные вопросы, как: (1) Является ли распределение хромосомных областей, разделяемое пораженными людьми, показателем локусов болезни? (2) Соответствуют ли наблюдаемые фенотипические различия внутри семей и моделей семейной агрегации генетическим моделям конкретных болезней? (3) Соответствуют ли модели передачи внутри семьи моделям генетики болезней? И (4) с учетом генетической модели конкретного заболевания, каков оптимальный размер семейной структуры для обнаружения хромосомных регионов, связанных и ассоциированных со сложными заболеваниями (т. е., братья и сестры, мультиплексные семьи, группы основателей или группы населения в целом)? Как и в случае популяционных исследований, разработка теоретических моделей генетики болезней освещает путь к совместному тестированию множества наблюдаемых генетических паттернов в семейных структурах. Рэй и Годдард начали исследовать некоторые из этих вопросов и показали, что три модели болезней примерно согласуются с данными о риске заболеваний у родственников (Wray and Goddard, 2010).
е., братья и сестры, мультиплексные семьи, группы основателей или группы населения в целом)? Как и в случае популяционных исследований, разработка теоретических моделей генетики болезней освещает путь к совместному тестированию множества наблюдаемых генетических паттернов в семейных структурах. Рэй и Годдард начали исследовать некоторые из этих вопросов и показали, что три модели болезней примерно согласуются с данными о риске заболеваний у родственников (Wray and Goddard, 2010).
Связанные области развития теории
Одной из областей активных исследований, которые могут помочь в продвижении теории генетики болезней, является разработка методов точного картирования для выявления причинных вариантов в ассоциированном с заболеванием регионе.Выявление причинных вариантов критически важно по нескольким причинам, в первую очередь из-за того, что дорогостоящие, длительные, последующие лабораторные эксперименты основываются на том, какой ген или функциональный мотив указан в генетических доказательствах. Эта проблема идентификации болезнетворных вариантов в регионах, часто имеющих сложные паттерны неравновесия по сцеплению и аллельной гетерогенности, хотя в прошлом она сильно мало изучалась, в настоящее время все чаще признается жизненно важной в инструментарии генетики человека.Одним из примеров является метод точного картирования Маллера и его коллег, который использует ранжированный набор байесовских факторов (по одному для каждого полиморфизма в ассоциированном регионе) (Wellcome Trust Case Control Consortium et al., 2012). Другие подходы включают Bim-Bam (Servin and Stephens, 2007), CAVIAR (Hormozdiari et al., 2014), CAVIARBF (Chen et al., 2015), методы, основанные на коалесценции (Graham, 1998; Morris et al., 2002; Zollner, Pritchard, 2005) и PAINTOR (Kichaev et al., 2014), который вероятностно включает функциональную информацию.Хотя я приветствую эти прекрасные, продуманные методы, как обобщение, эти подходы являются статистически подходящими и легко интерпретируемыми, но используют чрезмерно упрощенные модели генетики болезней.
Эта проблема идентификации болезнетворных вариантов в регионах, часто имеющих сложные паттерны неравновесия по сцеплению и аллельной гетерогенности, хотя в прошлом она сильно мало изучалась, в настоящее время все чаще признается жизненно важной в инструментарии генетики человека.Одним из примеров является метод точного картирования Маллера и его коллег, который использует ранжированный набор байесовских факторов (по одному для каждого полиморфизма в ассоциированном регионе) (Wellcome Trust Case Control Consortium et al., 2012). Другие подходы включают Bim-Bam (Servin and Stephens, 2007), CAVIAR (Hormozdiari et al., 2014), CAVIARBF (Chen et al., 2015), методы, основанные на коалесценции (Graham, 1998; Morris et al., 2002; Zollner, Pritchard, 2005) и PAINTOR (Kichaev et al., 2014), который вероятностно включает функциональную информацию.Хотя я приветствую эти прекрасные, продуманные методы, как обобщение, эти подходы являются статистически подходящими и легко интерпретируемыми, но используют чрезмерно упрощенные модели генетики болезней. Если бы у нас было более полное понимание теоретических свойств аллелей, лежащих в основе сложных заболеваний, и их моделей корреляции со связанными вариантами, можно было бы включить эту информацию в более мощные методы точного картирования.
Если бы у нас было более полное понимание теоретических свойств аллелей, лежащих в основе сложных заболеваний, и их моделей корреляции со связанными вариантами, можно было бы включить эту информацию в более мощные методы точного картирования.
Помимо необходимости разработки и анализа основанных на ДНК моделей предрасположенности к болезням, аналогичные модели других наследственных факторов, участвующих в патогенезе, таких как унаследованные пулы РНК, ацетилирование гистонов и эффекты метилирования ДНК, имеют важное значение для быстрого развития генетики заболеваний. .Становится все более очевидным, что эпигенетические факторы играют роль в наследственных заболеваниях (Uddin et al., 2010; Williams et al., 2010; Allum et al., 2015; Montano et al., 2016). Однако столь же очевидным является почти полное отсутствие теоретических моделей, описывающих эпигенетику как этиологический фактор болезней. Необходимо исследовать несколько простых вопросов: каковы вероятностные законы, управляющие передачей этих эпигенетических факторов? То есть каково распределение вероятностей того, что данное эпигенетическое состояние передается следующему поколению? Как эти вероятности уменьшаются в разных поколениях? Какова частота различных эпигенетических изменений и соответствующее влияние на риск заболевания? Какова доля индивидуального риска заболевания, вызванная эпигенетическими изменениями? И как эта доля распределяется по населению? Разработка этих теоретических моделей позволит рассчитывать проверяемые прогнозы и поможет в построении более эффективных экспериментальных схем.
Заключение
Чтобы быть сбалансированным, безусловно, существуют усилия в теории генетики человека, некоторые из которых обсуждались, позволяющие использовать статистические методы, использующие информативные теоретические прогнозы (Reich and Lander, 2001; Zhu et al., 2015). Суть аргумента, приведенного здесь, заключается в степени: дополнительное обучение генетиков-людей теоретическим моделям, дополняющим и мотивирующим статистические методы, было бы полезным. Жизненно необходимо дополнительное построение генетических моделей болезней для оценки их на основе эмпирических данных.Необходима дополнительная работа по выявлению закономерностей генетических данных, ожидаемых в рамках теоретических моделей. Дополнительная оценка эмпирических данных по большим мультиплексным семьям, затронутым парам братьев и сестер, изолированным популяциям, популяциям основателей, тестам на передачу, GWAS, исследованиям секвенирования всего генома / экзома в семьях и исследованиям популяционного секвенирования, чтобы определить, какие модели заболеваний поддерживаются и которые могут быть исключены на основании этих результатов, были бы очень продуктивными. Крайне важно дополнительное взаимодействие между теорией, экспериментом и анализом.Мой центральный тезис заключается в том, что финансирование и усилия должны быть сбалансированы таким образом, чтобы создать взаимодополняющую триаду теории, эксперимента и статистики, чтобы вся область генетики человека не ослабевала. В настоящее время экспериментальные исследования и статистические методы явно являются активными и хорошо функционирующими областями, в то время как в этой области не хватает теоретических моделей генетики болезней, что затрудняет работу по картированию генов болезней в целом. Время идеально подходит для введения этих изменений.Мы собрали огромное количество генетических данных для многих сотен распространенных заболеваний и более редких, родственных состояний, но наследственные причины каждого распространенного заболевания остаются малоизученными. Колоссальные и дорогостоящие смещения фокуса исторически были вызваны упрощенными, неразвитыми теоретическими моделями, например гипотезой общего заболевания / общего варианта (Reich and Lander, 2001), поэтому для нашей области может быть более плодотворным дальнейшее развитие ресурсов и возможностей, которые генерируют более полно разработаны теоретические модели генетики болезней.Возможно, пришло время для новой области теоретической генетики болезней.
Авторские взносы
Автор подтверждает, что является единственным соавтором данной работы, и одобрил ее к публикации.
Финансирование
Эта работа была поддержана щедрыми донорами Фонда клинических исследований Маршфилда, пилотного гранта от NIH-NCATS / Института клинических и трансляционных исследований Университета Висконсин-Мэдисон (UL1TR000427) и NIMH RO1MH097464. Автор несет полную ответственность за содержание и не обязательно отражает официальную точку зрения Национальных институтов здравоохранения.
Заявление о конфликте интересов
Автор заявляет, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
В основу данной рукописи положены беседы с Луисом Птачеком, Андреасом Зиглером, Мюрреем Бриллиантом, Скоттом Хеббрингом, Гарольдом Йе, Сарой Мюррей, Марком Леппертом, Нори Мацунами и Ингрид Борецки, а также комментарии рецензентов. Редакционные комментарии были особенно проницательными и сыграли важную роль в значительном улучшении рукописи.Я хотел бы особенно поблагодарить Тони Лонга и Рэя Уайта за то, что они поделились своими проницательными наблюдениями и очень тонкими взглядами на генетическую архитектуру признаков на протяжении многих лет. Эта работа была поддержана щедрыми донорами Фонда клинических исследований Маршфилда, пилотного гранта от NIH-NCATS / Института клинических и трансляционных исследований Университета Висконсин-Мэдисон (UL1TR000427) и NIMH RO1MH097464. Автор несет полную ответственность за содержание и не обязательно отражает официальную точку зрения Национальных институтов здравоохранения.
Список литературы
Агарвала, В., Фланник, Дж., Сюняев, С., и Консорциум GoT2D, Альтшулер, Д. (2013). Оценка эмпирических границ генетической архитектуры сложных заболеваний. Нат. Genet. 45, 1418–1427. DOI: 10,1038 / нг.2804
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эллисон А.С. (1954). Распространение серповидно-клеточного признака в Восточной Африке и в других местах и его очевидная связь с заболеваемостью субтертовой малярией. Пер. R. Soc. Троп. Med. Hyg. 48, 312–318. DOI: 10.1016 / 0035-9203 (54)
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Allum, F., Shao, X., Guenard, F., Simon, M. M., Busche, S., Caron, M., et al. (2015). Характеристика функциональных метиломов с помощью секвенирования захвата следующего поколения позволяет идентифицировать новые варианты, связанные с заболеванием. Нат. Commun. 6, 7211. DOI: 10.1038 / ncomms9016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Балик, Д.Дж., До, Р., Касса, К. А., Райх, Д., Сюняев, С. Р. (2015). Преобладание вредоносного контролирует реакцию на узкое место среди населения. PLoS Genet. 11: e1005436. DOI: 10.1371 / journal.pgen.1005436
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бланжеро, Дж., Диего, В. П., Дайер, Т. Д., Алмейда, М., Перальта, Дж., Кент, Дж. У. мл., И др. (2013). Ядро истины: статистические достижения в моделях компонентов полигенной дисперсии для сложных родословных людей. Adv. Genet. 81, 1–31. DOI: 10.1016 / B978-0-12-407677-8.00001-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ботштейн Д., Уайт Р. Л., Сколник М. и Дэвис Р. В. (1980). Построение карты генетического сцепления у человека с использованием полиморфизмов длины рестрикционных фрагментов. Am. J. Hum. Genet. 32, 314–331.
PubMed Аннотация | Google Scholar
Боттини, Н., Петерсон, Э. Дж. (2014). Тирозинфосфатаза PTPN22: многофункциональный регулятор иммунной сигнализации, развития и болезни. Annu. Rev. Immunol. 32, 83–119. DOI: 10.1146 / аннурев-иммунол-032713-120249
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Браунинг, С. Р., Томпсон, Э. А. (2012). Выявление ассоциаций редких вариантов путем сопоставления идентичности по происхождению в исследованиях случай-контроль. Генетика 190, 1521–1531. DOI: 10.1534 / genetics.111.136937
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Булик-Салливан, Б.К., Ло, П.Р., Финукейн, Х.К., Рипке, С., Ян, Дж. Рабочая группа по шизофрении Консорциума психиатрической геномики и др. (2015). Регрессия LD Score отличает искажение от полигенности в полногеномных ассоциативных исследованиях. Нат. Genet. 47, 291–295. DOI: 10,1038 / нг. 3211
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Беркетт, К. М., МакНени, Б., Грэм, Дж., И Гринвуд, К. М. Т. (2014). Использование генеалогии для выявления редких вариантов, связанных со сложными признаками. Хум. Hered. 78, 117–130. DOI: 10.1159 / 000363443
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Калафель, Ф., Григоренко, Э. Л., Чиканян, А. А., Кидд, К. К. (2001). Эволюция гаплотипа и неравновесие сцепления: исследование с помощью моделирования. Хум. Hered. 51, 85–96. DOI: 10.1159 / 000022963
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Каннингс, К., Томпсон, Э. А., и Сколник, М. Х. (1978). Вероятностные функции на сложных родословных. Adv. Прил. Вероятно. 10, 26–61. DOI: 10.2307 / 1426718
CrossRef Полный текст | Google Scholar
Чарльзуорт, Б., и Джейн, К. (2014). Очищающий отбор, дрейф и обратимая мутация с произвольно высокой частотой мутаций. Генетика 198, 1587–1602. DOI: 10.1534 / genetics.114.167973
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чарльзуорт, Б., Нордборг, М., и Чарльзуорт, Д. (1997). Влияние местного отбора, сбалансированного полиморфизма и фонового отбора на равновесные модели генетического разнообразия в подразделяющейся популяции. Genet. Res. 70, 155–174. DOI: 10.1017 / S0016672397002954
CrossRef Полный текст | Google Scholar
Чен В., Ларраби Б. Р., Овсянникова И. Г., Кеннеди Р. Б., Хараламбьева И. Х., Польша, Г. А. и др. (2015). Точное картирование причинных вариантов с помощью приближенного байесовского метода с использованием предельной тестовой статистики. Генетика 200, 719–736. DOI: 10.1534 / genetics.115.176107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Курноу, Р.Н. и Смит К. (1972). Многофакторные модели семейных болезней человека. J. R. Stat. Soc. Сер. А 138, 131–169. DOI: 10.2307 / 2984646
CrossRef Полный текст | Google Scholar
Эйнштейн, А. (1916). Die grundlage der allgemeinen relativitatstheorie. Ann. Phys. 49, 769–822. DOI: 10.1002 / andp.140702
CrossRef Полный текст | Google Scholar
Эверетт, Б. М., Смит, Р. Дж., И Хиатт, В. Р. (2015). Снижение ЛПНП с помощью ингибиторов PCSK9 — клиническая польза липидных препаратов. N. Engl. J. Med. 373, 1588–1591. DOI: 10.1056 / NEJMp1508120
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эйр-Уокер А. (2010). Генетическая архитектура сложного признака и ее значение для изучения пригодности и общегеномных ассоциаций. Proc. Natl. Акад. Sci. США 107 (Приложение 1), 1752–1756. DOI: 10.1073 / pnas.02107
PubMed Аннотация | CrossRef Полный текст
Фальконер, Д. С. (1965). Наследование предрасположенности к определенным заболеваниям оценивается по заболеваемости родственников. Ann. Гм. Genet. 29, 51–76. DOI: 10.1111 / j.1469-1809.1965.tb00500.x
CrossRef Полный текст | Google Scholar
Фалконер, Д. С., и Маккей, Т. Ф. С. (1996). Введение в количественную генетику, 4-е изд. . Харлоу: Лонгманс Грин.
Фишер, Р. А. (1918). Корреляция между родственниками по предположению менделевской наследственности. Пер. R. Soc. Edinb. 52, 399–433. DOI: 10.1017 / S0080456800012163
CrossRef Полный текст | Google Scholar
Фишер, Р.А. (1930). Генетическая теория естественного отбора . Оксфорд: Кларендон.
Google Scholar
Франк, С. А. (2011). «Адаптивный ландшафт Райта против фундаментальной теоремы Фишера» в . Адаптивный ландшафт в эволюционной биологии, , ред. Э. И. Свенссон и Р. Калсбек. Эту модель часто приписывают Фишеру, но эта точка зрения может быть не совсем правильной. (Оксфорд: издательство Оксфордского университета), 41–57.
Фриче, Л. Г., Фарисс, Р. Н., Стамбул, Д., Абекасис, Г. Р., Курсио, К. А., и Сваруп, А. (2014). Возрастная дегенерация желтого пятна: генетика и биология вместе. Ann. Rev. Genomics Hum. Genet. 15, 151–171. DOI: 10.1146 / annurev-genom-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гарсия В. Э., Чанг М., Брэндон Р., Ли Ю., Мацунами Н., Каллис-Даффин К. П. и др. (2008). Подробная генетическая характеристика рецептора интерлейкина-23 при псориазе. Genes Immun. 9, 546–555. DOI: 10.1038 / gene.2008.55
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гиллеспи, Дж. Х. (1993). Процессы замещения в молекулярной эволюции. I. Равномерные и кластерные замены в гаплоидной модели. Генетика 134, 971–981.
PubMed Аннотация | Google Scholar
Гиллеспи, Дж. Х. (2000). Генетический дрейф в бесконечной популяции: модель псевдостопа. Генетика 155, 909–919.
PubMed Аннотация | Google Scholar
Глэшоу, С.Л. (1961). Частичные симметрии слабых взаимодействий. Nucl. Phys. 22, 579–588. DOI: 10.1016 / 0029-5582 (61) -2
CrossRef Полный текст
Грэм, Дж. (1998). Неравновесное точное картирование редкого аллеля с помощью коалесцентных моделей генного происхождения . Анн-Арбор: Диссертационные услуги UMI.
Грин Р. Э., Краузе Дж., Бриггс А. В., Маричич Т., Стензель У., Кирчер М. и др. (2010). Предварительная последовательность генома неандертальца. Наука 328, 710–722.DOI: 10.1126 / science.1188021
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гринбаум, Г. (2015). Пересмотр времени до фиксации нейтрального мутанта в конечной популяции — подход объединенной теории. J. Theor. Биол. 380, 98–102. DOI: 10.1016 / j.jtbi.2015.05.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гронау, И., Хубиш, М. Дж., Гулко, Б., Данко, К. Г., и Зипель, А. (2011). Байесовский вывод о демографии древнего человека на основе отдельных последовательностей генома. Нат. Genet. 43, 1031–1034. DOI: 10,1038 / нг.937
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Hall, M., Frank, E., Holmes, G., Pfahringer, B., Reutemann, P., Witten, I.H., et al. (2009). Программное обеспечение интеллектуального анализа данных WEKA: обновление; Исследования SIGKDD. 11, 10–18. DOI: 10.1145 / 1656274.1656278
CrossRef Полный текст
Хиггс, П. У. (1964). Нарушенные симметрии и массы калибровочных бозонов. Phys. Rev. Lett. 13, 508–509.DOI: 10.1103 / PhysRevLett.13.508
CrossRef Полный текст | Google Scholar
Хилл, В. Г., Годдард, М. Э. и Вишер, П. М. (2008). Данные и теория указывают в основном на аддитивную генетическую изменчивость сложных признаков. PLoS Genet. 4: e1000008. DOI: 10.1371 / journal.pgen.1000008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ходж, С. Э. (1981). Некоторые эпистатические двухлокусные модели болезни. I. Относительные риски и распределение по происхождению в затронутых парах братьев и сестер. Am. J. Hum. Genet. 33, 381–395.
PubMed Аннотация | Google Scholar
Хормоздиари Ф., Костем Э., Канг Э. Ю., Пасанюк Б. и Эскин Э. (2014). Выявление причинных вариантов в локусах с множественными сигналами ассоциации. Генетика 198, 497–508. DOI: 10.1534 / genetics.114.167908
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Houwen, R.H.J., Baharloo, S., Blankenship, K., Raeymaekers, P., Juyn, J., Sandkuijl, L.A., et al. (1994). Скрининг генома путем поиска общих сегментов: картирование гена доброкачественного рецидивирующего внутрипеченочного холестаза. Нат. Genet. 8, 380–386. DOI: 10,1038 / нг1294-380
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хадсон Р. Р. (1982). Оценка генетической изменчивости с помощью эндонуклеаз рестрикции. Genetics (Нью-Йорк, Нью-Йорк: Oxford University Press) 100, 711–719.
PubMed Аннотация
Хадсон, Р. Р.(1991). «Генеалогия и процесс слияния», в Oxford Surveys in Evolutionary Biology , Vol. 7, ред. Д. Футуйма и Дж. Антоновикс (Нью-Йорк, штат Нью-Йорк: Oxford University Press), 1–44.
Хадсон Р. Р. и Каплан Н. (1985). Статистические свойства количества событий рекомбинации в истории выборки последовательностей ДНК. Генетика 111, 147–164.
PubMed Аннотация | Google Scholar
Хунд, Ф. (1926). Zur deutung einiger erscheinungen in den Molekelspektren. Zeitschrift Physik 36, 657–674. DOI: 10.1007 / BF01400155
CrossRef Полный текст | Google Scholar
Каплан, Н. Л., Дарден, Т., и Хадсон, Р. Р. (1988). Процесс слияния в моделях с отбором. Генетика 120, 819–829.
PubMed Аннотация | Google Scholar
Каплан, Н. Л., Хилл, В. Г., и Вейр, Б. С. (1995). Методы правдоподобия для локализации генов болезней в неравновесных популяциях. Am. J. Hum. Genet. 56, 18–32.
PubMed Аннотация | Google Scholar
Кавано, А., Ритчлин, К., Рахман, П., Пуиг, Л., Готтлиб, А. Б., Ли, С. и др. (2014). Устекинумаб, моноклональное антитело против IL-23/23 p40, подавляет рентгенологическое прогрессирование у пациентов с активным псориатическим артритом: результаты комплексного анализа рентгенографических данных фазы 3, многоцентрового, рандомизированного, двойного слепого, плацебо-контролируемого P SUMMIT -1 и П САММИТ-2. Ann. Реум. Дис. 73, 1000–1006. DOI: 10.1136 / annrheumdis-2013-204741
CrossRef Полный текст | Google Scholar
Кичаев Г., Янг В.-Й., Линдстрем С., Хормоздиари Ф., Эскин Э., Прайс А. Л. и др. (2014). Интеграция функциональных данных для определения приоритетности причинных вариантов в исследованиях с точным статистическим картированием. Ген PLoS 10: e1004722. DOI: 10.1371 / journal.pgen.1004722
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кирино Ю., Берциас Г., Исигацубо Ю., Мизуки Н., Тугал-Туткун И., Сеяхи Э. и др. (2013). Полногеномный ассоциативный анализ выявляет новые локусы восприимчивости к болезни Бехчета и эпистазу между HLA-B * 51 и ERAP1. Нат. Genet. 45, 202–207. DOI: 10,1038 / нг.2520
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лай, К., Лайман, Р. Ф., Лонг, А. Д., Лэнгли, К. Х., и Маккей, Т. Ф. (1994). Встречающиеся в природе вариации в количестве щетинок и полимопшимах ДНК в шероховатом локусе Drosophila melanogaster . Наука 266, 1697–1702. DOI: 10.1126 / science.79
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лох, П. Р., Бхатиа, Г., Гусев, А., Финукейн, Х. К., Булик-Салливан, Б. К., Поллак, С. Дж. И др. (2015). Противопоставление генетической архитектуры шизофрении и других сложных заболеваний с использованием быстрого дисперсионного анализа компонентов. Нат. Genet. 47, 1385–1392. DOI: 10,1038 / нг. 3431
CrossRef Полный текст | Google Scholar
Лонг, А.Д. и Лэнгли К. Х. (1999). Возможности ассоциативных исследований для выявления вклада генетических локусов-кандидатов в вариации сложных признаков. Genome Res. 9, 720–731.
PubMed Аннотация | Google Scholar
Лотка, А. Дж. (1925). Элементы физической биологии . Балтимор, Мэриленд: Уильямс и Уилкинс.
Google Scholar
Lueck, K., Busch, M., Moss, S.E., Greenwood, J., Kasper, M., Lommatzsch, A., et al. (2015). Комплемент стимулирует пигментные эпителиальные клетки сетчатки к провоспалительным изменениям. Ophthalmic Res. 54, 195–203. DOI: 10.1159 / 000439596
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Линч М. и Уолш Б. (1998). Генетика и анализ количественных признаков . Сандерленд, Массачусетс: Sinauer Associates.
Google Scholar
Линн, А. Х., Кво, К. К., Венглиш, К. М., Астон, К. Э. и Чакраварти, А. (1995). Генетическая эпидемиология ревматоидного артрита. Am. J. Hum. Genet. 57, 150–159.
PubMed Аннотация | Google Scholar
Маадоолят, М., Бансал, Н. К., Упадхья, Дж., Фарази, М., Йе, З., Ли, X. и др. (2016). Распад связи болезни с уменьшением неравновесия по сцеплению: теорема точного картирования. bioRxiv. DOI: 10.1101 / 052381
CrossRef Полный текст | Google Scholar
Мэдсен А. М., Оттман Р. и Ходж С. Э. (2011b). Причинные модели для исследования сложных генетических заболеваний: II. Что каузальные модели могут рассказать нам о пенетрантности для аддитивных, неоднородных и мультипликативных моделей с двумя локусами. Хум. Hered. 72, 63–72. DOI: 10.1159 / 000330780
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мендель, Г. (1866). «Versuche uber plflanzenhybriden», в Verhandlungen des Naturforschenden Vereines (Brunn), 3–47. IV fur das Jahr 1865, abhandlungen.
Михаэлис, Л., и Ментен, М. Л. (1913). Die kinetic der invertinwirkung. Biochem. Z. 49, 333–369.
Молитор, Дж., Майорам, П., и Томас, Д.(2003). Мелкомасштабное картирование генов болезней с множественными мутациями с помощью методов пространственной кластеризации. Am. J. Hum. Genet. 73, 1368–1384. DOI: 10.1086 / 380415
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Монтано К., Тауб М. А., Яффе А., Брим Э., Файнберг Дж. И., Трюгвадоттир Р. и др. (2016). Ассоциация различий в метилировании ДНК с шизофренией в исследовании ассоциации на уровне всего эпигенома. JAMA Psychol. 73, 506–514. DOI: 10.1001 / jamapsychiatry.2016.0144
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Моран, П. А. П. (1975). Блуждающие распределения и электрофоретический профиль. Теор. Поп. Биол. 8, 318–330. DOI: 10.1016 / 0040-5809 (75) -0
PubMed Аннотация | CrossRef Полный текст
Моррис, А. П., Уиттакер, Дж. К., и Болдинг, Д. Дж. (2002). Мелкомасштабное картирование очагов болезней с помощью моделирования генеалогий с разбитым слиянием. Am. J. Hum.Genet. 70, 686–707. DOI: 10.1086 / 339271
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Малликен Р. С. (1932). Электронные структуры многоатомных молекул и валентность. II. Общие Соображения. Phys. Rev. 41, 49–71. DOI: 10.1103 / PhysRev.41.49
CrossRef Полный текст | Google Scholar
Нельсон, Р. М., Петтерссон, М. Э., и Карлборг, О. (2013). Спустя столетие после Фишера: время для новой парадигмы в количественной генетике. Trends Genet. 29, 669–676. DOI: 10.1016 / j.tig.2013.09.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нильсен, Д. М., Эм, М. Г., и Вейр, Б. С. (1999). Выявление ассоциации маркерного заболевания путем тестирования на неравновесие Харди-Вайнберга в маркерном локусе. Am. J. Hum. Genet. 63, 1531–1540. DOI: 10.1086 / 302114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пан, W. (2010). Единая структура для обнаружения генетической ассоциации с несколькими SNP в гене-кандидате или регионе: сопоставление оценок генотипа и паттернов LD между случаями и контролями. Хум. Hered. 69, 1–13. DOI: 10.1159 / 000243149
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Перл, Дж. (2000). Причинность: модели, рассуждения и выводы . Кембридж, Великобритания: Издательство Кембриджского университета.
Google Scholar
Личное общение с Рэем Уайтом (2000-2010). Рэй Уайт был ярым сторонником моделей редких вариантов / аллельной гетерогенности, ведущих к распространенным заболеваниям с начала 1990-х годов. Он часто продвигал идею «генетики генов», чтобы подчеркнуть эту идею.
Пикеринг, Г. (1978). Нормотония и гипертония: загадочная жизнеспособность лжи. Am. J. Med. 65, 561–563. DOI: 10.1016 / 0002-9343 (78) -2
PubMed Аннотация | CrossRef Полный текст
Прайс, А. Л., Паттерсон, Н. Дж., Пленге, Р. М., Вайнблатт, М. Э., Шадик, Н. А., и Райх, Д. (2006). Анализ основных компонентов корректирует стратификацию в полногеномных ассоциативных исследованиях. Нат. Genet. 38, 904–909. DOI: 10.1038 / ng1847
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Причард, Дж.К. (2001). Ответственны ли редкие варианты за восприимчивость к сложным заболеваниям? Am. J. Hum. Genet. 69, 124–137.
PubMed Аннотация | Google Scholar
Райх, Д., Грин, Р. Э., Кирчер, М., Краузе, Дж., Паттерсон, Н., Дюран, Э. Ю. и др. (2010). Генетическая история архаической группы гомининов из Денисовой пещеры в Сибири. Природа 468, 1053–1060. DOI: 10.1038 / nature09710
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ридж, П.Г., Мукерджи, С., Крейн, П. К., Кауве, Дж. С. К., и Консорциум генетики болезни Альцгеймера (2013). Болезнь Альцгеймера: анализ недостающей наследственности. PLoS ONE 8: e79771. DOI: 10.1371 / journal.pone.0079771
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ричи, М. Д., Хан, Л. В., Руди, Н., Бейли, Л. Р., Дюпон, В. Д., Парл, Ф. Ф. и др. (2001). Уменьшение многофакторной размерности выявляет взаимодействия высокого порядка между генами метаболизма эстрогенов при спорадическом раке груди. Am. J. Hum. Genet. 69, 138–147. DOI: 10.1086 / 321276
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Саббаг, А., Дарлу, П. (2006). Методы интеллектуального анализа данных как полезные инструменты для прогнозирования индивидуальной реакции на лекарственные препараты: применение к данным CYP2D6. Хум. Hered. 62, 119–134. DOI: 10.1159 / 000096416
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Санджак, Дж. С., Лонг, А. Д., Торнтон, К. Р. (2016). Генетическая архитектура сложного признака более чувствительна к генетической модели, чем рост популяции. bioRxiv. DOI: 10.1101 / 048819
CrossRef Полный текст | Google Scholar
Санкарараман, С., Маллик, С., Паттерсон, Н., и Райх, Д. (2016). Комбинированный ландшафт денисовских и неандертальских предков у современных людей. Curr. Биол. 26, 1241–1247. DOI: 10.1016 / j.cub.2016.03.037
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шроди, С. Дж., Гарсия, В. Э. и Роуленд, К. М. (2009). «Теорема точного отображения для уточнения результатов ассоциативных генетических исследований», в ASHG Abstract .Гонолулу, штат Гавайи.
Шроди, С. Дж., Гарсия, В. Э., Роуленд, К., и Джонс, Х. Б. (2007). Неравновесие по парному сцеплению в моделях болезней. Eur. J. Hum. Genet. 15, 212–220. DOI: 10.1038 / sj.ejhg.5201731
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шроди, С. Дж., Мукерджи, С., Шан, Ю., Тромп, Г., Снински, Дж. Дж., Каллеар, А. П. и др. (2014). Прогнозирование признаков болезни на основе генетических данных: очень сложно предсказывать, особенно в отношении будущего. Фронт. Genet. 5: 162. DOI: 10.3389 / fgene.2014.00162
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сервин Б. и Стивенс М. (2007). Вмененный анализ ассоциативных исследований: регионы-кандидаты и количественные характеристики. PLoS Genet. 3: e114. DOI: 10.1371 / journal.pgen.0030114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Слаткин М., Раннала Б. (1997). Выборочное распределение аллелей, связанных с заболеванием. Генетика 147, 1855–1861.
PubMed Аннотация | Google Scholar
Шталь, Э. А., Вегманн, Д., Трынка, Г., Гутьеррес-Ачури, Дж., До, Р., Войт, Б. Ф. и др. (2012). Байесовский анализ полигенной архитектуры ревматоидного артрита. Нат. Genet. 44, 483–489. DOI: 10,1038 / нг. 2232
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Штейн, К. М., Ншути, Л., Чиунда, А. Б., Бум, В. Х., Элстон, Р. К., Мугерва, Р.D., et al. (2005). Доказательства основного влияния гена на экспрессию фактора некроза опухоли альфа при туберкулезе: анализ пути и сегрегации. Хум. Hered. 60, 109–118. DOI: 10.1159 / 000088913
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Стейнберг, А. Г., Беккер, С., Фицпатрик, Т. Б., и Кирланд, Р. Р. (1951). Генетическое и статистическое исследование псориаза. Am. J. Hum. Genet. 3, 267–281.
PubMed Аннотация | Google Scholar
Таджима, Ф.(1989). Статистический метод проверки гипотезы нейтральной мутации по полиморфизму ДНК. Генетика 123, 585–595.
PubMed Аннотация | Google Scholar
Те Меерман, Г. Дж., Ван дер Мейлен, М. А., и Сандкуейл, Л. А. (1995). Перспективы идентичности по происхождению. (IBD). картирование в популяциях основателей. Clin. Exp. Аллергия 25, 97–102. DOI: 10.1111 / j.1365-2222.1995.tb00433.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тервиллигер, Дж.Д., и Геринг, Х. Х. Х. (2000). Картирование генов в 20 -м и 21 -м веках: статистические методы, анализ данных и экспериментальный план. Хум. Биол. 72, 63–132. DOI: 10.3378 / 027.081.0615
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Томпсон, Э. А. (1978). «Связь и сила родословной структуры», в Генетическая эпидемиология , ред. Н. Э. Мортон и К. С. Чанг (Нью-Йорк, Нью-Йорк: академический), 247–253.
Google Scholar
Торнтон, К.Р., Форан А. Дж., Лонг А. Д. (2013). Свойства и моделирование GWAS, когда риск комплексного заболевания вызван некомплементарными вредными мутациями в генах с большим эффектом. PLoS Genet. 9: e1003258. DOI: 10.1371 / journal.pgen.1003258
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уддин М., Айелло А. Э., Вильдман Д. Э., Коенен К. К., Павелек Г., де лос Сантос Р. и др. (2010). Профили эпигенетической и иммунной функции, связанные с посттравматическим стрессовым расстройством. Proc. Natl. Акад. Sci. США 107, 9470–9475. DOI: 10.1073 / pnas.04107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вильхьялмссон, Б. Дж., Янг, Дж., Финукейн, Х. К., Гусев, А., Линдстрем, С., Рипке, С., и др. (2015). Моделирование неравновесия по сцеплению повышает точность оценок полигенного риска. Am. J. Hum. Genet. 97, 576–592. DOI: 10.1016 / j.ajhg.2015.09.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Винхуйзен, А.А., Рэй, Н. Р., Янг, Дж., Годдард, М. Э., и Вишер, П. М. (2013). Оценка и разделение наследственности в человеческих популяциях с использованием методов полногеномного анализа. Annu. Преподобный Жене. 47, 75–95. DOI: 10.1146 / annurev-genet-111212-133258
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вайнберг, В. (1908). Uber den nachweis der verebung beim menschen. Jahreshefte des vereins fur vaterlandische naturkunde в Вюртемберге. 64, 368–382.
Консорциум управления делами Wellcome Trust, Маллер, Дж. Б., Маквин, Г., Бирнс, Дж., Вукчевич, Д., Палин, К. и др. (2012). Байесовское уточнение ассоциативных сигналов для 14 локусов при трех распространенных заболеваниях. Нат. Genet. 44, 1294–1301. DOI: 10,1038 / нг.2435
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уильямс, С. Р., Олдред, М. А., Дер Калоустиан, В. М., Халяль, Ф., Гоуэнс, Г., МакЛеод, Д. Р. и др. (2010). Гаплонедостаточность HDAC4 вызывает синдром умственной отсталости брахидактилии с брахидактилией типа E, задержками в развитии и поведенческими проблемами. Am. J. Hum. Genet. 87, 219–228. DOI: 10.1016 / j.ajhg.2010.07.011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уилсон, А. Х. (1931). Теория электронных полупроводников. Proc. R. Soc. Лондон. А 133, 458–491. DOI: 10.1098 / rspa.1931.0162
CrossRef Полный текст | Google Scholar
Райт, С. (1932). «Роли мутации, инбридинга, скрещивания и отбора в эволюции», в Протоколах 6-го Международного конгресса генетики , Остин, Техас.Vol. 1, 356–366.
Райт, С. (1934). Анализ вариабельности числа пальцев у инбредной линии морских свинок. Генетика 19, 506–536.
PubMed Аннотация | Google Scholar
Янг, Дж., Беньямин, Б., МакЭвой, Б. П., Гордон, С., Хендерс, А. К., Найхолт, Д. Р., и др. (2010). Распространенные SNP объясняют большую часть наследуемости по росту человека. Нат. Genet. 42, 565–569. DOI: 10,1038 / нг.608
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Янг, Дж., Манолио, Т.А., Паскуале, Л.Р., Бурвинкл, Э., Капорасо, Н., Каннингем, Дж. М. и др. (2011a). Разделение генома генетической изменчивости по сложным признакам с использованием общих SNP. Нат. Genet. 43, 519–525. DOI: 10,1038 / нг. 823
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Янг, Дж., Видон, М. Н., Перселл, С., Леттр, Г., Эстрада, К., Виллер, К. Дж. И др. (2011b). Факторы геномной инфляции при полигенном наследовании. Eur. J. Hum. Genet. 19, 807–812.DOI: 10.1038 / ejhg.2011.39
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Зайкин Д. В., Шибата К. (2008). Генетический флип-флоп без сопутствующего изменения неравновесия по сцеплению. Am. J. Hum. Genet. 82, 794–796. DOI: 10.1016 / j.ajhg.2008.02.001
PubMed Аннотация | CrossRef Полный текст
Зайкин Д. В., Мэн З. и Эм М. Г. (2006). Противопоставление паттернов сцепления-неравновесия между случаями и контролем как новый метод сопоставления ассоциаций. Am. J. Hum. Genet. 78, 737–746. DOI: 10.1086 / 503710
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Zhu, Z., Baksji, A., Vinkhuysen, A. A., Hemani, G., Lee, S.H., Nolte, I.M, et al. (2015). Преобладающая генетическая изменчивость мало способствует отсутствию наследуемости сложных черт человека. Am. J. Hum. Genet. 96, 377–385. DOI: 10.1016 / j.ajhg.2015.01.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Циезун, А., Пулит, С. Л., Франсиоли, Л. К., ван Дейк, Ф., Сверц, М., Бумсма, Д. И. и др. (2013). Вредные аллели в геноме человека в среднем моложе нейтральных аллелей той же частоты. PLoS Genet. 9: e1003301. DOI: 10.1371 / journal.pgen.1003301
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Зук, О., Хечтер, Э., Сюняев, С. Р., Ландер, Э. С. (2012). Тайна отсутствия наследственности: генетические взаимодействия создают фантомную наследуемость. Proc. Natl. Акад. Sci. США 109, 1193–1198. DOI: 10.1073 / pnas.1119675109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
.
