Таблицы DPVA.ru — Инженерный Справочник |
Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Таблица Менделеева. Названия. Электронные формулы. Молярные массы. Структурные формулы. Таблицы степеней окисления и валентности. Изотопы.
Поделиться:
| ||
Вложите в письмо ссылку на страницу с ошибкой, пожалуйста. |
|||
Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса.
Free xml sitemap generator Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса.
Free xml sitemap generator
|
|||
Получайте сведения о химии и химических элементах в Excel
С помощью связанных типов данных вы можете легко добавлять химические данные и факты непосредственно в Excel. Для этого сначала преобразуйте текст в тип данныхХимия, а затем извлеките нужные факты в книгу. В этой статье представлены инструкции, как это сделать.
Преобразование в тип данных «Химия» и его использование
-
В ячейке введите название химического элемента, химического соединения, изотопа, минерала или химическую формулу. Например, можно ввести «Водород», «Вода» или «h3O». Если вы вводите несколько элементов, располагайте каждый из них в отдельной ячейке столбца.
-
Выделите эти ячейки и выберите Вставка > Таблица, чтобы создать таблицу.
 При желании добавьте заголовок столбца.
При желании добавьте заголовок столбца.Примечание: Хотя создавать таблицу необязательно, мы рекомендуем помещать текст в таблицу для оптимальной работы.
-
Выбрав таблицу, нажмите Данные, разверните раскрывающуюся коллекцию Типы данных
-
Excel преобразует текст в тип данных «Химия», соответствующий нашим онлайн-источникам. Вы узнаете, что преобразование выполнено, если в ячейках появится значок типа данных «Химия».
-
Чтобы добавить данные в таблицу, выделите одну или несколько преобразованных ячеек. После этого появится кнопка Добавить столбец . Нажмите эту кнопку и выберите любое из полей, чтобы добавить эти факты в таблицу.
-
После добавления нужных данных в книгу вы можете использовать любимые функции Excel, например формулы, чтобы ссылаться на данные и работать с ними.
Дополнительные сведения см. в статье Создание формул, которые ссылаются на типы данных.
Используйте средство выбора данных для уточнения типов данных «Химия».
Ниже приведены советы, которые помогут вам определить правильное соответствие для вашего текста. Если вам нужна помощь по использованию средства выбора данных, см. статью Указание типов данных с помощью мастера выбора данных.
-
При вводе химических формул для преобразования в тип данных «Химия» учитывается регистр. Если не возвращаются нужные вам результаты, проверьте регистр. Например, «Co» представляет «кобальт», а «CO» представляет монооксид углерода. .
-
В случае элементов из периодической таблицы может потребоваться выбрать между типом данных, который представляет химическое соединение,и типом данных, который представляет химический элемент:
-
Химические соединения представлены с помощью значка и содержат такие сведения, как структура, фазовая диаграмма, идентификаторы и т.
 д.
д. -
Химические элементы представлены с помощью значка и содержат такие сведения, как атомный размер, свойства из периодической таблицы, изотопы и т. д.
-
См. также
Связанные типы данных: вопросы, ответы и рекомендации
Какие типы связанных данных доступны в Excel?
Создание формул, которые ссылаются на типы данных
Функция ЗНАЧПОЛЯ
Ошибка #ПОЛЕ!
Помощь студентам в учёбе от Людмилы Фирмаль
Здравствуйте!
Я, Людмила Анатольевна Фирмаль, бывший преподаватель математического факультета Дальневосточного государственного физико-технического института со стажем работы более 17 лет. На данный момент занимаюсь онлайн обучением и помощью по любыми предметам. У меня своя команда грамотных, сильных бывших преподавателей ВУЗов. Мы справимся с любой поставленной перед нами работой технического и гуманитарного плана. И не важно: она по объёму на две формулы или огромная сложно структурированная на 125 страниц! Нам по силам всё, поэтому не стесняйтесь, присылайте.
На данный момент занимаюсь онлайн обучением и помощью по любыми предметам. У меня своя команда грамотных, сильных бывших преподавателей ВУЗов. Мы справимся с любой поставленной перед нами работой технического и гуманитарного плана. И не важно: она по объёму на две формулы или огромная сложно структурированная на 125 страниц! Нам по силам всё, поэтому не стесняйтесь, присылайте.
Срок выполнения разный: возможно онлайн (сразу пишите и сразу помогаю), а если у Вас что-то сложное – то от двух до пяти дней.
Для качественного оформления работы обязательно нужны методические указания и, желательно, лекции. Также я провожу онлайн-занятия и занятия в аудитории для студентов, чтобы дать им более качественные знания.
Моё видео:
Как вы работаете?
Вам нужно написать сообщение в WhatsApp . После этого я оценю Ваш заказ и укажу срок выполнения. Если условия Вас устроят, Вы оплатите, и преподаватель, который ответственен за заказ, начнёт выполнение и в согласованный срок или, возможно, раньше срока Вы получите файл заказа в личные сообщения.
После этого я оценю Ваш заказ и укажу срок выполнения. Если условия Вас устроят, Вы оплатите, и преподаватель, который ответственен за заказ, начнёт выполнение и в согласованный срок или, возможно, раньше срока Вы получите файл заказа в личные сообщения.
Стоимость заказа зависит от задания и требований Вашего учебного заведения. На цену влияют: сложность, количество заданий и срок выполнения. Поэтому для оценки стоимости заказа максимально качественно сфотографируйте или пришлите файл задания, при необходимости загружайте поясняющие фотографии лекций, файлы методичек, указывайте свой вариант.
Какой срок выполнения заказа?Минимальный срок выполнения заказа составляет 2-4 дня, но помните, срочные задания оцениваются дороже.
Как оплатить заказ?Сначала пришлите задание, я оценю, после вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
В течение 1 года с момента получения Вами заказа действует гарантия. В течении 1 года я и моя команда исправим любые ошибки в заказе.
Качественно сфотографируйте задание, или если у вас файлы, то прикрепите методички, лекции, примеры решения, и в сообщении напишите дополнительные пояснения, для того, чтобы я сразу поняла, что требуется и не уточняла у вас. Присланное качественное задание моментально изучается и оценивается.
Теперь напишите мне в Whatsapp или почту и прикрепите задания, методички и лекции с примерами решения, и укажите сроки выполнения. Я и моя команда изучим внимательно задание и сообщим цену.
Если цена Вас устроит, то я вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
Мы приступим к выполнению, соблюдая указанные сроки и требования. 80% заказов сдаются раньше срока.
80% заказов сдаются раньше срока.
После выполнения отправлю Вам заказ в чат, если у Вас будут вопросы по заказу – подробно объясню. Гарантия 1 год. В течении 1 года я и моя команда исправим любые ошибки в заказе.
Можете смело обращаться к нам, мы вас не подведем. Ошибки бывают у всех, мы готовы дорабатывать бесплатно и в сжатые сроки, а если у вас появятся вопросы, готовы на них ответить.
Ошибки бывают у всех, мы готовы дорабатывать бесплатно и в сжатые сроки, а если у вас появятся вопросы, готовы на них ответить.
В заключение хочу сказать: если Вы выберете меня для помощи на учебно-образовательном пути, у вас останутся только приятные впечатления от работы и от полученного результата!
Жду ваших заказов!
С уважением
Пользовательское соглашение
Политика конфиденциальности
Периодическая система химических элементов (таблица Менделеева)
https://ria.ru/20190129/1550014194.html
Периодическая система химических элементов (таблица Менделеева)
Периодическая система химических элементов (таблица Менделеева) — РИА Новости, 29.01.2019
Периодическая система химических элементов (таблица Менделеева)
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация. РИА Новости, 29. 01.2019
01.2019
2019-01-29T04:51
2019-01-29T04:51
2019-01-29T04:51
справки
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/99408/72/994087230_0:105:2000:1230_1920x0_80_0_0_b528d261d40438ab5524fc6ad7f580a3.jpg
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация. Является табличным представлением периодического закона, открытого Дмитрием Менделеевым. Современная формулировка этого закона звучит так: свойства элементов находятся в периодической зависимости от заряда их атомных ядер.Прообразом Периодической системы химических элементов служит таблица «Опыт системы элементов, основанной на их атомном весе и химическом сходств», составленная Менделеевым в 1869 году. По мере совершенствования этой таблицы он развил представления о периодах и группах элементов и о месте каждого элемента в системе. В 1871 году в книге «Основы химии» Менделеевым была включена «Естественная система элементов Д. Менделеева» – первая классическая короткая форма Периодической системы химических элементов. Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне. Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали «большой гонкой».Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером).
Менделеева» – первая классическая короткая форма Периодической системы химических элементов. Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне. Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали «большой гонкой».Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером).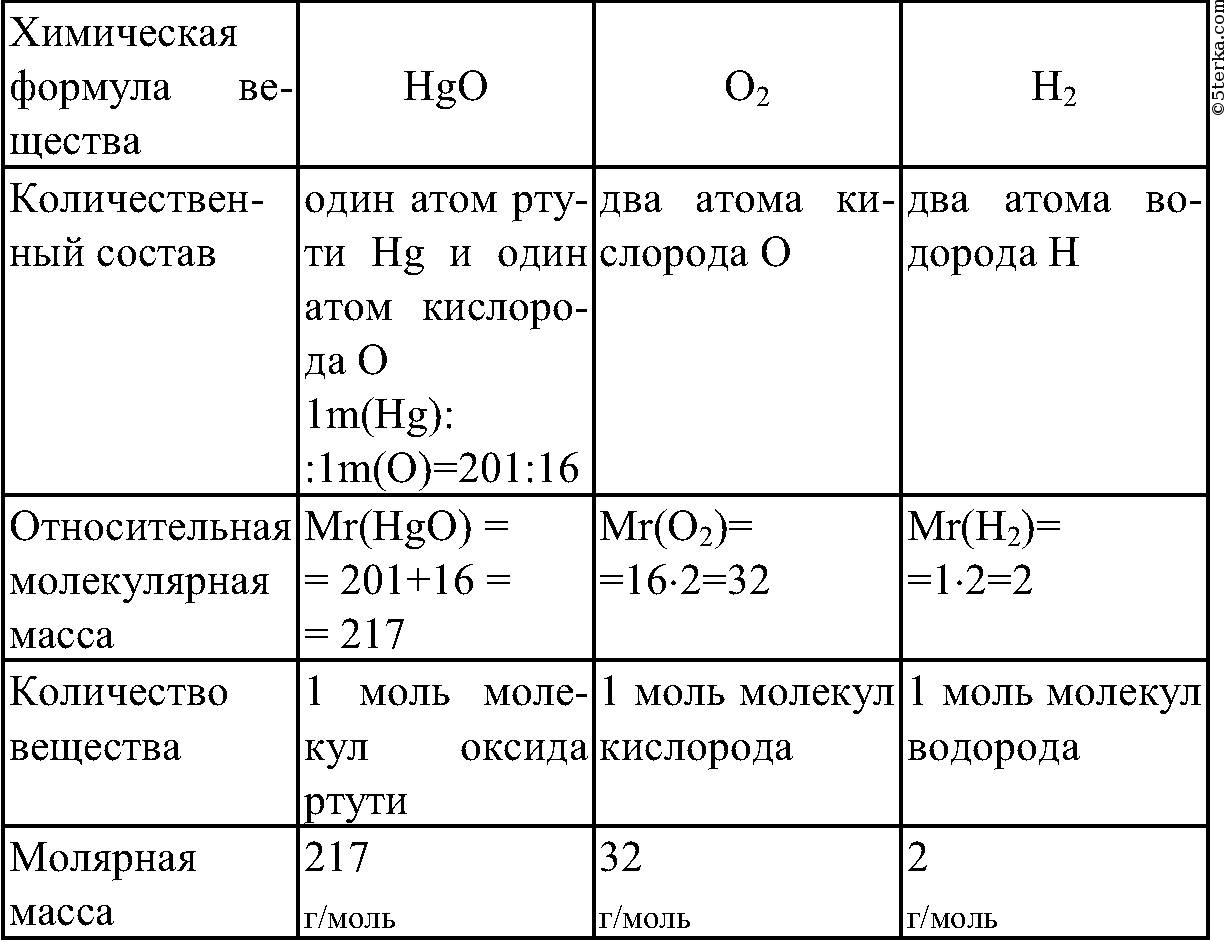 Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).
Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).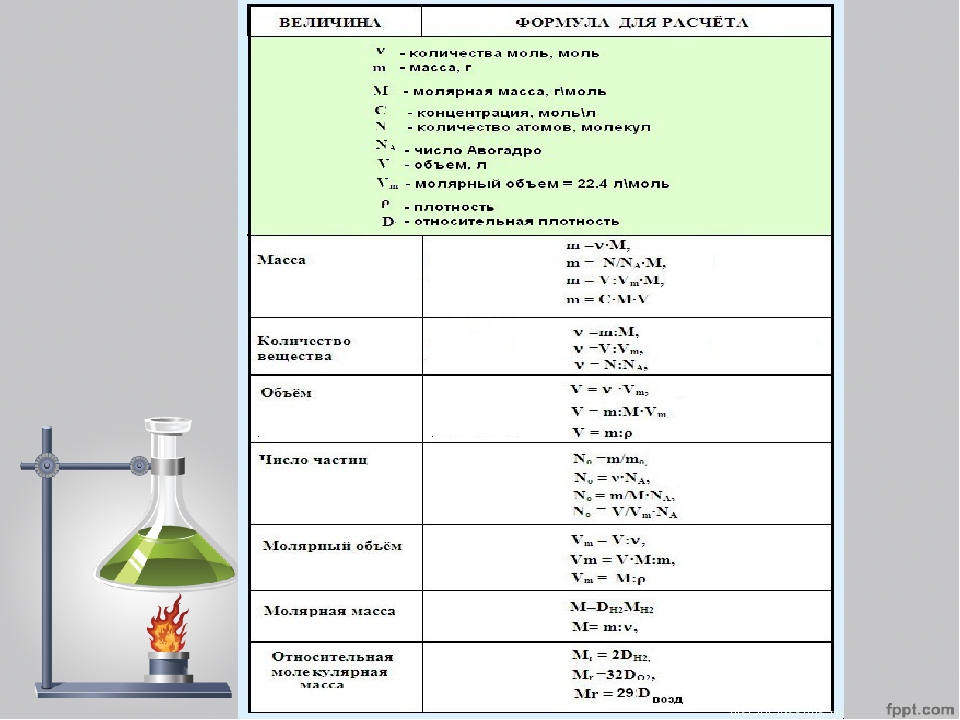 В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.Первый период содержит два элемента – водород и гелий. Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов. Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов. Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды. Лантаноиды и актиноиды помещены отдельно внизу таблицы.Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия «химический элемент» и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии.
В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.Первый период содержит два элемента – водород и гелий. Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов. Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов. Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды. Лантаноиды и актиноиды помещены отдельно внизу таблицы.Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия «химический элемент» и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии. С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
internet-group@rian. ru
ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/99408/72/994087230_112:0:1889:1333_1920x0_80_0_0_597a34ca28aa89475eedcbd63e1a68a3.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
справки
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация.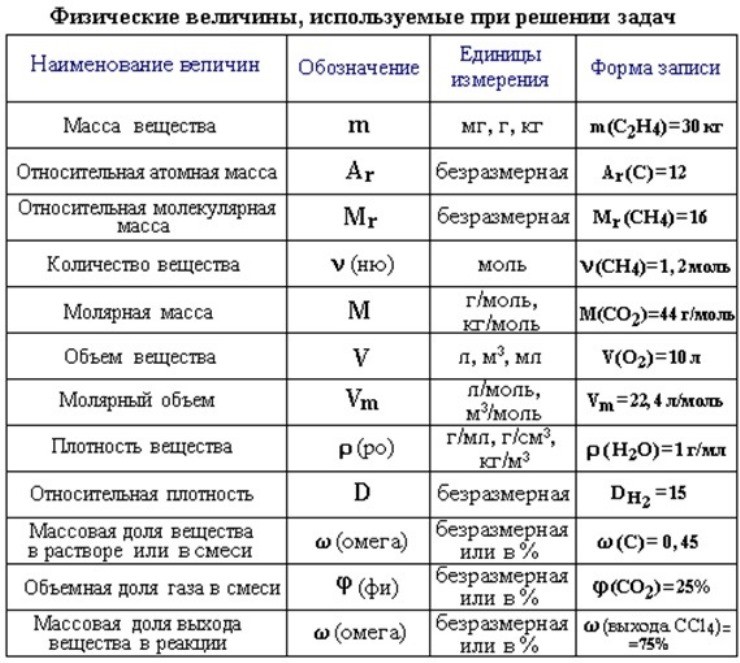
Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне.
 Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали «большой гонкой».Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером).
Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали «большой гонкой».Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером). Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.
Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).
В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.
Первый период содержит два элемента – водород и гелий.
Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов.
Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов.
Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.
Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды.
Лантаноиды и актиноиды помещены отдельно внизу таблицы.
Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия «химический элемент» и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии. С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.
Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
Химические элементы, названные в честь российских ученых и топонимов. Досье — Биографии и справки
ТАСС-ДОСЬЕ. 30 ноября Международный союз теоретической и прикладной химии (The International Union of Pure and Applied Chemistry, IUPAC) объявил об утверждении названий новооткрытых элементов периодической таблицы Менделеева.
113-й элемент получил имя нихониум (символ — Ni, в честь Японии), 115-й — московием (Mc, в честь Московской обл.), 117 — теннесином (Ts, в честь штата Теннеси) и 118-й — оганессоном (Og, в честь российского ученого Юрия Оганесяна).
Редакция ТАСС-ДОСЬЕ подготовила список других химических элементов, названных в честь российских ученых и топонимов.
Рутений
Рутений (Ruthenium, символ — Ru) — химический элемент с атомным номером 44. Представляет собой переходный металл платиновой группы серебристого цвета. Используется в электронике, химии, для создания износостойких электрических контактов, резисторах. Добывается из платиновой руды.
Был открыт в 1844 г. профессором Казанского университета Карлосом Клаусом, который решил назвать элемент в честь России (Ruthenia — один из вариантов средневекового латинского названия Руси).
Самарий
Самарий (Samarium, Sm) — химический элемент с атомным номером 62. Представляет собой редкоземельный металл из группы лантаноидов. Широко используется для изготовления магнитов, в медицине (для борьбы с раком), для изготовления аварийных регулирующих кассет в ядерных реакторах.
Был открыт в 1878-1880 гг. французским и швейцарским химиками Полем Лекоком де Буабодраном и Жаном Галиссар де Мариньяком. Они обнаружили новый элемент в найденном в Ильменских горах минерале самарските и назвали его самарием (как производное от минерала).
Однако сам минерал, в свою очередь, был назван по имени русского горного инженера, начальника штаба Корпуса горных инженеров Василия Самарского-Быховца, который передал его иностранным химикам для изучения.
Менделевий
Менделевий (Mendelevium, Md) — синтезированный химический элемент с атомным номером 101. Представляет собой высокорадиоактивный металл.
На эту тему
Наиболее из стабильных изотопов элемента имеет период полураспада 51,5 суток. Может быть получен в лабораторных условиях при бомбардировке атомов эйнштейния ионами гелия. Был открыт в 1955 г. американскими учеными из Национальной лаборатории имени Лоуренса в Беркли (США).
Несмотря на то, что в это время США и СССР находились в состоянии холодной войны, первооткрыватели элемента, среди которых был один из основателей ядерной химии, Гленн Сиборг, предложили назвать его в честь создателя периодической таблицы — русского ученого Дмитрия Менделеева. Правительство США согласилось с этим, в том же году IUPAC присвоил элементу название Менделевий.
Дубний
Дубний (Dubnium, Db) — синтезированный химический элемент с атомным номером 105, радиоактивный металл. Наиболее стабильный из изотопов имеет период полураспада около 1 часа. Получается при бомбардировке ядер амереция ионами неона. Был открыт в 1970 г. в ходе независимых экспериментов физиками Лаборатории ядерных реакций Объединенного института ядерных исследований в Дубне и лаборатории в Беркли.
После более чем 20-летнего спора о первенстве в открытии, IUPAC в 1993 г. принял решение признать оба коллектива первооткрывателями элемента и назвать его в честь Дубны (при этом в Советском Союзе предлагали назвать его нильсборием в честь датского физика — Нильса Бора).
Флеровий
Флеровий (Flerovium, Fl) — синтезированный химический элемент с атомным номером 114. Сильнорадиоактивное вещество с периодом полураспада не более 2,7 секунд. Впервые был получен группой физиков Объединенного института ядерных исследований в Дубне под руководством Юрия Оганесяна с участием ученых из Ливермоской национальной лаборатории США) путем слияния ядер кальция и плутония.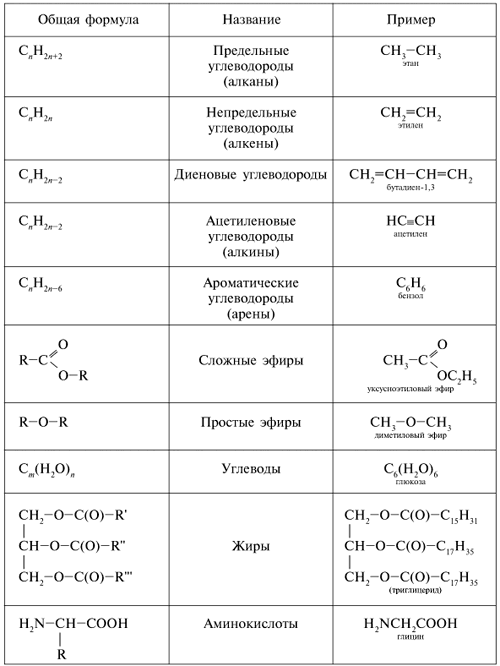
Назван по предложению российских ученых в честь одного из основателей института в Дубне, Георгия Флерова.
Московий и оганессон
8 июня комитет Международного союза теоретической и прикладной химии рекомендовал назвать 115-й элемент таблицы Менделеева московием в честь Московской области, где находится Объединенный институт ядерных исследований (город Дубна).
На эту тему
118-й элемент организация предложила называть оганессоном в честь его первооткрывателя, академика РАН Юрия Оганесяна.
Оба химических элементов являются синтезированными с периодом полураспада, не превышающим несколько долей секунд. Были открыты в Лаборатории ядерных реакций Объединенного института ядерных исследований в Дубне в ходе экспериментов в 2002-2005 гг. Предложенные IUPAC названия прошли публичное обсуждение и были утверждены им же 28 ноября 2016 г.
Также до 1997 г. в СССР и России синтезированный элемент с атомным номером 104 носил название курчатовий, в честь физика Игоря Курчатова, однако IUPAC принял решение назвать его в честь британского физика Эрнеста Резерфорда — резерфордием.
App Store: Химия и периодическая таблица
Легко решайте химические уравнения и ищите химические реакции. Вы всегда будете иметь с собой периодическую таблицу Менделеева и таблицу растворимости, прямо в телефоне!
Химия позволяет находить химические реакции и решать химические уравнения с одной или несколькими неизвестными переменными. Вы всегда будете иметь под рукой периодическую таблицу Менделеева и таблицу растворимости. И даже калькулятор молярных масс!
Приложение может найти уравнения химических реакций, даже если неизвестна правая или левая часть, это поможет вам в органической и неорганической химии.Обнаруженные реакции будут отображаться в обычном и ионном виде. Формулы органической химии рисуются приложением в виде изображений.
Удобная интерактивная таблица Менделеева. Коснитесь химического элемента в таблице, чтобы найти дополнительную информацию о нем. Используйте кнопку поиска, чтобы найти элемент по имени или символу.
Калькулятор молярных масс. Введите правильно химическое соединение, и оно покажет молярные массы и проценты элементов.
В приложение добавлена таблица растворимости веществ, а также таблица кислотности.Теперь ваши учебники станут отходами!
Лучший решатель химических уравнений для iPhone и iPad.
Добавляйте новые блестящие виджеты на рабочий стол и узнавайте информацию о химических элементах из таблицы Менделеева подсознательно. Это интересный способ узнать и запомнить данные о химических элементах.
Все эти таблицы и диаграммы доступны в бесплатном приложении Химия:
* Периодическая таблица
* Атомы в дополненной реальности
* Поиск химических реакций
* Автономный доступ к информации о химических элементах
* Таблица растворимости
* Калькулятор молярной массы
* Электроотрицательность элементов
* Молекулярные массы органических веществ
* Ряд реакционной способности
* Таблица сил кислот
* Список кислот, анионов, солей
* Стандартный электродный потенциал
* Виджеты для легкого запоминания таблицы Менделеева и химических элементов
Узнайте больше о нашем положения и условия здесь:
Условия использования: http://getchemistry. io/terms-and-conditions/ios/
io/terms-and-conditions/ios/
Политика конфиденциальности: http://getchemistry.io/privacy-policy/ios/
| Категория | Описание | Разрешить |
|---|---|---|
| Аналитические и эксплуатационные файлы cookie | Эти файлы cookie, в том числе файлы cookie из Google Analytics, позволяют нам распознавать и подсчитывать количество посетителей на сайтах TI и видеть, как посетители перемещаются по нашим сайтам.Это помогает нам улучшить работу сайтов TI (например, упрощая поиск информации на сайте). | |
| Рекламные и маркетинговые файлы cookie | Эти файлы cookie позволяют размещать рекламу на основе интересов на сайтах TI и сторонних веб-сайтах с использованием информации, которую вы предоставляете нам при взаимодействии с нашими сайтами.Объявления на основе интересов отображаются для вас на основе файлов cookie, связанных с вашими действиями в Интернете, такими как просмотр продуктов на наших сайтах. Мы также можем передавать эту информацию третьим лицам для этих целей. Эти файлы cookie помогают нам адаптировать рекламу, чтобы она лучше соответствовала вашим интересам, управлять частотой, с которой вы видите рекламу, и понимать эффективность нашей рекламы. Мы также можем передавать эту информацию третьим лицам для этих целей. Эти файлы cookie помогают нам адаптировать рекламу, чтобы она лучше соответствовала вашим интересам, управлять частотой, с которой вы видите рекламу, и понимать эффективность нашей рекламы. |
|
| Функциональные файлы cookie | Эти файлы cookie помогают определить, кто вы, и хранить информацию о вашей деятельности и учетной записи, чтобы обеспечить расширенные функциональные возможности, включая более персонализированный и актуальный опыт на наших сайтах.Если вы не разрешите использование этих файлов cookie, некоторые или все функции и службы сайта могут работать неправильно. Если вы не разрешите использование этих файлов cookie, некоторые или все функции и службы сайта могут работать неправильно. |
|
| Файлы cookie социальных сетей | Эти файлы cookie позволяют идентифицировать пользователей и контент, связанный с онлайн-социальными сетями, такими как Facebook, Twitter и другие платформы социальных сетей, и помогают TI улучшить охват социальных сетей. |
|
| Строго необходимо | Эти файлы cookie необходимы для работы сайтов TI или для выполнения ваших запросов (например, для отслеживания того, какие товары вы положили в свою корзину на TI.com, для доступа к безопасным областям сайта TI или для управления настроенными настройки файлов cookie). | Всегда включен |
Wolfram|Alpha Примеры: Химия
Другие примеры
Химические элементыИспользуйте Wolfram|Alpha для изучения элементов периодической таблицы.
Найдите количество элементов:
Получить информацию о химическом элементе:
Найдите элементы, соответствующие заданным критериям:
Постройте свойство для класса элементов:
Еще примеры
Другие примеры
Химические соединения Поиск химических веществ по названию, химической формуле или другому идентификатору.
Получить информацию о химическом соединении:
Укажите соединение по химическому идентификатору:
Сравните различные органические химические вещества:
См. примеры липидов, включая глицерофосфолипиды, жирные кислоты и многое другое:
примеры липидов, включая глицерофосфолипиды, жирные кислоты и многое другое:
Еще примеры
Другие примеры
ИоныУзнайте о положительно и отрицательно заряженных ионах и их свойствах.
Получить информацию об ионе:
Сравните ионы данного элемента:
Найдите конкретное значение свойства для класса ионов:
Еще примеры
Другие примеры
Химические количества Вычислить экстенсивные свойства химических веществ, которые зависят от количества присутствующего вещества, и преобразовать количества между различными единицами измерения.
Введите количество по массе:
Найдите количество молей данной массы:
Преобразование количества в объемы:
Еще примеры
Другие примеры
Химические растворы Исследуйте свойства различных растворов, которые зависят от растворителя, растворенного вещества и концентрации.
Вычислите свойства химического раствора:
Вычислить свойства количества раствора:
Выполните расчеты титрования:
Выполните расчеты разбавления:
Еще примеры
Другие примеры
Химические реакции Используйте Wolfram|Alpha, чтобы сбалансировать химические уравнения, определить стехиометрию реакции и предсказать продукты.
Сбалансируйте химическое уравнение:
Рассчитайте стехиометрию реакции:
Найти химические реакции с использованием реагентов или продуктов:
Еще примеры
Другие примеры
Химическая термодинамика Расчет термодинамических свойств, таких как энтропия, теплоемкость или давление паров, для широкого спектра химических веществ.
Найдите свойства вещества в данной фазе:
Вычислить свойства при заданной температуре:
Выполните расчеты по уравнению Аррениуса:
Оцените термодинамические свойства, используя метод Джобака:
Еще примеры
Другие примеры
Функциональные группы Исследуйте функциональные группы, такие как цианаты, пероксиды, алканы и галогениды.
Получить информацию о функциональной группе:
Получить информацию о защитной группе:
Найти защищающее групповое поведение при определенных условиях:
Еще примеры
Другие примеры
Хеминформатика Используйте Wolfram|Alpha для изучения свойств хемоинформатики от инвариантов графа, таких как индекс Балабана J или индекс Хосоя, до дескрипторов QSAR, таких как количество доноров водорода или самая длинная цепь.
Найдите наибольшую общую субструктуру между двумя молекулами:
Найдите доноров и акцепторов водородной связи:
Вычислите набор топологических индексов для молекулы:
Еще примеры
Другие примеры
Квантовая химия Свяжите химические свойства с лежащей в основе квантово-механической природой атомов и молекул.
Соберите электронную конфигурацию:
Соберите орбитальную диаграмму основного состояния:
Найдите атомный радиус:
Подсчитайте количество валентных электронов:
Еще примеры
Другие примеры
Облигации и орбитали Исследуйте свойства электронных орбиталей и связи, которые они образуют. Найдите связи по составляющим их атомам, по типу связи или по исходному химическому веществу.
Найдите связи по составляющим их атомам, по типу связи или по исходному химическому веществу.
Получите сводную информацию о связях для химического вещества:
Вычислить гибридизацию в соединении:
Сравните гибридизацию в двух соединениях:
Еще примеры
Другие примеры
Ядерная химия Изучите ядерную химию с помощью Wolfram|Alpha.
Запишите символ нуклида:
Рассчитать энергии связи:
Исследуйте источник элементов:
Еще примеры
Химические формулы — оборотная сторона, онлайн-редактор LaTeX
Существует несколько пакетов LaTeX для создания химических формул: chemfig, ochem, streetex и xymtex. Наиболее интуитивно понятным, вероятно, является пакет
Наиболее интуитивно понятным, вероятно, является пакет chemfig . В этой статье объясняется, как использовать пакет chemfig для создания химических формул в LaTeX.
Введение
Рисунок молекулы состоит в основном из соединения групп атомов линиями. Простые линейные формулы можно легко нарисовать с помощью пакета chemfig , как показано в следующем примере:
\documentclass{статья}
\usepackage{химфиг}
\начать{документ}
\section{Введение}
Писать химические формулы с помощью chemfig очень просто.\chemfig{O=H}
\конец{документ}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Пакет импортируется с помощью \usepackage{chemfig} в преамбуле. Команда \chemfig{O=H} рисует молекулу. Символ = определяет тип облигации. Список типов облигаций см. в справочном руководстве.
в справочном руководстве.
Уголки
Существует несколько способов определения углов между связями в молекулах.
Для определения химических формул можно использовать единицы измерения углов.
\chemfig{A-[1]B-[7]C}
Абсолютные углы
\chemfig{A-[:50]B-[:-25]C}
Относительные углы
\chemfig{A-[::50]B-[::-25]C}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Каждая из трех команд в приведенном выше примере использует другой метод для определения угла между связями.
-
единицы по умолчанию: В команде\chemfig{A-[1]B-[7]C}параметры в скобках задают угол в специальных единицах, каждая единица равна 45°. Следовательно, в примере углы равны 45° и 315°. -
абсолютные единицы: Углы могут быть установлены в абсолютных единицах, в команде\chemfig{A-[:50]B-[:-25]C}параметр в скобках представляет собой угол в градусах, измеряется от горизонтальной базовой линии. Допускаются отрицательные углы.
Допускаются отрицательные углы. -
относительных углов: В третьем примере\chemfig{A-[::50]B-[::-25]C}углы измеряются от предыдущей связи, а не от базовой линии.
Кольца
В приведенном ниже примере представлен синтаксис для рисования правильных многоугольников:
Правильные многоугольники:
\chemfig{A*5(-B=C-D-E=)}
Также возможны неполные кольца:
\chemfig{A*5(-B=C-D)}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Синтаксис команды \chemfig{A*5(-B=C-D-E=)} поясняется ниже:
-
A: Это первый атом, остальные атомы будут взяты отсюда -
*5: Количество сторон многоугольника -
(-B=C-D-E=): Остальные атомы и связи.Если для завершения многоугольника передано недостаточно, будет нарисовано незавершенное кольцо.
В эту команду можно передать дополнительный параметр: двойную звездочку. Например, если установить **5 вместо *5 , внутри многоугольника будет нарисован круг.
Филиалы
Химические формулы не всегда линейны, на самом деле наиболее распространены разветвленные формулы. Ниже пример того, как их создать.
Разветвленная молекула \vspace{.5см}
\chemfig{H-C(-[2]H)(-[6]H)-C(=[1]O)-[7]H}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Ветви в каждом узле создаются путем добавления формул в круглых скобках. Например, код
создает две ветви в «C», одну с углом 2 единицы (90°), а другую с углом 6 единиц (270°).
Ответвления также могут быть добавлены к кольцам:
Разветвленное кольцо
\vspace{.5см}
\chemfig{A*6(-B=C(-CH_3)-D-E-F(=G)=)}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Синтаксис аналогичен, с помощью круглых скобок ветвь может быть присоединена к узлу (атому). Например
присоединяет ветку к узлу «F». Более сложные примеры могут быть созданы с использованием вложенных ветвей и даже прикрепления колец в качестве ветвей.
Настройка формул
Можно изменить несколько параметров, таких как цвета и разделение узлов, а также добавить дополнительный текст для описания формулы.
{\ огромный
\setchemfig{atom sep=2em,bond style={ширина линии=1pt,красный,шаблон тире=on 2pt off 2pt}}
\имя_химии
{\ chemfig {HC (- [2] H) (- [6] H) - C (= [1] O) - [7] H}}
{Этанал}
}
Откройте этот пример chemfig на обороте.
На следующем изображении показан результат, полученный в приведенном выше примере:
Здесь есть три новые команды:
-
\setbondstyle{ }: Внутри фигурных скобок можно передать несколько команд, связанных со стилем, используя синтаксис
-
\setatomstep{2em}: Расстояние между атомами (узлами) в формуле установлено равным 2em. Можно использовать другие устройства LaTeX.
-
\chemname{}{}: Первый параметр в этой команде — это формулаchemfig, второй — некоторый текст, который будет напечатан под формулой. В примере текст «Этанал».
Обратите также внимание на то, что используется шрифт огромный . Вы можете использовать любой другой размер шрифта, и формула будет соответствующим образом масштабирована.
Открыть все примеры
Чтобы открыть все примеры в одном файле LaTeX, вы можете
открыть этот проект chemfig на обратной стороне
.
Справочник
Типы связки
Дальнейшее чтение
Для получения дополнительной информации см.
Периодическая таблица элементов
- 1. Проценты к массе
- 2. Масса на моль
- 3. Разделить на наименьшее количество молей.
- 4. Умножайте на целые числа, пока результат не будет целым числом.
Если указан процентный состав, измените каждый процент на массу каждого элемента в граммах. Если указана масса, пропустите шаг 1.
Если указана масса, пропустите шаг 1.
Переведите количество каждого элемента в граммах в его количество в молях.
Разделите каждое из найденных значений на шаге 2 на наименьшее количество молей.
При необходимости умножьте эти числа на целые числа, чтобы получить целые числа.Если умножение производится с одним из чисел, оно должно быть сделано со всеми числами. Если шаг 3 приводит к целым числам, пропустите шаг 4.
Пример:
200 г химического соединения содержат 71,5% кальция и 28,5% кислорода по массе. Вычислите эмпирическую формулу этого соединения.
- 1. Проценты к массе
- 2. Масса на моль
- 3. Разделить на наименьшее количество молей.
- 4. Умножайте на целые числа, пока результат не будет целым числом.
100 г химического соединения содержат 71,5 г кальция и 28.5 грамм кислорода. 200 граммов химического соединения содержат 143 грамма кальция и 57 граммов кислорода.
Найдите массы каждого элемента. Посмотрите на периодическую таблицу или периодическую диаграмму, чтобы найти массы каждого элемента.
Масса кальция = 40,1 грамма.
Масса кислорода = 16,0 грамм.
Найдите количества молей, разделив массы, полученные на шаге 1, на массы элементов.
кальций=143 грамма40.1 грамм/часть=3,56 части
кислород=57 грамм 16,0 грамм/часть=3,56 части
Посмотрите на периодическую таблицу или периодическую диаграмму, чтобы найти массы каждого элемента.
Масса кальция = 40,1 грамма.
Масса кислорода = 16,0 грамм.
Найдите количества молей, разделив массы, полученные на шаге 1, на массы элементов.
кальций=143 грамма40.1 грамм/часть=3,56 части
кислород=57 грамм 16,0 грамм/часть=3,56 части
кальций = 3,56 кислород = 3,56 Соотношение 1 Ca: 1 O Эмпирическая формула = CaO
Поскольку шаг 3 приводит к целым числам, пропустите шаг 4. Эмпирическая формула = CaO
- 1.Найдите эмпирическую формулу
- 2. Вычислите массу по эмпирической формуле
- 3. Разделите молярную массу на эмпирическую формулу Масса
- 4. Умножить эмпирическую формулу на коэффициент, полученный на шаге 3
Пример:
Эмпирическая формула химического соединения — HO, молярная масса — 32,02 грамма. Какова молекулярная формула этого соединения?
Какова молекулярная формула этого соединения?
- 1. Найдите эмпирическую формулу
- 2. Вычислите массу по эмпирической формуле
- 3. Разделите молярную массу на эмпирическую формулу Масса
- 4. Умножить эмпирическую формулу на коэффициент, полученный на шаге 3
Дано, что эмпирическая формула HO.Дано, что молярная масса равна 32,02 грамма.
Найдите массы каждого элемента. Посмотрите на периодическую таблицу или периодическую диаграмму, чтобы найти массу каждого элемента. Масса водорода = 1,01 грамма. Масса кислорода = 16,0 грамм. Эмпирическая масса равна 1,01 г + 16,00 г = 16,01 грамма.
фактор=32.02 грамм16,01 грамм/часть=2
Молекулярная формула = (эмпирическая формула) n Молекулярная формула = (HO) 2 Эмпирическая формула = H 2 O 2
Химические формулы | Важные химические формулы Pdf
Химические формулы Советы, ярлыки и интеллект-карты
Химия является предметом применения химических формул и понимания реакций.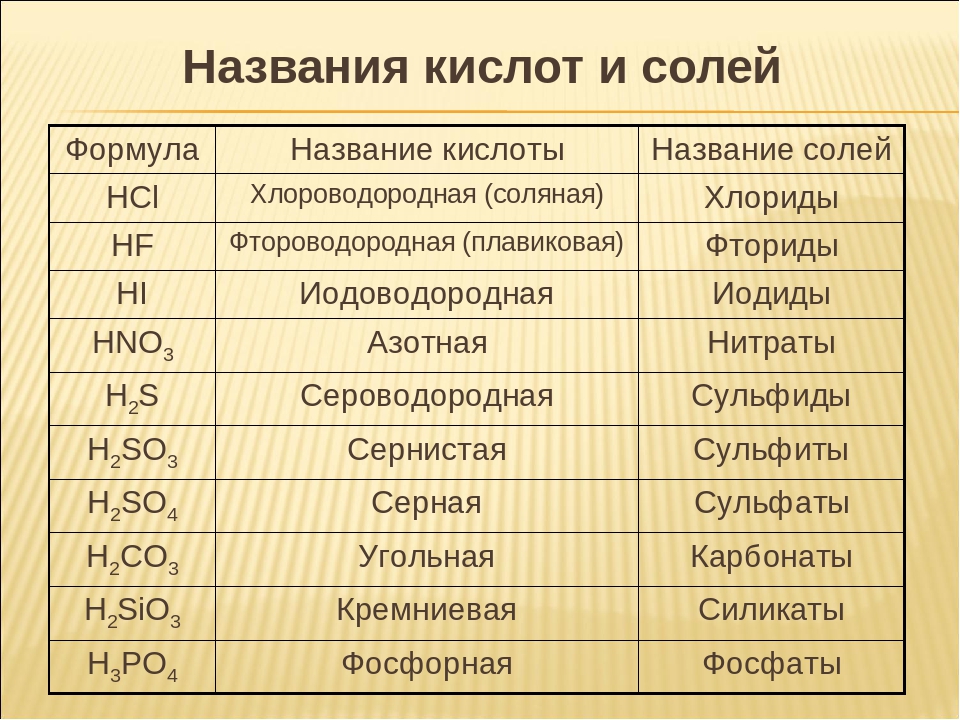 Основы химии необходимы для понимания химии в 11 и 12 классах. Академическая команда учащихся подготовила формулы по химии на основе важных глав химии из 11 и 12 классов. Мы подготовили формулы по химии по главам, которые включают главы по физической, неорганической и органической химии. Академическая группа Entrancei тщательно отобрала все важные формулы всех трех разделов химии и добавила химических формул . При решении числовой физической химии вам потребуются все важные химические формулы, и чтобы написать химическую реакцию органической химии, нужно иметь очень четкое представление. понимание механизма, используемого в органической химии.Entrancei добавил все реакции в формулы химии разделов органической химии. Решите упражнение NCERT с помощью решений Entrancei NCERT для 12 класса по химии.
Основы химии необходимы для понимания химии в 11 и 12 классах. Академическая команда учащихся подготовила формулы по химии на основе важных глав химии из 11 и 12 классов. Мы подготовили формулы по химии по главам, которые включают главы по физической, неорганической и органической химии. Академическая группа Entrancei тщательно отобрала все важные формулы всех трех разделов химии и добавила химических формул . При решении числовой физической химии вам потребуются все важные химические формулы, и чтобы написать химическую реакцию органической химии, нужно иметь очень четкое представление. понимание механизма, используемого в органической химии.Entrancei добавил все реакции в формулы химии разделов органической химии. Решите упражнение NCERT с помощью решений Entrancei NCERT для 12 класса по химии.
Chapter wise Chemistry Formulas for 11th & 12th class pdf
Список ментальных карт и кратких заметок по химии
Химия — это предмет фактов и их применения.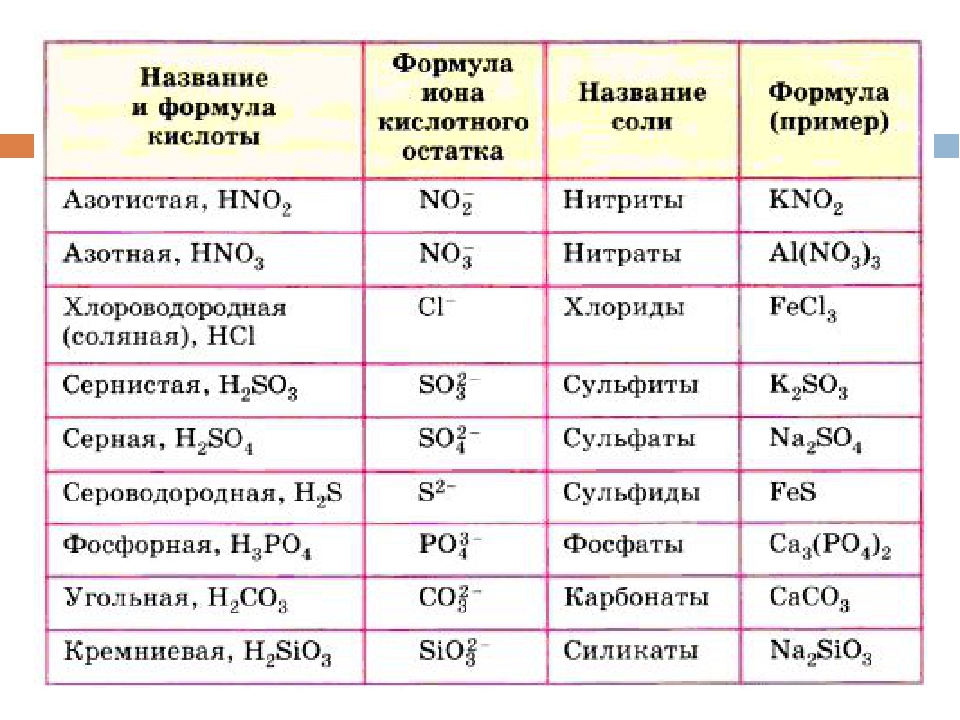 Лучший способ добиться концептуальной ясности в химии — начать со знания химии формулы. Когда вы учитесь в классе 11 или в классе 12, химия подразделяется на три части, называемые физической, органической и неорганической химией.Эта страница состоит из всех формул, необходимых для построения прочного фундамента по химии.
Лучший способ добиться концептуальной ясности в химии — начать со знания химии формулы. Когда вы учитесь в классе 11 или в классе 12, химия подразделяется на три части, называемые физической, органической и неорганической химией.Эта страница состоит из всех формул, необходимых для построения прочного фундамента по химии.
- Формулы физической химии
- Формулы органической химии
- Формулы неорганической химии
Чтобы стать экспертом во всех трех разделах химии, формула очень поможет вам. На этой странице академическая группа, состоящая из опытных преподавателей, загрузила химические формулы физической химии, неорганической химии и органической химии в формате pdf.Выберите нужную главу и загрузите необходимые химические формулы.
Об основах химии
Химия является предметом понимания того, как действуют элементы и соединения. Мы предоставили вам список важных химических формул, которые могут быть вам полезны. Так как свойства вещества очень сильно различаются. Понимание их свойств очень важно. Так как окружающая температура сильно влияет на свойства веществ.Мы подготовили подробный анализ каждого химического соединения. Эти химические формулы помогают учащимся глубоко понять элементы, лежащие в основе образования соединений. Поскольку формулы необходимо выучить наизусть непосредственно перед экзаменом, крайне важно выбрать лучшее.
Так как свойства вещества очень сильно различаются. Понимание их свойств очень важно. Так как окружающая температура сильно влияет на свойства веществ.Мы подготовили подробный анализ каждого химического соединения. Эти химические формулы помогают учащимся глубоко понять элементы, лежащие в основе образования соединений. Поскольку формулы необходимо выучить наизусть непосредственно перед экзаменом, крайне важно выбрать лучшее.
Прежде чем решать вопросы Убедитесь, что вы прошли все химические формулы, подготовленные Entrancei.
Почему химические формулы важны?
Учащиеся, желающие получить высшие оценки на экзамене, должны хорошо знать формулы по химии.Учебный материал, который мы предоставляем в Entrancei, очень важен для студентов, стремящихся получить высшие оценки. Поскольку химия включает в себя обширную программу, наши формулы по химии очень лаконичны.
Они помогают учащимся изложить суть темы при минимальном освещении. Команда Entrancei — это специалисты по химии из ИИТ. Мы проводим обширные исследования, чтобы предложить нашим студентам лучшие учебные материалы по химическим формулам. Поскольку мы полны решимости предложить студентам легкое изучение химии, мы предлагаем различные стратегии.Студенты могут найти различные важные формулы химии для экзамена.
Мы проводим обширные исследования, чтобы предложить нашим студентам лучшие учебные материалы по химическим формулам. Поскольку мы полны решимости предложить студентам легкое изучение химии, мы предлагаем различные стратегии.Студенты могут найти различные важные формулы химии для экзамена.
Химические формулы всегда предпочитают топперы класса. Подробное положение о формулах по химии заключается в том, чтобы обеспечить всем учащимся максимальные оценки. У нас есть специальное специальное положение для всех важных химических формул в нашем учебном материале. Список химических формул подготовлен после тщательного изучения вопросников предыдущего года. Мы гарантируем, что учебный материал, который мы предоставляем, максимально полезен для студентов, готовящихся к экзамену.
Команда Entrancei стремится предоставить первоклассный учебный материал. В исследовании дается подробное объяснение каждой части химических формул. Мы гарантируем, что студенты, хорошо владеющие учебным материалом, получат высшие оценки. Решите вопросы из учебника NCERT и воспользуйтесь помощью входных решений NCERT.
Решите вопросы из учебника NCERT и воспользуйтесь помощью входных решений NCERT.
Как эффективно изучать химические формулы?
Химия в большинстве случаев считается сложной для большей части учащихся.Мы приложили усилия, чтобы упростить изучение химии, предоставив химические формулы каждому учащемуся. Исследование предлагает полную ясность для студентов. Поскольку химия очень разнообразна, студентам, изучающим химические формулы, не о чем беспокоиться. Полное знание химических формул поможет вам в будущих конкурсных экзаменах. Студенты могут легко использовать эту формулу химии для повторения непосредственно перед экзаменом. Студентам будет предоставлена необходимая информация для написания и запоминания формул.
Как использовать химическую формулу физической химии
Физическая химия — это предмет, который требует применения концепции в числовом виде, начните с концепции крота и ее применения, до этого выучите химическую формулу и ее символы из таблицы Менделеева. После изучения концепции крота пересмотреть все формулы, используемые в моле, и перейти к главе «Атомная структура».
После изучения концепции крота пересмотреть все формулы, используемые в моле, и перейти к главе «Атомная структура».
Академическая группа вступительных загрузила все важные формулы использования в атомной структуре, загрузите pdf формулы химии главы сразу после того, как вы завершили тему и пересмотрите ее из pdf.Это поможет вам очень быстро завершить пересмотр главы, а затем вы сможете перейти к решению числовой части главы. Наша академическая группа загрузила все формулы глав физической химии в формате pdf, которые вы можете скачать для ознакомления всего одним щелчком мыши.
Как использовать химическую формулу органической химии
Органическая химия требует иного подхода по сравнению с физической химией. Когда вы начинаете заниматься органической химией, всегда начинайте думать о том, как протекает реакция, а не почему.Попытайтесь понять разницу между «как» и «почему».
Начните изучать органическую химию с общей органической химии. Загрузите формулу органической химии в формате pdf, которая состоит из всех указателей, которые часто требуются при написании механизма реакции.
Мы добавили весь порядок силы кислоты, реакции и их механизм, важные сведения об изотопном эффекте в органических реакциях и все важные механизмы органических реакций, такие как реакция элиминации, реакции замещения с участием различных групп, применение окислителей и восстановителей.Таким образом, в химической формуле органической химии вы можете получить реакции по главам и указатель их применения на очень небольшом количестве страниц, что очень полезно для пересмотра и быстрого подведения итогов.
Как использовать химическую формулу неорганической химии
Неорганическая химия является предметом фактов и приложений, поэтому химическая формула неорганической химии очень полезна для повторения, а также для сохранения предметов. Entrancei выложил все темы неорганической химии для доработки.Начните неорганическую химию с главы о химическом связывании и попытайтесь понять гибридизацию и форму молекул, а также выучите химическую формулу различных важных молекул. Для неорганической химии следуйте учебнику NCERT и воспользуйтесь справочной формой решений NCERT для химии класса 12.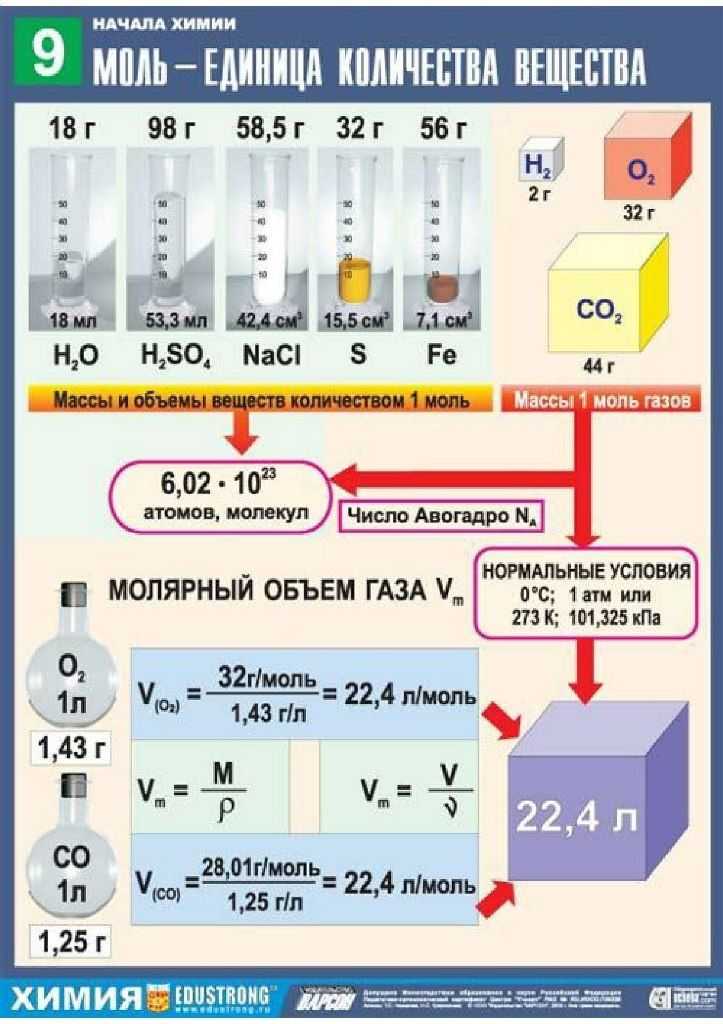 Это будет полезно во всех главах химии. Начните с периодической таблицы и изучите все химические формулы, приведенные в периодической таблице, и тенденцию кислотных и основных свойств. Entrancei загрузил все важные моменты, которые необходимы для всех тем.
Это будет полезно во всех главах химии. Начните с периодической таблицы и изучите все химические формулы, приведенные в периодической таблице, и тенденцию кислотных и основных свойств. Entrancei загрузил все важные моменты, которые необходимы для всех тем.
Почему Entrancei лучше всего подходит для формулы химии?
Специалисты-химики подготовили этот учебный материал. Команда Entrancei всегда готова помочь студентам с их сомнениями в химии. Поскольку мы искренне верим в обмен информацией с нуждающимися студентами. Все химические формулы предоставляются на сайте совершенно бесплатно. Студенты также могут поделиться этой формулой химии со своими друзьями. Все, что нужно сделать студентам, — это зарегистрироваться на нашем веб-сайте и получить доступ к учебным материалам мирового уровня.
Часто задаваемые вопросы по химическим формулам
Q-1. Кто может использовать приведенные выше химические формулы?
Ответ — Эта страница подготовлена для учащихся 11 и 12 классов, изучающих химию. Все учащиеся, которые готовятся к экзамену по химии для CBSE board, олимпиады, JEE и NEET, могут использовать эти формулы химии по главам для эффективного повторения. Каждая глава состоит из всех формул, используемых в главе для решения вопросов, основанных на числах или MCQ.
Все учащиеся, которые готовятся к экзамену по химии для CBSE board, олимпиады, JEE и NEET, могут использовать эти формулы химии по главам для эффективного повторения. Каждая глава состоит из всех формул, используемых в главе для решения вопросов, основанных на числах или MCQ.
Q-2.Как лучше всего использовать химические формулы?
Ответ — Лучший способ использовать химические формулы — это начать главу из вашего учебника, прочитать теорию, изложенную в учебнике, сделать примечания к главе, записать все важные определения и реакции, данные в учебнике. Прежде чем перейти к решению упражнения по главам, пересмотрите всю главу из приведенного выше PDF-файла с химическими формулами. Таким образом, вы можете эффективно пересмотреть главу, и если вы пропустили несколько формул, вы можете получить их, чтобы сформировать лист, указанный в формулах химии.
Q-3. Являются ли химические формулы мудрыми главами?
Ans- Наша академическая команда подготовила формулы по химии для каждого класса и выгрузила формулы по химии для 11 класса и формулы по химии для 12 класса отдельно, чтобы дать вам дополнительное преимущество. Формулы каждого класса по химии готовятся по главам и состоят из всех важных формул, необходимых для решения вопросов и числовых значений. Помимо глав, мы подготовили отдельный раздел важных химических формул, которые используются в общих вопросах химии в разделах общих формул химии.
Формулы каждого класса по химии готовятся по главам и состоят из всех важных формул, необходимых для решения вопросов и числовых значений. Помимо глав, мы подготовили отдельный раздел важных химических формул, которые используются в общих вопросах химии в разделах общих формул химии.
Q-4. Эти формулы полезны для того, чтобы стать экспертами в таких предметах, как химия.
Ans- Химия предмет знания и его применение. Он состоит из нескольких частей, требующих понимания, и нескольких глав, посвященных неорганической химии, для которых требуются факты и ее приложения. Чтобы стать экспертом в области химии, необходимо помнить все факты, приведенные в главе «Химические формулы», загруженные Entrancei.
Q-5. Какие основы химии необходимо придать дополнительный вес?
Ответ — первая глава по химии для 11 класса содержит концепции родинок, требующих дополнительной практики, поскольку она используется во всех остальных главах.Нужно иметь очень четкое представление об атомной структуре и химических связях, чтобы понимать концепции химии в других главах.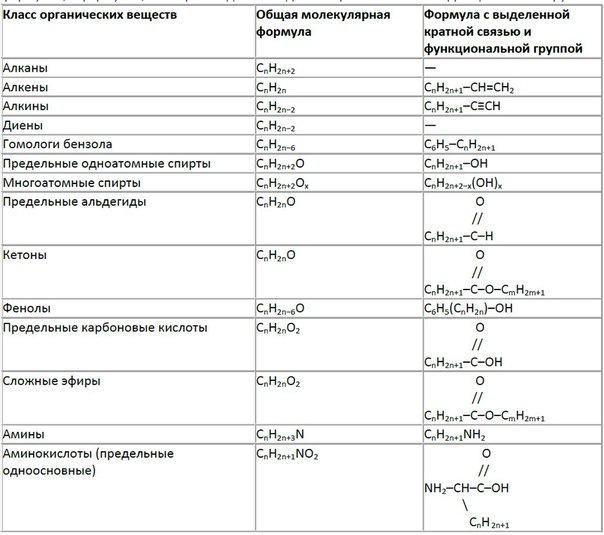 Периодическая таблица поможет вам понять всю неорганическую химию. при подготовке органической химии надо иметь очень четкое представление об общей органической химии и углеводородах.
Периодическая таблица поможет вам понять всю неорганическую химию. при подготовке органической химии надо иметь очень четкое представление об общей органической химии и углеводородах.
Q-6. Где взять дополнительные вопросы по химии?
Ответ — Академическая команда Entrancei загрузила множество вопросов на основе MCQ, которые можно бесплатно загрузить. Вы можете загрузить вопросы и ответы по химии из формы Entrancei для дополнительной практики.
Q-7. Онлайн-викторина по химии поможет мне преуспеть в таком предмете, как химия.
Ответ -Конечно, да, как только вы подготовили свою главу и прошли лист с формулами химии по главам Entrancei, после этого нужно проверить свою концепцию с помощью онлайн-теста. Чтобы помочь вам в этом, наша команда загрузила главы мудрой викторины по химии, которая выглядит следующим образом.
Q-8.Что такое химическая формула?
Ans — Химическая формула соединения может быть символом его химического состава. Химические формулы дают представление об элементах, из которых состоят молекулы соединений, и о соотношении атомов этих элементов, образующих такие молекулы. Например, химическая формула воды h3O предполагает, что два атома водорода соединяются с одним атомом кислорода, образуя молекулу воды.
Химические формулы дают представление об элементах, из которых состоят молекулы соединений, и о соотношении атомов этих элементов, образующих такие молекулы. Например, химическая формула воды h3O предполагает, что два атома водорода соединяются с одним атомом кислорода, образуя молекулу воды.
Q-9. Каково значение химической формулы?
1. Химические формулы дают представление о химическом составе соединения.
2.Они также представляют пропорции, в которых ингредиенты объединяются для образования соединения.
3. Химическая формула соединения имеет решающее значение, когда оно представлено в чрезвычайно химическом уравнении.
4. Химические формулы также могут использоваться для представления ионов, свободных радикалов и других типов химических веществ.
Q-10. Какие бывают типы химических формул?
Ans- Хотя термин «химическая формула» обычно относится к молекулярной формуле соединения, составы химических соединений будут выражаться различными способами, как указано здесь-
Молекулярная формула. элементы обозначаются их символами (как в таблице Менделеева), а также число атомов каждого элемента в молекуле записывается индексом.
элементы обозначаются их символами (как в таблице Менделеева), а также число атомов каждого элемента в молекуле записывается индексом.
Эмпирическая формула. Эмпирическая формула вещества представляет соотношение элементов, присутствующих в этом соединении. Эмпирические формулы обычно получают из анализа экспериментальных данных. Эмпирическая формула глюкозы – Ch3O. Эмпирические формулы будут получены из молекулярных формул.
Структурная формула. Структурная формула химического соединения дает представление о расположении атомов в молекуле.
Q-11.Как написать химическую формулу?
Ответ — Для написания химической формулы важно знать символ элементов, присутствующих в соединении, формулу радикалов и, следовательно, валентность элементов в этом соединении.
В-12. Каково значение химической формулы?
Ответ -Значение химических формул:
1. Формула представляет собой название вещества.
2. Формула представляет одну молекулу вещества.
3. Формула представляет 6,022 x 1023 (один моль) молекул вещества.
4. Формула представляет собой название содержащихся в ней элементов.
5. Формула – число атомов каждого элемента, присутствующего в молекуле вещества.
7. Формула представляет заданную массу вещества (т.е. массу вещества в граммах).
В-13. Что говорит формула о соединении?
Ans — Основной состав соединения может быть задан химической формулой. Химическая формула использует символы из периодической таблицы для обозначения типов элементов, которые присутствуют в конкретном соединении, а индексы используются для представления количества каждого типа присутствующего элемента.Соединения могут быть ковалентными или ионными.
Химические формулы и уравнения | CPD
Вы когда-нибудь добавляли в ванну английскую соль, принимали магнезиальное молоко от расстройства желудка или клали цветы серы на свои розы? Вы, наверное, знаете химический состав этих продуктов, но как насчет спирта рогового или купороса; а можно сделать глауберову соль?
Эти алхимические названия могут быть вызывающими воспоминания и таинственными, но они плохо передают химические знания. Хотя мы до сих пор цепляемся за некоторые из этих названий, большинство химических веществ в настоящее время систематически именуются на основе их состава. Несмотря на это, для начинающего химика аммиак и серная кислота могут быть столь же двусмысленными, как винный спирт или купоросное масло. Даже систематические названия, такие как хлорид меди, дают только частичную информацию — количественная связь между элементами отсутствует.
Хотя мы до сих пор цепляемся за некоторые из этих названий, большинство химических веществ в настоящее время систематически именуются на основе их состава. Несмотря на это, для начинающего химика аммиак и серная кислота могут быть столь же двусмысленными, как винный спирт или купоросное масло. Даже систематические названия, такие как хлорид меди, дают только частичную информацию — количественная связь между элементами отсутствует.
Аналогичные проблемы возникают при описании реакций. Естественный язык очень хорош для обозначения вещей, но ему трудно выразить точное количество — вот почему мы используем числа.Представьте, что вы пытаетесь ответить на вопрос: «Сколько вам лет?» без использования цифр.
Двести лет назад шведский химик Йонс Якоб Берцелиус ввел символическую систему для описания химического состава веществ. Символы, обычно первые или первые два символа имени элемента, в сочетании с цифрами, чтобы показать присутствующие относительные количества. Элементы в этих формулах соединялись знаком +. Итак, оксид меди стал Cu+O, а вода стала 2H+O. Эти формулы устранили как тайну состава, вызванную алхимическим названием, так и отсутствие количественной информации.Система Берцелиуса с годами превратилась в химические формулы, которые мы знаем сегодня: CuO и H 2 O.
Итак, оксид меди стал Cu+O, а вода стала 2H+O. Эти формулы устранили как тайну состава, вызванную алхимическим названием, так и отсутствие количественной информации.Система Берцелиуса с годами превратилась в химические формулы, которые мы знаем сегодня: CuO и H 2 O.
Что нужно знать учащимся
Химические уравнения и формулы являются важной частью изучения химии в 11–19 классах. Умение правильно их использовать — это часть того, что значит быть химиком. Формулы и уравнения позволяют химикам эффективно передавать химические знания.
Учащиеся должны понимать, что химические формулы:
- укажите название вещества – например, K 2 SO 4 – сульфат калия;
- предоставить список элементов в составе вещества – например, калий, сера и кислород;
- обеспечивают соотношение элементов в веществе – например, две части калия, 1 часть серы, 4 части кислорода;
и что химические уравнения:
- описывает, как изменяются вещества, например, углерод + кислород → двуокись углерода становится C + O 2 → CO 2 ;
- говорит нам о соотношении реагентов и продуктов реакции – например, 2Mg + O 2 → 2MgO означает, что две порции магния реагируют с одной порцией кислорода с образованием двух порций оксида магния;
- может включать символы состояния — (g), (l), (s) и (aq) — которые могут помочь учащимся визуализировать реакцию и объяснить наблюдения.

Учащиеся должны уметь:
- напишите формулы элементов и простых соединений, используя химические символы и числа.
- называют простые соединения по химической формуле, используя такие префиксы, как моно-, ди-, три- и такие слова, как оксид, хлорид, гидроксид, сульфат, нитрат и карбонат.
- составить словесные уравнения для реакций.
- представляют реагенты и продукты химической реакции в сбалансированном уравнении.
Идеи для вашего класса
Общая последовательность обучения формулам и уравнениям может быть следующей:
- проводить простые реакции в пробирке или в микромасштабе;
- выучить общие уравнения химических реакций;
- научиться писать определенные словесные уравнения;
- научиться составлять химические формулы;
- и используйте химические формулы и слово уравнение для построения сбалансированных химических уравнений.
На сайте Learn Chemistry можно найти два отличных ресурса для обучения написанию словесных уравнений.
После того, как учащиеся освоят словесные уравнения, вы можете перейти к написанию химических формул. К сожалению, названия некоторых веществ не всегда напрямую переводятся в химические формулы. Например, формулы воды, метана, аммиака, азотной кислоты и т. д. придется выучить наизусть. Покажите имена и формулы и дайте учащимся стратегии, чтобы запомнить их.
Называние неметаллических соединений начинается с понимания приставок моно-, ди-, три- и т. д. Свяжите их со словами из повседневной жизни и посмотрите, сколько учащихся смогут придумать. Затем назовите формулы некоторых соединений, о которых они, возможно, уже слышали. Например, углекислый газ как углерод с двумя атомами кислорода. Чтобы помочь учащимся овладеть этими преобразованиями, потребуется множество примеров. Затем вы можете попросить учащихся придумать свои собственные примеры и предложить их сверстникам сделать преобразования.
Наконец, вы можете перейти к именованию солей и ионных соединений. Опять же, потребуется некоторое механическое заучивание, чтобы убедиться, что они знают названия многоатомных ионов, таких как аммоний, гидроксид и карбонат.
Опять же, потребуется некоторое механическое заучивание, чтобы убедиться, что они знают названия многоатомных ионов, таких как аммоний, гидроксид и карбонат.
Распространенные заблуждения
- Все формулы представляют молекулы, например, «NaCl означает молекулы хлорида натрия».
- Многоатомные ионы не признаются отдельными химическими соединениями, например MgSO 4 , названный тетроксидом серы магния, а не сульфатом магния.
- Путают многоатомные ионы с элементами, например: «Я не могу найти гидроксид в периодической таблице».
- Смешение символа элемента, например Cl, и его формулы в виде вещества, например Cl 2 . Это может быть осложнено использованием символа элемента для гигантских структур — например, алмаза как C и железа Fe — и некоторых, казалось бы, нелогичных исключений, например S 8 и P 4 .
- Смешение формулы вещества с химическим уравнением его получения.Например, дать «водород + кислород → вода», когда его спросят о формуле воды.
 Это заблуждение проистекает из математики, где эти два слова часто используются взаимозаменяемо, и из повседневной жизни, где формула слова часто ассоциируется с тем, как что-то делается.
Это заблуждение проистекает из математики, где эти два слова часто используются взаимозаменяемо, и из повседневной жизни, где формула слова часто ассоциируется с тем, как что-то делается. - Учащиеся часто затрудняются с числовыми соотношениями в уравнениях и формулах, это может затруднить балансировку уравнений и химических расчетов.
Формирующее оценивание
Написание формул и уравнений — это не тот навык, который можно развить за один-два урока.Это навык, который должен быть постоянной частью уроков химии. Используйте регулярные низкие ставки тестирования словесных уравнений и простых химических уравнений наряду с вспоминанием формул. Сосредоточьтесь на двухатомных элементах, а также на распространенных кислотах, основаниях и солях, чтобы помочь учащимся получить общие химические знания и уверенность. Популярны игры в формулу или уравнение бинго, а мини-доски полезны для быстрой формирующей оценки.
Баллы на вынос
- Формулы — это не просто сокращение для химического названия, они предоставляют информацию об относительном количестве элементов в веществе.

- Формулы некоторых соединений не могут быть получены из названия вещества, и их необходимо выучить.
- Написание химических формул и уравнений требует частого подкрепления.
- Не спешите писать сбалансированные уравнения. Сначала помогите учащимся освоить написание формул и словесных уравнений.
Прогресс до 14‒16 лет
После того, как учащиеся освоят написание формул и сбалансированных химических уравнений, их можно расширить, включив в них написание ионных уравнений для реакций осаждения и половинных уравнений для электрохимических и окислительно-восстановительных процессов.
На этом уровне формулы и уравнения используются для выполнения многих химических расчетов, включая относительную формульную массу, моль вещества, реакционную массу и расчеты титрования. Овладение этими формулами и уравнениями помогает сгладить эти вычисления.
Олли Хантер — руководитель отдела химии и координатор EPQ в Benenden School, Кент, а также студент, работающий неполный рабочий день, на педагогическом факультете Кембриджского университета
Что скрыто в формулах и уравнениях?
Балансировка уравнений и выполнение химических расчетов требуют четкого понимания роли чисел в формулах. Разница между числами перед и числами внутри формулы может вызвать путаницу.
Разница между числами перед и числами внутри формулы может вызвать путаницу.
Число в формуле означает число, кратное элементу (или группам элементов) слева от числа.
Таким образом, формула гидроксида меди Cu(OH) 2 читается как:
1 x Cu + 2 x (O+H) или Cu + 2 x O + 2 x H
Более сложная формула, например сульфат аммония (NH 4 ) 2 SO 4 , читается как:
2 x (N + (4 x H)) + 1 x S + 4 x O или 2 x N + 8 x H + S + 4 x O
Число, используемое перед формулой в уравнении, говорит нам, сколько молекул (или молей) вещества вступает в реакцию.Например, в уравнении 2H 2 +O 2 → 2H 2 O читается как:
2 x H 2 + 1 x O 2 → 2 x (H 2 O)
или
две молекулы водорода реагируют с одной молекулой кислорода с образованием двух молекул воды.
Имейте в виду, что некоторые учащиеся предполагают, что число перед химической формулой является частью формулы или относится только к первому элементу.


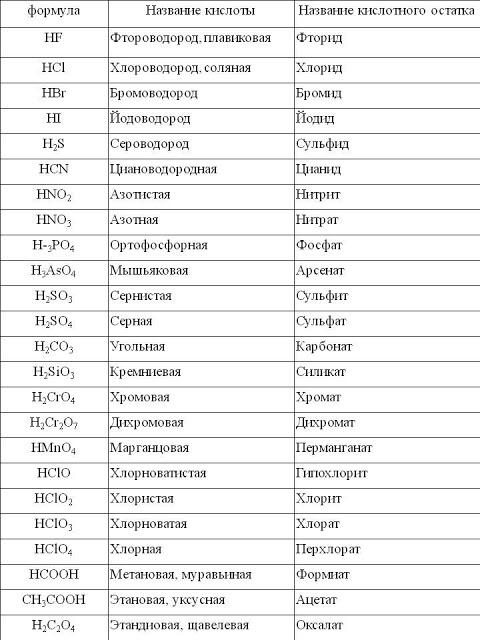
 Амфолиты. Кислые соли
Амфолиты. Кислые соли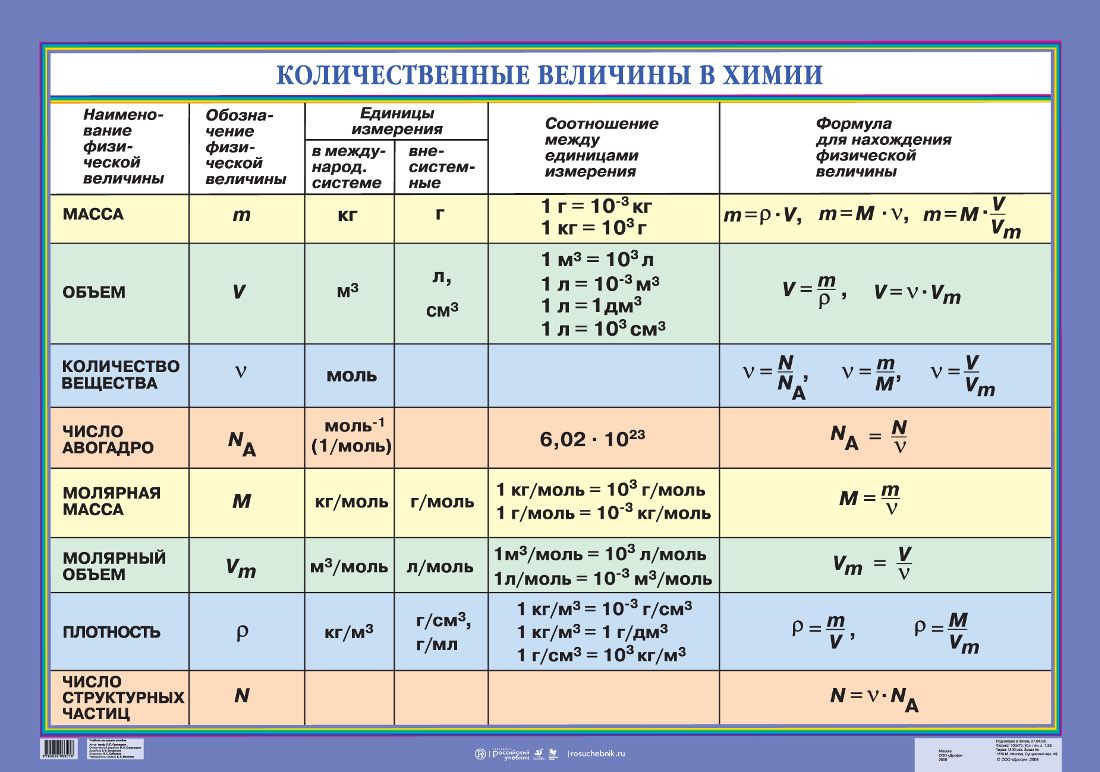 Как определить наличие анионов?
Как определить наличие анионов?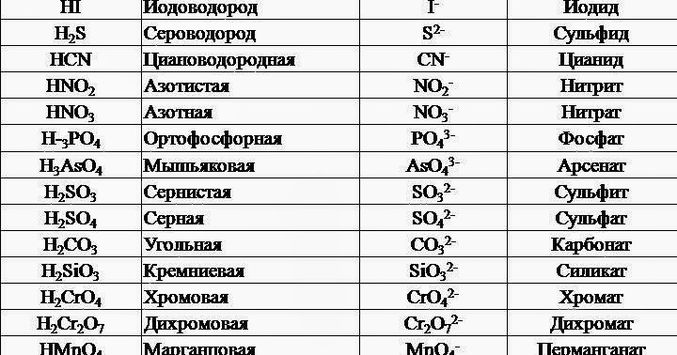 Пассивная защита. Электродные потенциалы — таблица.
Пассивная защита. Электродные потенциалы — таблица.