ОГЭ по химии: онлайн подготовка
Для школьников, которые планируют в будущем освоить профессию, связанную химией, ОГЭ по этому предмету очень важен. Если вы хотите получить на испытаниях лучшую оценку, начните подготовку немедленно. Лучшее количество баллов при выполнении работы – 34. Показатели данного экзамена могут использоваться при направлении в профильные классы средней школы. При этом минимальная граница показателя по баллам в этом случае — 23.
Из чего состоят варианты
ОГЭ по химии, как и в предыдущие годы, включает теорию и практику. С помощью теоретических заданий проверяют, как юноши и девушки знают основные формулы и определения органической и неорганической химии и умеют их применять на практике. Вторая часть соответственно направлена на проверку способностей школьников проводить реакции окислительно-восстановительного и ионно-обменного типа, иметь представление о молярных массах и объемах веществ.
Почему необходимо проходить тестирование
ОГЭ 2018 по химии требует серьезной подготовки, так как предмет достаточно сложен. Многие уже забыли теорию, может быть, плохо ее поняли, а без нее невозможно правильно решить практическую часть задания.
Стоит выделить время на тренировку сейчас, чтобы в будущем показать достойный результат. Сегодня школьники имеют отличную возможность оценить свои силы, решая реальные прошлогодние тесты. Никаких затрат — можно бесплатно использовать школьные знания и понять, как будет проходить экзамен. Ученики смогут не только повторить пройденный материал и выполнить практическую часть, но и почувствовать атмосферу настоящих испытаний.
Удобно и эффективно
Отличная возможность – готовиться к ОГЭ прямо за компьютером. Надо лишь нажать кнопку пуск и начать прохождение тестов онлайн. Это очень эффективно и может заменить занятия с репетитором. Для удобства все задания сгруппированы по номерам билетов и полностью соответствуют реальным, поскольку взяты с сайта Федерального института педагогических измерений.
Если вы не уверены в своих силах, испытываете страх перед предстоящими испытаниями, у вас есть пробелы в теории, вы выполняли недостаточно экспериментальных заданий –включайте компьютер и начинайте подготовку. Желаем вам успехов и самых высоких оценок!
examer.ru
Пробный (репетиционный) вариант ОГЭ по химии 2018 (Санкт-Петербург)
Пробный ОГЭ по химии
Вариант № 1
1. В атоме химического элемента содержится 16 электронов. Сколько из них находятся на внешнем энергетическом уровне?
1) 2 2) 4 3) 6 4) 8
2. В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) алюминий → фосфор → хлор
2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
3. Какой вид химической связи характерен для меди?
1) ионная 2) металлическая 3) ковалентная полярная 4) ковалентная неполярная
4. В каком соединении сера имеет наивысшую степень окисления?
1) 2) 3) 4)
5. Сложным является каждое из двух веществ:
1) нитрат калия и хлор 2) белый фосфор и озон
3) гидроксид калия и аргон 4) угарный газ и аммиак
6. Взаимодействие между оксидом меди(II) и водородом при нагревании – это
реакция
1) разложения 2) замещения 3) соединения 4) обмена
7. Больше всего ионов водорода образуется в водном растворе из одного моля
1) 2) 3) 4)
8. Осадок образуется при взаимодействии водных растворов
1) нитрата аммония и гидроксида калия
2) соляной кислоты и гидроксида бария
3) нитрата серебра и бромида кальция
4) азотной кислоты и карбоната натрия
9. С кислородом может реагировать
1) медь
2) оксид углерода(IV)
3) гидроксид натрия
4) серная кислота10. Оксид серы(VI) реагирует с
1) нитратом натрия
2) хлором
3) оксидом алюминия
4) оксидом кремния
11. Азотная кислота образуется в реакции между соляной кислотой и
1) аммиаком
2) нитратом бария
3) азотом
4) нитратом серебра
12. В реакцию и с гидроксидом кальция, и с нитратом серебра вступает
1) карбонат магния
2) хлорид аммония
3) нитрат натрия
4) сульфат бария
13. Верны ли следующие суждения о правилах безопасной работы в лаборатории?
А. При получении кислорода из раствора пероксида водорода необходимо использовать резиновые перчатки.
Б. При растворении соды в воде необходимо надеть защитные очки.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
14. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
РЕАКТИВ
А) (р-р) и (р-р)
Б) (р-р) и (р-р)
В) (р-р) и (р-р)
1) (р-р)
2) (р-р)
3) (р-р)
4) (р-р)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
15. На какой диаграмме распределение массовых долей элементов соответствует ?
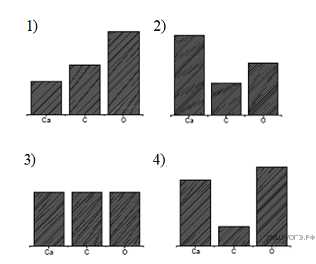
16. В ряду химических элементов: происходит уменьшение (ослабление)
1) заряда ядра
2) степени окисления в высших оксидах
3) числа атомов водорода в летучем водородном соединении
4) радиуса атома
5) числа электронов на внешнем энергетическом уровне17. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
Этилен
1) относится к непредельным углеводородам
2) не реагирует с кислородом
3) реагирует с водородом
4) имеет только одинарные связи
5) вступает в реакции замещения
18. Хлороводород является восстановителем в реакции с
1) 2) 3) 4)
19. Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВАПРОДУКТЫ РЕАКЦИИ
А)
Б)
В)
1)
2)
3)
4)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
20. Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
21. К 340 г раствора с массовой долей нитрата серебра 6 % добавили избыток раствора хлорида железа (III). Вычислите массу образовавшегося осадка.
22. Даны вещества: FeCl3, H2SO4(конц.), Fe, Cu, NaOH, CuSO4.
Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид железа(II).
Запишите уравнения проведённых химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
Пробный ОГЭ по химии
Вариант № 2
1. На внешнем энергетическом уровне элемента 2-го периода – в два раза больше электронов, чем на внутреннем уровне. Этот элемент –
1) литий 2) бериллий 3) углерод 4) кислород
2. Неметаллические свойства углерода выражены сильнее, чем неметаллические свойства
1) кислорода 2) кремния 3) азота 4) фтора
3. Ковалентной полярной связью образовано каждое из веществ в группе
1)
2)
3)
4)
4. Сера имеет самую низкую степень окисления в
1) 2) 3) 4)
5. Оксиду меди(I) и гидроксиду меди(I) соответствуют формулы
1) и 2) и
3) и 4) и
6. Пример реакции обмена:
1)
2)
3)
4)
7. В растворе сульфата аммония находится 0,6 моль положительных ионов. Количество отрицательных ионов в этом растворе равно
1) 0,2 моль 2) 0,3 моль 3) 0,6 моль 4) 1,2 моль
8. Взаимодействию карбоната магния с бромоводородной кислотой соответствует сокращённое ионное уравнение
1)
2)
3)
4)
9. Хлор реагирует с
1) 2) 3) 4)
10. Химическая реакция возможна между
1) оксидом серы(IV) и соляной кислотой
2) оксидом алюминия и гидроксидом натрия
3) оксидом бериллия и кислородом
4) оксидом железа(II) и оксидом калия
11. Какие вещества из приведённых ниже образуются при взаимодействии гидроксида меди(II) с соляной кислотой?
A) Б) B) Г) Д)
Выберите ответ с набором букв, которые соответствуют образующимся веществам.
1) БГ 2) БВ 3) АД 4) АГ
12. При взаимодействии растворов силиката натрия и соляной кислоты образуется(-ются) хлорид натрия и
1) 2) 3) 4)
13. Верны ли следующие суждения об обращении с растворами щелочей?
А. При попадании раствора щелочи на кожу рук его надо смыть водой.
Б. При попадании раствора щелочи на кожу рук его надо смыть раствором соды.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
14. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
ВЕЩЕСТВА
РЕАКТИВ
А) (р-р) и (р-р)
Б) (р-р) и (р-р)
В) (р-р) и (р-р)
1) лакмус (р-р)
2) (р-р)
3) (р-р)
4) (р-р)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
15. На какой диаграмме распределение массовых долей элементов соответствует ?
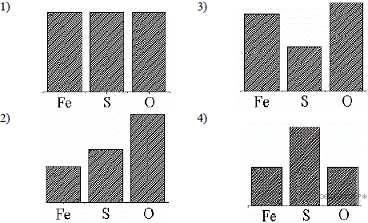
1) 1 2) 2 3) 3 4) 4
16. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
В ряду химических элементов
1) увеличивается заряд ядер атомов
2) возрастают кислотные свойства образуемых гидроксидов
3) увеличивается число электронных уровней
4) уменьшается электроотрицательность
5) возрастает атомный радиус
17. Для этилена верны следующие утверждения:
1) составу молекулы соответствует общая формула
2) является непредельным углеводородом
3) атомы углерода в молекуле соединены одинарной связью
4) вступает в реакции присоединения
5) при горении образуется углерод и водород
18. Подтвердить качественный состав сульфата железа(II) можно с помощью двух растворов, содержащих соответственно ионы
1) и 2) и 3) и 4) и
19. Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВАПРОДУКТЫ РЕАКЦИИ
A)
1)
Б)
2)
B)
3)
4)
5)
20. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
Определите окислитель и восстановитель
21. Для определения концентрации серной кислоты к её раствору добавляли хлорид бария до прекращения выпадения осадка. Для взаимодействия с 20 г раствора кислоты потребовалось 52 г 10-процентного раствора хлорида бария. Определите массовую долю серной кислоты в исходном растворе.
22. Даны вещества: Cu, NaOH, HCl, AgNO3, MgSO4.
Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид меди (II).
Запишите уравнения проведённых химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
infourok.ru
Химия Огэ 2018 | Fitweb
ОГЭ по химии 2018
Подготовка к ОГЭ по химии
уроки по химии
Химия подготовка
Решение задач по химии
Экзамен по химии
Подготовка к ОГЭ
Обучение онлайн
подготовка к экзамену
лайфхаки для подготовки к ОГЭ
экзамен по химии
ОГЭ на сто процентов
подготовка к ОГЭ
Подготовка к ЕГЭ по химии
Подготовка по химии
Интерактивный учебник по химии
Онлайн подготовка химия
Курсы по химии
Дистанционная подготовка химия
репетитор по химии
подготовка к огэ по химии
курсы по химии
задачи по химии
решение задач по химии
Демоверсия ОГЭ по химии
подготовка к экзаменам
покупки к лету
100 баллов на егэ по химии
экзамены по биологии и химии 2018
биология химия огэ
экзамены по биологии и химии
мои результаты экзамена 2018
как я сдала биологию
как я сдала химию
как я сдала экзамены
как я сдала экзамены 2018
мои результаты огэ 2018
мои результаты огэ
подготовка к огэ по химии 2018
школьная химия
химия на отлично
огэ по химии 2018
Демо-версия ОГЭ по химии 2019
таблица менделеева
ОГЭ по химии подготовка
ОГЭ по химии за 7 уроков
онлайн уроки по химии
подготовка к ОГЭ по химии
строение атома
ОГЭ по химии 2019
курсы по химии онлайн
тесты по химии
#огэ #школа #советы
как я сдавала?
огэ по химии 2017
Разбор заданий ОГЭ по химии 2018
Типы связей химия
Как расставлять степени окисления
решение ОГЭ по химии
разборы тестов по химии
пробный тест по химии
химические связи
неметаллические свойства
английский язык
как выучить химию
желтая кровяная соль
красная кровяная соль
как понять химию
окраска индикаторов
лайфхаки по запоминанию химии
Арина Воллерт
разбор огэ про химии
огэ по химии часть 2
окислительно-восстановительные реакции
массовая доля вещества
задание №21 из ОГЭ по химии
задание №22 из ОГЭ по химии
Демо-версии ЕГЭ по химии 2018
подготовка к огэ
массовая доля растворенного вещества в растворе
курсы по подготовке к егэ по химии
#огэ #школа #экзамен #россия #2018
егэ русский язык
как сдать егэ на 100
как получить 100 на егэ
самые сложные задания на егэ
как сдать егэ на 100 баллов
поступление 2018
100 баллов на егэ
коля паничкин
егэ химия демо
егэ химия видеоуроки
егэ химия видео
подготовка к егэ химия
подготовка к егэ по химии
видеоуроки егэ
химия видеоуроки
егэ подготовка
подготовка к егэ
fitweb.me
