1. Предмет органической химии
ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
Органическая химия – наука, изучающая соединения углерода, называемые органическими веществами. В связи с этим органическую химию называют также химией соединений углерода.
Важнейшие причины выделения органической химии в отдельную науку заключаются в следующем.
1.Многочисленность органических соединений по сравнению с неорганическими.
Число известных органических соединений (около 6 млн.) значительно превышает число соединений всех остальных элементов периодической системы Менделеева. В настоящее время известно около 700 тыс. неорганических соединений, примерно 150 тыс. новых органических соединений получают сейчас в один год. Это объясняется не только тем, что химики особенно интенсивно занимаются синтезом и исследованием органических соединений, но и особой способностью элемента углерода давать соединения, содержащие практически неограниченное число атомов углерода, связанных в цепи и циклы.
2. Органические вещества имеют исключительное значение как вследствие их крайне многообразного практического применения, так и потому, что они играют важнейшую роль в процессах жизнедеятельности организмов.
3. Имеются существенные отличия в свойствах и реакционной способности органических соединений от неорганических, вследствие чего возникла необходимость в развитии многих специфических методов исследования органических соединений.
Предметом органической химии является изучение способов получения, состава, строения и областей применения важнейших классов органических соединений.
2. Краткий исторический обзор развития органической химии
Органическая химия как наука оформилась в начале XIX в., однако знакомство человека с органическими веществами и применение их для практических целей началось еще в глубокой древности. Первой известной кислотой был уксус, или водный раствор уксусной кислоты. Древним народам было известно брожение виноградного сока, они знали примитивный способ перегонки и применяли его для получения скипидара; галлы и германцы знали способы варки мыла; в Египте, Галлии и Германии умели варить пиво.
В Индии, Финикии и Египте было весьма развито искусство крашения при помощи органических веществ. Кроме того, древние народы пользовались такими органическими веществами, как масла, жиры, сахар, крахмал, камедь, смолы, индиго и т. д.
Период развития химических знаний в средние века (приблизительно до XVI в.) получил название периода алхимии. Однако изучение неорганических веществ было значительно более успешным, чем изучение веществ органических. Сведения о последних остались почти столь же ограниченными, как и в более древние века. Некоторый шаг вперед был сделан благодаря совершенствованию методов перегонки. Таким путем, в частности, было выделено несколько эфирных масел и получен крепкий винный спирт, считавшийся одним из веществ, с помощью которых можно приготовить философский камень.
Конец XVIII в. ознаменовался заметными успехами в изучении органических веществ, причем органические вещества начали исследовать с чисто научной точки зрения. В этот период был выделен из растений и описан ряд важнейших органических кислот (щавелевая, лимонная, яблочная, галловая) и установлено, что масла и жиры содержат в качестве общей составной части «сладкое начало масел» (глицерин) и т. д.
Постепенно начали развиваться исследования органических веществ — продуктов жизнедеятельности животных организмов. Так, например, из мочи человека были выделены мочевина и мочевая кислота, а из мочи коровы и лошади — гиппуровая кислота.
Накопление значительного фактического материала явилось сильным толчком к более глубокому изучению органического вещества.
Впервые понятия об органических веществах и об органической химии ввел шведский ученый Берцелиус (1827). В учебнике химии, выдержавшем много изданий, Берцелиус высказывает убеждение, что «в живой природе элементы повинуются иным законам, чем в безжизненной» и что органические вещества не могут образовываться под влиянием обычных физических и химических сил, но требуют для своего образования особой «жизненной силы». Органическую химию он и определял как «химию растительных и животных веществ, или веществ, образующихся под влиянием жизненной силы». Последующее развитие органической химии доказало ошибочность этих взглядов.
В 1828 г. Вёлер показал, что неорганическое вещество — циановокислый аммоний — при нагревании превращается в продукт жизнедеятельности животного организма — мочевину.
В 1845 г. Кольбе синтезировал типичное органическое вещество — уксусную кислоту, использовав в качестве исходных веществ древесный уголь, серу, хлор и воду. За сравнительно короткий период был синтезирован ряд других органических кислот, которые до этого выделялись только из растений.
В 1854 г. Бертло удалось синтезировать вещества, относящиеся к классу жиров.
В 1861 г. А. М, Бутлеров действием известковой воды на параформальдегид впервые осуществил синтез метиленитана — вещества, относящегося к классу Сахаров, которые, как известно, играют важную роль в процессах жизнедеятельности организмов.
Все эти научные открытия привели к краху витализма — идеалистического учения о «жизненной силе».
studfiles.netОрганическая химия — Юнциклопедия
Органическая химия — наука об органических соединениях и их превращениях. Термин «органическая химия» был введен шведским ученым Я. Берцелиусом в начале XIX в. До этого вещества классифицировали по источнику их получения. Поэтому в XVIII в. различали три химии: «растительную», «животную» и «минеральную». В конце XVIII в. французский химик А. Лавуазье показал, что вещества, получаемые из организмов растений и животных (отсюда их название «органические соединения»), содержат в отличие от минеральных соединений лишь немногие элементы: углерод, водород, кислород, азот, а иногда фосфор и серу. Так как углерод непременно присутствует во всех органических соединениях, органическую химию с середины XIX в. часто называют химией соединений углерода.
Способность атомов углерода образовывать длинные неразветвленные и разветвленные цепи, а также кольца и присоединять к ним другие элементы или их группы является причиной разнообразия органических соединений и того, что они по своему числу значительно превосходят неорганические соединения. Ныне известно около 7 млн. органических соединений, а неорганических — примерно 200 тыс.
После работ А. Лавуазье и до середины XIX в. химики вели интенсивный поиск новых веществ в природных продуктах и разрабатывали новые способы их превращения. Особенное внимание уделялось определению элементного состава соединений, выводу их молекулярных формул и установлению зависимости свойств соединений от их состава. Оказалось, что некоторые соединения, обладая одинаковым составом, отличаются по своим свойствам. Такие соединения назвали изомерами (см. Изомерия). Было замечено, что многие соединения в химических реакциях обмениваются остающимися без изменения группами элементов. Эти группы получили наименование радикалов, а учение, пытавшееся представить органические соединения состоящими из таких радикалов,— теории радикалов. В 40—50-х гг. XIX в. предпринимались попытки классифицировать органические соединения по типу неорганических (например, этиловый спирт С2Н5—О—Н и диэтиловый эфир С2Н5—О—С2Н5 относили к типу воды Н—О—Н). Однако все эти теории, так же как и определение элементного состава и молекулярной массы органических соединений, еще не опирались на твердый фундамент достаточно разработанного атомно-молекулярного учения. Поэтому в органической химии существовал разнобой в способах записи состава веществ, и даже такое простое соединение, как уксусная кислота, изображалось разными эмпирическими формулами: С4Н4o4, С8Н804, СгН402, из которых правильной была лишь последняя.
Только после создания русским ученым А. М. Бутлеровым теории химического строения (1861) органическая химия получила прочную научную основу, обеспечившую ее стремительное развитие в последующем. Предпосылками для ее создания послужили успехи в разработке атомно-молекулярного учения, представлений о валентности и химической связи в 50-е гг. XIX в. Эта теория позволила предсказывать существование новых соединений и их свойства. Ученые приступили к систематическому химическому синтезу предсказываемых наукой органических соединений, не встречающихся в природе. Таким образом, органическая химия стала в значительной степени химией искусственных соединений.
В первой половине XIX в. химики-органики занимались синтезом и исследованием главным образом спиртов, альдегидов, кислот и некоторых других соединений — алициклических и бензоидных (см. Алифатические соединения; Алициклические соединения). Из веществ, не встречающихся в природе, были синтезированы производные хлора, иода и брома, а также первые металлоорганические соединения (см. Элемен-тоорганические соединения). Новым источником органических соединений стала каменноугольная смола. Из нее выделены бензол, нафталин, фенол и другие бензоидные соединения, а также гетероциклические соединения — хинолин, пиридин.
Во второй половине XIX в. синтезированы углеводороды, спирты, кислоты с разветвленной углеродной цепью, начались изучение строения и синтез соединений, важных в практическом отношении (индиго, изопрен, сахара). Синтез Сахаров (см. Углеводы) и многих других соединений стал возможен после возникновения стереохимии, продолжившей развитие теории химического строения. Органическая химия первой половины XIX в. была тесно связана с фармацией — наукой о лекарственных веществах.
Во второй половине XIX в. наметился прочный союз органической химии с промышленностью, в первую очередь анилинокрасочной. Перед химиками были поставлены задачи расшифровки строения известных природных красителей (ализарин, индиго и др.), создания новых красителей, а также разработки технически приемлемых способов их синтеза. Так, в 70— 80-х гг. XIX в. возникла прикладная органическая химия.
Конец XIX — начало XX в. ознаменовались созданием новых направлений в развитии органической химии. В промышленном масштабе стал использоваться богатейший источник органических соединений — нефть, и с этим было связано бурное развитие химии алициклических соединений и вообще химии углеводородов (см. Нефтехимия). Появились практически важные каталитические методы превращения органических соединений, созданные П. Сабатьё во Франции, В. Н. Ипатьевым и позднее Н. Д. Зелинским в России (см. Катализ). Теория химического строения значительно углубилась в результате открытия электрона и создания электронных представлений о строении атомов и молекул. Были открыты и разработаны мощные методы физико-химических и физических исследований молекул, в первую очередь рентгеноструктурный анализ. Это позволило выяснить строение, а следовательно, понять свойства и облегчить синтез огромного числа орган! ческих соединений.
С начала 30-х гг. XX в. в связи с возникновением квантовой механики появились вычислительные методы, позволяющие расчетным путем делать заключения о строении и свойствах органических соединений (см. Квантовая химия).
Среди новых направлений химической науки — химия органических производных фтора, получивших большое практическое значение. В 50-х гг. XX в. возникла химия ценовых соединений (ферроцен и др.), представляющая соединительное звено между органической и неорганической химией. В практику химиков-органиков прочно вошло применение изотопов. Еще в начале XX в. были открыты свободно существующие органические радикалы (см. Радикалы свободные), а впоследствии создана химия неполнова-лентных органических соединений — ионов карбония, карбанионов, радикал-ионов, молекулярных ионов (см. Ионы). В 60-х гг. были синтезированы совершенно новые типы органических соединений, например катенаны, в которых отдельные циклические молекулы связаны друг с другом, подобно тому как изображают пять переплетенных олимпийских колец.
Органическая химия в XX в. приобрела огромное практическое значение, особенно для переработки нефти, синтеза полимеров, синтеза и изучения физиологически активных веществ. В результате из органической химии выделились в самостоятельные дисциплины такие ее направления, как нефтехимия, химия полимеров, биоорганическая химия.
Современная органическая химия имеет сложную структуру. Сердцевину ее составляет препаративная органическая химия, занимающаяся выделением из природных продуктов и искусственным приготовлением индивидуальных органических соединений, а также созданием новых методов их получения. Решить эти задачи невозможно без опоры на аналитическую химию, позволяющую судить о степени очистки, гомогенности (однородности) и индивидуальности органических соединений, предоставляющую данные об их составе и строении в изолированном состоянии, а также тогда, когда они выступают в качестве исходных веществ, промежуточных и конечных продуктов реакции. Для этой цели аналитическая химия использует различные химические, физико-химические и физические методы исследования. Сознательный подход к решению задач, стоящих перед препаративной и аналитической органической химией, обеспечивается опорой их на теоретическую органическую химию. Предметом этой науки является дальнейшая разработка теории строения, а также формулирование зависимостей между составом и строением органических соединений и их свойствами, между условиями протекания органических реакций и их скоростью и достижением химического равновесия. Объектами теоретической органической химии могут быть как нереагирующие соединения, так и соединения во время их превращений, а также промежуточные, нестойкие образования, возникающие в ходе реакций.
Такая структура органической химии сложилась под влиянием различных факторов, важнейшим из которых были и остаются запросы практики. Именно этим объясняется то, например, обстоятельство, что в современной органической химии ускоренно развивается химия гетероциклических соединений, тесно связанная с таким прикладным направлением, как химия синтетических и природных лекарственных средств.
yunc.org
Органическая химия на сайте Игоря Гаршина
Органическая химия на сайте Игоря Гаршина Ни одна вещь не возникает, не уничтожается, но каждая составляется из смешения существующих вещей или выделяется из них. (Анаксагор)|
Органическая химия изучает свойства и реакции органических соединений — веществ, построенных на основе «углеродного скелета». Наибольшее количество соединений углерод образует с так элементами-органогенами: H, N, O, S, P. Способность углерода соединяться с большинством элементов и образовывать молекулы различного состава и строения обусловливает многообразие органических соединений. Название «органические соединения» связано со словом «организм»: из этих соединений в основном состоят все живые организмы. Бурное развитие органической химии началось после создания выдающимся русским химиком А.М. Бутлеровым ее теоретической основы – структурной теории, основная идея которой в том, что свойства органических соединений зависят не только от их состава, но и от структуры, т.е. последовательности связи атомов в молекуле. А.М. Бутлеров ввел понятие изомеров. Изомеры — это варианты веществ с одинаковым молекулярным составом и массой, но с разной структурой и потому с разными свойствами. Именно возможность построения из одних и тех же немногих элементов большого числа изомерных структур объясняет существование огромного количества органических соединений (их более пяти миллионов, тогда как неорганических – около пятисот тысяч). Конец ХIХ века был периодом триумфального шествия органического синтеза; в эти годы были впервые получены анилиновые красители, взрывчатые органические вещества, многие лекарства. |
Простые «органические» соединения могут образовываться абиогенно (даже в космосе), сложные — результат жизнедеятельности биоты. Абиогенную (пребиотическую) эволюцию неорганических соединений в органические изучет эволюционная химия. Химическая эволюция закономерно приводит к образованию самокаталитических веществ и дальнейшему биогенезу.
Разделы страницы о химии органических соединений:
- Органические вещества
- Химия элементоорганических соединений
- Химия полимеров
Органические вещества
Основными классами органических соединений являются:
-
Углеводороды — соединения, состоящие только из атомов углерода и водорода, которые делятся на:
- Насыщенные — не содержат кратные связи в своей структуре.
- Ненасыщенные — имеют в своём составе хотя бы одну двойную и/или тройную связь.
- С открытой цепью.
- С замкнутой цепью — содержат цикл — это алканы, алкены, алкины, диены, циклоалканы, арены.
-
Соединения с гетероатомами в функциональных группах —
соединения, в которых углеродный радикал R связан с функциональной группой.
По характеру функциональных групп они делятся на:
- Галогенсодержащие.
- Спирты, фенолы.
- Простые эфиры (этеры).
- Сложные эфиры (эстеры).
- Соединения, содержащие карбонильную группу.
- Альдегиды.
- Кетоны.
- Хиноны.
- Соединения, содержащие карбоксильную группу (карбоновые кислоты, сложные эфиры).
- Серосодержащие соединения.
- Азотсодержащие соединения.
- Металлоорганические соединения.
- Гетероциклические — содержат гетероатомы в составе кольца. Различаются по числу атомов в цикле, по виду гетероатома, по количеству гетероатомов в цикле.
- Органического происхождения — как правило соединения очень сложной структуры, зачастую принадлежат сразу к нескольким классам органических веществ, часто полимеры. Из-за этого их сложно классифицировать и их выделяют в отдельный класс веществ.
- Полимеры — вещества очень большой молекулярной массы, которые состоят из периодически повторяющихся фрагментов — мономеров.
Химия полимеров
В ХХ веке начала интенсивно развиваться и другая область органической химии – химия полимеров. Полимеры — это длинноцепочечные структуры, состоящие из повторяющихся звеньев, число которых может достигать десятков и даже сотен тысяч. Основной элемент, входящий в органические молекулы – углерод – в отличие от всех других химических элементов способен образовывать длинные цепочки. Такие большие молекулы называют макромолекулами. К полимерам относятся все пластмассы, синтетические каучуки, без которых было бы невозможно развитие автомобильной промышленности и, наконец, искусственные (на природной основе) и синтетические волокна.
ХХ век по праву можно назвать не только веком выхода в космос и освоения ядерной энергии, но также и веком полимеров. Были синтезированы десятки тысяч новых веществ с полезными человеку свойствами, которых не создала природа. Оборотной стороной этих успехов полимерной химии явилось возникновение проблемы утилизации отходов производства и быта.
Химия элементоорганических соединений
В ХХ веке появился еще один молодой раздел химии – химия элементоорганических соединений. Это соединения, в состав которых, кроме углерода, водорода, кислорода, азота и серы входят кремний, фтор, бор, а также некоторые металлы. На основе кремнийорганических соединений созданы полимеры, обладающие уникальными свойствами, что делает их незаменимыми в авиации и энергетике. Фторорганические соединения обладают исключительной устойчивостью даже в кислотах и щелочах, из них изготавливают всевозможные покрытия (фторопласты). Некоторые металлоорганические соединения (например, ферроцен) используют в качестве лекарств и кровезаменителей.
Создателем школы элементоорганической химии, внесшим огромный вклад в развитие этого раздела химической науки, был выдающийся русский ученый академик Александр Николаевич Несмеянов (1899-1980).
|
Ключевые слова для поиска сведений об органической химии и органических веществах: На русском языке: органическая химия, элементы-органогены, углеродный скелет, полимеры, углеводороды; На английском языке: organic chemistry. |
|
www.garshin.ru
Конспект Предмет органической химии | СТУДЕНТОРИЙ
Органическая химия
Понятие органической химии и причины её выделения в самостоятельную дисциплину
Органическая химия – химия углеводородов и их производных, т. е. продуктов, образующихся при замене водорода в молекулах этих веществ другими атомами или группами атомов.
Признаки органических веществ:
- Содержат углерод в валентности 4
- Горят или разлагаются с образованием углеродсодержащих продуктов
- Связь в молекуле, как правило, ковалентные
Причины выделения в самостоятельную дисциплину органическую химию:
- Многообразие органических соединений
- Многочисленность органических соединений
- Специфическое строение и свойства органических соединений
- Большое практическое значение соединений углерода: нефть и способы её переработки
Причины многообразия органических соединений:
- Соединение атомов углерода в цепи различной длины
- Разный характер углеродных цепей: прямые, разветвленные циклические
- Способность атома углерода образовывать простые и кратные связи друг с другом и другими атомами
- Множество элементов, входящих в состав органических соединений
- Изомерия
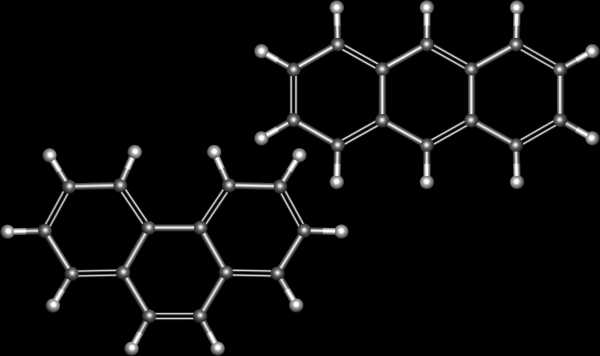
Изомеры – вещества одинакового качественного и количественного состава (т.е. имеющие одинаковую суммарную формулу), но разного строения, следовательно, различными физическими и химическими свойствами.
Фенантрен (справа) и антрацен (слева) – структурные изомеры.
Краткий очерк развития органической химии
Первый период развития органической химии, называемый эмпирическим (с середины XVII до конца XVIII века), охватывает большой промежуток времени от первоначального знакомства человека с органическими веществами до возникновения органической химии как науки. В этот период познание органических веществ, способов их выделения и переработки происходило опытным путем. По определению знаменитого шведского химика И. Берцелиуса, органическая химия этого периода была «химией растительных и животных веществ». К концу эмпирического периода были известны многие органические соединения. Из растений были выделены лимонная, щавелевая, яблочная, галловая, молочная кислоты, из мочи человека – мочевина, из мочи лошади – гиппуровая кислота. Обилие органических веществ послужило стимулом для углубленного изучения их состава и свойств.
Следующий период, аналитический (конец XVIII – середина XIX века), связан с появлением методов установления состава органических веществ. Важнейшую роль в этом сыграл открытый М. В. Ломоносовым и А. Лавуазье закон сохранения массы (1748), положенный в основу количественных методов химического анализа.
Именно в этот период было установлено, что все органические соединения содержат углерод. Кроме углерода, в составе органических соединений были обнаружены такие элементы, как водород, азот, сера, кислород, фосфор, которые в настоящее время называют элементами-органогенами. Стало ясно, что органические соединения отличаются от неорганических прежде всего по составу. К органическим соединениям существовал тогда особое отношение: их продолжали считать продуктами жизнедеятельности растительных или животных организмов, которые можно получить только с участием нематериальной «жизненной силы». Эти идеалистические воззрения были опровергнуты практикой. В 1828 г. немецкий химик Ф. Велер синтезировал органическое соединение мочевину из неорганического цианата аммония.
С момента исторического опыта Ф. Велера начинается бурное развитие органического синтеза. И. Н. Зинин восстановлением нитробензола получил анилин, положив тем самым начало анилинокрасочной промышленности (1842). А. Кольбе синтезировал уксусную кислоту (1845). М, Бертло – вещества типа жиров (1854). А. М. Бутлеров – первое сахаристое вещество (1861). В наши дни органический синтез составляет основу многих отраслей промышленности.
Важное значение в истории органической химии имеет структурный период (вторая половина XIX – начало XX века), ознаменовавшийся рождением научной теории строения органических соединений, основоположником которой был великий русский химик А. М. Бутлеров. Основные положения теории строения имели большое значение не только для своего времени, но служат научной платформой и для современной органической химии.
В начале XX века органическая химия вступила в современный период развития. В настоящее время в органической химии для объяснения ряда сложных явлений используются квантово-механические представления; химический эксперимент все больше сочетается с использованием физических методов; возросла роль различных расчетных методов. Органическая химия превратилась в такую обширную область знаний, что от нее отделяются новые дисциплины – биоорганическая химия, химия элементоорганических соединений и др.
Теория химического строения органических соединений А. М. Бутлерова
Решающая роль в создании теории строения органических соединений принадлежит великому русскому ученому Александру Михайловичу Бутлерову. 19 сентября 1861 года на 36-м съезде немецких естествоиспытателей А.М.Бутлеров обнародовал ее в докладе «О химическом строении вещества».
Основные положения теории химического строения А.М.Бутлерова:
- Все атомы в молекуле органического соединения связаны друг с другом в определенной последовательности в соответствии с их валентностью. Изменение последовательности расположения атомов приводит к образованию нового вещества с новыми свойствами. Например, составу вещества С2Н6О отвечают два разных соединения: диметиловый эфир (СН3-О-СН3) и этиловый спирт (С2Н5ОН) – смотрите Изомерия.
- Свойства веществ зависят от их химического строения. Химическое строение – это определенный порядок в чередовании атомов в молекуле, во взаимодействии и взаимном влиянии атомов друг на друга – как соседних, так и через другие атомы. В результате каждое вещество имеет свои особые физические и химические свойства. Например, диметиловый эфир – это газ без запаха, нерастворимый в воде, t°пл. = -138°C, t°кип. = 23,6°C; этиловый спирт – жидкость с запахом, растворимая в воде, t°пл. = -114,5°C, t°кип. = 78,3°C.
Данное положение теории строения органических веществ объяснило явление изомерии, широко распространенное в органической химии. Приведенная пара соединений – диметиловый эфир и этиловый спирт – один из примеров, иллюстрирующих явление изомерии. - Изучение свойств веществ позволяет определить их химическое строение, а химическое строение веществ определяет их физические и химические свойства.
- Атомы углерода способны соединятся между собой, образовывая углеродные цепи различного вида. Они могут быть как открытыми, так и замкнутыми (циклическими), как прямыми, так и разветвленными. В зависимости от числа связей, затрачиваемых атомами углерода на соединение друг с другом, цепи могут быть насыщенными (с одинарными связями) или ненасыщенными (с двойными и тройными связями).
- Каждое органическое соединение имеет одну определенную формулу строения или структурную формулу, которую строят, основываясь на положении о четырехвалентном углероде и способности его атомов образовывать цепи и циклы. Строение молекулы как реального объекта можно изучить экспериментально химическими и физическими методами.
А.М.Бутлеров не ограничился теоретическими объяснениями своей теории строения органических соединений. Он провел ряд экспериментов, подтвердив предсказания теории получением изобутана, трет. бутилового спирта и т.д. Это дало возможность А.М.Бутлерову заявить в 1864 году, что имеющиеся факты позволяют ручаться за возможность синтетического получения любого органического вещества.
studentoriy.ru
ХИМИЯ ОРГАНИЧЕСКАЯ | Энциклопедия Кругосвет
Содержание статьиХИМИЯ ОРГАНИЧЕСКАЯ – раздел химической науки, изучающий углеводороды – вещества, содержащие углерод и водород, а также различные производные этих соединений, включающие атомы кислорода, азота и галогенов. Все такие соединения называют органическими.
Органическая химия возникла в процессе изучения тех веществ, которые добывались из растительных и животных организмов, состоящих в основной своей массе из органических соединений. Именно это определило чисто историческое название таких соединений (организм – органический). Некоторые технологии органической химии возникли еще в глубокой древности, например, спиртовое и уксуснокислое брожение, использование органических красителей индиго и ализарина, процессы дубления кожи и др. В течение долгого времени химики умели лишь выделять и анализировать органические соединения, но не могли получать их искусственно, в результате чего возникло убеждение, что органические соединения могут быть получены только с помощью живых организмов.
Начиная со второй половины 19 в. методы органического синтеза стали интенсивно развиваться, что позволило постепенно преодолеть устоявшееся заблуждение. Впервые синтез органических соединений в лаборатории удалось осуществить Фридриху Велеру (в период 1824–1828), при гидролизе дициана он получил щавелевую кислоту, выделяемую до этого из растений, а при нагревании циановокислого аммония за счет перестройки молекулы (см. ИЗОМЕРИЯ) получил мочевину – продукт жизнедеятельности живых организмов (рис. 1. Первые синтезы органических соединений).
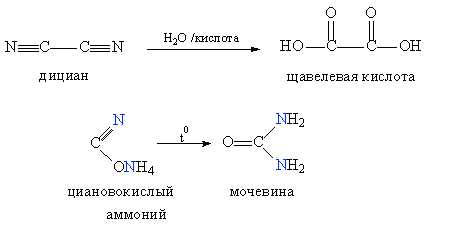
Сейчас многие из соединений, присутствующих в живых организмах, можно получить в лаборатории, кроме того, химики постоянно получают органические соединения, не встречающиеся в живой природе.
Становление органической химии как самостоятельной науки произошло в середине 19 в., когда благодаря усилиям ученых-химиков, стали формироваться представления о строении органических соединений. Наиболее заметную роль сыграли работы Э.Франкланда (определил понятие валентности), Ф.Кекуле (установил четырехвалентность углерода и строение бензола), А. Купера (предложил используемый и поныне символ валентной черты, соединяющей атомы при изображении структурных формул), А.М.Бутлерова (создал теорию химического строения, в основе которой лежит положение, согласно которому свойства соединения определяются не только его составом, но и тем, в каком порядке соединены атомы).
Следующий важный этап в развитии органической химии связан с работами Я.Вант-Гоффа, который изменил сам способ мышления химиков, предложив перейти от плоского изображения структурных формул к пространственному расположению атомов в молекуле, в итоге химики стали рассматривать молекулы как объемные тела.
Представления о природе химической связи в органических соединениях впервые сформулировал Г.Льюис, предположивший, что атомы в молекуле связаны с помощью электронов: пара обобщенных электронов создает простую связь, а две или три пары образуют, соответственно, двойную и тройную связь. Рассматривая распределение электронной плотности в молекулах (например, ее смещение под влиянием электроотрицательных атомов O, Cl и др.) химики смогли объяснить реакционную способность многих соединений, т.е. возможность их участия в тех или иных реакциях.
Учет свойств электрона, определяемых квантовой механикой, привел к развитию квантовой химии, использующей представления о молекулярных орбиталях. Сейчас квантовая химия, показавшая на многих примерах свою предсказательную силу, успешно сотрудничает с экспериментальной органической химией.
Небольшую группу соединений углерода не относят к органическим: угольная кислота и ее соли (карбонаты), цианистоводородная кислота HCN и ее соли (цианиды), карбиды металлов и некоторые другие соединения углерода, которые изучает неорганическая химия.
Главная особенность органической химии – исключительное разнообразие соединений, которое возникло из-за способности атомов углерода соединяться друг с другом в практически неограниченном количестве, образуя молекулы в виде цепочек и циклов. Еще большее разнообразие достигается за счет включения между атомами углерода атомов кислорода, азота и др. Явление изомерии, благодаря которому молекулы, обладающие одинаковым составом, могут иметь различное строение, дополнительно увеличивает многообразие органических соединений. Сейчас известно свыше 10 млн. органических соединений, причем их количество ежегодно увеличивается на 200–300 тысяч.
Классификация органических соединений.
В качестве основы при классификации приняты углеводороды, их считают базовыми соединениями в органической химии. Все остальные органические соединения рассматривают как их производные.
При систематизации углеводородов принимают во внимание строение углеродного скелета и тип связей, соединяющих атомы углерода.
I. АЛИФАТИЧЕСКИЕ (aleiphatos. греч. масло) углеводороды представляют собой линейные или разветвленные цепочки и не содержат циклических фрагментов, они образуют две крупные группы.
1. Предельные или насыщенные углеводороды (названы так потому, что не способны что-либо присоединять) представляют собой цепочки атомов углерода, соединенных простыми связями и окруженных атомами водорода (рис. 1). В том случае, когда цепочка имеет разветвления, к названию добавляют приставку изо. Простейший насыщенный углеводород – метан, с него начинается ряд этих соединений.

Рис. 2. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
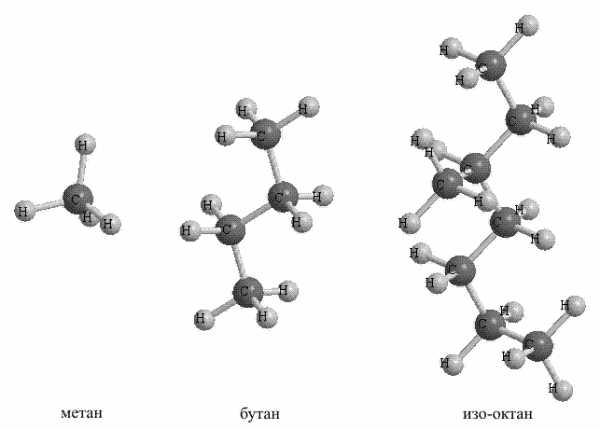
Основные источники насыщенных углеводородов – нефть и природный газ. Реакционная способность насыщенных углеводородов очень низкая, они могут реагировать только с наиболее агрессивными веществами, например, с галогенами или с азотной кислотой. При нагревании насыщенных углеводородов выше 450 С° без доступа воздуха разрываются связи С-С и образуются соединения с укороченной углеродной цепью. Высокотемпературное воздействие в присутствии кислорода приводит к их полному сгоранию до СО2 и воды, что позволяет эффективно использовать их в качестве газообразного (метан – пропан) или жидкого моторного топлива (октан).
При замещении одного или нескольких атомов водорода какой-либо функциональной (т.е. способной к последующим превращениям) группой образуются соответствующие производные углеводородов. Соединения, содержащие группировку С-ОН, называют спиртами, НС=О – альдегидами, СООН – карбоновыми кислотами (слово «карбоновая» добавляют для того, чтобы отличить их от обычных минеральных кислот, например, соляной или серной). Соединение может содержать одновременно различные функциональные группы, например, СООН и NH2, такие соединения называют аминокислотами. Введение в состав углеводорода галогенов или нитрогрупп приводит соответственно к галоген- или нитропроизводным (рис. 3).
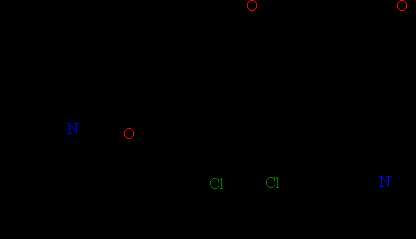
Рис. 4. ПРИМЕРЫ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ с функциональными группами
Все показанные производные углеводородов образуют крупные группы органических соединений: спирты, альдегиды, кислоты, галогенпроизводные и т.д. Поскольку углеводородная часть молекулы имеет очень низкую реакционную способность, химическое поведение таких соединений определяется химическими свойствами функциональных групп –ОН, -СООН, -Cl, -NO2 и др..
2. Ненасыщенные углеводороды имеют те же варианты строения основной цепи, что и насыщенные, но содержат двойные или тройные связи между атомами углерода (рис. 6). Простейший ненасыщенный углеводород – этилен.

Рис. 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
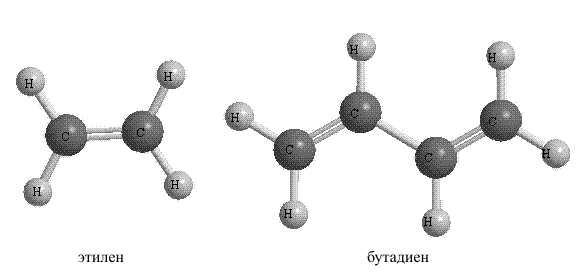
Наиболее характерно для ненасыщенных углеводородов присоединение по кратной связи (рис. 8), что позволяет синтезировать на их основе разнообразные органические соединения.
Рис. 8. ПРИСОЕДИНЕНИЕ РЕАГЕНТОВ к ненасыщенным соединениям по кратной связи
Другое важное свойство соединений с двойными связями — их способность полимеризоваться (рис. 9.), двойные связи при этом раскрываются, в результате образуются длинные углеводородные цепи.
Рис. 9. ПОЛИМЕРИЗАЦИЯ ЭТИЛЕНА
Введение в состав ненасыщенных углеводородов упомянутых ранее функциональных групп так же, как и в случае насыщенных углеводородов, приводит к соответствующим производным, которые также образуют крупные группы соответствующих органических соединений – ненасыщенные спирты, альдегиды и т.д. (рис. 10).
Рис. 10. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ с функциональными группами
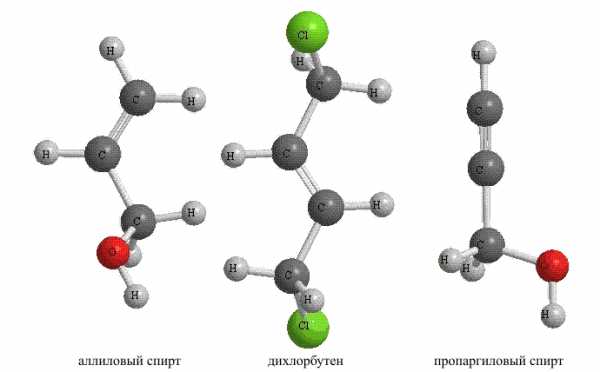
Для показанных соединений приведены упрощенные названия, точное положение в молекуле кратных связей и функциональных групп указывают в названии соединения, которое составляют по специально разработанным правилам.
Химическое поведение таких соединений определяется как свойствами кратных связей, так и свойствами функциональных групп.
II. КАРБОЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ содержат циклические фрагменты, образованные только атомами углерода. Они образуют две крупные группы.
1. Алициклические (т.е. и алифатические и циклические одновременно) углеводороды. В этих соединениях циклические фрагменты могут содержать как простые, так и кратные связи, кроме того, соединения могут содержать несколько циклических фрагментов, к названию этих соединений добавляют приставку «цикло», простейшее алициклическое соединение – циклопропан (рис. 12).

Рис. 12. АЛИЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ
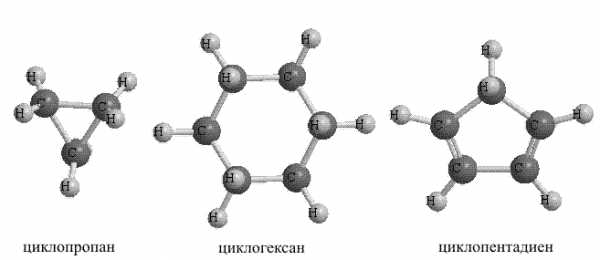
Помимо показанных выше существуют иные варианты соединения циклических фрагментов, например, они могут иметь один общий атом, (так называемые, спироциклические соединения), либо соединяться таким образом, чтобы два или более атомов были общими для обоих циклов (бициклические соединения), при объединении трех и более циклов возможно также образование углеводородных каркасов (рис. 14).

Рис. 14. ВАРИАНТЫ СОЕДИНЕНИЯ ЦИКЛОВ в алициклических соединениях: спироциклы, бициклы и каркасы. В названии спиро- и бициклических соединений указывают тот алифатический углеводород, который содержит такое же общее число атомов углерода, например, в показанном на рисунке спироцикле содержится восемь атомов углерода, поэтому его название построено на основе слова «октан». В адамантане атомы расположены так же, как в кристаллической решетке алмаза, что определило его название (греч. adamantos – алмаз)
Многие моно- и бициклические алициклические углеводороды, а также производные адамантана входят в состав нефти, их обобщенное название – нафтены.
По химическим свойствам алициклические углеводороды близки соответствующим алифатическим соединениям, однако, у них появляется дополнительное свойство, связанное с их циклическим строением: небольшие циклы (3–6-членные) способны раскрываться, присоединяя некоторые реагенты (рис. 15).
Рис. 15. РЕАКЦИИ АЛИЦИКЛИЧЕСКИХ УГЛЕВОДОРОДОВ, протекающие с раскрытием цикла
Введение в состав алициклических углеводородов различных функциональных групп приводит к соответствующим производным – спиртам, кетонам и т.п. (рис. 16).

Рис. 16. АЛИЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ с функциональными группами
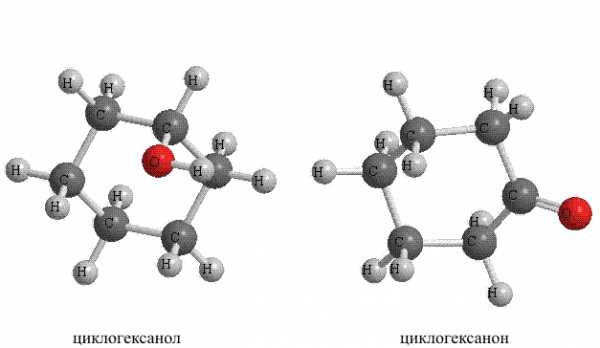
2. Вторую крупную группу карбоциклических соединений образуют ароматические углеводороды бензольного типа, т.е содержащие в своем составе один или несколько бензольных циклов (существуют также ароматические соединения небензольного типа (см. АРОМАТИЧНОСТЬ). При этом они могут также содержать фрагменты насыщенных или ненасыщенных углеводородных цепей (рис. 18).

Рис. 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ.

Существуют группа соединений, в которых бензольные кольца как бы спаяны между собой, это так называемые конденсированные ароматические соединения (Рис. 20).

Рис. 20. КОНДЕНСИРОВАННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
Многие ароматические соединения, в том числе и конденсированные (нафталин и его производные) входят в состав нефти, второй источник этих соединений – каменноугольная смола.
Для бензольных циклов не характерны реакции присоединения, которые проходят с большим трудом и в жестких условиях, наиболее типичны для них реакции замещения атомов водорода (рис.21).
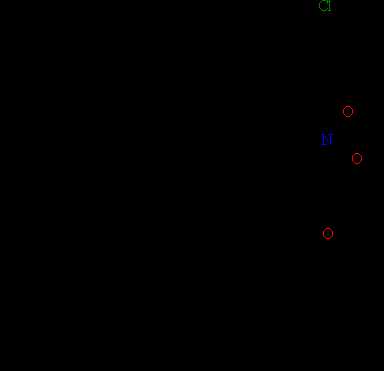
Рис. 21. РЕАКЦИИ ЗАМЕЩЕНИЯ атомов водорода в ароматическом ядре.
Помимо функциональных групп (галогена, нитро- и ацетильной группы), присоединенных к бензольному ядру (рис. 21), можно также ввести иные группы, в результате получаются соответствующе производные ароматических соединений (рис. 22), образующие крупные классы органических соединений – фенолы, ароматические амины и др.
Рис. 22. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ с функциональными группами. Соединения, в которых neгруппа -ОН соединена с атомом углерода в ароматическом ядре, называют фенолами, в отличие от алифатических соединений, где такие соединения называют спиртами.
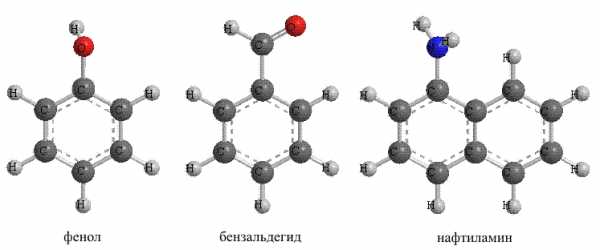
III. ГЕТЕРОЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ содержат в составе цикла (помимо атомов углерода) различные гетероатомы: O, N, S. Циклы могут быть различного размера, содержать как простые, так и кратные связи, а также присоединенные к гетероциклу углеводородные заместители. Существуют варианты, когда гетероцикл «спаян» с бензольным ядром (рис. 24).
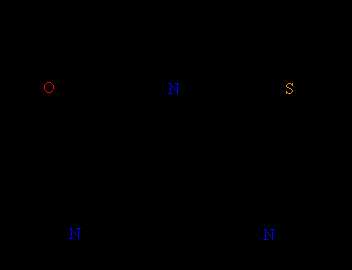
Рис. 24. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ. Их названия сложились исторически, например, фуран получил название от фуранового альдегида – фурфурола, получаемого из отрубей (лат. furfur – отруби). Для всех показанных соединений реакции присоединения затруднены, а реакции замещения проходят достаточно легко. Таким образом, это ароматические соединения небензольного типа.
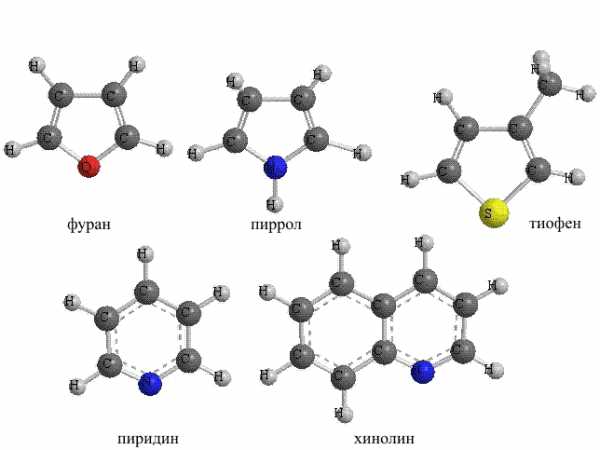
Разнообразие соединений этого класса увеличивается дополнительно за счет того, что гетероцикл может содержать два и более гетероатомов в цикле (рис. 26).
Рис. 26. ГЕТЕРОЦИКЛЫ с двумя и более гетероатомами.
Точно так же, как и рассмотренные ранее алифатические, алициклические и ароматические углеводороды, гетероциклы могут содержать в своем составе различные функциональные группы (-ОН, -СООН, -NH2 и др.), причем гетероатом в цикле в некоторых случаях также можно рассматривать как функциональную группу, поскольку он способен принимать участие в соответствующих превращениях (рис. 27).
Рис. 27. ГЕТЕРОАТОМ N в роли функциональной группы. В названии последнего соединения буква «N» указывает, к какому атому присоединена метильная группа.
Реакции органической химии.
В отличие от реакций неорганической химии, где с высокой скоростью (иногда мгновенно) взаимодействуют ионы, в реакциях органических соединений обычно участвуют молекулы, содержащие ковалентные связи. В результате все взаимодействия протекают гораздо медленнее, чем в случае ионных соединений (иногда десятки часов), часто при повышенной температуре и в присутствии ускоряющих процесс веществ – катализаторов. Многие реакции протекают через промежуточные стадии или в нескольких параллельных направлениях, что приводит к заметному снижению выхода нужного соединения. Поэтому при описании реакций вместо уравнений с числовыми коэффициентами (что традиционно принято в неорганической химии) часто используют схемы реакций без указания стехиометрических соотношений.
Название крупных классов органических реакций часто связывают с химической природой действующего реагента или с типом вводимой в соединение органической группы:
а) галогенирование – введение атома галогена (рис. 8, первая схема реакции),
б) гидрохлорирование, т.е. воздействие HCl (рис. 8, вторая схема реакции)
в) нитрование – введение нитрогруппы NO2 (рис. 21, второе направление реакции)
г) металлирование – введение атома металла (рис. 27, первая стадия)
а) алкилирование – введение алкильной группы (рис. 27, вторая стадия)
б) ацилирование – введение ацильной группы RC(O)- (рис. 27, вторая стадия)
Иногда название реакции указывает на особенности перестройки молекулы, например, циклизация – образование цикла, дециклизация – раскрытие цикла (рис.15).
Крупный класс образуют реакции конденсации (лат. condensatio – уплотнение, сгущение), при которых происходит формирование новых связей С-С с одновременным образованием легко удаляемых неорганических или органических соединений. Конденсацию, сопровождаемую выделением воды, называют дегидратацией. Конденсационные процессы могут также проходить внутримолекулярно, то есть, в пределах одной молекулы (рис. 28).

Рис. 28. РЕАКЦИИ КОНДЕНСАЦИИ
В конденсации бензола (рис. 28) роль функциональных групп выполняют фрагменты С-Н.
Классификация органических реакций не имеет строгого характера, например, показанную на рис. 28 внутримолекулярную конденсацию малеиновой кислоты можно также отнести к реакциям циклизации, а конденсацию бензола – к дегидрированию.
Существуют внутримолекулярные реакции, несколько отличающиеся от конденсационных процессов, когда фрагмент (молекула) отщепляется в виде легко удаляемого соединения без очевидного участия функциональных групп. Такие реакции называют элиминированием (лат. eliminare – изгонять), при этом образуются новые связи (рис. 29).

Рис. 29. РЕАКЦИИ ЭЛИМИНИРОВАНИЯ
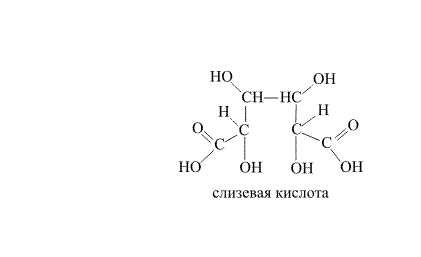
Возможны варианты, когда совместно реализуются несколько типов превращений, что показано далее на примере соединения, в котором при нагревании протекают разнотипные процессы. При термической конденсации слизевой кислоты (рис. 30) проходит внутримолекулярная дегидратация и последующее элиминирование СО2.

Рис. 30. ПРЕВРАЩЕНИЕ СЛИЗЕВОЙ КИСЛОТЫ (получаемой из желудевого сиропа) в пирослизевую кислоту, названную так потому, что получают ее нагреванием слизевой. Пирослизевая кислота представляет собой гетероциклическое соединение – фуран с присоединенной функциональной (карбоксильной) группой. В процессе реакции разрываются связи С-О, С-Н и образуются новые связи С-Н и С-С.
Существуют реакции, при которых происходит перестраивание молекулы без изменения состава (см. ИЗОМЕРИЗАЦИЯ).
Методы исследования в органической химии.
Современная органическая химия помимо элементного анализа использует многие физические методы исследования. Сложнейшие смеси веществ разделяют на составляющие компоненты с помощью хроматографии, основанной на перемещении растворов или паров веществ через слой сорбента. Инфракрасная спектроскопия – пропускание инфракрасных (тепловых) лучей через раствор или сквозь тонкий слой вещества – позволяет установить наличие в веществе определенных фрагментов молекулы, например, групп С6Н5, С=О, NH2 и др.
Ультрафиолетовая спектроскопия, называемая также электронной, несет информацию об электронном состоянии молекулы, она чувствительна к присутствию в веществе кратных связей и ароматических фрагментов. Анализ кристаллических веществ с помощью лучей рентгеновского диапазона (рентгеноструктурный анализ) дает объемную картину расположения атомов в молекуле, подобную тем, что показаны на приведенных выше анимированных рисунках, иными словами, позволяет как бы увидеть строение молекулы своими глазами.
Спектральный метод – ядерный магнитный резонанс, основанный на резонансном взаимодействии магнитных моментов ядер с внешним магнитным полем, дает возможность различить атомы одного элемента, например, водорода, расположенные в различных фрагментах молекулы (в углеводородном скелете, в гидроксильной, карбоксильной или аминогруппе), а также определить их количественное соотношение. Подобный анализ возможен также для ядер С, N, F и др. Все эти современные физические методы привели к интенсивным исследованиям в органической химии – стало возможным быстро решать те задачи, на которые ранее уходили долгие годы.
Некоторые разделы органической химии выделились в крупные самостоятельные области, например, химия природных веществ, лекарственных препаратов, красителей, химия полимеров. В середине 20 в. химия элементоорганических соединений стала развиваться как самостоятельная дисциплина, которая изучает вещества, содержащие связь С-Э, где символ Э обозначает любой элемент(кроме углерода, водорода, кислорода, азота и галогенов). Велики успехи биохимии, изучающей синтез и превращения органических веществ, происходящие в живых организмах. Развитие всех этих областей основано на общих законах органической химии.
Современный промышленный органический синтез включат в себя широкий набор различных процессов – это, прежде всего, крупнотоннажные производства – переработка нефти, газа и получение моторных топлив, растворителей, теплоносителей, смазочных масел, кроме того, синтез полимеров, синтетических волокон, разнообразных смол для покрытий, клеев и эмалей. К малотоннажным производствам относят получение лекарственных препаратов, витаминов, красителей, пищевых добавок и душистых веществ.
Михаил Левицкий
www.krugosvet.ru
История органической химии
Стр 1 из 199Следующая ⇒Череватова Н.К.
Часть I-V
Учебное пособие для студентов вузов
Уральск – 2009
УДК 547
ББК 24.2я 73
Ч 46
Автор:Череватова Н.К. –кандидат химических наук,профессор ЗКГУ им. М. Утемисова
Рецензенты:
Киянский В.В. – академик МАНЭБ и МАЭ, доктор технических наук, профессор
Мендалиева Д.К. – доктор химических наук, профессор
Строкова З.П. – доцент, кандидат химических наук
Костарев А.С. – доцент, кандидат биологических наук
Череватова Н.К.
Ч 46 Органическая химия.Часть I-V: Учебное пособие для студентов вузов. – Уральск: Издательский центр и СМИ ЗКГУ им. М.Утемисова, 2009.- 400 с.
ISBN 9965-748-24-1
Учебное пособие на современном уровне рассматривает взаимосвязь электронного строения веществ с их свойствами. Предложенные к изучению темы отражают свойства веществ, где находит свое место собственная точка зрения автора на некоторые аспекты взаимосвязи свойств веществ с их электонным строением, где присутствуют разные электронные эффекты в органических молекулах.
Учебное пособие рекомендовано студентам вузов, изучающим органическую химию, учителям школ, магистрантам, аспирантам.
ББК 24.2я 73
Ч
ISBN 9965-748-24-1
Ó Череватова Н.К., 2009.
Ó ЗКГУ им. М. Утемисова, 2009.
Содержание
Стр.
1. Введение …………………………………………………………………..4
2. Теория химического строения А.М.Бутлерова …………………..….… 8
3. Электронная теория химической связи …………………………………9
4. Теория направленных валентностей ……………………………………..17
5. Конформационная изомерия ………………………………………….….22
6. Конфигурационная изомерия …………………………………….………26
7. Электронные эффекты в органических соединениях ……………….….30
8. Классификация реакций ……………………………………………….…37
9. Классификация органических соединений ………………………….…. 42
10. Ациклические соединения ……………………………………………………………… 48
11. Предельные углеводороды. Алканы ………………………………………………. 49
12. Непредельные углеводороды ………………………………………………………….. 65
13. Алкены ………………………………………………………………………………………….. 65
14. Алкины. ………………………………………………………………………………………… 95
15. Диеновые углеводороды (алкадиены). …………………………………………. 107
16. Галогенопроизводные углеводородов. Галогеноалканы…………………. 118
17. Спирты. Одноатомные спирты ……………………………………………………… 130
18. Двухатомные спирты ……………………………………………………142
19. Тиолы и тиоэфиры …………………………………………………..…..152
20. Альдегиды и кетоны ……………………………………………..………163
21. Карбоновые кислоты и их производные………………………….….…187
22. Амины. Нитросоединения…………………………………………..…. 224
23. Элементоорганические соединения…………………………………….233
24. Оксикислоты………………………………………………………..……237
25.Оптическая изомерия. Асимметрический синтез…………………..… 243
26.Альдегидо- и кетокислоты. Таутомерия……………………………….. 258
27.Аминокислоты…………………………………………………………. 268
28. Углеводы…………………………………………………………………279
Органическая химия
– это химия соединений углерода, а органические соединения – это вещества, содержащие углерод, за исключением CO, CO2, соли угольной кислоты и т. д., которые изучаются в курсе неорганической химии.
На заре развития органической химии, то есть до середины ХIХ века органической химией называли науку, изучающую вещества, образующиеся в организмах растений и животных. От слова «организм» и произошло название «органическая химия». Это название сохранилось до сих пор, хотя смысл его коренным образом изменился.
Общепринято, что органическая химия – это наука об органических соединениях и законах, которым они подчиняются; она изучает методы получения, строение, превращение и пути практического применения органических веществ.
Органические соединения содержат в своём составе атомы углерода, связанные или между собой, или с иными элементами периодической системы Д.И. Менделеева.
Известно большое число органических соединений (более 5 млн.), число которых постоянно увеличивается, в то время как количество неорганических соединений составляет 850-900 тысяч.
Причина многообразия органических соединений:
1) способность углеродных атомов к образованию четырёх простых, а также кратных связей, как с атомами углерода, так и другими атомами;
2) склонность атомов углерода соединяться в прямые и разветвлённые цепи, состоящие из двух и более (до 1000) атомов углерода.
3) углеродные атомы в виде цепочек могут замыкаться в циклы, образуя карбоциклы или ароматические циклы. Если наряду с атомом углерода в цикле содержится гетероатом ( S, O, P и т. д.), то образуется гетероцикл.
В основе большого числа органических соединений лежат цепочки углеродных атомов, связанные либо с атомами водорода
(CH3 — CH2-CH3 ), либо с другими атомами периодической системы
(S, N, O, P, Si и т. д.), например:(CH3 — CH = O, CH3 — SH, CH3 — NH2). Происходит стремительное увеличение числа и возрастание значения элементоорганических соединений с открытой цепью и циклических, которые выделились в самостоятельные науки, например: химия фторорганических соединений, химия азоторганических соединений, химия кремнийорганических соединений и т. д.
Относительные признаки, характеризующие органические соединения:
1) химическая и термическая неустойчивость. Большинство органических соединений разрушается при температуре 3000-4000C, но фторуглероды устойчивы и при температуре более 5000С;
2) сложность строения, молекулярная масса достигает сотни тысяч;
3) скорость многих органических реакций меньше скорости неорганических реакций;
4) реакции органических соединений протекают часто не в одном, а в нескольких направлениях, образуются смеси различных продуктов, что затрудняет выделение нужных веществ и одновременно даёт возможность получать с наибольшим выходом главный продукт, изменяя скорости отдельных реакций; поэтому в уравнениях реакций ставится не знак «=»,а «→»:
C6H5NO2 + 3H2 → C6H5NH2 + 2H2O;
5) органические соединения имеют, в основном, ковалентную связь;
6) органические соединения являются носителями жизнедеятельности.
История органической химии
История органической химии имеет четыре периода:
· Эмпирический – начинается с середины XVII века, когда органические соединения стали отличать от неорганических. Этот период характерен накоплением органических веществ. Люди научились получать вещества и материалы, не существующие в природе, изучать механизмы химических процессов. Одним из первых методов переработки природных веществ была перегонка. С её помощью из уксуса была получена уксусная кислота (IХ в.), из бродящих жидкостей был получен этиловый спирт (XI в.), а затем из спирта перегонкой с серной кислотой был получен этиловый эфир (ХVI в.).
· Аналитический – начинается с конца XVIII в. с работ Лавуазье и Ломоносова М.В., установивших закон сохранения вещества и положивших начало количественным методам исследования в химии. С этого же времени в химию входит и химический анализ, то есть определение качественного и количественного состава веществ. В аналитический период начинает обособляться органическая химия.
Лавуазье, изучая элементный состав органических соединений, обнаружил элементы: C, O, H, N, S, P, которые позже стали называться органогенами. Например, состав организма человека, весом ≈ 70 кг: О – 45,5кг; Н – 7кг; С – 12,6кг; N – 2,1кг; Р – 700г; К – 200г; Са – 1,5кг; Na – 150г; Fe – 60г; Аl – 60г и другие почти все элементы периодической системы Д.И. Менделеева.
Первая классификация химических соединений была дана в учебнике Лемери в 1675 году. Лемери делил соединения по происхождению на минеральные, растительные и животные. Это не позволяло отделить органические вещества от неорганических, например, янтарная кислота относилась к группе минеральных веществ, так как её получали перегонкой ископаемого янтаря; поташ попадал в группу растительных веществ, а фосфат кальция попадал в группу животных веществ, так как их получали прокаливанием соответственно растительных (древесина) или животных материалов.
В XIX в. в химии господствовало виталистическое учение, сторонником которого был знаменитый шведский химик Берцелиус. Учёные полагали, что органические вещества возникают только в живом организме под влиянием особой «жизненной силы». Это учение тормозило развитие органической химии, а именно, синтез органических соединений. Однако витализм был вскоре опровергнут практикой. Так, немецкий химик Вёлер получил в 1824 г. из неорганических веществ щавелевую кислоту:
(CN)2 +4H2O → HOOC — COOH + 2NH3
дициан
и получил мочевину в 1828 г. из циановокислого аммония:
NH4CNO → H2N — CO — NH2
Вёлер писал своему учителю Берцелиусу: «Я должен Вам заявить, что могу делать мочевину, не нуждаясь при этом в почках и вообще в животном, будь то человек или собака».
Русский учёный Н.Н. Зинин получил в 1842 г. анилин, который ранее получали из растительного сырья, в 1845 г. немецкий химик Кольбе синтезировал уксусную кислоту, а в 1854 г. французский учёный Бертло синтезировал жиры, в 1861 г. русский учёный А.М. Бутлеров получил первое синтетическое сахарное вещество. Гибель витализму принёс успешно развивающийся в первой половине XIX в. основной метод органической химии – метод органического синтеза.
Сначала синтез органических веществ осуществлялся интуитивно. Однако подмечалось сходство многих веществ по свойствам, по реакциям, что дало возможность создать теорию радикалов – первой теории органической химии. Её авторами были Дюма, Либих, Берцелиус. Они полагали, что радикалы играют в органических превращениях роль атомов и не могут изменяться при химических реакциях. Однако практика показала, что в органических радикалах атомы водорода могут замещаться на другие атомы, например, на атомы хлора, и при этом тип химического соединения сохраняется:
CH3Cl + Cl2 → CH2Cl2 + НCl
Авторами были Лоран, Жерар, Дюма. Большинство сторонников этой теории были идеалистами-агностиками. Они исходили из того, что невозможно определить строение вещества опытным путём, можно только классифицировать органические вещества по типам превращений. При такой классификации одно и то же вещество можно было относить к разным типам. Выделялось 5 типов органических соединений: тип водорода, тип хлористого водорода, тип воды, тип аммиака и тип метана.
Н H H N C
Н Cl O H H
H H H
H H
H
Заменив атом водорода на радикал, например, метил, можно соотнести то или иное органическое соединение к какому-либо типу соединений. Например:
(CH3H) (CH3Cl) (CH3OH) (CH3NH2) (CH3 – CH3)
Теория типов искусственна, но она как-то классифицировала большой материал, накопившийся к середине XIX в.. Однако предсказать существование и пути синтеза органических соединений не известных классов она не могла. Органическая химия в то время представляла собой, по выражению Вёлера, «дремучий лес, полный чудесных вещей, огромную чащу без выхода, без конца, куда не осмеливаешься проникнуть … Нужен был фонарь, маяк, чтобы выйти из этого леса». Таким фонарём и явилась теория Бутлерова.
· Структурный период начинается с середины XIX в.. Он характеризуется созданием структурной теории А.М. Бутлерова. В этот период бурно изучается строение, структура органических соединений, получают новые соединения, не существующие в природе, но предсказанные теорией Бутлерова. Сам А.М. Бутлеров синтезировал три изомера пентана, предсказанные структурной теорией.
· Современный период начинается в XX в.. Он характеризуется тесной связью между свойствами и структурой веществ. Для изучения структуры веществ применяются различные физические методы исследования: УФ — , ИК — , ЯМР – спектроскопия. Например, ИК – спектры (инфракрасные) показывают функциональные группы, двойные связи, ароматические кольца:
См-1 700 1700 2000 2800 3600
С6Н6 С = О С = С СН3 ОН
ЯМР – спектры (ядерный магнитный резонанс) показывают химические сдвиги от сигналов протонов (протонный магнитный резонанс), измеряется в миллионных долях (м.д.) или в МГц.
ТМС
7 6 5 4 3 2 1 0 (м.д.)
С6Н6 ОН СН2 СН3 С6Н12
Органическая химия основана на материалистическом мировоззрении. Долгое время это была качественная наука. Сейчас она превратилась в количественную науку, построенную в соответствии с законами внутренней логики, в которой отдельные части объединены тесными внутренними генетическими связями. Она обладает фундаментальной теорией строения, опирающейся на результаты синтетических, физико-химических, квантовомеханических исследований. Огромное число органических соединений укладывается в рамки непрерывно развивающихся теоретических закономерностей.
Объективные законы диалектики убедительно раскрываются на конкретном материале органической химии, которая материалистична по своему существу. Органическая химия изучает реально существующие объекты – химические соединения, представляющие собой дискретные формы вещества: молекулы (мономеры и полимеры), свободные радикалы, ионы и комплексы, и отражает специфические закономерности, присущие данному этапу развития материи, способствуя познанию природы вещества. Химические соединения и их превращения являются одной из важнейших форм движения материи, переходной между неживой и живой природой. Законы диалектики: переход количества в качество, единства и борьбы противоположностей и отрицание отрицания, — лежат в основе органической химии и наглядно проявляются при её изучении, например, изучение гомологических рядов.
Органические соединения составляют основу многих отраслей химической промышленности (пластмассы, синтетические каучуки, резина, моторное топливо, смазочные материалы, растворители, лаки, краски и т. д.) и широко используются в производстве.
Органическая химия связана с биологией, медициной, физикой, математикой и т. д. О связи с медициной М.В. Ломоносов в 1871 г. говорил в труде «Слово о пользе химии»: «Медик без довольного познания химии совершенен быть не может».
Без знаний органической химии невозможно понять глубоко биологические процессы в организме.
mykonspekts.ru
ОРГАНИЧЕСКАЯ ХИМИЯ — Большая Медицинская Энциклопедия
ОРГАНИЧЕСКАЯ ХИМИЯ — раздел химии, естественнонаучная дисциплина, предметом изучения к-рой являются органические соединения, т. е. соединения углерода с другими элементами, а также законы превращения этих веществ; иногда органическую химию определяют как химию углеводородов и их производных.
Влияние О. х. на развитие биологии и медицины очень велико. Все живое построено в основном из органических соединений (см.), и обмен веществ, лежащий в основе жизненных процессов, представляет собой превращения гл. обр. органических соединений. О. х. лежит в основе биохимии (см.) — науки, являющейся одной из естественнонаучных основ медицины. Большинство лекарственных веществ представляет собой органические соединения; поэтому О. х. наряду с физиологией и биохимией является основой фармакологии (см.). Методы О. х. сыграли важную роль в установлении строения нуклеиновых к-т, многих белков и других сложных природных соединении; с их помощью были раскрыты механизмы и регуляция синтеза белков. Благодаря возросшим возможностям органического синтеза были искусственно получены такие сложные природные вещества, как полинуклеотиды с заданным чередованием нуклеотидных звеньев, цианокобаламин и др.
Успехом органич. химии, имеющим принципиальное значение, явилась разработка методов синтеза многих биологически активных полипептидов, в т. ч. ферментов и нек-рых гормонов или их фармакологически активных аналогов, а также многих лекарственных средств.
Кроме того, большое значение приобрели методы О. х. в совр, технологии производства каучуков, пластмасс, синтетических красителей, пестицидов, гербицидов, стимуляторов роста растений.
О. х. изучает тонкое строение органических веществ: порядок соединения атомов в их молекулах, взаимное пространственное расположение атомов в молекулах органических соединений, электронное строение атомов и их связей в органических соединениях. Кроме того, предметом О. х. является изучение органических реакций, в т. ч. их кинетики (см. Кинетика биологических процессов), энергетики и электронных механизмов, а также разработка новых методов синтеза органических веществ в лабораторных и производственных условиях.
Разделы О. х. посвящены изучению отдельных групп органических веществ в соответствии с их классификацией, напр, химия углеводородов, химия аминокислот и т. д., или общетеоретическим вопросам, напр, стереоизомерия органических соединений, механизмы органических реакций, а также практически важным аспектам О. х., напр, химия красителей, химия органических лекарственных средств и т. д.
Органические соединения и нек-рые их свойства были известны людям с древних времен; уже тогда знали о спиртовом и уксусном брожении, крашении индиго и ализарином и т. п.
Начиная с 16 века — периода ятрохимии (см.)— исследования были направлены в основном на выделение и использование различных органических лекарственных веществ: из растений были выделены эфирные масла, приготовлен диэтиловый эфир, сухой перегонкой древесины получены метиловый (древесный) спирт и уксусная к-та, перегонкой янтаря — янтарная к-та. Однако возникновение О. х. как самостоятельной научной дисциплины относится лишь к 19 в. Впервые понятие «органическая химия» было использовано И. Берцелиусом, к-рый называл так химию веществ, образующихся в организме животных и растений. Важными этапами становления О. х. было осуществление первых хим. синтезов органических веществ — щавелевой к-ты и мочевины, показавшее возможность получения органических соединений вне живого организма, без участия «жизненной силы» (см. Витализм). Эти синтезы, а также работы Ю. Либиха, доказавшего, что во всех образующихся в живом организме (органических) веществах содержится углерод, способствовали появлению определения О. х. как химии соединений углерода, предложенного Л. Гмелином. С первой четверти 19 в. начались попытки обобщить фактический материал, имеющийся в распоряжении О. х., в виде тех или иных теорий. Первой такой теорией можно считать теорию радикалов, сформулированную Ж. Гей-Люссаком, согласно к-рой молекулы органических веществ состоят из групп атомов — радикалов, постоянных и неизменных и способных переходить из одного соединения в другое. Такие радикалы, по мнению Ж. Гей-Люссака, могут длительное время существовать в свободном состоянии, а в молекуле они удерживаются благодаря своим разноименным зарядам. Представление о радикалах как группах атомов, способных переходить из одной молекулы в другую, сохранилось и поныне. Однако все остальные положения этой теории оказались ошибочными.
Вслед за теорией радикалов появилась теория типов Жерара (F. Gerard) и Лорана (A. Laurent). По этой теории все органические вещества представляют собой соединения, образованные путем замены определенных атомов в молекуле нек-рых неорганических веществ (напр., воды, аммиака и др.) на органические остатки. Т. о. могут быть получены органические соединения, относящиеся к типам воды (спирты, простые эфиры), типам аммиака (первичные, вторичные и третичные амины) и т. д. Теория типов в свое время сыграла положительную роль, т. к. она позволила создать первую классификацию органических веществ, нек-рые элементы к-рой сохранились и в позднейших классификациях. Однако по мере накопления фактов и знакомства с более сложными веществами теория типов все чаще оказывалась несостоятельной.
Важным этапом в развитии О. х. явилось создание теории строения органических соединений. Одной из предпосылок создания этой теории было установление Кекуле (F. A. Kekule) в 1857 г. постоянной четырехвалентности углерода и открытие Купером (A. Cooper) в 1858 г. способности атомов углерода соединяться друг с другом, образуя цепи. Создателем теории строения органических соединений явился А. М. Бутлеров (1861). Основные положения этой теории заключаются в следующем. Все атомы, образующие молекулу органического вещества, связаны в определенной последовательности; они могут быть связаны одинарной —С—С—, двойной >С=С< или тройной —С-С— связью. От строения молекул, т. е. от порядка соединения атомов и характера связей между ними, зависят свойства вещества; этими положениями объяснялось непонятное ранее явление изомерии (см.). Хим. свойства каждого атома и атомной группы не неизменны, они зависят от других атомов и атомных групп, присутствующих в молекуле. Это положение теории строения органических соединений о взаимном влиянии атомов было развито учеником А. М.Бутлерова — В. В. Марковниковым. Теория А. М. Бутлерова, глубоко материалистическая, дает возможность выбрать наилучшую схему синтеза и по формуле строения, как по чертежу, синтезировать разнообразные органические вещества.
С момента создания теории строения органических соединений начинается интенсивное развитие О. х. Многие разделы О. х. становятся теоретической основой для ряда отраслей промышленности (химия топлива, химия красителей, химия лекарственных средств и т. д.).
В развитии О. х. выдающуюся роль сыграли также H. Н. Зинин, С. В. Лебедев, А. Е. Фаворский, Н. Д. Зелинский, В. М. Родионов, А. Н. Несмеянов, А. П. Орехов и многие другие. Среди зарубежных ученых в области О. х. широко известны Л. Пастер, Э. Фишер, Бертло (Р. E. М. Berthelot), А. Байер, Р. Вилъштеттер, Вудворд (R. В. Woodward) и др.
Под влиянием бурного развития физики в теории О. х. стали широко использоваться принципы квантовой, или волновой механики (см. Квантовая теория). Возникли понятия об орбиталях электрона (пространствах атома, в к-рых вероятность пребывания электрона наиболее велика). Электронные представления в О. х. дали возможность понять и классифицировать разнообразные факты взаимного влияния атомов, в основе к-рого, как выяснилось, лежит перераспределение электронной плотности. Большое внимание в О. х. уделяется изучению электронногомеханизма органических реакций. Эти реакции протекают с образованием свободных радикалов, имеющих атом с неспаренным электроном, магнитно некомпенсированным, а потому активным, или же ионов, несущих положительный или отрицательный заряд (карбокатионов и карбоанионов).
Глубокая связь О. х. с физикой и физической химией (см.) проявляется не только в изучении электронной природы хим. связей, взаимного влияния атомов и электронных механизмов реакций, но и в широкой разработке проблем кинетики и энергетики хим. реакций.
Особенностью О. х. второй половины 20 в. являются ее успехи в расшифровке строения и в синтезе таких сложнейших природных веществ, как белки (см.), нуклеиновые кислоты (см.) и др. Залогом успеха в этой области явилось установление взаимного пространственного расположения атомов в молекулах, т. е. стереохимии (см.) и конформации органических молекул (см. Конформация). Параллельно была решена задача изучения причин оптической изомерии и синтеза оптически активных соединений.
К успехам О. х. следует отнести открытие и изучение новых классов органических соединений, среди к-рых первое место занимают небензольные ароматические соединения (циклопеитадиенильный анион и металлоцены, катион тропилия, азу-лены и др.), нек-рые группы элемент-органических соединений с очень ценными в практическом отношении свойствами.
Во второй половине 20 в. продолжается дальнейшее сближение О. х. с биохимией и биологией, в результате к-рого возник новый раздел химии — биоорганическая химия.
Успехи О. х. стали возможны благодаря широкому использованию наряду с химическими ряда физических методов, к к-рым прежде всего относятся дифракционные методы (рентгенография и электронография), оптическая спектроскопия (в видимой, ультрафиолетовой и инфракрасной областях спектра), магнитная радиоспектроскопия: электронный парамагнитный резонанс (ЭПР), ядерный магнитный резонанс (ЯМР), масс-спектрометрия, определение электрических моментов диполя. Среди названных методов наиболее эффективным по информативности является ядерный магнитный резонанс (см.), в т. ч. его разновидности — протонно-магннтный резонанс и находящий все большее применение метод 13С-ЯМР. Эти методы не только во много раз ускорили расшифровку строения молекул органических соединений, но и позволили создать условия для получения их полной геометрической и энергетической характеристики, а также раскрыть электронные механизмы реакций. В органической химии используют и биохим, методы, напр, строго специфичные ферментативные методы, иммунол, методы и т. п.
С развитием естествознания появились такие новые дисциплины, как молекулярная патология и молекулярная фармакология. Все большее число болезней удается объяснить появлением в тканях измененных молекул органических веществ. Бурно развивающаяся молекулярная фармакология позволяет найти в клетках и охарактеризовать большое число рецепторов, специфически связывающих изучаемое лекарственное вещество. Изучение рецепторов на молекулярном уровне открывает перспективы для поисков новых лекарственных средств. Проникновение О. х. в биологию и медицину позволило вскрыть сущность нек-рых процессов, считавшихся ранее чисто биологическими. Так, было установлено, что наследственные признаки организмов «записаны» в молекулах ДНК в виде определенной последовательности нуклеотидов. О. х. проникла и в самую сложную сферу — в сферу изучения психической деятельности человека. Оказалось возможным одними органическими веществами вызвать у здорового человека галлюцинации, подобные галлюцинациям у психически больных, другими веществами эти галлюцинации снять. Из мозга человека и животных были выделены пептиды, обладающие действием, подобным действию морфина и его аналогов (см. Опиаты эндогенные). Возможно, что нарушение биосинтеза или рецепции этих пептидов лежит в основе патогенеза психических заболеваний, а органический синтез их устойчивых к действию пептидаз крови аналогов будет иметь огромное значение для анестезиологии, психиатрии и т. д.
По-видпмому, самые эффективные достижения следует ожидать именно в тех областях О. х., к-рые граничат с биологией и медициной. Это раскрытие хим. основ злокачественного роста п борьбы со злокачественными опухолями, расшифровка хим. основ памяти, механизма динамики развития и дифференцировки тканей, раскрытие хим. основ иммунитета и т. д. В областях О. х., пограничных с физикой и физической химией, будут продолжаться исследования по более глубокому проникновению в природу хим. связи между атомами в органической молекуле, будут более точно установлены количественные соотношения между строением и реакционной способностью таких молекул, глубже изучены механизмы реакций, в к-рые вступают органические соединения. В СССР научную работу по О. х. проводят НИИ АН СССР: Ин-т органической химии им. Н. Д. Зелинского (ИОХ), Ин-т органической и физической химии им. А. Е. Арбузова (ИОФХ), Ин-т нефтехимического синтеза им. А. В. Топчиева (ИНХС), Ин-т элементоорганических соединений (ИНЭОС), Ин-т биоорганической химии им. М. М. Шемякина, H PI И Сибирского отделения АН СССР: Новосибирский ин-т органической химии (НИОХ), Иркутский ин-т органической химии (ИНОХ), Ин-т химии нефти, а также НИИ республиканских академий — ин-ты органической химии Армянской ССР, Киргизской ССР, УССР, Ин-т тонкой органической химии им. А. Л. Мгджаяна (Арм. ССР), Ин-т физикоорганической химии (БССР), Ин-т физической и органической химии им. П. Г. Меликишвили (Груз. ССР), Ин-т органического синтеза (Латв. ССР) и др.
Национальный комитет советских химиков является членом Международного союза чистой и прикладной химии — IUPAC (International Union of Pure and Applied Chemie), к-рый организует один раз в два года конгрессы, конференции и симпозиумы, в т. ч. и по органической химии.
В связи с общей тенденцией медицины приблизиться к молекулярному уровню медик должен ясно представлять себе строение и пространственную конфигурацию молекул веществ, принимающих участие в метаболизме (нуклеиновых к-т, белков, ферментов, коферментов, углеводов, липидов и т. д.) в норме и патологии, а также строение молекул лекарственных средств.
О. х. является основой для изучения в медвузах и средних мед. учебных заведениях биохимии, фармакологии, физиологии и других дисциплин. Ей посвящен самостоятельный курс или она читается в составе курса по общей химии. Многие данные, полученные в исследованиях по О. х., используются в физической и коллоидной химии, биологии, гистологии, патофизиологии, общей гигиене, курсе профзаболеваний и т. д.
Библиография: Ингольд К. Теоретические основы органической химии, пер. с англ., М., 1973; Крам Д. и X э м-м о н д Дж. Органическая химия, пер. с англ., М., 1964; Матье Ж.-П. и П а-н и ко Р. Курс теоретических основ органической химии, пер. с франц., М., 1975; M о p р и сон Р. и Б о й д Р. Органическая химия, пер. с англ., М., 1974; Несмеянов А. Н. и Несмеянов Н. А. Начала органической химии, т. 1—2, М., 1974; Пальм В. А. Введение в теоретическую органическую химию, М., 1974; Райд К. Курс физической органической химии, пер. с англ., М., 1972; P е-в о А. Я. и 3 e л e н к о в а В. В. Малый практикум по органической химии, М., 1980; Реутов О. А. Теоретические проблемы органической химии, М., 1964; Робертс Дж. и К а с е-р и о М. Основы органической химии, пер. с англ., т. 1—2, М., 1978; С тепа-ненко Б. Н. Курс органической химии, ч. 1—2, М., 1976; он же, Курс органической химии, М., 1979.
Периодические издания — Журнал общей химии, М.— Л., с 1931; Журнал органической химии, М.— Л., с 1965; Химия гетероциклических соединений, Рига, с 1965; Химия природных соединений, Ташкент, с 1965; Bulletin de la Societe chi-mique de France, P., с 1863; Journal of the Chemical Society, Perkin Transaction, I. Organic and Bio-organic Chemistry, II. Physical Organic Chemistry, L., с 1972; Journal of Heterocyclic Chemistry, L., с 1964; Journal of Organic Chemistry, Washington, с 1936; Journal of the Orgariometailic Chemistry, Lausanne, с 1964; Journal of the Society of Organic Synthetic Chemistry of Japan, Tokyo, с 1943; Justus Liebigs Anna-len der Chemie, Weinheim, с 1832; Organic Magnetic Resonance, L., с 1969; Organic Mass Spectrometry, L., с 1968; Organic Preparations and Procedures, N. Y., с 1969; Synthesis, Stuttgart, с 1969; Synthetic Communication, N. Y., с 1971; Tetrahedron, N. Y.— L., с 1957; Tetrahedron Letters, L., с 1959.
Б. H. Степаненко.
xn--90aw5c.xn--c1avg
