Пруста закон — Справочник химика 21
Закон постоянства состава веществ (Ж.-Л. Пруст, 1799 г.) [c.13]Сторонником теории непрерывного изменения состава веществ выступил Бертолле, сторонником скачкообразного — Пруст. В результате полемики, продолжавшейся несколько лет (1801—1807), признание химиков получили взгляды Пруста. Тем самым был установлен второй основной закон химии — закон постоянства состава, заключающийся в том, что каждое химическое соединение имеет вполне определенный и постоянный состав. Как следствие отсюда вытекает, что состав химического соединения,не зависит от способа его получения. [c.18]
Закон постоянства состава. Был открыт французским химиком Ж. Прустом после тщательного анализа многочисленных химических соединений. Закон можно сформулировать следующим образом всякое чистое вещество (химическое соединение), каким бы путем оно ни было получено, имеет строго определенный и постоянный состав (качественный и количественный). Например, вода может быть получена в результате следующих химических реакций
XIX в. накопился уже большой экспериментальный материал, обобщив который французский ученый Ж- Л. Пруст сформулировал закон постоянства состава [c.26]
Формулировка закона постоянных отношений французским химиком Жозефом Луи Прустом (1755—1826 гг.). [c.280]
Закон постоянных отношений, или постоянства состава, открытый работавшим в Испании французом Жозефом Луи Прустом (1755—1862), утвердился в полемике с французским химиком Клодом Луи Бертолле (1748—1822). Последний считал, что направление химической реакции, т. е. состав ее продуктов, зависит не только от природы взаимодействующих веществ, но и от их относительных количеств. Абсолютизируя результаты своих экспериментальных исследований химических равновесий, он утверждал, что все вещества имеют переменный состав, который может меняться непрерывно от одного компонента к другому например, оксиды получаются постепенным насыщением металлов кислородом. В то же время Пруст, используя значительно более точные методы анализа, показал, что на самом деле таких непрершвных переходов нет. На примере карбоната меди, оксидов олова и сурьмы, сульфидов железа в разных степенях окисления, а также других веществ он доказал определенность [c.23]
Более того, Пруст установил, что постоянство соотношений компонентов наблюдается и в ряде других соединений. Он сформулировал общее правило, согласно которому все соединения содержат элементы в строго определенных пропорциях (а не в любых сочетаниях) вне зависимости от условий получения этих соединений. Это правило называется законом постоянства состава, или иногда законом Пруста. (Пруст также показал, что Бертолле, пытаясь доказать, что состав определенных соединений меняется в зависимости от метода их получения, пришел к ошибочным выводам из-за неточности анализов и использования недостаточно чистых исходных соединений.)
В заключение еще раз отметим, что сформулированный Прустом закон постоянства состава Пропорции, в которых два элемента соединяются при образовании определенного химического вида, не способны к непрерывным изменениям — действителен лишь для молекул, состоящих из небольшого числа атомов и настолько мало взаимодействующих между собой, что этим можно пренебречь. Любое кристаллическое вещество, не имеющее молекулярного строения, в большей или меньшей степени должно иметь переменный состав. Причина этого лежит в энергетических закономерностях—проявлении энтропийного фактора (см. с. 124). Полное структурное упорядочение может реализоваться лишь при абсолютном нуле, О К. [c.107]
И только в начале XIX столетия английский ученый Джон Дальтон возвращается к атомам как наименьшим частицам материи и вводит в науку этот термин. Этому предшествовали работы таких замечательных ученых, как Р. Бойль (в книге Химик-скептик он нанес сокрушительный удар по представлениям алхимиков), Дж. Пристли и К. В. Шееле (открытие кислорода), Г. Кавендиш (открытие водорода), А. Л. Лавуазье (попытка составить первую таблицу простых веществ), М. В. Ломоносов (основные положения атомно-молекулярного учения, закон сохранения массы), Ж. л. Пруст (закон постоянства состава) и многие другие. [c.3]
ВИДНО, что Пруст прав. Закон постоянства состава был уточнен и стал краеугольным камнем химии . [c.55]
Выводы Канниццаро были последним звеном в цепи логических рассуждений, которая вела свое начало от Пруста и его закона постоянства состава. Спор был окончен, настало время расчетов. Ученые могли находить точную атомную массу любого элемента, входящего в соединения, плотность паров которых удавалось измерить. Зная атомные массы элементов, можно было вычислять процентный состав новых соединений, что давало возможность однозначно устанавливать их химические формулы. На этой основе было введено понятие моля, которое мы уже сформулировали в гл. 1. Моль определялся как количество вещества в граммах, численно равное его молекулярной массе в шкале Канниццаро (которой мы пользуемся и сегодня разумеется, к нашему времени точность ее стала значительно выше). Отсюда ясно, что моль любого вещества должен содержать одинаковое число молекул. Хотя значение этого числа сначала было неизвестным, ему присвоили название числа Авогадро N в знак запоздалой признательности ученому, внесшему столь большой вклад в развитие химии.
Закон постоянства состава (Пруст, 1808) всякое чистое вещество независимо от способа его получения всегда имеет постоянный качественный и количественный состав. [c.4]
Ж- Пруст тщательно изучил состав и свойства большого числа веществ и сформулировал закон постоянства состава всякое химически чистое (индивидуальное) вещество имеет постоянный состав и свойства. [c.17]
Это утверждение получило название закона постоянства состава Пруста. Спор между Бертолле и Прустом принес большую пользу, потому что многие химики отправились в свои лаборатории доказывать идеи, приверженцами которых они были, а результатом явилось быстрое накопление большого объема знаний о составе химических соединений. Конечно, прав оказался Пруст и все же существуют твердые кристаллические вещества, в которых из-за наличия дефектов кристаллической структуры подлинное отношение атомов не совпадает с предсказываемым идеальной химической формулой. Например, состав сульфида железа может варьировать от Fe, (S до FeS,, в зависимости от способа получения образца. [c.275]
И тем не менее с момента открытия закона Пруста существовали серьезные сомнения в его справедливости. В конце концов, почему закон постоянства состава всегда должен быть справедлив Почему какое-то соединение всегда должно содержать 4 части л и 1 часть у, и почему оно не может содержать, например, 4,1 или 3,9 части х и 1 часть у Если допустить, что материя является сплошной (а не дискретной), то понять это трудно. Почему элементы не могут смешиваться в несколько иных пропорциях
Только на основе закона Ломоносова и новой химической систематики стала возможна постановка проблемы, послужившей в самом начале XIX века предметом спора между Бертолле и Прустом. Сущность проблемы заключалась в том, соединяются ли вещества в некоторых определенных количественных соотношениях, зависящих от их п р и-роды, или же соотношения эти неопределенны, переменны и зависят исключительно от вводимых в реакцию количеств веществ. В первом случае следовало ожидать образования из каких-нибудь двух элементов только немногих соединений, резко отличающихся по составу, во втором—должен был бы получаться ряд таких соединений с постепенно изменяющимся составом. Отсюда вытекало, что в первом случае состав любого данного вещества предполагается вполне определенным и не зависящим от способа его получения, а во втором случае определенность состава исключалась. В общем, следовательно, спор шел о том, происходит ли изменение состава веществ скачками или непрерывно. Вопрос этот является основным для химии, так как химию [c.17]
В начале XIX в. Ж- Пруст в длительном споре с К- Бертолле отстаивал мысль, что вещество независимо от способов получения обладает одним и тем же составом. Это утверждение было сформулировано в закон постоянства состава. Исходя из данных о составе вещества выводилась его химическая формула с постоянным количественным соотношением элементов ( Oj, HjO, СН4). Поэтому соединения постоянного состава были названы стехиометрическими соединениями (стехиометрия от греческого stoi heian — основание, элемент и metreo — мерю). Закон постоянства состава и стехио-метричность соединений долгое время считались незыблемыми. Однако в начале XX в. И. С. Курнаков на основании своих исследований пришел к выводу о существовании нестехиометрических соединений, т. е. характеризующихся переменным составом. Н. С. Курнаков отмечал, что было бы ошибкой считать соединения переменного состава… чем-то редким и исключительным . Соединения постоянного состава Н. С. Курнаков назвал дальтонидами в честь Д. Дальтона, широко применявшего атомно-молекулярную теорию к химическим явлениям. Нестехиометрические соединения были названы в честь К. Бертолле бертоллидами.
С 1797 по 1809 г. Ж. Л. Пруст выполнил большую серию работ, посвященную изучению состава различных оксидов металлов. Он установил, что существуют два оксида железа, содержащие соответственно 27 и 48% кислорода. Эти данные послужили ученому основой для открытия закона постоянства состава. Он писал [c.108]
Однако вопрос о постоянстве состава химических соединений явился предметом семилетней (1801—1807) полемики между Ж- Прустом и К. Бертолле. В результате тщательной экспериментальной проверки восторжествовала точка зрения Пруста — был признан закон постоянства состава каждое индивидуальное химическое соединение независимо от метода его получения имеет вполне определенный и постоянный элементный состав. Однако определенному составу может соответствовать несколько химических соединений. [c.9]
В самом начале XIX в., после горячей дискуссии К. Бертолле с Ж. Прустом, утвердился один из основных законов химии — закон постоянства состава. К давно открытому закону Бойля — Мариотта присоединились другие газовые законы закон Гей-Люссака (1802 г.), закон соединительных весов (1808 г.). На основе дальнейшего изучения свойств газов возникла гипотеза А. Аво-гадро (1811 г.). К концу первого десятилетия XIX в. появились работы Д. Дальтона, о которых Ф. Энгельс впоследствии сказал …новая эпоха в химии начинается с атомистики (следовательно не Лавуазье, а Дальтон — отец современной химии) . На базе атомистических представлений Д. Дальтон в 1806—1808 гг. сформулировал закон кратных отношений.
Близкие закону действия масс идеи содержались уже в работах Бертолле. Он не смог их обобщить и правильно выразить, так как в то время неясна была разница между концентрацией и общим количеством вещества. В результате поражения Бертолле при полемике с Прустом, как это часто бывает, вместе со всем неверным в его идеях было отвергнуто и все верное. Из-за этого закон действия масс и вошел в науку сравнительно поздно. В его разработке участвовал ряд исследователей и современная формулировка этого закона складывалась постепенно. [c.127]
Рассмотрим в качестве примера состав воды она состоит нз водорода и кислорода (качественный состав), причем по массе в воде содержится водорода 11,19%, кислорода 88,81% (количественный состав). Воду можно получить различными способами синте зом из водорода и кислорода, реакцией нейтрализации, из кристаллогидратов и др. Во всех случаях чистая вода, независимо от способа получения, имеет приведенный выше состав. Закон постоянства состава впервые сформулировал французский ученый Пруст (1808). [c.10]
Закон постоянных отношений Пруста. [c.23]
Эти совершенно неизменные пропорции, — писал Ж. Пруст,— эти постоянные атрибуты, характеризующие собой истинные соединения, как природные, так и искусственные,. .. все это, но моему мнению, подвластно химику не больше, чем закон избирательности, господствующий во всех соединениях. Исходя из всего это- [c.108]
Итак, Ж. Л. Пруст четко сформулировал закон постоянства состава химических соединений согласно этому закону их состав не зависит от внешних факторов, например от количества исходных веществ, имевшихся при его образовании, температуры, давления и т. д. [c.109]
Аналитическая химия как научная дисциплина сложилась, по-видимому, на рубеже XVIII и XIX столетий, явившись, по существу, важнейшей экспериментальной базой для установления основных законов химии — закона эквивалентов (1792—1802) Рихтера, закона кратных отношений (1802—1808) Дальтона, закона постоянства состава (1799—1806) Пруста, закона Авогадро (1811) и ряда других законов. Сам факт установления этих законов стал возможным только тогда, когда химики-экспериментаторы научились получать индивидуальные соединения определенной степени чистоты и довольно точно анализировать их содержание. [c.7]
Установленный Прустом закон постоянства состава химических соединений может быть сформулирован так каждое химическое соединение, независимо от споссба его получения, имеет один и тот же постоянный состав. Последующее развитие химии показало, что закон постоянства состава химических соединений, будучи точным и оставаясь справедливым до настоящего времени, имеет строго определенные границы своего приложения. Исследования Д. И. Менделеева, Д. П. Коновалова в области растворов и особенно работы Н. С. Курнакова в области растворов и сплавов позволили прийти к утверждению, что наряду с соединениями постоянного состава, т. е. с определенными химическими соединениями, существует многочисленный класс соединений переменного состава, или неопределенных химических соединений. Открытый Прустом закон постоянства состава приложим только к соединениям постоянного состава и не может быть распространен на соединения переменного состава. В свете этих фактов утверждения Бертолле также были справедливы, так как они относились главным образом к соединениям переменного состава. По предложению Курнакова, соединения постоянного состава называют дальтонидами — в честь Дальтона, а соединения переменного состава бертоллидами — в честь Бертолле, впервые исследовавшего эти соединения. [c.12]
Названные законы были установлены на рубеже XVIII п XIX вв. почти совершенно независимо один от другого в различных странах Европы. Закон постоянства состава был открыт и доказан французскими химиками (Лавуазье, Прустом) закон паев был установлен в работах немецких химиков (Рихтера, Венцеля, Фишера) закон кратных отношений был нащупан (Хиггинсом) и открыт (Дальтоном) в Англии, и еще раньше предвосхищен (Ломоносовым) в России. [c.101]
Последнее утверждение, высказанное итальянским ученым А. Авогадро в 1811 г., вошло в химию под именем закона Авогадро. Однако в начале XIX в. эти воззрения не получили должного признания даже крупные химики того времени Д. Дальтон и И. Берцелиус отрицали возможность существования молекул, состоящих из нескольких одинаковых атомов. Прошло еще полвека, прежде чем на I Мен-сдународном съезде химиков, состоявшемся в Карлсруэ (Германия) в сентябре 1860 г., были окончательно приняты основные химические представления (понятия об атомах и молекулах), зародившиеся в виде философского учения в Древней Греции (Левкипп, Демокрит, Эпикур), впервые развитые в виде научной концепции Д. Дальтоном, подтвержденные опытами Ж. Пруста, Ж. Г е й-Л ю с с а к а и окончательно сформулированные в трудах А. Авогадро и его ученика С. Канниццаро. [c.16]
Рихтер (1791г.), Пруст (1799г.) и Дальтон (1799 и 1802гг.) сформулировали основные законы химической стехиометрии (экспериментальное подтверждение получено путем измерения массы веществ, вступающих в химические реакции) [c.12]
Ж. Пруст, 1801—1808 гг.). Это значит, что соотношения между массами элементов, входящих в состав соединения, постоянны. Закон всегда выполняется для газообрг13ных и жидких веществ. Для вещества, находящегося в твердом состоянии, строго говоря, закон не справедлив. Это связано с тем, что в кристаллической структуре любого твердого вещества всегда, в той или иной мере, имеются пустоты, не заполненные атомами, примесные атомы других элементов и другие отклонения от идеальной структуры. На все это, наряду с температурой, давлением, концентрациями веществ, влияет очень большое число других факторов, связанных уже с технологией получения, выделения и очистки вещества. Так, в соединении висмута с таллием на единицу массы таллия может [c.19]
Закон кратных отношений представляет собой логическое развитие закона постоянства состава. Как выяснилось позже, правы были и Пруст, п Бертолле последний в своих работах значительно опередил свое время, хотя экспериментальные возможности не позволяли ему строго доказать защищаемые положения. Возможности современной науки гораздо шире. За последние 50 лет получены интересные и. многочисленные экспериментальные данные, подтверждающие взгляды Бертолле. При этом закон Пруста не отвергается, но глубже раскрываются его смысл и области прнменения. [c.18]
Н. С. Куриаков — создатель метода физико-химического анализа — и его ученики. Н. С. Куриаков в работе Введение в физико-химиче-ский анализ указал, что идеи Бертолле и, казалось бы, противоположные им представления Пруста и Дальтона подтверждаются данными физико-химического анализа Куриаков отмечал, что обе стороны правы, но точка зрения Бертолле является более общей… Как ни странно на первый взгляд, но именно принципу непрерывности отныне суждено защищать незыблемость закона постоянства состава… . [c.18]
Создание химической атомистики было завершено в XIX в. Подготовительный этап для количественной разработки атомно-молекулярного учения был сделан в результате быстрого развития химии в конце XVIII и начале XIX в. (работы А. Лавуазье, Ж. Пруста, К. Бертолле и др.). Завершением его было открытие законов стехиометрии. Выдающаяся роль здесь т1ринадлежит Дж. Дальтону,, А. Авогадро и др. Дальтон создал химическую атомистику, позволившую теоретически обобщить и выяснить наблюдаемые химические факты и предвидеть явления,- еще не обнаруженные на опыте. Он ввел представление об атомной массе, т. е, специфической массе, характерной для каждого химического элемента. В атомной массе нашли свое выражение мера химического элемента, представляющая собой единство его качественной (химическая индивидуальность) и количественной (величина атомной массы) сторон. Развитие этого представления привело впоследствии к созданию Д. И. Менделеевым периодической системы химических элементов. [c.11]
Краеугольным камнем в учении о стехиометрии явился закон постоянства состава. Честь открытия (1799) и эмпирического обос иования этого закона принадлежит Ж Л. Прусту, который посрел ством воспроизводимых экспериментов доказал, что вне зависимости от способов получения химически индивидуальные сложные те.ча имеют постоянный состав. Так, например, свинец с кис юро-дом образует четыре соединения с содержанием свинца и кислорода соответственно 1) 92,9 и 7,1% 2) 90,7 и 9,3% 3) 89,4 и 10,6% и 4) 86,7 и 13,3%. Переход от одного соединения к другому имеет, гаким образом, дискретный характер. Конечно, и все числа Пруста, равно как и скачки при переходе от одного оксида свинца к другому, оставались бы таинственными, если бы не атомистика Даль тона. [c.61]
Если компоненты А и В химически взаимодействуют между собой и образуют соединение постоянного состава (АВг, А2В3, АВ ИТ. п.), то оно отражается на диаграмме состав — свойство в виде сингулярной, или дальтоновской, точки (М, т, рис. 3, 4). Состав, отвечающий этой точке, является инвариантным для всех свойств, например, для температуры плавления Тпл, температуры кристаллизации Гкр, вязкости Т1 и т. д. (рис. 3). Образующиеся таким путем соединения подчиняются закону постоянства состава Пруста и закону кратных отношений Дальтона. Поэтому Н. С. Курнаковым они названы дальтонидами. В точке М дальтониды представляют собой чистые индивидуальные соединения АВ. В точках, близких к М, это растворы компонентов А и В в соединении АВ, а в точках, отдаленных от М. где концентрация соединения АВ невелика, имеет место раствор этого соединения в избытке того или другого компонента, А или В. В общем же все другие точки по обе стороны от М (и, следовательно, кроме М) отвечают образованию растворов или фаз переменного состава. [c.67]
Первые теории химического процесса. Первые теории, описывающие. химический процесс, появились одновременно с первыми структурными представлениями на граяи ХУНТ и XIX вв. Спор между Бертолле и Прустом явился результатом борьбы за сущест-воваиие этих двух направлений, противопоставленных друг другу. Структурные теории тогда пустили глубокие корни и послужили началом стройного атомно-молекулярного учения. Ростки же кинетических теории, как было сказано в гл. II, увяли, так как появились преждевременно. И тем ие менее почвой для их произрастания, правда более чем полувеком спустя, явились открытия, подтвердившие химическую статику Бертолле, т. е. его идеи об обратимости реакций и о влиянии на ход реакций действующих масс. В 1861 г. Д. И. Менделеев под влиянием результатов изучения реакций омыления сложных эфиров одним из первых осмелился ввести понятие об обратимости реа кций в свой учебник Органическая химия [5]. При этом он заметил, что при суждении о химических процессах никогда не должно забывать закона масс, указанного Бертоллетом [5, с. 285]. [c.111]
В основе контроля чистоты веществ по их свойствам лежит закон постоянства свойств (Пруст, 1806 г.) свойства чистого вещества не зависят от его происхождения и предыдуи ей обработки. Закон этот строго соблюдается только для газов и жидкостей, тогда как у твердых веществ может иметь место изменение некоторых свойств в зависимости от обработки. Поэтому применительно к твердым веществам законом постоянства свойств приходится пользоваться с известной осторожностью. [c.58]
Аналитическая химия сформировалась в современную науку в процессе длительного исторического развития. Становление аналитической химии как науки относят к XIX в. В XVIII в. были открыты законы стехиометрии (И. Рихтер), постоянства состава (Ж. Л. Пруст), сохранения массы вещества (М. В. Ломоносов, А. Л. Лавуазье). В распоряжении химиков-аналитиков имелись различные методы качественного анализа и количественных определений были усовершенствованы процедуры осаждения, отделения, подготовки аналитической формы вещества, заложены основы газового анализа. [c.5]
chem21.info
формулировка Ж. Пруста и современная — урок. Химия, 8–9 класс.
Пример:
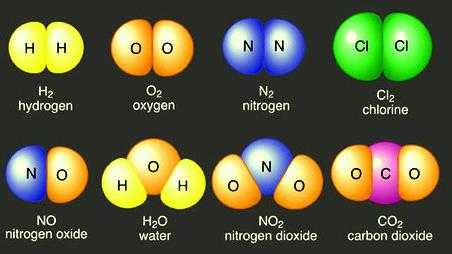
углекислый газ может быть получен в результате сгорания угля, метана или при разложении известняка. Но в любом случае в порции углекислого газа число атомов кислорода будет в два раза больше числа атомов углерода, а массовые доли углерода и кислорода всегда равны \(27,29\) % и \(72,71\) %.
Развитие химии внесло дополнения в закон постоянства состава. Оказалось, что этот закон строго выполняется только для веществ молекулярного строения. Так, в любой молекуле углекислого газа содержится один атом углерода и два атома кислорода, и состав этого вещества изменяться не может.
Молекула углекислого газа
Молекулярное строение имеют все газообразные и жидкие вещества, а также твёрдые вещества с низкими температурами плавления. Постоянный состав имеют: вода, сернистый газ, сероводород, метан, аммиак, кислоты, спирт, сахар, глюкоза и т. д.
Количественный состав веществ немолекулярного строения может несколько изменяться в зависимости от способа получения.
Поваренная соль состоит из атомов натрия и хлора, расположенных в определённом порядке. Этот порядок может нарушаться, поэтому состав разных образцов соли несколько отличается. В поваренной соли, полученной разными способами, на \(1\) атом натрия может приходиться от \(0,99\) до \(1,01\) атомов хлора. Однако условно для простоты обычно указывают округлённые целые числа.
Кристалл поваренной соли
Немолекулярное строение имеют и другие соединения (питьевая сода, мел, оксиды металлов, их соли), песок и некоторые другие вещества. Для этих веществ закон постоянства состава выполняется только приблизительно.
Современная формулировка закона постоянства состава:
Всякое чистое вещество молекулярного строения независимо от места нахождения и способа получения имеет постоянный качественный и количественный состав.
Из закона постоянства состава следует, что при образовании сложного вещества химические элементы соединяются в определённых численных и массовых соотношениях.
www.yaklass.ru
Закон постоянства состава
Уже к началу XIX в. накопилось много данных о составе отдельных веществ и их изменениях. Развитие техники количественных измерений и методов химического анализа позволило определять соотношения элементов в соединениях. Французский химик Ж. Пруст (1754–1826) после тщательнейших экспериментов с рядом веществ установил закон постоянства состава– один из основных законов химии.
Согласно закону постоянства состава, всякое чистое вещество, независимо от способов его получения и нахождения в природе, имеет постоянный качественный и количественный состав.
Это означает, что все соединения содержат элементы в строго определенных весовых пропорциях, независимо от способа получения, Так, например, сернистый газ, полученный сжиганием серы, или действием кислот на сульфиты, или любым другим способом, всегда содержит одну весовую часть серы и одну весовую часть кислорода.
Закон постоянства состава веществ был установлен в результате семилетнего спора между Прустом и его оппонентом, французским химиком К. Бертолле (1748–1822), утверждавшим, что состав соединений зависит от способа их получения.
Бертолле в результате анализа растворов, которые он считал химическими соединениями, сделал общий вывод о существовании химических соединений переменного состава. Получалось, что два элемента могут образовать непрерывный ряд соединений с изменяющимися свойствами и составом.
Пруст утверждал, что состав чистого вещества всегда один и тот же, любое химическое вещество имеет всегда одни и те же свойства, одинаковую температуру плавления, кипения, удельный вес. Пруст заявлял, что природа даже через посредство людей никогда не производит соединений иначе, как только по весу и мере. Одни и те же соединения имеют всегда тождественный состав. Внешний их вид может быть различен, но свойства – никогда. Нет разницы между окисью железа из южного полушария и из северного, хлористое серебро из Перу совершенно тождественно хлористому серебру из Сибири; во всем мире имеется только один хлористый натрий, одна селитра и т.д. Проделав в течение 1799–1887 гг. массу анализов, Пруст доказал справедливость своих выводов.
Дальнейшее развитие химии показало, что закон постоянства состава характеризует соединения с молекулярной структурой, состав же соединений с немолекулярной структурой (атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения.
В начале XX в. русский химик Курнаков, изучая сплавы металлов, открыл соединения переменного состава. В дальнейшем было выяснено, что соединения переменного состава встречаются также среди оксидов, соединений металлов с серой, азотом, углеродом, водородом а также – среди других неорганических веществ, имеющих кристаллическую структуру. Вещества переменного состава были названы бертоллидами, в отличие от соединений постоянного состава –дальтонидов. Для многих соединений переменного состава установлены пределы, в которых может изменяться их состав. Так, в диоксиде титанаTiO2на единицу массы титана может приходиться от0,65до0,67единиц массы кислорода, что соответствует формулеТi O1,9 – 2,0 ( таб.4.1).
Таблица 4.1
-
ДАЛЬТОНИДЫ
(вещества постоянного состава)
примеры соединений
БЕРТОЛЛИДЫ
(вещества переменного состава)
примеры соединений
H2O
H Cl
C Cl4
CO2
Ti O1,9 – 2,0
V O0,9 –1,3
Таким образом, закон постоянства состава, в отличие от закона сохранения массы вещества, не является столь всеобщим. Однако для своего времени закон постоянства состава имел фундаментальное значение. Он привел к мысли о существовании молекул и подтвердил неделимость атомов. В самом деле, почему в сернистом газе весовое отношение серы и кислорода всегда 1:1, а не1,1:0,9или0,95:1.05? Этот результат легко объяснить, если предположить, что атомы серы соединяются с определенным числом атомов кислорода и образуют частицы сернистого газа (эти частицы впоследствии были названы молекулами).
studfiles.net
Закон — пруст — Большая Энциклопедия Нефти и Газа, статья, страница 1
Закон — пруст
Cтраница 1
Закон Пруста выражают и в такой форме: химические элементы соединяются между собой в строго определенных количествах. Именно поэтому и образуются вещества определенного, а не произвольного состава. [1]
Этот закон Пруста оспаривался Бертолле, который считал, что в зависимости от способа получения данного вещества состав его может изменяться в тех или иных пределах; победу в этом споре одержал Пруст, доказавший на основании количественного анализа, что утверждение Бертолле о переменном составе данного соединения является несостоятельным. [2]
Из закона Пруста не следует, что данному составу отвечает только одно единственное химическое соединение. Например, этиловый спирт и диметиловый эфир имеют одинаковый состав, но это разные вещества со своими особыми физическими и химическими свойствами. Таких примеров можно привести много, и все они говорят о том, что свойства веществ зависят не только от их состава, но и от способов соединения атомов друг с другом. [3]
Из закона Пруста ( в его второй формулировке) следует, что существуют такие соотношения масс элементов, при которых последние взаимодействуют друг с другом без остатка. Например, опыты показывают, что 1 г водорода соединяется с 8 г кислорода, с 16 г серы и может быть вытеснен из соединений 23 г натрия или 20 г кальция; в свою очередь 23 г натрия и 20 г кальция могут соединиться без остатка с 8 г кислорода или 16 0 серы. Поэтому можно сказать, что данному количеству одного из элементов соответствует определенное ( прямо пропорциональное) количество другого элемента. [4]
Для подтверждения закона Пруста получим воду несколькими различными способами и выясним, в каком весовом отношении соединены водород и кислород в воде. [5]
Закон постоянства состава ( закон Пруста), который заключается в том, что тела соединяются между собой только в определенных количественных отношениях, так что каждое химическое соединение имеет свой постоянный, неизменный состав. [6]
Размышляя над причиной, по которой элементы соединяются в простых кратных отношениях, Дальтон вспомнил о законе Пруста. [7]
Его заинте — ресовало, очевидно, отклонение примерно в 1 % от вели — f чины 16, — которая требовалась в соответствии с законом Пруста. [8]
В течение полувека взгляды Бертолле не получили подтверждения, поскольку все это время исследовались относительно простые химические соединения, которые вполне удовлетворительно можно было объяснить в рамках закона Пруста. [9]
Более того, Пруст установил, что постоянство соотношений компонентов наблюдается и в ряде других соединений. Он сформулировал общее правило, согласно которому все соединения содержат элементы в строго определенных пропорциях ( а не в любых сочетаниях) вне зависимости от условий получения этих соединений. Это правило называется законом постоянства состава, или иногда законом Пруста. Пруст также показал, что Бертолле, пытаясь доказать, что состав определенных соединений меняется в зависимости от метода их получения, пришел к ошибочным выводам из-за неточности анализов и использования недостаточно чистых исходных соединений. [10]
В своей президентской речи в 1882 г. перед Британской ассоциацией содействия развитию науки [11] он ссылается на опыты по определению относительных плотностей водорода и кислорода. Целью этого исследования было определить, отклоняются ли относительные веса водорода и кислорода от простого целочисленного отношения 1: 16, которое требовалось по закону Пруста. Он специально обратился, несмотря на неуверенность в себе, к этому закону, согласно которому атомные веса элементов, по крайней мере большинства из них, находятся в простом отношении к атомному весу водорода. Он добавил: Некоторые химики энергично осуждают привлечение априорных воззрений при рассмотрении вопроса и утверждают, что достойны внимания только величины, полученные непосредственно в результате эксперимента. Другие, более убежденные в правильности представления, что близость отношений к простым числам не может быть случайностью, и верящие в неизбежное несовершенство наших измерений, считают опытное опровержение закона простых кратных отношений весьма неубедительным, которое уравновешивается, если не перевешивается, априорным утверждением в пользу простоты. Предмет достоин дополнительного исследования; а так как он сейчас привлекает внимание химиков, мы можем ожидать решения этого вопроса нынешним поколением. [11]
Закон кратных отношений представляет собой логическое развитие закона постоянства состава. Как выяснилось позже, правы были и Пруст, и Бертолле; последний в своих работах значительно опередил свое время, хотя экспериментальные возможности не позволяли ему строго доказать защищаемые положения. За последние 50 лет получены интересные и многочисленные экспериментальные данные, подтверждающие взгляды Бертолле. При этом закон Пруста не отвергается, но глубже раскрываются его смысл и области применения. [12]
Страницы: 1
www.ngpedia.ru
Закон постоянства состава: формулировка, примеры, значение
Одно и то же химическое соединение имеет постоянный состав, вне зависимости от места и способа получения образца. К такому выводу одним из первых пришел основатель современной химии, французский ученый А. де Лавуазье. Он сумел определить состав воды, воздуха, органических веществ, считал, что частицы входят в состав веществ в определенных пропорциях. Позже другим химиком из Франции Ж. Л. Прустом был сформулирован закон постоянства состава. Оба исследователя немало сил приложили, чтобы отстоять свои идеи в споре с научным сообществом.

Взгляды на строение вещества на рубеже XVIII и XIX веков
Химические элементы, соединяясь друг с другом в разных соотношениях, образуют множество веществ. Каждое из них характеризуется определенным набором атомов и соотношением их масс. Но до конца XVIII столетия многие ученые считали иначе. Проблема для них заключалась в неточности количественных методик. К тому же позиции атомно-молекулярных воззрений в то время были зыбкими, господствовала теория флогистона — мифического элемента. В установление количественного состава вещества значительный вклад внесли:
- А. де Лавуазье;
- М. В. Ломоносов;
- Ж. Л. Пруст;
- Д. Дальтон.
Заслуга Ж. Л. Пруста заключается в том, что он усовершенствовал количественные методы Лавуазье, строго им следовал. Ученый предложил закон постоянства состава, сохранения соотношений элементов в образцах соединений. Работу в этом направлении Пруст начал еще в конце XVIII века, но признание его труды получили только в 1808 году. Джон Дальтон примерно в это же время ввел представление об атомах и массах этих частиц, кратных соотношениях.
Биография Ж. Л. Пруста
Ученый, предложивший закон постоянства состава, появился на свет 26 сентября 1754 года на западе Франции. Отец Жозефа Луи был аптекарем в городе Анже. Он и приобщил сына к опытам с химическими веществами. Юноша продолжил обучение в Париже, где познакомился с Лавуазье и его научными идеями. В 1776 году Пруст опубликовал свои первые серьезные труды в области химии. С 1799 по 1806 год ученый руководил лабораторией в Мадриде. Во Францию Пруст вернулся в 1806 году. После краткого пребывания в Париже Жозеф Луи отправился в родные места. В 1808–1816 годах получили признание его труды в области изучения состава веществ, в том числе глюкозы. В 1817-м он вышел в отставку и жил в одиночестве до конца своих дней (1826). Пруст был одним из выдающихся ученых своего времени, Рыцарем Почетного легиона, членом Королевской академии наук Неаполя.
Закон постоянства состава. Примеры
Ж. Л. Пруст открыл глюкозу, прославился блестящей победой в научной полемике с соотечественником Бертолле, причиной которой стал закон постоянства состава. Формулировка, предложенная Прустом, гласит: когда несколько элементов образуют химически чистый образец, то он состоит из одних и тех же атомов. Отношения их масс и числа также носят постоянный характер. Примеры:
- Хлорид натрия (NaCl) можно получить при взаимодействии соляной кислоты с гидроксидом натрия. Второй способ — обработка соляной кислотой карбоната натрия. В двух разных химических реакциях получаем соединение, формула которого NaCl. И в первом, и во втором случае вещество содержит 39,33% натрия и 60,66% хлора.
- Кислород (химический знак O) при образовании молекулы воды соединяется с одним и тем же количеством водорода (H). Если взаимодействует 1,11 г водорода с 8,89 г кислорода, то образуется 10 г воды (H2O). Увеличение количества одного из веществ приводит к такому же результату. Не прореагируют атомы того элемента, которого взяли в избытке. Масса воды в этом опыте остается такой же – 10 г, состав ее молекул отражает формула H2O.
Значение открытия постоянства состава
В начале XIX века в теоретической химии утвердились законы, которые соединяют вещества, описывают их соотношения. Изучали качественные и количественные характеристики многие ученые, предложившие универсальные формулировки. Основополагающими были идеи М. В. Ломоносова о сохранении массы в химических превращениях. Установленный Ж. Л. Прустом закон постоянства состава также имеет большое значение для науки и практики. На основании этой закономерности формулу воды записывают только в виде H2O, а состав серной кислоты – H2SO4. Но закон Пруста не имеет такого всеобъемлющего характера, как учение Ломоносова. Поэтому его формулировку уточнили после открытия изотопов. Так называют атомы одного и того же элемента, имеющие разную массу. Соотношение частиц в составе образца является постоянной величиной, но только при условии неизменного изотопного состава. Например, массовый состав водорода и кислорода в обычной и тяжелой воде отличается. Вторая жидкость содержит изотоп водорода — дейтерий. Масса тяжелой воды больше, чем обычной.
Современные взгляды на состав вещества

В соответствии с формулировкой Пруста соотношение масс атомов, составляющих определенное вещество, носит постоянный характер, не зависит от способа получения образца. В начале XX столетия при изучении сплавов металлов были открыты соединения с переменным составом. В этом случае единице веса одного химического элемента могут соответствовать различные массы другого элемента. Например, в соединениях таллия с висмутом на единицу массы первого приходится от 1,2 до 1,8 единицы веса второго элемента. Такие примеры можно найти среди интерметаллических веществ, оксидов, соединений серы, азота, углерода, водорода с металлами. Следовательно, законы, открытые Прустом и Дальтоном, справедливы полностью только в отношении тех веществ, что имеют молекулярное строение. К ним относятся многие кислоты, оксиды, гидриды. Качественная и количественная структура подобных соединений является постоянной. Например, состав воды в атмосфере, Мировом океане, ледниках и живых организмах отражает формула H2O.
fb.ru
Закон постоянства состава — это… Что такое Закон постоянства состава?
- Закон постоянства состава
-
Закон постоянства состава (Ж.Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами. Это один из основных законов химии.
Закон постоянства состава не выполняется для бертоллидов (соединений переменного состава). Однако условно для простоты состав многих бертоллидов записывают как постоянный. Например, состав оксида железа(II) записывают в виде FeO (вместо более точной формулы Fe1-xO).
См. также
Категории:- Основные законы в химии
- Стехиометрия
- Количество вещества
Wikimedia Foundation. 2010.
- Порфирины
- Потенциометрия
Смотреть что такое «Закон постоянства состава» в других словарях:
ЗАКОН ПОСТОЯНСТВА СОСТАВА — один из основных законов химии, открытый в 1799 г. Ж. Л. Прустом; согласно этому закону определённое химически чистое соединение независимо от способа его получения состоит из одних и тех же хим. элементов, имеющих постоянные состав и свойства,… … Большая политехническая энциклопедия
закон постоянства состава — pastoviųjų santykių dėsnis statusas T sritis fizika atitikmenys: angl. law of constant proportions; law of definite composition vok. Gesetz der konstanten Gewichtsverhältnisse, n; Gesetz der konstanten Proportionen, n; Gesetz der konstanten… … Fizikos terminų žodynas
закон постоянства состава — закон паёв … Cловарь химических синонимов I
ПОСТОЯНСТВА СОСТАВА ЗАКОН — ПОСТОЯНСТВА СОСТАВА ЗАКОН: каждое химическое соединение независимо от способа его получения, состоит из одних и тех же элементов, причем отношения их масс постоянны. Строго применим к газообразным и жидким соединениям. Состав кристаллических… … Большой Энциклопедический словарь
ПОСТОЯНСТВА СОСТАВА ЗАКОН — ПОСТОЯНСТВА СОСТАВА ЗАКОН: каждое химическое соединение, независимо от способа его получения, состоит из одних и тех же элементов, причем отношения их масс постоянны. Строго применим к газообразным и жидким соединениям. Состав кристаллических… … Энциклопедический словарь
ПОСТОЯНСТВА СОСТАВА ЗАКОН — в каждом определенном хим. соед., независимо от способа его получения, соотношения масс составляющих элементов постоянны. Сформулирован в нач. 19 в. Ж. Прустом: Соединение есть привилегированный продукт, которому природа дала постоянный состав.… … Химическая энциклопедия
Постоянства состава закон — один из основных законов химии: каждое определённое химическое соединение, независимо от способа его получения, состоит из одних и тех же элементов, причём отношения их масс постоянны, а относительные количества их атомов выражаются… … Большая советская энциклопедия
ПОСТОЯНСТВА СОСТАВА ЗАКОН — один из осн. законов химии, заключающийся в том, что каждое хим. соединение, независимо от способа его получения, состоит из одних и тех же хим. элементов, соединённых друг с другом в одних и тех же отношениях (по массе). П. с. з. был установлен… … Большой энциклопедический политехнический словарь
постоянства состава закон{:} — каждое химическое соединение, независимо от способа его получения, состоит из одних и тех же элементов, причём отношения их масс постоянны. Строго применим к газообразным и жидким соединениям. Состав кристаллических соединений может быть и… … Энциклопедический словарь
ПОСТОЯНСТВА СОСТАВА 3AKОH — каждое хим. соединение, независимо от способа его получения, состоит из одних и тех же элементов, причём отношения их масс постоянны. Строго применим к газообразным и жидким соединениям. Состав кристаллич. соед. может быть и неременным (см.… … Естествознание. Энциклопедический словарь
dic.academic.ru
Закон постоянства состава вещества. Законы сохранения в химии
Химия относится к разряду точных наук, и наряду с математикой и физикой устанавливает закономерности существования и развития материи, состоящей из атомов и молекул. Все процессы, протекающие как в живых организмах, так и среди объектов неживой природы, имеют в своей основе явления превращения массы и энергии. Закон постоянства состава вещества, изучению которого будет посвящена эта статья, и лежит в основе протекания процессов в неорганическом и органическом мире.

Атомно-молекулярное учение
Чтобы понять суть законов, управляющих материальной действительностью, нужно иметь представление о том, из чего она состоит. По словам великого российского ученого М. В. Ломоносова «Во тьме должны пребывать физики и, особенно, химики, не зная внутреннего частиц строения». Именно он в 1741 году, сначала теоретически, а затем и подтвердив опытами, открыл законы химии, служащие основой для изучения живой и неживой материи, а именно: все вещества состоят из атомов, способных образовывать молекулы. Все эти частицы находятся в непрерывном движении.

Открытия и ошибки Дж. Дальтона
Спустя 50 лет идеи Ломоносова стал развивать английский ученый Дж. Дальтон. Ученый выполнил важнейшие расчеты по определению атомных масс химических элементов. Это послужило главным доказательством таких предположений: массу молекулы и вещества можно вычислить, зная атомный вес частиц, входящих в её состав. Как Ломоносов, так и Дальтон считали, что, независимо от способа получения, молекула соединения всегда будет иметь неизменный количественный и качественный состав. Первоначально именно в таком виде был сформулирован закон постоянства состава вещества. Признавая огромный вклад Дальтона в развитие науки, нельзя умолчать о досадных ошибках: отрицании молекулярного строения простых веществ, таких как кислород, азот, водород. Ученый считал, что молекулы есть только у сложных химических веществ. Учитывая огромный авторитет Дальтона в научных кругах, его заблуждения негативно повлияли на развитие химии.

Как взвешивают атомы и молекулы
Открытие такого химического постулата, как закон постоянства состава вещества, стало возможным благодаря представлению о сохранении массы веществ, вступивших в реакцию и образовавшихся после нее. Кроме Дальтона, измерение атомных масс проводил И. Берцелиус, составивший таблицу атомных весов химических элементов и предложивший современное их обозначение в виде латинских букв. В настоящее время массу атомов и молекул определяют с помощью углеродной нанотрубки. Результаты, полученные в данных исследованиях, подтверждают существующие законы химии. Ранее ученые использовали такой прибор, как масс-спектрометр, но усложненная методика взвешивания явилась серьёзным недостатком в спектрометрии.
Почему так важен закон сохранения массы веществ
Сформулированный М. В. Ломоносовым выше названный химический постулат доказывает тот факт, что во время реакции атомы, входящие в состав реагентов и продуктов, никуда не исчезают и не появляются из ничего. Их количество сохраняется без изменения до и после химического процесса. Так как масса атомов константна, данный факт логически приводит к закону сохранения массы и энергии. Более того, ученый декларировал эту закономерность, как всеобщий принцип природы, подтверждающий взаимопревращение энергии и постоянство состава вещества.
Идеи Ж. Пруста как подтверждение атомно-молекулярной теории
Обратимся к открытию такого постулата, как закон постоянства состава. Химия конца 18 – начала 19 века — наука, в рамках которой велись научные споры между двумя французскими учеными, Ж. Прустом и К. Бертолле. Первый утверждал, что состав веществ, образовавшихся в результате химической реакции, зависит главным образом от природы реагентов. Бертолле был уверен, что на состав соединений – продуктов реакции влияет еще и относительное количество взаимодействующих между собой веществ. Большинство химиков в начале исследований поддержали идеи Пруста, который сформулировал их следующим образом: состав сложного соединения всегда постоянный и не завит от того, каким способом оно было получено. Однако дальнейшее исследование жидких и твердых растворов (сплавов) подтвердило мысли К. Бертолле. К этим веществам закон постоянства состава был неприменим. Более того, он не действует для соединений с ионными кристаллическими решетками. Состав этих веществ зависит от методов, которыми их добывают.
Каждое химическое вещество, независимо от способа его получения, имеет постоянный качественный и количественный состав. Эта формулировка характеризует закон постоянства состава вещества, предложенный Ж. Прустом в 1808 году. В качестве доказательств он приводит следующие образные примеры: малахит из Сибири имеет такой же состав, как и минерал, добытый в Испании; в мире есть только одно вещество киноварь, и не имеет значения, из какого месторождения она получена. Таким образом Пруст подчеркивал постоянство состава вещества, независимо от места и способа его добычи.
Не бывает правил без исключений
Из закона постоянства состава следует, что при образовании сложного соединения химические элементы соединяются друг с другом в определённых весовых соотношениях. Вскоре в химической науке появились сведения о существовании веществ, имеющих переменный состав, который зависел от способа получения. Русский ученый М. Курнаков предложил назвать эти соединения бертоллидами, например оксид титана, тяжелая вода, нитрид циркония.

У этих веществ на 1 весовую часть одного элемента приходится различное количество другого элемента. Так, в бинарном соединении висмута с галлием на одну весовую часть галлия приходится от 1,24 до 1,82 части висмута. Позже химики установили, что, кроме соединения металлов друг с другом, вещества, не подчиняющиеся закону постоянства состава, есть в таком классе неорганических соединений, как оксиды. Бертоллиды характерны также для сульфидов, карбидов, нитридов и гидридов.
Роль изотопов
Получив в свое распоряжение закон постоянства вещества, химия как точная наука смогла увязать весовую характеристику соединения с изотопным содержанием элементов, образующих его. Вспомним, что изотопами считают атомы одного химического элемента с одинаковыми протонными, но различными нуклонными числами. Учитывая наличие изотопов, понятно, что весовой состав соединения может быть переменным при условии постоянства элементов, входящих в это вещество. Если элемент увеличивает содержание какого-либо изотопа, то и весовой состав вещества тоже изменяется. Например, обычная вода содержит 11 % водорода, а тяжелая, образованная его изотопом (дейтерием), – 20 %.
Характеристика бертоллидов
Как мы уже выяснили ранее, законы сохранения в химии подтверждают основные положения атомно-молекулярной теории и являются абсолютно верными для веществ постоянного состава – дальтонидов. А бертоллиды имеют границы, в которых возможно изменение весовых частей элементов. Например, в оксиде четырёхвалентного титана на одну весовую часть металла приходится от 0,65 до 0,67 части кислорода. Вещества непостоянного состава не имеют молекулярного строения, их кристаллические решетки состоят из атомов. Поэтому химические формулы соединений лишь отражают границы их состава. У различных веществ они разные. Температура также может влиять на интервалы изменения весового состава элементов. Если два химических элемента образуют между собой несколько веществ – бертоллидов, то для них также неприменим и закон кратных отношений.

Из всех вышеприведенных примеров сделаем вывод: теоретически в химии присутствуют две группы веществ: с постоянным и переменным составом. Наличие в природе этих соединений служит прекрасным подтверждением атомно-молекулярного учения. А вот сам закон постоянства состава уже не является доминирующим в химической науке. Зато он наглядно иллюстрирует историю её развития.
fb.ru