Закон сохранения массы в химии. Открытие закона :: SYL.ru
Закон сохранения массы является основой для расчета физических процессов во всех сферах человеческой деятельности. Его справедливость не оспаривается ни физиками, ни химиками, ни представителями других наук. Этот закон, как строгий бухгалтер, следит за соблюдением точной массы вещества до и после его взаимодействия с другими веществами. Честь открытия этого закона принадлежит русскому ученому М. В. Ломоносову.
Первоначальные представления о составе веществ
Строение вещества на протяжении многих веков оставалось тайной для любого человека. Различные гипотезы будоражили ученые умы и подвигали мудрецов на длительные и бессмысленные споры. Один утверждал, что все состоит из огня, другой отстаивал совершенно иную точку зрения. В массе теорий промелькнула и была незаслуженно забыта теория древнегреческого мудреца Демокрита о том, что все вещества состоят из крошечных, невидимых глазу мельчайших частиц вещества. Демокрит назвал их «атомами», что значит «неделимые». К сожалению, в течение целых 23 веков его предположение было забыто.
Алхимия
В основном научные данные средних веков базировались на предрассудках и различных домыслах. Возникает и широко распространяется алхимия, которая представляла собой свод скромных практических познаний, тесно сдобренных самыми фантастическими теориями. Например, известные умы того времени старались превратить свинец в золото и найти неведомый философский камень, исцеляющий от всех болезней. В процессе поисков постепенно накапливался научный опыт, состоящий из многих необъясненных реакций химических элементов. Например, было выяснено, что многие вещества, названные впоследствии простыми, не распадаются. Таким образом возродилась древняя теория о неделимых частичках материи. Понадобился великий ум, чтобы превратить этот склад информации в стройную и логичную теорию.
Теория Ломоносова
Точным количественным методом исследования химия обязана русскому ученому М. В. Ломоносову. За блестящие способности и упорный труд он получил звание профессора химии и стал членом Российской академии наук. При нем была организованна первая в стране современная химическая лаборатория, в которой и был открыт знаменитый закон сохранения массы веществ.
В процессе изучения течения химических реакций Ломоносов взвешивал исходные химические вещества и продукты, появившиеся после проведения реакции. При этом он открыл и сформулировал закон сохранения массы вещества. В 17 веке понятие массы часто путали с термином «вес». Поэтому массы веществ часто называли «весами». Ломоносов определил, что строение вещества находится в прямой зависимости от частичек, из которых оно построено. Если содержит частички одного сорта, то такое вещество ученый называл простым. При разнородном составе корпускул получается сложное вещество. Эти теоретические данные позволили Ломоносову сформулировать закон сохранения массы.
Определение закона
После многочисленных экспериментов М. В. Ломоносов установил закон, суть которого сводилась к следующему: вес веществ, которые вступили в реакцию, равен весу веществ, которые получились в итоге реакции.
В русской науке данный постулат носит название «Закон сохранения массы веществ Ломоносова».
Это закон был сформулирован в 1748 году, а самые точные эксперименты с реакцией обжига металлов в запаянных сосудах были проведены в 1756 году.
Опыты Лавуазье
Европейская наука открыла закон сохранения массы после публикации описания работ великого французского химика Антуана Лавуазье.  Этот ученый смело применял в своих экспериментах теоретические представления и физические методы того времени, что позволило ему разработать химическую номенклатуру и создать реестр всех известных на то время химических веществ.
Этот ученый смело применял в своих экспериментах теоретические представления и физические методы того времени, что позволило ему разработать химическую номенклатуру и создать реестр всех известных на то время химических веществ.
Своими экспериментами Лавуазье доказал, что в процессе любой химической реакции соблюдается закон сохранения массы веществ, вступающих в соединение. Кроме этого, он расширил распространение закона сохранения на массу каждого из элементов, которые принимали участие в реакции в составе сложных веществ.
Таким образом, на вопрос, кто открыл закон сохранения массы веществ, можно ответить двояко. М. В. Ломоносов первым провел эксперименты, наглядно демонстрирующие закон сохранения, и подвел его под теоретическую базу. А. Лавуазье в 1789 году независимо от русского ученого самостоятельно открывает закон сохранения масс и распространяет его принцип на все элементы, участвующие в химической реакции.
Масса и энергия
В 1905 году великий А. Эйнштейн показал связь между массой вещества и его энергией. Она выражалась формулой:
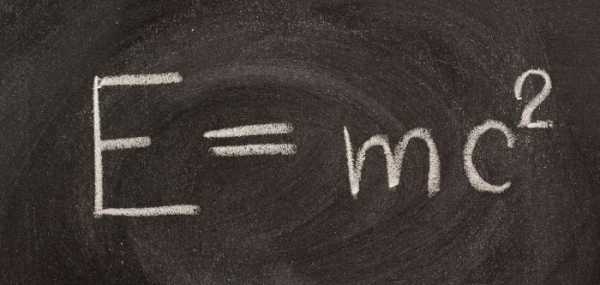
Уравнение Эйнштейна подтверждает закон сохранения массы и энергии. Данная теория утверждает, что всякая энергия имеет массу и изменение этой энергии несет изменение массы тела. Потенциальная энергия любого тела очень велика, и высвободиться она может лишь в особых условиях.
Закон сохранения массы справедлив для любых тел микро- и макромира. Любая химическая реакция принимает участие в преобразовании внутренней энергии вещества. Поэтому при расчете массы веществ, участвующих в химических реакциях, нужно было бы учитывать прирост или убыль массы, вызванных выделением или поглощением энергии в данной реакции. На самом деле в макромире этот эффект настолько незначителен, что такие изменения можно не принимать во внимание.
www.syl.ru
Закон сохранения массы (закон Ломоносова)
Экспериментальное доказательство закона сохранения массы при химических взаимодействиях явилось первым примером количественного химического анализа. Гениальный русский ученый М. В. Ломоносов (1711— 1765), впервые применивший весы и взвешивание для количественного контроля химических превращений и открывший закон сохранения массы, является основоположником количественного анализа. [c.7]Закон сохранения массы и энергии. В 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий естест венный закон распространяется и в самые правила движения, ибо тело, движущее своею силою другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает». Однако до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А.Эйнштейн показал, что между массой и энергией существует взаимосвязь, выражаемая уравнением
М. Б. Ломоносов (1711 — 1765) впервые стал систематически применять весы при изучении химических реакций. Б 1756 г. он экспериментально установил один из основных законов природы — закон сохранения массы вещества, составивший основу количественного анализа и имеющий огромное значение для всей науки. М. В. Ломоносов разработал многие приемы химического анализа и исследования, не потерявшие значения до наших дней [c.8]
Химия как точная наука зародилась еще в эпоху полного господства теории флогистона Более определенным временем ее возникновения можно условно считать середину XVIII в., когда М. В. Ломоносов (1711 — 1765) сформулировал закон сохранения массы вещества в химических процессах и доказал его экспериментально. Он же первый высказал мысль, что при нагревании металл соединяется, как он говорил, с частичками воздуха. Заслуга полного и окончательного ниспровержения флогистонной теории принадлежит великому французскому химику А. Лавуазье (1743—1794), который, изучая горение и обжиг металлов, не только выяснил и сделал очевидной для других роль кислорода в этих явлениях, разрушив тем самым теорию флогистона, но также внес ясность в понятия химического элемента, простого и сложного вещества и независимо от Ломоносова экспериментально установил закон сохранения массы в химических реакциях. Начиная с Лавуазье химия заговорила на современном нам языке. Именно его трудами завершился процесс превращения химии в науку. Если Бойль начал этот процесс, то Лавуазье довел его до конца. [c.22]
Закон сохранения массы. На основании молекулярно-атомистических представлений М. В. Ломоносов сделал вывод Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте . Позднее, применяя точные методы исследования, ученые подтвердили опытным путем, что при химических превращениях общая масса веществ остается неизменной. Этот закон — закон сохранения массы — в настоящее время формулируется так
В связи со сказанным необходимо реабилитировать гения русской науки — Михаила Васильевича Ломоносова. До сих пор приходится встречаться с ложным утверждением о том, что закон сохранения энергии открыт Ломоносовым. Это утверждение основывается не на каких-либо работах Ломоносова, а на одной фразе в его письме Эйлеру 5 июля 1748 года Так, сколько материи прибавляется какому-либо телу, столько же теряется у другого… Так как это всеобщий закон природы, то он распространяется и на правила движения тело, которое своим толчком возбуждает другое к движению, столько же теряет от своего движения, сколько сообщает другому, им двинутому . Слова очень содержательные. Но, во-первых, они касаются не энергии, а движения — понятия неопределенного, и, во-вторых, сходные мысли были высказаны еще в XVH веке Декартом, утверждавшим, что во Вселенной в.сегда сохраняется одно и то же количество движения. Закона сохранения энергии здесь нет, да и невозможно было открыть его до наступления века пара и электричества. Ломоносов, открывший закон сохранения массы, обосновавший кинетическую теорию тепла, так много сделавший в науке и искусстве, не нуждается в том, чтобы ему приписывали мнимые открытия. [c.16]
Закон сохранения массы и э н е р г и и. Несмотря на то что еще в 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии , до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А. Эйнштейн показал, что между массой и энергией существует взаимосвязь, количественно выражаемая уравнением
На основе достижений современной атомной физики и теории относительности было установлено, что закон сохранения массы тесно связан с законом сохранения энергии (Ломоносов, 1748 г., Мейер, 1842 г.). Соотношение между массой и энергией было установлено Эйнштейном, который показал, что изменение энергии системы прямо пропорционально изменению массы [c.11]
Закон сохранения массы вещества. Впервые его высказал М. В. Ломоносов в письме к Эйлеру от 5 июня 1748 г., опубликованном на русском языке в 1760 г. Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому… Это определение, за исключением архаичности языка, не устарело. [c.13]
Закон сохранения массы при химических реакциях. В 1756 г. Ломоносов, применяя количественные методы при исследовании химических процессов, установил, что при химических превращениях масса веществ остается неизменной. Это открытие Ломоносова стало одним из основных законов химии, который в настоящее время формулируется следующим образом масса веществ, вступивших в реакцию, всегда равна массе вешаете, образовавшихся в результате реакции. [c.8]
Творческая деятельность Ломоносова отличается исключительной широтой интересов и глубиной проникновения в тайны природы. Его исследования относятся к области физики, химии, астрономии и др. Результаты этих работ заложили основы современного естествознания. Ломоносов указал (1765) на основополагающее значение закона сохранения массы вещества в химических реакциях изложил (1741 —1750) основы корпускулярного (атомно-молекулярного) учения выдвинул (1744—1748) кинетическую теорию теплоты. Был зачинателем применения математических и физических методов исследования в химии и первым начал читать в Петербургской АН самостоятельный Курс истинно физической химии , заложил основы русского химического языка.
Закон сохранения массы вещества. Применяя количественные методы исследования химических реакций, М. В. Ломоносов установил, что при химических превращениях общий вес вещества остается неизменным. На основании своих опытов он сформулировал закон сохранения массы веш,еств [c.25]
Ломоносов первый из отечественных ученых начал применять физические методы исследований в химии. Закон сохранения массы вещества и энергии был одним из важнейших открытий Ломоносова в области физической химии. Ломоносовым установлено, что понижение температуры замерзания раствора зависит от его концентрации, и эта температура бывает всегда ниже температуры замерзания чистого растворителя. Им сделан и ряд других открытий и исследований. [c.6]
Из этой формулировки видно, что М. В. Ломоносов закон сохранения массы веществ рассматривал в единстве с законом сохранения энергии и понимал его как всеобщий закон природы. [c.56]
Закон сохранения массы. Исключительное значение для химии имело установление закона сохранения массы, являющегося следствием всеобщего естественного закона сохранения материи и движения, сформулированного М. В. Ломоносовым (1711 —1765 гг.) как всеобщий естественный закон в 1748 г. в письме к Д. Эйлеру Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимется, столько присовокупится к другому, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий закон простирается и в самые правила движения ибо тело, движущее своей силой другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает (Ломоносов М. В. Труды по физике и химии,— М.. 1951.— Т. II.— С. 183).
В 1749 г, по чертежам и указаниям Ломоносова была построена первая в России химическая научная и учебная лаборатория на Васильевском острове в Петербурге. В лаборатории Ломоносов экспериментально обосновывает закон сохранения массы веществ, сформулированный нм еще в 1748 г. [c.8]
М. В. Ломоносов сначала высказал теоретически (1748), а затем экспериментально обосновал (1756 ) закон сохранения массы веществ. В настоящее время он формулируется так [c.15]
М. В. Ломоносов связывал закон сохранения массы веществ с законом сохранения энергии (количества движения) и рассматривал их в единстве как всеобщий закон природы. Этот закон он сформулировал в 1748 г. следующим образом Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения ибо тело, движущее [c.15]
М. В. Ломоносов сначала теоретически, а затем опытным путем открыл и обосновал закон сохранения массы веществ, который лежит в основе всех химических реакций. В настоящее время он формулируется следующим образом масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. [c.18]
М. В. Ломоносов связывал закон сохранения массы веществ с законом сохранения энергии (количества движения) и рассматривал их в единстве как всеобщий закон природы. Этот закон он сформулировал в 1748 г. следующим образом [c.18]
В 1748 г. М. В. Ломоносов сформулировал положение, которое в дальнейшем сыграло большую роль в развитии химии и получило название закона сохранения массы веш,еств масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. [c.21]
Впоследствии М. В. Ломоносов экспериментально подтвердил правильность своих выводов. Независимо от М. В. Ломоносова закон сохранения массы веществ был сформулирован позднее французским химиком Лавуазье. [c.21]
Одним из первых химических явлений, с которым человечество познакомилось на заре своего существования, было горение. Вна-ч-але оно использовалось для варки пищи и обогрева жилища. Лишь через многие тысячелетия человек научился использовать его для превращения химической анергии горючих веществ в механическую, электрическую и другие формы энергии. Представления об этом явлении менялись у человека по мере накопления им все новых и новых фактов. Впервые правильное представление о процессе горения высказал гениальный русский ученый Михаил Васильевич Ломоносов (1711—1765 гг.), заложивший основы отечественной науки и установивший ряд важнейших законов современной химии и физики. Он провел большое количество опытов с прокаливанием свинца и олова в открытых и запаянных сосудах. Во всех опытах М. В. Ломоносов производил взвешивание вещества до прокаливания и после него. Он убедился, что металлы при прокаливании увеличиваются в весе за счет соединения их с воздухом (в то время кислород был неизвестен). В этих опытах он впервые установил основной закон химии — закон сохранения массы вещества. [c.5]
М. В. Ломоносов первым из ученых (в 1748 г.) сформулировал закон сохранения массы вещества при химической реакции. Q писал … все перСхМены, в., натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимается, столько присовокупится к другому . Этот закон в современной формулировке гласит Масса веществ, вступивших в реакцию, всегда равна массе веществ, образовавшихся в результате реакции. [c.3]
Химическая промышленность в период домонополистического капитализма. Во второй половине ХУП1 в. возникает одновременно с химией химическая технология. Большое значение для обеих наук имеет закон сохранения массы, открытый М. В. Ломоносовым. В применении к химическим производствам этот закон позволяет вычислять максимально возможные (стехиометрические) выходы продуктов и составлять материальные балансы, а это является первым шагом при проектировании технологического процесса. М. В. Ломоносов уделял много внимания и непосредственно химической технологии. Своими трудами он содействовал развитию в России металлургии, стекловарения, производства фарфора. [c.11]
Закон сохранения массы. Ломоносов создал при Академии наук химическую лабораторию. В ней он изучал протекаиие химических реакций, взвешивая исходные вещества и продукты реакции. При этом он установил закон сохранения массы (веса) [c.18]
Закон сохранения массы при химических реакциях. Применяя количественные методы при исследовании химических процессов, Ломоносов в 1756 г. установил, что ири химических превращениях общая масса веществ остается неизменной. Это открытие Ломоносова ста ю одним из основных закогюв химии, который в настоя-огсе время формулируется следующим образом [c.12]
Возникновение физической хнмии как самостоятельной науки относится к середине XVIII в. Первый в мире курс физической химии был создан М. В. Ломоносовым (1752—1754). На основе своих физико-химических исследований М. В. Ломоносов пришел к принципиально новому определению химии как науки о свойствах тел, исходя из того, что все изменения в природе связаны с движением материи. Он первым обосновал основной закон сохранения массы вещества и пришел к определению принципа сохранения материи и движения, получившего признание как всеобщий закон природы. [c.6]
Михаил Васильевич Ломоносов — великий русский ученый — одни из основоположников новой химии. Он открыл основной закон химии — закон сохранения массы веществ. Разработал теорию атомно-молекуляриого строения веществ, являющуюся основой физики и химии. Ввел в химию количественные методы исследования. Объединил химию с физикой, создал новую науку — физическую химию. Большим вкладом в науку являются его работы по исследованию растворов. С имеием Ломоносова связано развитие в России различных иаук. Историк, ритор, механик, химик, минералог, художник и сти.хотворец — он все испытал и все проник , — писал о нем А. С. Пушкин. [c.4]
Ломоносов первый из отечественных ученых начал применять физические методы исследований в химии. Закон сохранения массы вещества и энергии был одним из важнейших открытий Ломо- [c.6]
Атомно-молекулярная теория. Создатель атомно-молекулярного учения и первооткрыватель закона сохранения массы веществ М.В.Ломоно-сов по праву считается основателем научной химии. Ломоносов четко различал две ступени в строении вещества элементы (в нашем понимании — атомы) и корпускулы (молекулы). Согласно Ломоносову, молекулы простых веществ состоят из одинаковых атомов, а молекулы сложных веществ — из разных атомов. Всеобщее признание атомно-молекулярная теория получила в начале XIX в. после утверждения в химии атомистики Дальтона. С тех пор главным объектом иссле- [c.7]
Систематическое изучение количественных соотношений между составом веществ и физическими свойствами началось в XVIII в. Основополагающими в этой области являются труды М. В. Ломоносова и А. Лавуазье. М. В. Ломоносов в 1748 г. сформулировал закон сохранения массы и энергии. Он же первый сформулировал основную задачу физико-химического анализа как установление зависимости свойств от состава системы для выяснения природы составляющих ее частей . К сожалению, труды М. Е5. Ломоносова оставались долгое время неизвестными и были опубликованы Б. Н. Меншуткиным лишь в 1904 г. [c.265]
Закон сохранения массы. Химические уравнения. и расчеты по ним. Закон сохранения массы веи еств масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции (М. В. Ломоносов, 1848). С точки зрения атомно-молекулярного учения при химич еских реакциях атомы не образуются из ничего и не исчезают, поэтому число атомов всех видов в ходе химической реакции остается неизменным. А так. hMi маестгданного атома постоянна, [c.17]
И только в начале XIX столетия английский ученый Джон Дальтон возвращается к атомам как наименьшим частицам материи и вводит в науку этот термин. Этому предшествовали работы таких замечательных ученых, как Р. Бойль (в книге Химик-скептик он нанес сокрушительный удар по представлениям алхимиков), Дж. Пристли и К. В. Шееле (открытие кислорода), Г. Кавендиш (открытие водорода), А. Л. Лавуазье (попытка составить первую таблицу простых веществ), М. В. Ломоносов (основные положения атомно-молекулярного учения, закон сохранения массы), Ж. Л. Ируст (закон постоянства состава) и многие другие. [c.3]
chem21.info
Закон сохранения массы веществ (м.В.Ломоносов, 1748 г.; а.Лавуазье, 1789 г.).
Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции. Атомно-молекулярное учение этот закон объясняет следующим образом: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка (т.е. химическое превращение — это процесс разрыва одних связей между атомами и образование других, в результате чего из молекул исходных веществ получаются молекулы продуктов реакции). Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Под массой понимали величину, характеризующую количество материи.
В начале 20 века формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (А.Эйнштейн, 1905 г.), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, но и ее движение. Полученная телом энергия DE связана с увеличением его массы Dm соотношением DE = Dm · c2 , где с — скорость света. Это соотношение не используется в химических реакциях, т.к. 1 кДж энергии соответствует изменению массы на ~10-11 г и Dm практически не может быть измерено. В ядерных реакциях, где DЕ в ~106 раз больше, чем в химических реакциях, Dm следует учитывать.
Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Он является основой количественного химического анализа.
Закон постоянства состава. Впервые сформулировал ж.Пруст (1808 г).
Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения. Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных массовых соотношениях.
Пример.
CuS — сульфид меди. m(Cu) : m(S) = Ar(Cu) : Ar(S) = 64 : 32 = 2 : 1 Чтобы получить сульфид меди (CuS) необходимо смешать порошки меди и серы в массовых отношениях 2 : 1. Если взятые количества исходных веществ не соответствуют их соотношению в химической формуле соединения, одно из них останется в избытке.
Например, если взять 3 г меди и 1 г серы, то после реакции останется 1 г меди, который не вступил в химическую реакцию. Вещества немолекулярного строения не обладают строго постоянным составом. Их состав зависит от условий получения.
Массовая доля элементаw(Э) показывает, какую часть составляет масса данного элемента от всей массы вещества: где n — число атомов; Ar(Э) — относительная атомная масса элемента; Mr — относительная молекулярная масса вещества.
w(Э) = (n · Ar(Э)) / Mr
Зная количественный элементный состав соединения можно установить его простейшую молекулярную формулу:
Обозначают формулу соединения Ax By Cz
Рассчитывают отношение X: Y: Z через массовые доли элементов:
w(A) = (х · Ar(А)) / Mr(AxByCz) w(B) = (y · Ar(B)) / Mr(AxByCz) w(C) = (z · Ar(C)) / Mr(AxByCz)
X = (w(A) · Mr) / Ar(А) Y = (w(B) · Mr) / Ar(B) Z = (w(C) · Mr) / Ar(C)
x : y : z = (w(A) / Ar(А)) : (w(B) / Ar(B)) : (w(C) / Ar(C))
Полученные цифры делят на наименьшее для получения целых чисел X, Y, Z.
Записывают формулу соединения.
studfiles.net
В 1748 году Ломоносов впервые формулирует «всеобщий закон природы» — закон сохранения материи и движения
Ученый-энциклопедист (физик и астроном, историк и филолог) Михаил Васильевич Ломоносов работал в самых различных отраслях науки, но наибольших успехов достиг в области физики и химии.
Он сформулировал самый общий закон естествознания – закон сохранения материи и движения. До Ломоносова закон сохранения движения был выведен Декартом и Лейбницем, которые считали, что при всех явлениях в природе неизменным остается только количество механического движения.
Ломоносов же сформулировал свой закон в 1748 году в следующем виде: «Все перемены, в натуре случающиеся, такого суть состояния, что сколько у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения: ибо тело, движущее своею силою другое, столько же оные у себя теряет, сколько сообщает другому, которое от него движение получает». Его обоснование закона было дано в письме Ломоносова от 16 (5 ст.ст.) июля 1748 года, адресованном великому математику Леонарду Эйлеру.
Замечательно, что под движением Ломоносов понимал не только механическое перемещение, но и тепловое; по сути дела он высказывал мысль о переходе одних форм движения в другие.
Ломоносов не только сформулировал свой закон, но и применял его. Так, пользуясь этим законом, он объяснил процесс перехода энергии при теплопередаче, процессы, происходящие в охлаждающих смесях, и другие случаи перехода энергии.
Открытый Ломоносовым закон получил более полное обоснование в его работах: «Об отношении количества материи и веса» (1758) и в «Рассуждении о твердости и жидкости тел» (1760). Обе эти работы были опубликованы на латинском языке и, следовательно, получили известность за пределами России. Но осознать значение открытия, сделанного Ломоносовым, многие ученые тех лет так и не смогли.
Однако с развитием физики и техники формулировка закона сохранения энергии все более и более уточняется. Необходимость улучшения тепловых машин и их коэффициента полезного действия заставила более обстоятельно заняться изучением тепловых процессов. Это привело к окончательному выяснению того, что теплота является формой энергии, и к установлению впоследствии Майером, Джоулем, Гельмгольцем и Ленцом механического эквивалента теплоты. Таким образом, Ломоносов является прямым предшественником этих ученых.
www.molgvardia.ru
Закон сохранения ломоносова-лавуазье — Adm-kuzminskiy.ru
Справочник химика 21
Химия и химическая технология
Закон Ломоносова — Лавуазье — Лапласа. Закон Гесса
Т. возникла в сер. 18 в. На необходимость измерения тепловых эффектов р-ций и теплоемкостей указывал еще М. В. Ломоносов первые термохйм. измерения провели Дж. Блэк, А. Лавуазье, П. Лаплас. Развитие Т. в 19 в. тесно связано с именами Г. И. Гесса, М. Бертло, X. Томсена. Гесса закон, открытый в 1840, дает возможность определять тепловые эффекты хим. р-ций расчетньпу путем, в частности по теплотам образования исходных в-в и продуктов. Тем самым открывается путъ для расчета таких тепловых эффектов, прямое измерение к-рых затруднительно, а нногда невозможно. Необходимые для расчета стандартные теплоты образования собраны в фундам. термодинамнч. справочники. [c.547]
Т. возникла в 18 в. На необходимость измерения тепловых. эффектов р-цнй и теплоемкостей указывал еще М. В. Ломоносов. Первые термохим, измерения провели А, Лавуазье, П. Лаплас, Развитие Т. в 19 в. тесно связано с.именами Г. И. Гесса, М. Бертло, X. Ю. Томсена. Гесса закон, открвггый в 1840, дает возможность определять тепловые эффекты хим. р-ций расчетным путем, в частности по теплотан образована исходных в-в и продуктов. Томсен и Бертло высказали идею, что хим. р-ции самопроизвольно протекают в направлении выделения теплоты (принцип Бертло), и разработали осн. эксперим. методики Т. Ими и их учениками бы.1и измерены тепловые эффекты мн. р-ций. Хотя в общем виде принцип Бертло оказался неверен, за Т. сохранилась ведущая роль в исследовании возможности самопроизвольного протекания р-ции в заданных условиях. Так, по ур-нию ДН — ГДЗ = —ЛПагСр, являющемуся обобщением первого и второго начал термодинамики (Н — энтальпия, S — энтропия, Г — т-ра, R — газовая постоянная), можно рассчитать константу равновесия Кр любой р-ции через тепловые величины. [c.569]
Смотреть страницы где упоминается термин Закон Ломоносова — Лавуазье — Лапласа. Закон Гесса: [c.569] Смотреть главы в:
chem21.info
Часть I
1. Закон Ломоносова-Лавуазье – закон сохранения массы веществ:
2. Уравнения химической реакции – это условная запись химической реакции с помощью химических формул и математических знаков.
3. Химическое уравнение должно соответствовать закону сохранения массы веществ, что достигается расстановкой коэффициентов в уравнении реакции.
4. Что показывает химическое уравнение?
1) Какие вещества вступают в реакцию.
2) Какие вещества образуются в результате.
3) Количественные отношения веществ в реакции, т. е. количества реагирующих и образующихся веществ в реакции.
4) Тип химической реакции.
5. Правила расстановки коэффициентов в схеме химической реакции на примере взаимодействия гидроксида бария и фосфорной кислоты с образованием фосфата бария и воды.
а) Запишите схему реакции, т. е. формулы реагирующих и образующихся веществ:
б) начинайте уравнивать схему реакции с формулы соли (если она имеется). При этом помните, что несколько сложных ионов в составе основания или соли обозначаются скобками, а их число – индексами за скобками:
в) водород уравняйте в предпоследнюю очередь:
г) кислород уравняйте последним – это индикатор верной расстановки коэффициентов.
Перед формулой простого вещества возможна запись дробного коэффициента, после чего уравнение необходимо переписать с удвоенными коэффициентами.
Часть II
1. Составьте уравнения реакций, схемы которых:
2. Напишите уравнения химических реакций:

3. Установите соответствие между схемой и суммой коэффициентов в химической реакции.

4. Установите соответствие между исходными веществами и продуктами реакции.

5. Что показывает уравнение следующей химической реакции:
1) Вступили в реакцию гидроксид меди и соляная кислота;
2) Образовались в результате реакции соль и вода;
3) Коэффициенты перед исходными веществами 1 и 2.
6. С помощью следующей схемы составьте уравнение химической реакции, используя удвоение дробного коэффициента:
7. Уравнение химической реакции:
4P+5O2=2P2O5
показывает количество вещества исходных веществ и продуктов, их массу или объём:
1) фосфора – 4 моль или 124 г;
2) оксида фосфора (V) – 2 моль, 284 г;
3) кислорода – 5 моль или 160 л.
www.superhimik.ru
Закон сохранения вещества
Закон сохранения массы — исторический закон физики, согласно которому масса как мера количества вещества сохраняется при всех природных процессах, то есть несотворима и неуничтожима.
Содержание
Исторический очерк
Закон сохранения массы исторически понимался как одна из формулировок закона сохранения материи. Одним из первых его сформулировал древнегреческий философ Эмпедокл (V век до н. э.):
Ничто не может произойти из ничего, и никак не может то, что есть, уничтожиться.
Позже аналогичный тезис высказывали Демокрит, Аристотель и Эпикур (в пересказе Лукреция Кара). Средневековые учёные также не высказывали никаких сомнений в истинности этого закона.
С появлением понятия массы как меры количества вещества, пропорциональной весу, формулировка закона сохранения материи была уточнена: масса есть инвариант, то есть при всех процессах общая масса не уменьшается и не увеличивается. В 1630 году Жан Рэ (Jean Rey, 1583-1645), доктор из Перигора, писал Мерсенну [1]
Вес настолько тесно привязан к веществу элементов, что, превращаясь из одного в другой, они всегда сохраняют тот же самый вес.
В середине XVIII века опыты Роберта Бойля поставили закон сохранения массы под сомнение — у него при химической реакции вес вещества увеличился. Однако Ломоносов и другие физики вскоре указали Бойлю на его ошибку: увеличение веса происходило за счёт воздуха, а в запаянном сосуде вес сохранялся неизменным. Ломоносов писал Эйлеру:
В дальнейшем, вплоть до создания физики микромира, закон сохранения массы считался истинным и очевидным. Лавуазье в «Начальном учебнике химии» (1789), приводит точную количественную формулировку закона сохранения массы вещества, однако не объявляет его каким-то новым и важным законом, а просто упоминает мимоходом как о хорошо известном и давно установленном факте. Для химических реакций Лавуазье сформулировал закон так: «Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции».
Современное состояние
Как выяснилось, в общефизическом смысле закон сохранения массы, строго говоря, неверен. Ведь, например, электрон и позитрон, каждый из которых обладает массой, могут аннигилировать в фотоны, не имеющие массы покоя. Другой пример: масса дейтрона, состоящего из одного протона и одного нейтрона, не равна сумме масс своих составляющих, поскольку следует учесть энергию взаимодействия частиц.
Таким образом, закон сохранения массы в физике работает с известными оговорками, а на самом деле является ограниченным и частным случаем закона сохранения энергии, с учётом известного соотношения для энергии массы покоя частиц: E=mc².
dic.academic.ru
Закон ломоносова сохранения массы
Последнее обстоятельство – пропускание внешнего воздуха – и было причиною того, что у Бойля, вскрывавшего всегда свои реторты перед взвешиванием, наблюдалось увеличение веса.
“Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте; сколько часов положит кто на бдение, столько же сну отнимет. Сей всеобщей естественной закон простирается и в самые правила движения: ибо тело, движущее своею силою другое, столько же оные у себя теряет, сколько сообщает другому, которое от него движение получает”.
Опыты Бойля заключались в том, что Бойль брал стеклянные реторты, клал в них свинец или олово, запаивал герметически на огне горлышко реторты и взвешивал их. При нагревании такой реторты свинец переходил в окалину; когда, после двухчасового нагревания, он открывал запаянный кончик реторты, воздух с шумом врывался в неё – признак того, как указывает Бойль, что реторта была действительно герметически запаяна – и при вторичном взвешивании оказывалась прибыль веса. Отсюда Бойль заключил, что материя огня проходит через стекло и соединяется с металлом.
Таким образом, опыты Ломоносова с полною определённостью показали, что образование окалины происходит именно от соединения металла с воздухом при прокаливании. Результат этот чрезвычайно важен: истинное объяснение явлений горения, как соединения горящего или обжигаемого тела с кислородом воздуха, судя по известной нам истории науки, принадлежит Лавуазье, который начал свои классические исследования именно с повторения опытов Бойля и в 1773-м году, через 17 лет после Ломоносова, получил совершенно такой же результат, как и Ломоносов. Лавуазье затем изучил те изменения, которые происходят с воздухом при обжигании металлов, и получил отсюда верное объяснение явлений горения.
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВА
Лавуазье в 1789-м году в своём “Элементарном руководстве химии” даёт описания явлений брожения виноградного сахара, распадающегося при этом на углекислоту и винный спирт, вес которых равен весу взятого сахара, Лавуазье пишет: “Так как ничто не творится, ни в искусственных процессах, ни в природных, и можно выставить положение, что во всякой операции имеется одинаковое количество материи до и после операции, что качество и количество начал остались теми же самыми, произошли лишь изменения. На этом положении основано всё искусство делать опыты в химии: необходимо предполагать во всех действительное равенство между началами исследуемого тела и получаемого из него анализом”.
Эти-то опыты Ломоносов повторил в 1756-м году и, как он сам пишет в ежегодных отчётах о своих занятиях, со следующим результатом: “Между разными химическими опытами, которых журнал на 13-ти листах, деланы опыты в заплавленных накрепко стеклянных сосудах, чтобы исследовать, прибывает ли вес металлов от чистого жара. Оными опытами нашлось, что славного Роберта Бойля мнение ложно, ибо без пропускания внешнего воздуха вес сожжённого металла остается в одной мере”.
В химической лаборатории М.В.Ломоносов обосновал в 1748-м году закон сохранения массы вещества, который в современной формулировке звучит так: “Вес всех веществ, вступающих в реакцию, равен весу всех продуктов реакции”. Этот закон был им экспериментально подтверждён в 1756-м году на примере обжигания металлов в запаянных сосудах.
Опыты Лавуазье повторяются в каждом учебнике химии, об опытах же Ломоносова никто не знает, и даже русские химики не находят нужным упоминать о них; а между тем, Ломоносов был несомненно предшественником Лавуазье.
Первоначально мысль о сохранении вещества и энергии была высказана великими философами XVII-го и XVIII-го века, как аксиома, т.е. как явление, не нуждающееся в доказательствах. Ломоносов был первым, высказавшим “всеобщий закон природы” совершенно ясно и, главное, подтвердившим его количественными опытами, среди которых наиболее доказательными являлись, конечно, опыты превращения металлов в окалины в запаянных сосудах.
В изложении на русском языке этот закон сформулирован в “Рассуждении о твёрдости и жидкости тел” (1760), где он дан в таких выражениях:
Р.Бойль показал, что при обжигании металлов увеличивается вес их, и объяснял это увеличение веса соединением с металлами весомой части пламени, материи огня.
Закон сохранения массы вещества при химических реакциях подвергался проверке много раз в XIX-м и начале XX-го столетия и теперь может считаться правильным в пределах тысячных долей миллиграмма. Что же касается закона сохранения энергии, открытого Ломоносовым, то этот закон стал общепризнанным не ранее второй половины XIX-го века.
Зная количественный элементный состав соединения можно установить его простейшую молекулярную формулу:
106 раз больше, чем в химических реакциях, Dm следует учитывать.
Например, если взять 3 г меди и 1 г серы, то после реакции останется 1 г меди, который не вступил в химическую реакцию. Вещества немолекулярного строения не обладают строго постоянным составом. Их состав зависит от условий получения.
Обозначают формулу соединения Ax By Cz
X = (w(A) · Mr) / Ar(А) Y = (w(B) · Mr) / Ar(B) Z = (w(C) · Mr) / Ar(C)
Закон сохранения массы веществ (осов, 1748 г; зье, 1789 г
Массовая доля элементаw(Э) показывает, какую часть составляет масса данного элемента от всей массы вещества: где n — число атомов; Ar(Э) — относительная атомная масса элемента; Mr — относительная молекулярная масса вещества.
Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции. Атомно-молекулярное учение этот закон объясняет следующим образом: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка (т.е. химическое превращение — это процесс разрыва одних связей между атомами и образование других, в результате чего из молекул исходных веществ получаются молекулы продуктов реакции). Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Под массой понимали величину, характеризующую количество материи.
Рассчитывают отношение X: Y: Z через массовые доли элементов:
Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Он является основой количественного химического анализа.
Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения. Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных массовых соотношениях.
CuS — сульфид меди. m(Cu) : m(S) = Ar(Cu) : Ar(S) = 64 : 32 = 2 : 1 Чтобы получить сульфид меди (CuS) необходимо смешать порошки меди и серы в массовых отношениях 2 : 1. Если взятые количества исходных веществ не соответствуют их соотношению в химической формуле соединения, одно из них останется в избытке.
В начале 20 века формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (А.Эйнштейн, 1905 г.), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, но и ее движение. Полученная телом энергия DE связана с увеличением его массы Dm соотношением DE = Dm · c2 , где с — скорость света. Это соотношение не используется в химических реакциях, т.к. 1 кДж энергии соответствует изменению массы на
Закон сохранения массы
Для стационарного движения плотность, скорость, давление, температура в фиксированной точке потока не изменяются, тогда и равенство (5.17) запишется так
. Закон сохранения массы применительно к движению воздуха формулируется следующим образом: масса любого объема воздуха остается постоянной в процессе его движения.
Выразим массовый расход воздуха в выработке в виде
Движение воздуха в шахте подчиняется законам сохранения массы и энергии
Из выражения (5.22), называемогоуравнением расхода, следует, что для стационарного движения объемный расход воздуха в выработке постоянный.
Для случая стационарного движения воздуха в выработке из уравнения (5.16) получим
Через проекции скорости потока в рассматриваемой точке на оси координат этот закон запишется так:
а при постоянной плотности потока ρ=const
В выработке постоянного сечения v=w=0 тогда из уравнения (5.19) найдем, что u=const, т. е. скорости движения воздуха в сходственных точках постоянны. Из уравнения (5.19) также следует, что увеличение скорости в одном направлении должно вызывать уменьшение ее в другом направлении, так как сумма членов в его левой части будет равна нулю тогда, когда одни из них будут положительны (ускорение течения), другие отрицательными (замедление).
Тогда для изотермического процесса (т.е. при ρ=const) из выражения (5.21) получим
Если в потоке выделить элементарный объем ω, достаточно малый, чтобы плотность воздуха в нем можно было считать постоянной, то закон сохранения массы можно записать так:
При разветвлении потока уравнение (5.22) примет вид
- Электрон и позитрон, каждый из которых обладает массой, могут аннигилировать в фотоны, не имеющие массы поодиночке, а обладающие ею только как система.
- Масса дейтрона, состоящего из одного протона и одного нейтрона, не равна сумме масс своих составляющих, поскольку следует учесть энергию взаимодействия частиц.
- При термоядерных реакциях, происходящих внутри Солнца, масса водорода не равна массе получившегося из него гелия.
- Особенно яркий пример: масса протона (≈938 МэВ) в несколько десятков раз больше массы составляющих его кварков (около 11 МэВ).
как и остальные связанные с нею формулы (и мы ниже будем для краткости использовать именно такую систему единиц).
Все встречающиеся в природе изменения происходят так, что если к чему-либо нечто прибавилось, то это отнимается у чего-то другого. Так, сколько материи прибавляется к какому-либо телу, столько же теряется у другого, сколько часов я затрачиваю на сон, столько же отнимаю от бодрствования и т. д.
Закон сохранения массы исторически понимался как одна из формулировок закона сохранения материи. Одним из первых его сформулировал древнегреческий философ Эмпедокл (V век до н. э.) [1] :
Другими словами, сохраняется масса закрытой физической системы, в которой происходит химическая реакция, а сумма масс всех веществ, вступивших в эту реакцию, равна сумме масс всех продуктов реакции (то есть тоже сохраняется). Масса считается аддитивной.
Рассмотрим теперь систему этих двух фотонов как целое, посчитав ее импульс и энергию. Как видим, импульс этой системы равен нулю (импульсы фотонов, сложившись, уничтожились, так как эти фотоны летят в противоположных направлениях) [8] :
В середине XVIII века опыты Роберта Бойля поставили закон сохранения массы под сомнение — у него при химической реакции вес вещества увеличился. Однако М. В. Ломоносов и другие физики вскоре указали Р. Бойлю на его ошибку: увеличение веса происходило за счёт воздуха, а в запаянном сосуде вес сохранялся неизменным. Ломоносов писал Л. Эйлеру:
(M2) Масса не является аддитивной величиной: масса системы не равна сумме масс её составляющих. Примеры неаддитивности:
С точки зрения классической механики и химии, сохраняются общая масса закрытой физической системы, равная сумме масс компонентов этой системы (то есть масса считается аддитивной. Этот закон с большой точностью верен в области применимости ньютоновской механики и химии, так как релятивистские поправки в этих случаях пренебрежимо малы.
Ничто не творится ни в искусственных процессах, ни в природных, и можно выставить положение, что во всякой операции [химической реакции] имеется одинаковое количество материи до и после, что качество и количество начал остались теми же самыми, произошли лишь перемещения, перегруппировки. На этом положении основано всё искусство делать опыты в химии.
В XX веке обнаружились два новых свойства массы.
Позже аналогичный тезис высказывали Демокрит, Аристотель и Эпикур (в пересказе Лукреция Кара). Средневековые учёные также не высказывали никаких сомнений в истинности этого закона. В 1630 году Жан Рэ (Jean Rey, 1583—1645), доктор из Перигора, писал Мерсенну [3] :
1. Определить неизвестную валентность элемента:
Отсюда следует, что: m (СO2)= m (малахита)- m (СuO) — m(h3O)
Ломоносов подчеркнул, что корпускулы движутся согласно законам механики и сталкиваясь друг с другом изменяются. Поэтому химические превращения должны изучаться не только методами химии, но и методами физики и математики.
Задача: При разложение 44,4 г малахита образуется 32 г СuO и 3,6 г воды Н2О. Какая масса углекислого газа СО2 образуется? (Слайд № 20)
Вывод является формулировкой закона сохранения массы веществ.
Конспект урока: Атомно — молекулярное учение
Вопрос: а изменилась ли масса получившихся веществ?
Ломоносов принадлежал к числу тех редких, исключительно одаренных натур, научные идеи которых на многие десятилетия опережают свою эпоху. Его кипучая научная деятельность отличалась поразительной широтой разносторонностью. По словам академика Вавилова: «Достигнутое им одним в областях физики, химии, астрономии, приборостроения, геологии, географии, языкознания, истории достойно было деятельности целой академии.
Естественно, не только Ломоносов думал над этой проблемой. Независимо от него, но чуть позже, в 1789 году закон сохранения массы веществ был установлен французским химиком Антуаном Лораном Лавуазье (имя записывается на доске и в тетради).
8.У веществ с немолекулярным строением в узлах кристаллических решеток находятся атомы или другие частицы. Между этими частицами существуют сильные химические связи, для разрушения которых потребуется много энергии. Поэтому эти вещества имеют высокие температуры плавления.
2. Составить формулу, зная валентности хим. элементов:
Развивающие: развить наблюдательность при просмотре компьютерной презентации и проведении демонстрационного эксперимента. Развить умение прогнозировать, обобщать и делать выводы. Используя эксперимент, рассмотреть важность закона сохранения массы веществ. Развить информационную культуру и логическое мышление учащихся.
o-v-m.ru
Закон сохранения ломоносова-лавуазье
Гипермаркет знаний>>Химия>>Химия 7 класс>> Схема химической реакции. Закон сохранения массы вещества при химической реакции. Химическое уравнение
Схема химической реакции. Закон сохранения массы веществ при химической реакции. Химическое уравнение
Материал параграфа поможет вам:
> выяснить, что такое схема химической реакции;
> понять суть закона сохранения массы веществ при химической реакции;
> превращать схемы реакций в химические уравнения.
Схема химической реакции.
Существует несколько способов записи химических реакций. Co «словесной» схемой реакции вы ознакомились в § 13.
Приводим еще один пример:
сера + кислород —> сернистый газ.
Эта запись дает мало информации; она не указывает на химический состав реагентов и продуктов.
Этого недостатка лишен другой способ записи — химическая схема реакции. В ней вместо названий веществ содержатся химические формулы 1 :
Химическую схему в дальнейшем будем называть просто схемой реакции.
Над стрелкой часто указывают условия, при которых происходит реакция: нагревание , повышенное давление , освещение , наличие дополнительных веществ .
1 Для серы здесь и далее будем использовать формулу S, а не Ss, которую в действительности имеют молекулы вещества.
Если продуктом реакции является газ, то после его формулы записывают стрелку, направленную вверх , а если образуется осадок, — стрелку, направленную вниз . В случаях, когда и продукт, и реагент — газы или нерастворимые вещества, вертикальные стрелки не ставят. Иногда под формулами реагентов и продуктов пишут их названия.
Пример схемы реакции с дополнительными обозначениями и названиями веществ:
Вам необходимо научиться не только записывать схемы реакций, но и комментировать их. Последнюю схему реакции комментируют так: при нагревании мела образуются негашеная известь и углекислый газ.
► Какими химическими элементами образовано исходное вещество и продукты этой реакции?
Схема реакции дает возможность сделать важный вывод: все химические элементы во время реакции сохраняются.
Закон сохранения массы веществ при химической реакции.
Общеизвестно, что после сжигания бумаги остается пепел, масса которого намного меньше массы бумаги. Если же сильно нагревать (прокаливать) порошок меди или медный предмет на воздухе, то обнаружим противоположное масса вещества будет возрастать (металл покроется черным налетом).
Осуществим оба химических превращения в закрытых сосудах. Результаты опытов будут другими. Взвесив закрытые сосуды с веществами до и после каждого эксперимента, обнаружим, что суммарная масса веществ в результате реакций неизменяется. Это впервые установил в середине XVIII в. русский ученый М. В. Ломоносов. He зная об открытии Ломоносова, к аналогичному выводу пришел в 1789 г. французский ученый А.-Л. Лавуазье.
Михаил Васильевич Ломоносов (1711—1765)
Выдающийся русский ученый, первый русский академик Петербургской академии наук. Разработал одну из теорий строения веществ (40-е годы XVIII в.). Открыл и сформулировал законы сохранения массы веществ и движения (1748— 1760). Изучал химические свойства металлов, анализировал состав минералов, разработал способы получения минеральных красок, цветного стекла. Внес существенный вклад в развитие «химического языка». Автор книг по истории России, поэт, художник, геолог, географ, инженер, педагог. Один из основателей первого в России Московского университета.
Ломоносов и Лавуазье открыли закон сохранения массы веществ при химической реакции. Он формулируется так:
масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции.
Объясним, почему массы пепла и прокаленной меди отличаются от масс бумаги и меди до ее нагревания.
В процессе горения бумаги принимает участие кислород, который содержится в воздухе (рис. 48, а).
Следовательно, в реакцию вступают два вещества. Кроме пепла, образуются углекислый газ и вода (в виде пара), которые попадают в воздух и рассеиваются.
Рис. 48. Реакции бумаги (а) и меди (б) с кислородом
Антуан-Лоран Лавуазье (1743—1794)
Выдающийся французский химик, один из основателей научной химии. Академик Парижской академии наук. Ввел в химию количественные (точные) методы исследования. Экспериментально определил состав воздуха и доказал, что горение — это реакция вещества с кислородом, а вода — соединение Гидрогена с Оксигеном (1774— 1777).
Составил первую таблицу простых веществ (1789), предложив фактически классификацию химических элементов. Независимо от М. В. Ломоносова открыл закон сохранения массы веществ при химических реакциях.
Рис. 49. Опыт, подтверждающий закон Ломоносова — Лавуазье:а — начало опыта; б — окончание опыта
Их масса превышает массу кислорода. Поэтому масса пепла меньше массы бумаги.
При нагревании меди кислород воздуха «соединяется» с ней (рис. 48, б). Металл превращается в вещество черного цвета (его формула — CuO, а на звание — купрум(П) оксид). Очевидно, что масса продукта реакции должна превышать массу меди.
► Прокомментируйте опыт, изображенный на рисунке 49, и сделайте вывод.
Закон как форма научных знаний.
Открытие законов в химии, физике, других науках происходит после проведения учеными многих экспериментов и анализа полученных результатов.
Закон — это обобщение объективных, независимых от человека связей между явлениями, свойствами и т. д.
Закон сохранения массы веществ при химической реакции — важнейший закон химии. Он распространяется на все превращения веществ, которые происходят и в лаборатории, и в природе.
Химические законы дают возможность прогнозировать свойства веществ и протекание химических реакций, регулировать процессы в химической технологии.
Для того чтобы объяснить закон, выдвигают гипотезы, которые проверяют с помощью соответствующих экспериментов. Если одна из гипотез подтверждается, на ее основе создают теорию. В старших классах вы ознакомитесь с несколькими теориями, которые разработали ученые-химики.
Общая масса веществ при химической реакции не изменяется потому, что атомы химических элементов во время реакции не возникают и не исчезают, а происходит только их перегруппировка. Другими словами,
количество атомов каждого элемента до реакции равно количеству его атомов после реакции. На это указывают схемы реакций, приведенные в начале параграфа. Заменим в них стрелки между левыми и правыми частями на знаки равенства:
Такие записи называют химическими уравнениями.
Химическое уравнение — это запись химической реакции с помощью формул реагентов и продуктов, которая согласуется с законом сохранения массы веществ.
Существует много схем реакций^ которые не соответствуют закону Ломоносова — Лавуазье.
Например, схема реакции образования воды:
В обеих частях схемы содержится одинаковое количество атомов Гидрогена, но разное количество атомов Оксигена.
Превратим эту схему в химическое уравнение.
Для того чтобы в правой части было 2 атома Оксигена, поставим перед формулой воды коэффициент 2:
Теперь справа стало четыре атома Гидрогена. Чтобы такое же количество атомов Гидрогена было и в левой части, запишем перед формулой водорода коэффициент 2. Получаем химическое уравнение:
Таким образом, чтобы превратить схему реак ции в химическое уравнение, нужно подобрать коэффициенты для каждого вещества ( в случае необходимости), записать их перед химическими формулами и заменить стрелку на знак равенства.
Возможно, кто-то из вас составит такое уравнение: 4Н2 + 202 = 4Н20. В нем левая и правая части содержат одинаковые количества атомов каждого элемента, но все коэффициенты можно уменьшить, разделив на 2. Это и следует сделать.
Химическое уравнение имеет много общего с математическим.
Ниже представлены различные способы записи рассмотренной реакции.
► Превратите схему реакции Cu + O2 —> CuO в химическое уравнение.
Выполним более сложное задание: превратим в химическое уравнение схему реакции
В левой части схемы — I атом Алюминия, а в правой — 2. Поставим перед формулой металла коэффициент 2:
Атомов Сульфура справа в три раза больше, чем слева. Запишем в левой части перед формулой соединения Сульфура коэффициент 3:
Теперь в левой части количество атомов Гидрогена равно 3 • 2 = 6, а в правой — только 2. Для того чтобы и справа их было 6, поставим перед формулой водорода коэффициент 3 (6 : 2 = 3):
Сопоставим количество атомов Оксигена в обеих частях схемы. Они одинаковы: 3 • 4 = 4 * 3. Заменим стрелку на знак равенства:
Химические реакции записывают с помощью схем реакций и химических уравнений.
Схема реакции содержит формулы реагентов и продуктов, а химическое уравнение — еще и коэффициенты.
Химическое уравнение согласуется с законом сохранения массы веществ Ломоносова — Лавуазье:
Атомы химических элементов во время реакций не появляются и не исчезают, а происходит лишь их перегруппировка.
?
105. Чем отличается химическое уравнение от схемы реакции?
106. Расставьте пропущенные коэффициенты в записях реакций:
107. Превратите в химические уравнения такие схемы реакций:
108. Составьте формулы продуктов реакций и соответствующие химические уравнения:
109. Вместо точек запишите формулы простых веществ и составьте хими ческие уравнения:
Примите во внимание, что бор и углерод состоят из атомов; фтор, хлор, водород и кислород — из двухатомных молекул, а фосфор (белый) — из четырехатомных молекул.
110. Прокомментируйте схемы реакций и превратите их в химические уравнения:
111. Какая масса негашеной извести образовалась при длительном прока ливании 25 г мела, если известно, что выделилось 11 г углекислого газа?
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. — К.: ВЦ «Академія», 2008. — 136 с.: іл.
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь — Образовательный форум.
edufuture.biz
adm-kuzminskiy.ru
Закон сохранения массы и энергии. Величайшее достижение мировой науки
Открытие молекул и атомов явилось важнейшим событием в развитии атомно-молекулярной теории. Ещё в 1748 году великий русский учёный Михаил Васильевич Ломоносов сформулировал закон сохранения массы как философскую концепцию. Он впоследствии сам же подвёл под её доказательство мощную практико-теоретическую базу, и произошло это в 1756 году. Параллельно с российским учёным над этой проблемой работал химик-француз А.Л.Лавуазье. Свой вариант доказательства он предложил в 1789 году.
Закон сохранения массы вещества гласит, что сумма масс всех веществ, которые вступают в химическую реакцию, численно равна массе веществ, являющихся продуктами реакции. Первоначальные способы практически доказать тогда ещё предположение о сохранении масс не увенчались успехом. Дело в том, что опыты, которые проводились ещё до Ломоносова, основывались на сжигании веществ. Результаты взвешивания до и после реакции никак не согласовывались с очевидной, но не подтверждённой на практике теорией. Нагревание на воздухе ртути в результате давало красную окалину, и масса её была больше чем масса вступающего в реакцию металла. С золой, появляющейся после сгорания древесины, результат был противоположный, масса продукта всегда оказывалась меньше массы вещества до осуществления реакции.
Заслуга Ломоносова заключается в том, что он, чтобы доказать закон сохранения массы, впервые проводил опыт с замкнутыми системами. Простота опыта в очередной раз доказала гениальность российского учёного. Прокаливаемые металлы Ломоносов помещал в запаянный стеклянный сосуд. После успешно проведенной реакции вес сосуда оставался неизменным. И только когда сосуд разбивали, и вовнутрь устремлялся воздух, наблюдалось увеличение массы сосуда.
Теоретическое объяснение проведённого эксперимента было дано присоединительным характером реакции горения металла. Увеличение массы происходило за счёт присоединения атомов кислорода в продукт окисления. Доказав закон сохранения массы, Ломоносов осуществил весомый вклад в развитие атомно-молекулярной теории. Практически он ещё раз доказал, что атомы химически неделимы. Конструкции молекул в ходе реакций меняются, они обмениваются между собой атомами, но суммарное их количество (атомов) в замкнутой системе остаётся неизменным. Соответственно и общая масса вещества является величиной постоянной.
Закон сохранения массы стал первым вкладом в познании более глобальной природной закономерности. Дальнейшие исследования в этом направлении позволили выявить, что в замкнутых системах происходит не только сохранение масс. Энергия изолированной системы тоже является величиной постоянной. Любой процесс, происходящий в изолированной системе, не производит и не уничтожает ни массу, ни энергию. А выявленная закономерность впоследствии получила название: закон сохранения массы и энергии. Труды Ломоносова стали лишь доказательством частного случая величайшего закона природы.
Но на этом познание окружающего нас мира не заканчивается. Труды Эйнштейна продвинули науку ещё дальше, в своей теории он не только доказал взаимосвязь энергии и массы, но и сделал смелое предположение о возможности их преобразования. То, что сейчас кажется понятным обыкновенному школьнику, формировалось в ходе практических опытов и теоретических исследований на протяжении трех последних столетий. Учёные в самых различных областях естествознания по крупицам собирали мощную платформу для доказательства закономерностей и осознания понятий «энергия» и «масса».
Не только физика и химия, но и множество других наук активно используют взаимосвязь и принцип сохранения массы и энергии. Биология, география, астрономия находят применение закону сохранения массы и энергии. Даже философия под влиянием этого закона сформировала современное представление человека о бытии.
fb.ru
Закон сохранения массы веществ 1756 год Михаил Васильевич Ломоносов Закон сохранения массы веществ
Закон сохранения массы веществ 1756 год Михаил Васильевич Ломоносов Закон сохранения массы веществ
|
Закон сохранения массы веществ 1756 год Ломоносов В результате химической реакции атомы не исчезают бесследно и не возникают ниоткуда, а происходит только их перегруппировка.
Бойль проделал множество опытов по прокаливанию металлов в запаянных ретортах и всякий раз масса окалины оказывалась больше массы прокаливаемого металла.
Все перемены в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет материи, то умножится в другом месте…Спустя 41 год после опытов Ломоносова французский учёный Антуан Лоран Лавуазье практически повторил формулировку закона в своём учебнике. |
По нашему наблюдению при этой операции была прибыль в весе на 8 граммов…»
Русский учёный
Русский учёный
М.В. Ломоносов предположил, что чувственный опыт обманывает нас. 5 июля 1748 года он написал об этом в письме Леонарду Эйлеру.
Лишь в 1756 году Ломоносову удалось проверить опытным путём теоретически открытый закон сохранения массы вещества при химических реакциях.
Подобно Бойлю русский учёный делал опыт в запаянных ретортах. Но, в отличие от Бойля, Ломоносов взвешивал сосуды как до, так и после прокаливания не вскрывая их.
«Оными опытами нашлось, что славного Роберта Бойля мнение ложно, ибо без пропущения внешнего воздуха вес сожжённого металла остаётся в одной мере…»
Русский учёный
5 июля 1748 года он написал об этом в письме Леонарду Эйлеру.
Лишь в 1756 году Ломоносову удалось проверить опытным путём теоретически открытый закон сохранения массы вещества при химических реакциях.
Подобно Бойлю русский учёный делал опыт в запаянных ретортах. Но, в отличие от Бойля, Ломоносов взвешивал сосуды как до, так и после прокаливания не вскрывая их.
«Оными опытами нашлось, что славного Роберта Бойля мнение ложно, ибо без пропущения внешнего воздуха вес сожжённого металла остаётся в одной мере…»
Закон сохранения массы веществ
2. На основании закона сохранения массы веществ производят практически важные расчёты. 3. На основании закона сохранения массы веществ составляют уравнения химических реакций.
Похожие:
| Закон сохранения массы Закон сохранения массы Периодический закон (общие сведения) Закон постоянства состава Закон кратных отношений Закон объёмных отношений М. Ломоносов, 1748; А. Лавуазье, 1789 Масса веществ, вступивших в реакцию, равна массе всех продуктов реакции | Закон сохранения массы веществ в химических реакциях, который открыл М. В. Ломоносов Показал опыт : Вуквун Е. ученик 11 класса Под руководством: Павловой Т. М Опыт, подтверждающий закон сохранения массы веществ в химических реакциях, который открыл М. В. Ломоносов | ||
| Закон сохранения массы веществ Выполнили: ученики 9 «Б» класса моу сош №3 г. Хвалынска Учитель: Грачёва Ирина Александровна Цели и задачи Цели В течение тысячелетий люди верили в то, что вещество может бесследно исчезать, а также возникать из ничего. Это чисто житейское утверждение… | Лекция 2 Аэродинамика Эти законы называются «законами сохранения», так как они выражают свойство сохранения массы, энергии и импульса для каждого элементарного… | ||
| Ломоносов михаил Васильевич ломоносов михаил Васильевич Много горя и нужды претерпел здесь Ломоносов: укоры отца, «несказанная бедность», насмешки школьников | Михаил Васильевич Ломоносов родился Михаил Васильевич Ломоносов родился В 1736 году Ломоносов был отправлен Академией наук в германию для обучения математике, физике, философии, химии и металлургии. За… | ||
| Михаил васильевич Ломоносов Его вклад в технику Михаил Васильевич Ломоносов «…по объёму и оригинальности своей оптико-строительной деятельности Ломоносов был … одним из самых передовых оптиков своего времени… | «Наш первый университет» Михаил Васильевич Ломоносов Биография Михаил Васильевич Ломоносов родился в 1711 году в одной из деревень близи Холмогор Архангельской губернии. Семья имела… | ||
| Ломоносов михаил васильевич В 1711 году, родился Михаил Васильевич Ломоносов, человек, который окончательно разделил науку и искусство, чудесным образом сочетая… | Михаил Васильевич Ломоносов биография Михаил Васильевич Ломоносов (1711-1765) первый русский ученый-естествоиспытатель мирового значения, поэт, заложивший основы современного… |
rpp.nashaucheba.ru rpp.nashaucheba.ru
rpp.nashaucheba.ru
