Что такое раствор? Как сделать раствор? Свойства растворов. Применение растворов
Много ли в природе химически чистых веществ? Что представляет собой морская вода, молоко, проволока из стали – индивидуальные вещества, или же они состоят из нескольких компонентов? В нашей статье мы ознакомимся со свойствами растворов – наиболее распространенных физико-химических систем, имеющих переменный состав. Они могут содержать несколько компонентов. Так, молоко – это органический раствор, содержащий воду, капли жира, молекулы белка и минеральных солей. Что такое раствор и как его можно получить? На этот и другие вопросы мы ответим в нашей статье.
Применение растворов и их роль в природе
Обмен веществ в биогеоценозах осуществляется в виде взаимодействия соединений, растворенных в воде. Например, всасывание почвенного раствора корнями растений, накопление крахмала в результате фотосинтеза у растений, пищеварительные процессы животных и человека – все они представляют собой реакции, протекающие в химических растворах. Невозможно представить современные отрасли: космическое и авиастроение, военную промышленность, атомную энергетику без применения сплавов — твердых растворов с уникальными техническими характеристиками. Несколько газов также могут образовывать смеси, которые мы можем назвать растворами. Например, воздух — это физико-химическая система, которая содержит такие компоненты как азот, кислород, углекислый газ и т. д.

Что такое раствор?
Смешивая между собой сульфатную кислоту и воду, получим ее водный раствор. Рассмотрим, из чего он состоит. Мы обнаружим растворитель – воду, растворенное вещество – серную кислоту и продукты их взаимодействия. К ним относятся катионы водорода, гидросульфат — и сульфат ионы. Состав физико-химической системы, состоящей из растворителя и компонентов, будет зависеть не только от того, какое вещество является растворителем.
Наиболее распространенный и важный растворитель — это вода. Большое значение имеет и природа растворяемых компонентов. Их можно условно разделить на три группы. Это практически нерастворимые соединения, малорастворимые и хорошо растворимые. Последняя группа является наиболее важной. К ней относится большинство солей, кислоты, щелочи, спирты, моносахариды. Малорастворимые соединения тоже встречаются в природе достаточно часто. Это гипс, азот, метан, кислород. Практически нерастворимыми в воде будут металлы, благородные газы: аргон, гелий и т. д., керосин, масла.

Как количественно выразить растворимость соединения
Концентрация насыщенного раствора – наиболее важная величина, показывающая растворимость вещества. Ее выражают величиной, численно равной массе соединения в 100 г раствора. Например, дезинфицирующее медицинское средство – салициловый спирт продается в аптеках в виде 1 % спиртового раствора. Это значит, что в 100 г раствора содержится 1 грамм действующего вещества. Какую наибольшую массу хлорида натрия можно растворить в 100 г растворителя при определенной температуре? Найти ответ на этот вопрос можно с помощью специальной таблицы кривых растворимости твердых соединений. Так, при температуре 10 ⁰С можно растворить 38 г поваренной соли в 100 г воды, при 80 ⁰С — 40 г вещества. Как сделать раствор разбавленным? Нужно прилить к нему определенный объем воды. Увеличить концентрацию физико-химической системы можно, выпаривая раствор, или же, прибавляя к нему определенную порцию растворяемого соединения.

Виды растворов
При определенной температуре система может пребывать в равновесии с растворяемым соединением в виде его осадка. В этом случае говорят о насыщенном растворе. Как сделать раствор насыщенным? Для этого нужно обратиться к таблице растворимости твердых веществ. Например, поваренную соль массой 31 г вводят в воду при температуре 20 ºС и нормальном давлении, затем хорошо размешивают. При дополнительном нагревании и введении дополнительной порции соли ее избыток обеспечивает образование пересыщенного раствора. Остывание системы приведет к процессу выпадения кристаллов хлорида натрия. Разбавленными будут называться такие растворы, в которых концентрация соединений по сравнению с объемом растворителя будет достаточной малой. Например, физиологический раствор, входящий в состав кровяной плазмы и применяемый в медицине после перенесенных хирургических вмешательств, представляет собой 0,9 % раствор хлорида натрия.
Механизм растворения веществ
Рассмотрев вопрос, что такое раствор, определим, какие процессы лежат в основе его образования. В основе явления растворения веществ мы видим взаимодействие как физических, так и химических превращений. Главную роль в них играет явление разрушения химических связей: ковалентных полярных или ионных, в молекулах растворяемого соединения. Физический аспект разрыва связей выражается в поглощении энергии. Также происходит взаимодействие частиц растворителя с молекулами растворенного вещества, называемое сольватацией, в случае водных растворов – гидратацией. Оно сопровождается не только возникновением новых связей, но и выделением энергии.

В нашей статье мы рассмотрели вопрос, что такое раствор, а также выяснили механизм образования растворов и их значение.
fb.ru
Растворы — это… Что такое Растворы?
Растворение соли в воде
Раство́р — гомогенная (однородная) смесь, образованная не менее чем двумя компонентами, один из которых называется растворителем, а другой растворимым веществом, это также система переменного состава, находящаяся в состоянии химического равновесия
Твердые, жидкие, газообразные растворы
Чаще под раствором подразумевается жидкое вещество, например раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама).
Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше.
В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким, твердым (твёрдый раствор), газообразным. Однако нередко допускается и микрогетерогенность — см. «Золи».
Раствором именуют и смесь цемента с водой, песком и т.д. Хотя это и не является раствором в химическом смысле этого слова.
Истинные и коллоидные растворы
В истинных растворах размер частиц менее 1·10−9 м, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах размер частиц 1·10−9 м — 5·10−7 м, частицы в таких растворах можно обнаружить при помощи ультрамикроскопа (см. эффект Тиндаля).
Растворение
Растворение — переход молекул вещества из одной фазы в другую (раствор, растворенное состояние). Происходит в результате взаимодействия атомов (молекул) растворителя и растворённого вещества и сопровождается увеличением энтропии. При растворении межфазная граница исчезает, при этом многие физические свойства раствора (например, плотность, вязкость, иногда — цвет, и другие) меняются.
В случае химического взаимодействия растворителя и растворенного вещества сильно меняются и химические свойства — например, при растворении газа хлороводорода в воде образуется жидкая соляная кислота.
См. также
Растворы электролитов и неэлектролитов
Электролиты при растворении в подходящих растворителях (вода, другие полярные растворители) диссоциируют на ионы. Сильное физико-химическое взаимодействие при растворении приводит к сильному изменению свойств раствора (химическая теория растворов).
См. также
Растворы полимеров
Растворы высокомолекулярных веществ ВМС — белков, углеводов и др. обладают одновременно многими свойствами истинных и коллоидных растворов. Средняя молекулярная масса растворенного
В зависимости от цели для выражения концентрации растворов используются разные единицы измерения — весовой и объёмный процент, молярность, моляльность, г/л, мольная доля и др.
Мнемонические правила
В случаях приготовления растворов сильных кислот согласно правилам техники безопасности кислоту нужно лить в воду, но ни в коем случае не наоборот. Для запоминания этого лабораторного приема существует несколько мнемонических правил:
Сначала вода,
Потом кислота,
Иначе случится
Большая беда
- Не плюй в кислоту!
- Чай с лимоном (здесь нужно представить, как в чай Вы кладете дольку лимона).
См. также
Wikimedia Foundation. 2010.
dic.academic.ru
Истинные растворы — это… Что такое Истинные растворы?
Растворение соли в воде
Раство́р — гомогенная (однородная) смесь, образованная не менее чем двумя компонентами, один из которых называется растворителем, а другой растворимым веществом, это также система переменного состава, находящаяся в состоянии химического равновесия
Твердые, жидкие, газообразные растворы
Чаще под раствором подразумевается жидкое вещество, например раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама).
Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше.
В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким, твердым (твёрдый раствор), газообразным. Однако нередко допускается и микрогетерогенность — см. «Золи».
Раствором именуют и смесь цемента с водой, песком и т.д. Хотя это и не является раствором в химическом смысле этого слова.
Истинные и коллоидные растворы
Коллоидные и истинные растворы (изучением коллоидных систем занимается коллоидная химия) отличаются главным образом размерами частиц.
В истинных растворах размер частиц менее 1·10−9 м, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах размер частиц 1·10−9 м — 5·10−7 м, частицы в таких растворах можно обнаружить при помощи ультрамикроскопа (см. эффект Тиндаля).
Растворение
В случае химического взаимодействия растворителя и растворенного вещества сильно меняются и химические свойства — например, при растворении газа хлороводорода в воде образуется жидкая соляная кислота.
См. также
Растворы электролитов и неэлектролитов
Электролиты при растворении в подходящих растворителях (вода, другие полярные растворители) диссоциируют на ионы. Сильное физико-химическое взаимодействие при растворении приводит к сильному изменению свойств раствора (химическая теория растворов).
См. также
Растворы полимеров
Растворы высокомолекулярных веществ ВМС — белков, углеводов и др. обладают одновременно многими свойствами истинных и коллоидных растворов. Средняя молекулярная масса растворенного
В зависимости от цели для выражения концентрации растворов используются разные единицы измерения — весовой и объёмный процент, молярность, моляльность, г/л, мольная доля и др.
Мнемонические правила
В случаях приготовления растворов сильных кислот согласно правилам техники безопасности кислоту нужно лить в воду, но ни в коем случае не наоборот. Для запоминания этого лабораторного приема существует несколько мнемонических правил:
Сначала вода,
Потом кислота,
Иначе случится
Большая беда
- Не плюй в кислоту!
- Чай с лимоном (здесь нужно представить, как в чай Вы кладете дольку лимона).
См. также
Wikimedia Foundation. 2010.
dic.academic.ru
РАСТВОРЫ | Энциклопедия Кругосвет
Содержание статьиРАСТВОРЫ, однофазные системы, состоящие из двух или более компонентов. По своему агрегатному состоянию растворы могут быть твердыми, жидкими или газообразными. Так, воздух – это газообразный раствор, гомогенная смесь газов; водка – жидкий раствор, смесь нескольких веществ, образующих одну жидкую фазу; морская вода – жидкий раствор, смесь твердого (соль) и жидкого (вода) веществ, образующих одну жидкую фазу; латунь – твердый раствор, смесь двух твердых веществ (меди и цинка), образующих одну твердую фазу. Смесь бензина и воды не является раствором, поскольку эти жидкости не растворяются друг в друге, оставаясь в виде двух жидких фаз с границей раздела. Компоненты растворов сохраняют свои уникальные свойства и не вступают в химические реакции между собой с образованием новых соединений. Так, при смешивании двух объемов водорода с одним объемом кислорода получается газообразный раствор. Если эту газовую смесь поджечь, то образуется новое вещество – вода, которая сама по себе раствором не является. Компонент, присутствующий в растворе в большем количестве, принято называть растворителем, остальные компоненты – растворенными веществами.
Однако иногда бывает трудно провести грань между физическим перемешиванием веществ и их химическим взаимодействием. Например, при смешивании газообразного хлороводорода HCl с водой H2O образуются ионы H3O+ и Cl–. Они притягивают к себе соседние молекулы воды, образуя гидраты. Таким образом, исходные компоненты – HCl и H2O – после смешивания претерпевают существенные изменения. Тем не менее ионизация и гидратация (в общем случае – сольватация) рассматриваются как физические процессы, происходящие при образовании растворов.
Одним из важнейших типов смесей, представляющих собой гомогенную фазу, являются коллоидные растворы: гели, золи, эмульсии и аэрозоли. Размер частиц в коллоидных растворах составляет 1–1000 нм, в истинных растворах ~0,1 нм (порядка размера молекул).
Основные понятия.
Два вещества, растворяющиеся друг в друге в любых пропорциях с образованием истинных растворов, называют полностью взаиморастворимыми. Такими веществами являются все газы, многие жидкости (например, этиловый спирт – вода, глицерин – вода, бензол – бензин), некоторые твердые вещества (например, серебро – золото). Для получения твердых растворов необходимо сначала расплавить исходные вещества, затем смешать их и дать затвердеть. При их полной взаиморастворимости образуется одна твердая фаза; если же растворимость частичная, то в образовавшемся твердом веществе сохраняются мелкие кристаллы одного из исходных компонентов.
Если два компонента образуют одну фазу при смешивании только в определенных пропорциях, а в других случаях возникают две фазы, то они называются частично взаиморастворимыми. Таковы, например, вода и бензол: истинные растворы получаются из них только при добавлении незначительного количества воды к большому объему бензола или незначительного количества бензола к большому объему воды. Если же смешать равные количества воды и бензола, то образуется двухфазная жидкая система. Нижний ее слой – это вода с небольшим количеством бензола, а верхний – бензол с малой примесью воды. Известны также вещества, совсем не растворяющиеся одно в другом, например, вода и ртуть. Если два вещества лишь частично взаиморастворимы, то при данных температуре и давлении существует предельное количество одного вещества, которое способно образовать истинный раствор с другим в равновесных условиях. Раствор с предельной концентрацией растворенного вещества называют насыщенным. Можно приготовить и так называемый пересыщенный раствор, в котором концентрация растворенного вещества даже больше, чем в насыщенном. Однако пересыщенные растворы неустойчивы, и при малейшем изменении условий, например при перемешивании, попадании частичек пыли или добавлении кристалликов растворяемого вещества, избыток растворенного вещества выпадает в осадок.
Всякая жидкость начинает кипеть при той температуре, при которой давление ее насыщенного пара достигает величины внешнего давления. Например, вода под давлением 101,3 кПа кипит при 100° С потому, что при этой температуре давление водяного пара как раз равно 101,3 кПа. Если же растворить в воде какое-нибудь нелетучее вещество, то давление ее пара понизится. Чтобы довести давление пара полученного раствора до 101,3 кПа, нужно нагреть раствор выше 100° С. Отсюда следует, что температура кипения раствора всегда выше температуры кипения чистого растворителя. Аналогично объясняется и понижение температуры замерзания растворов.
Закон Рауля.
В 1887 французский физик Ф.Рауль, изучая растворы различных нелетучих жидкостей и твердых веществ, установил закон, связывающий понижение давления пара над разбавленными растворами неэлектролитов с концентрацией: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества. Из закона Рауля следует, что повышение температуры кипения или понижение температуры замерзания разбавленного раствора по сравнению с чистым растворителем пропорционально молярной концентрации (или мольной доле) растворенного вещества и может быть использовано для определения его молекулярной массы.
Раствор, поведение которого подчиняется закону Рауля, называется идеальным. Наиболее близки к идеальным растворы неполярных газов и жидкостей (молекулы которых не меняют ориентации в электрическом поле). В этом случае теплота растворения равна нулю, а свойства растворов можно прямо предсказать, зная свойства исходных компонентов и пропорции, в которых они смешиваются. Для реальных растворов сделать такое предсказание нельзя. При образовании реальных растворов обычно выделяется или поглощается тепло. Процессы с выделением тепла называются экзотермическими, а с поглощением – эндотермическими.
Те характеристики раствора, которые зависят в основном от его концентрации (числа молекул растворенного вещества на единицу объема или массы растворителя), а не от природы растворенного вещества, называют коллигативными. Например, температура кипения чистой воды при нормальном атмосферном давлении равна 100° С, а температура кипения раствора, содержащего 1 моль растворенного (недиссоциирующего) вещества в 1000 г воды, составляет уже 100,52° С независимо от природы этого вещества. Если же вещество диссоциирует, образуя ионы, то температура кипения увеличивается пропорционально росту общего числа частиц растворенного вещества, которое благодаря диссоциации превышает число молекул вещества, добавленных в раствор. Другими важными коллигативными величинами являются температура замерзания раствора, осмотическое давление и парциальное давление паров растворителя.
Концентрация раствора
– это величина, отражающая пропорции между растворенным веществом и растворителем. Такие качественные понятия, как «разбавленный» и «концентрированный», говорят только о том, что раствор содержит мало или много растворенного вещества. Для количественного выражения концентрации растворов часто используют проценты (массовые или объемные), а в научной литературе – число молей или химических эквивалентов (см. ЭКВИВАЛЕНТНАЯ МАССА) растворенного вещества на единицу массы или объема растворителя либо раствора. Чтобы не возникало путаницы, следует всегда точно указывать единицы измерения концентрации. Рассмотрим следующий пример. Раствор, состоящий из 90 г воды (ее объем равен 90 мл, поскольку плотность воды равна 1г/мл) и 10 г этилового спирта (его объем равен 12,6 мл, поскольку плотность спирта равна 0,794 г/мл), имеет массу 100 г, но объем этого раствора равен 101,6 мл (а был бы равен 102,6 мл, если бы при смешивании воды и спирта их объемы просто складывались). Процентную концентрацию раствора можно рассчитать по-разному:
или
или
Единицы концентраций, используемые в научной литературе, основаны на таких понятиях, как моль и эквивалент, поскольку все химические расчеты и уравнения химических реакций должны основываться на том, что вещества вступают в реакции между собой в определенных соотношениях. Например, 1 экв. NaCl, равный 58,5 г, взаимодействует с 1 экв. AgNO3, равным 170 г. Ясно, что растворы, содержащие по 1 экв. этих веществ, имеют совершенно разные процентные концентрации.
Молярность
(M или моль/л) – число молей растворенного веществ, содержащихся в 1 л раствора.
Моляльность
(м) – число молей растворенного вещества, содержащихся в 1000 г растворителя.
Нормальность
(н.) – число химических эквивалентов растворенного вещества, содержащихся в 1 л раствора.
Мольная доля
(безразмерная величина) – число молей данного компонента, отнесенное к общему числу молей растворенного вещества и растворителя. (Мольный процент – мольная доля, умноженная на 100.)
Наиболее распространенная единица – молярность, но при ее расчете следует учитывать некоторые неоднозначности. Например, чтобы получить 1M раствор данного вещества, растворяют в заведомо небольшом количестве воды точную его навеску, равную мол. массе в граммах, и доводят объем раствора до 1 л. Количество воды, необходимое для приготовления данного раствора, может слегка различаться в зависимости от температуры и давления. Поэтому два одномолярных раствора, приготовленных в разных условиях, в действительности имеют не совсем одинаковые концентрации. Моляльность вычисляется исходя из определенной массы растворителя (1000 г), которая не зависит от температуры и давления. В лабораторной практике гораздо удобнее отмеривать определенные объемы жидкостей (для этого существуют бюретки, пипетки, мерные колбы), чем взвешивать их, поэтому в научной литературе концентрации чаще выражают в молях, а моляльность обычно применяют только при особо точных измерениях.
Нормальность используется для упрощения расчетов. Как мы уже говорили, вещества взаимодействуют друг с другом в количествах, соответствующих их эквивалентам. Приготовив растворы разных веществ одинаковой нормальности и взяв равные их объемы, мы можем быть уверены в том, что они содержат одно и то же количество эквивалентов.
В тех случаях, когда трудно (или нет необходимости) делать различие между растворителем и растворенным веществом, концентрацию измеряют в мольных долях. Мольные доли, как и моляльности, не зависят от температуры и давления.
Зная плотности растворенного вещества и раствора, можно пересчитать одну концентрацию в другую: молярность в моляльность, мольную долю и наоборот. Для разбавленных растворов данного растворенного вещества и растворителя эти три величины пропорциональны друг другу.
Растворимость
данного вещества – это его способность образовывать растворы с другими веществами. Количественно растворимость газа, жидкости или твердого тела измеряется концентрацией их насыщенного раствора при данной температуре. Это важная характеристика вещества, помогающая понять его природу, а также влиять на ход реакций, в которых это вещество участвует.
Газы.
В отсутствие химического взаимодействия газы смешиваются друг с другом в любых пропорциях, и в этом случае говорить о насыщении нет смысла. Однако при растворении газа в жидкости существует некая предельная концентрация, зависящая от давления и температуры. Растворимость газов в некоторых жидкостях коррелирует с их способностью к сжижению. Наиболее легко сжижаемые газы, например NH3, HCl, SO2, более растворимы, чем трудно сжижаемые газы, например O2, H2 и He. При наличии химического взаимодействия между растворителем и газом (например, между водой и NH3 или HCl) растворимость увеличивается. Растворимость данного газа изменяется с природой растворителя, однако порядок, в котором располагаются газы в соответствии с увеличением их растворимости, остается примерно одинаковым для разных растворителей.
Процесс растворения подчиняется принципу Ле Шателье (1884): если на систему, находящуюся в равновесии, оказывается какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится. Растворение газов в жидкостях обычно сопровождается выделением тепла. При этом, в соответствии с принципом Ле Шателье, растворимость газов уменьшается. Это уменьшение тем заметнее, чем выше растворимость газов: такие газы имеют и бóльшую теплоту растворения. «Мягкий» вкус кипяченой или дистиллированной воды объясняется отсутствием в ней воздуха, поскольку его растворимость при высокой температуре весьма мала.
С ростом давления растворимость газов увеличивается. Согласно закону Генри (1803), масса газа, который может раствориться в данном объеме жидкости при постоянной температуре, пропорциональна его давлению. Это свойство используется для приготовления газированных напитков. Углекислый газ растворяют в жидкости при давлении 3–4 атм.; в этих условиях в данном объеме может раствориться в 3–4 раза больше газа (по массе), чем при 1 атм. Когда емкость с такой жидкостью открывают, давление в ней падает, и часть растворенного газа выделяется в виде пузырьков. Аналогичный эффект наблюдается при открывании бутылки шампанского или выходе на поверхность подземных вод, насыщенных на большой глубине углекислым газом.
При растворении в одной жидкости смеси газов растворимость каждого из них остается такой же, как и в отсутствие других компонентов при таком же давлении, как в случае смеси (закон Дальтона).
Жидкости.
Взаимная растворимость двух жидкостей определяется тем, насколько сходно строение их молекул («подобное растворяется в подобном»). Для неполярных жидкостей, например углеводородов, характерны слабые межмолекулярные взаимодействия, поэтому молекулы одной жидкости легко проникают между молекулами другой, т.е. жидкости хорошо смешиваются. Напротив, полярные и неполярные жидкости, например вода и углеводороды, смешиваются друг с другом плохо. Каждой молекуле воды нужно сначала вырваться из окружения других таких же молекул, сильно притягивающими ее к себе, и проникнуть между молекулами углеводорода, притягивающими ее слабо. И наоборот, молекулы углеводорода, чтобы раствориться в воде, должны протиснуться между молекулами воды, преодолевая их сильное взаимное притяжение, а для этого нужна энергия. При повышении температуры кинетическая энергия молекул возрастает, межмолекулярное взаимодействие ослабевает и растворимость воды и углеводородов увеличивается. При значительном повышении температуры можно добиться их полной взаимной растворимости. Такую температуру называют верхней критической температурой растворения (ВКТР).
В некоторых случаях взаимная растворимость двух частично смешивающихся жидкостей увеличивается при понижении температуры. Этот эффект наблюдается в том случае, когда при смешивании выделяется тепло, обычно в результате химической реакции. При значительном понижении температуры, но не ниже точки замерзания, можно достичь нижней критической температуры растворения (НКТР). Можно предположить, что все системы, имеющие НКТР, имеют и ВКТР (обратное не обязательно). Однако в большинстве случаев одна из смешивающихся жидкостей кипит при температуре ниже ВКТР. У системы никотин–вода НКТР равна 61° С, а ВКТР составляет 208° C. В интервале 61–208° C эти жидкости ограниченно растворимы, а вне этого интервала обладают полной взаимной растворимостью.
Твердые вещества.
Все твердые вещества проявляют ограниченную растворимость в жидкостях. Их насыщенные растворы имеют при данной температуре определенный состав, который зависит от природы растворенного вещества и растворителя. Так, растворимость хлорида натрия в воде в несколько миллионов раз выше растворимости нафталина в воде, а при растворении их в бензоле наблюдается обратная картина. Этот пример иллюстрирует общее правило, согласно которому твердое вещество легко растворяется в жидкости, имеющей с ним сходные химические и физические свойства, но не растворяется в жидкости с противоположными свойствами.
Соли обычно легко растворяются в воде и хуже – в других полярных растворителях, например в спирте и жидком аммиаке. Однако растворимость солей тоже существенно различается: например, нитрат аммония обладает в миллионы раз большей растворимостью в воде, чем хлорид серебра.
Растворение твердых веществ в жидкостях обычно сопровождается поглощением тепла, и в соответствии с принципом Ле Шателье их растворимость должна увеличиваться при нагревании. Этот эффект можно использовать для очистки веществ методом перекристаллизации. Для этого их растворяют при высокой температуре до получения насыщенного раствора, затем раствор охлаждают и после выпадения растворенного вещества в осадок профильтровывают. Есть вещества (например, гидроксид, сульфат и ацетат кальция), растворимость которых в воде с ростом температуры уменьшается.
Твердые вещества, как и жидкости, тоже могут растворяться друг в друге полностью, образуя гомогенную смесь – истинный твердый раствор, аналогичный жидкому раствору. Частично растворимые друг в друге вещества образуют два равновесных сопряженных твердых раствора, составы которых изменяются с температурой.
Коэффициент распределения.
Если к равновесной системе двух несмешивающихся или частично смешивающихся жидкостей добавить раствор какого-либо вещества, то оно распределяется между жидкостями в определенной пропорции, не зависящей от общего количества вещества, в отсутствие химических взаимодействий в системе. Это правило получило название закона распределения, а отношение концентраций растворенного вещества в жидкостях – коэффициента распределения. Коэффициент распределения примерно равен отношению растворимостей данного вещества в двух жидкостях, т.е. вещество распределяется между жидкостями соответственно его растворимостям. Это свойство используется для экстракции данного вещества из его раствора в одном растворителе с помощью другого растворителя. Еще одним примером его применения является процесс экстракции серебра из руд, в состав которых оно часто входит вместе со свинцом. Для этого в расплавленную руду добавляют цинк, который не смешивается со свинцом. Серебро распределяется между расплавленным свинцом и цинком, преимущественно в верхнем слое последнего. Этот слой собирают и отделяют серебро дистилляцией цинка.
Произведение растворимости
(ПР). Между избытком (осадком) твердого вещества MxBy и его насыщенным раствором устанавливается динамическое равновесие, описываемое уравнением
Константа равновесия этой реакции равна
и называется произведением растворимости. Она постоянна при данных температуре и давлении и является величиной, на основании которой рассчитывают растворимость осадка и изменяют ее. Если в раствор добавить соединение, диссоциирующее на ионы, одноименные с ионами малорастворимой соли, то в соответствии с выражением для ПР растворимость соли уменьшается. При добавлении же соединения, реагирующего с одним из ионов, она, напротив, увеличится.
О некоторых свойствах растворов ионных соединений см. также ЭЛЕКТРОЛИТЫ.
www.krugosvet.ru
Понятие о растворах. Растворимость веществ
Растворы — гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов.


Наиболее распространены жидкие растворы. Они состоят из растворителя (жидкости) и растворенных веществ (газообразных, жидких, твердых):
Жидкие растворы могут быть водные и неводные. Водные растворы — это растворы, в которых растворителем является вода. Неводные растворы — это растворы, в которых растворителями являются другие жидкости (бензол, спирт, эфир и т. д.). На практике чаще применяются водные растворы.
Растворение веществ
Растворение — сложный физико-химический процесс. Разрушение структуры растворяемого вещества и распределение его частиц между молекулами растворителя — это физический процесс. Одновременно происходит взаимодействие молекул растворителя с частицами растворенного вещества, т.е. химический процесс. В результате этого взаимодействия образуются сольваты.
Сольваты — продукты переменного состава, которые образуются при химическом взаимодействии частиц растворенного вещества с молекулами растворителя.
Если растворителем является вода, то образующиеся сольваты называются гидратами. Процесс образования сольватов называется сольватацией. Процесс образования гидратов называется гидратацией. Гидраты некоторых веществ можно выделить в кристаллическом виде при выпаривании растворов. Например:
Что представляет собой и как образуется кристаллическое вещество синего цвета? При растворении в воде сульфата меди (II) происходит его диссоциация на ионы:
Образующиеся ионы взаимодействуют с молекулами воды:
При выпаривании раствора образуется кристаллогидрат сульфата меди (II) — CuSО4 • 5Н2О.
Кристаллические вещества, содержащие молекулы воды, называются кристаллогидратами. Вода, входящая в их состав, называется кристаллизационной водой. Примеры кристаллогидратов:


Впервые идею о химическом характере процесса растворения высказал Д. И. Менделеев в разработанной им химической (гидратной) теории растворов (1887 г.). Доказательством физико-химического характера процесса растворения являются тепловые эффекты при растворении, т. е. выделение или поглощение теплоты.
Тепловой эффект растворения равен сумме тепловых эффектов физического и химического процессов. Физический процесс протекает с поглощением теплоты, химический — с выделением.
Если в результате гидратации (сольватации) выделяется больше теплоты, чем ее поглощается при разрушении структуры вещества, то растворение — экзотермический процесс. Выделение теплоты наблюдается, например, при растворении в воде таких веществ, как NaOH, AgNО3, H2SО4, ZnSО4 и др.
Если для разрушения структуры вещества необходимо больше теплоты, чем ее образуется при гидратации, то растворение — эндотермический процесс. Это происходит, например, при растворении в воде NaNО3, KCl, K2SO4, KNO2, NH4Cl и др.
Растворимость веществ
Мы знаем, что одни вещества хорошо растворяются, другие — плохо. При растворении веществ образуются насыщенные и ненасыщенные растворы.
Насыщенный раствор — это раствор, который содержит максимальное количество растворяемого вещества при данной температуре.
Ненасыщенный раствор — это раствор, который содержит меньше растворяемого вещества, чем насыщенный при данной температуре.
Количественной характеристикой растворимости является коэффициент растворимости. Коэффициент растворимости показывает, какая максимальная масса вещества может раствориться в 1000 мл растворителя при данной температуре.
Растворимость выражают в граммах на литр (г/л).
По растворимости в воде вещества делят на 3 группы: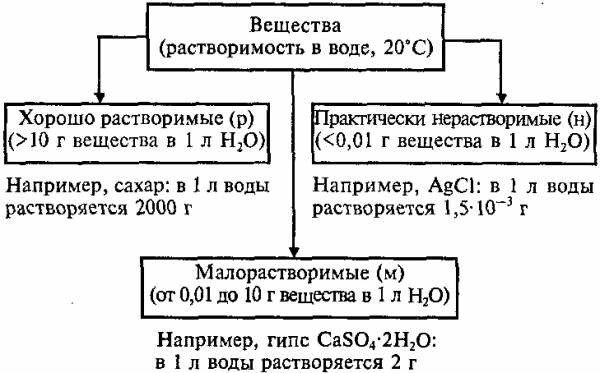

Таблица растворимости солей, кислот и оснований в воде: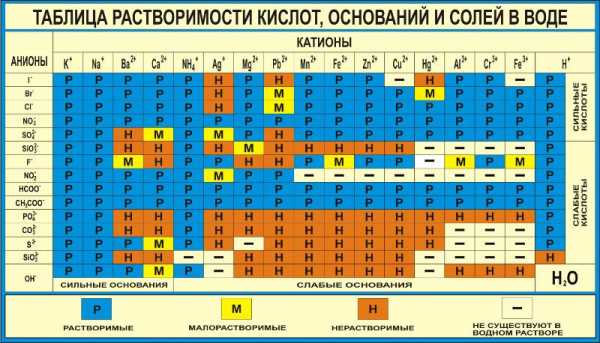

Растворимость веществ зависит от природы растворителя, от природы растворенного вещества, температуры, давления (для газов). Растворимость газов при повышении температуры уменьшается, при повышении давления — увеличивается.
Зависимость растворимости твердых веществ от температуры показывают кривые растворимости. Растворимость многих твердых веществ увеличивается при повышении температуры.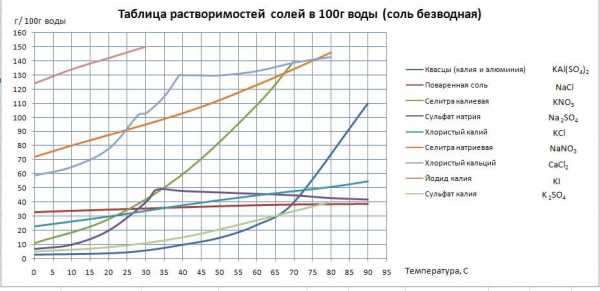

По кривым растворимости можно определить: 1) коэффициент растворимости веществ при различных температурах; 2) массу растворенного вещества, которое выпадает в осадок при охлаждении раствора от t1oC до t2oC.
Процесс выделения вещества путем испарения или охлаждения его насыщенного раствора называется перекристаллизацией. Перекристаллизация используется для очистки веществ.
Читайте также
Похожее
al-himik.ru
Раствор — WiKi
 Растворение поваренной соли (NaCl) в воде
Растворение поваренной соли (NaCl) в воде
Раство́р — гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия. «Гомогенный» — значит, что каждый из компонентов распределен в массе другого в виде своих частиц, то есть атомов, молекул или ионов[1].
Раствор — однофазная система переменного, или гетерогенного, состава, состоящая из двух или более компонентов.
Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает[1].
Образование того или иного типа раствора обусловливается интенсивностью межмолекулярного, межатомного, межионного или другого вида взаимодействия, то есть теми же силами, которые определяют возникновение того или иного агрегатного состояния. Отличия: образование раствора зависит от характера и интенсивности взаимодействия частиц разных веществ[1].
По сравнению с индивидуальными веществами по структуре растворы сложнее[1].
Химическое взаимодействие растворенного вещества с водой приводит к образованию соединений, которые называются гидратами. Их формулы выражают с помощью формул растворенного вещества и воды, соединённых знаком «.»
Гидратную теорию растворов предложил русский учёный Д. И. Менделеев.
Гидратация — процесс взаимодействия растворяемого вещества с водой.
Кристаллогидраты — кристаллы, в состав которых входят молекулы воды; вода, содержащаяся в кристаллогидратах, — кристаллизационная.
Твёрдые, жидкие, газообразные растворы
Чаще всего под раствором подразумевается жидкое вещество, например, раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама).
Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше.
В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким (водный раствор), твёрдым (твёрдый раствор), газообразным. Однако нередко допускается и гетерогенность — см. «Золи».
«Раствором» именуют и смесь цемента с водой, песком и так далее. Хотя это и не является раствором в химическом смысле этого слова.
Истинные и коллоидные растворы
Коллоидные и истинные/молекулярные растворы (изучением коллоидных систем занимается коллоидная химия) отличаются главным образом размерами частиц.
В истинных растворах размер частиц менее 1 нм, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах размер частиц 1 нм — 500000 нм, частицы в таких растворах можно обнаружить при помощи ультрамикроскопа (см. эффект Тиндаля).
Растворение
Растворение — переход молекул вещества из одной фазы в другую (раствор, растворенное состояние). Происходит в результате взаимодействия атомов (молекул) растворителя и растворённого вещества и сопровождается увеличением энтропии при растворении твёрдых веществ и её уменьшением при растворении газов. При растворении межфазная граница исчезает, при этом многие физические свойства раствора (например, плотность, вязкость, иногда — цвет, и другие) меняются.
В случае химического взаимодействия растворителя и растворённого вещества сильно меняются и химические свойства — например, при растворении газа хлороводорода в воде образуется жидкая соляная кислота.
При растворении кристаллических веществ, растворимость которых увеличивается с увеличением температуры, происходит охлаждение раствора ввиду того, что у раствора внутренняя энергия больше, чем у кристаллического вещества и растворителя, взятых отдельно. Например, кипяток, в котором растворяют сахар, сильно охлаждается[2].
Растворы электролитов и неэлектролитов
Электролиты — вещества, проводящие в расплавах или водных растворах электрический ток. В расплавах или водных растворах они диссоциируют на ионы.
Неэлектролиты — вещества, водные растворы и расплавы которых не проводят электрический ток, так как их молекулы не диссоциируют на ионы. Электролиты при растворении в подходящих растворителях (вода, другие полярные растворители) диссоциируют на ионы. Сильное физико-химическое взаимодействие при растворении приводит к сильному изменению свойств раствора (химическая теория растворов).
Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
К электролитам относятся кислоты, основания и почти все соли, к неэлектролитам — большинство органических соединений, а также вещества, в молекулах которых имеются только ковалентные неполярные или малополярные связи.
Растворы полимеров
Растворы высокомолекулярных веществ ВМС — белков, углеводов и др. обладают одновременно многими свойствами истинных и коллоидных растворов.
В зависимости от цели для описания концентрации растворов используются разные физические величины.
- Ненасыщенный раствор — раствор, в котором концентрация растворенного вещества меньше, чем в насыщенном растворе, и в котором при данных условиях можно растворить ещё некоторое его количество.
- Насыщенный раствор — раствор, в котором растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе.
- Пересыщенный раствор (изредка используется термин перенасыщенный) — раствор, содержащий при данных условиях больше растворённого вещества, чем в насыщенном растворе. Пересыщенные растворы неустойчивы, избыток вещества легко выпадает в осадок. Такой раствор нельзя получить путём растворения в нормальных условиях, обычно пересыщенный раствор получают охлаждением раствора, насыщенного при более высокой температуре (пересыщение).
- Концентрированный раствор — раствор с высоким содержанием растворённого вещества в противоположность разбавленному раствору, содержащему малое количество растворённого вещества. Деление растворов на концентрированные и разбавленные не связано с делением на насыщенные и ненасыщеные. Так насыщенный 0,0000134М раствор хлорида серебра является очень разбавленным, а 4М раствор бромида калия, будучи очень концентрированным, не является насыщенным.
- Разбавленный раствор — раствор с низким содержанием растворённого вещества. Отметим, что не всегда разбавленный раствор является ненасыщенным — например, насыщенный 0,0000134М раствор практически нерастворимого хлорида серебра является очень разбавленным. Граница между разбавленным и концентрированным растворами весьма условна.
См. также
Примечания
Литература
- Шахпаронов М. И. Введение в молекулярную теорию растворов. — М.: Государственное издательство технико-теоретической литературы, 1956. — 508 с.
- Реми Г. Курс неорганической химии. — М.: Издательство иностранной литературы, 1963, 1966. — Т. 1—2.
- Streitwieser, Andrew. Introduction to Organic Chemistry. — 4th ed. — Macmillan Publishing Company, New York, 1992. — ISBN ISBN 0-02-418170-6.
Ссылки
ru-wiki.org
Химические растворы
Приглашение к размышлению
Столкновение с неведомым всегда вызывает шок и резкую реакцию: этого не может быть, потому что этого не может быть никогда. Именно такой шок вызвало у научной общественности сообщение Бенвениста (если нет действующего начала – вещества, то нет и действия). Действительно, теория растворов настолько неотъемлемая часть современной науки, что усомниться в ее основах практически невозможно. Сегодняшние представления заложили исследования классиков науки (Менделеева, Ван-Гоффа, Аррениуса), выполненные в 80-х годах ХIХ века, и если эффект существует, его объяснение не должно противоречить основам разработанной теории. Поэтому рассмотрим для начала классический подход к разгадке эффекта сверхмалых концентраций (СМК).
Из теории растворов следует необходимость учета взаимодействия растворителя и растворяемого вещества. Учет того факта, что внесение примеси в воду может существенно изменить объемные и поверхностные характеристики самой воды, способен дать многое. Вода всегда имеет примеси. Поэтому вполне возможно, что изменяется уникальное сочетание примесных характеристик воды, модифицированной белком или иным активным веществом (по примесным компонентам, поверхностному натяжению, объемному содержанию микропузырьков и образующих их газов). Тогда, если растворение примеси вызвало изменение в свойствах воды-растворителя, то при добавлении новой воды разводится уже не примесь в воде, а сама вода, в которой первоначально проводилось растворение. Смешивается «измененная» и стандартная вода, что приводит к иному расчету концентрации, и в этом случае, если такого рода расчет работает, объяснение эффекта СМК будет вполне классическим.
Однако при сумасшедшем разведении (10-30 — 10-102) не останется даже следов исходной воды, которой в единице объема было ровно столько, сколько определяется числом Авогадро 6,02х1023, и потому стоит задуматься о неклассических объяснениях…
Неклассическое (но не противоречащее теории растворов!) объяснение действия эффекта СМК может заключаться в предположении, что примесь вызывает образование определенных структур воды во всем объеме или на поверхности, от которой, как показывает история развития науки (например, в связи с открытием сверхтекучести гелия), весьма нелегко избавиться. Отмеченная в статье В.Е. Жвирблиса страсть воды к ассоциации, структурообразованию сегодня бесспорна. Более того, данные ИК-спектрометрии показывают, что существует широкий и почти непрерывный спектр структур. Реальная вода представляет набор объемных сетевых структур, в каждую из которых входит до сотни молекул воды. Видимо, набором структур воды и обусловлена фрактальная структура льда, обнаруженная не столь давно.
Для реализации неклассического механизма эффекта СМК следует предположить возможность самокопирования структур, возникших под действием растворенного вещества. Самокопирование или самоподдержание необходимо, так как оригинальный механизм «улыбки чеширского кота» — пустые «шубы» из-под молекул примеси, предложенный в статье
В.Е. Жвирблиса, не может объяснить эффект, при котором число «шуб» равно исходному числу молекул примеси. Это позволяет предположить, что измененная структура способна к воспроизведению. А вот далее можно только догадываться. Возможно, «шубы», как дефектные области, копируются водой в процессе, подобном пластической деформации кристаллов при встряхивании и перемешивании, и размножаются как дислокации в кристалле. Возможно, запускается некий автокаталитический процесс самокопирования. В сильно разбавленных растворах (там, где зарождается эффект СМК) мы можем столкнуться с автоволновым процессом, когда структурные ансамбли переходят из одного выделенного состояния в другое под действием самовозбуждающихся в растворе волн неравновесных условий. Периодические реакции Жаботинского—Белоусова сегодня прочно вошли в обиход науки. Быть может, в воде запускается некоторая периодическая реакция — циклический переход одной структуры воды в другую, в результате которого самоподобные структуры размножаются? Причем разнообразие «продукции» такого «завода» воспроизводства структур может быть весьма велико при наличии непрерывного структурного спектра.
Возбудив один или несколько таких процессов в объеме воды, исходная примесь, видимо, становится уже не нужна — мавр сделал свое дело. Дальнейшее добавление воды в раствор должно приводить к разрастанию процесса самокопирования структур подобно тому, как кристалл растет от затравки — маленького кристаллика, провоцирующего процесс кристаллизации. Причем в новой порции воды для процесса структуризации важен только фактор времени, необходимого для образования «действующей» концентрации структур. При этом нет ограничений на количество воды, которое может быть охвачено процессом. Все реки зимой замерзают, кроме горячих… В результате критическим экспериментом для «структурного» механизма должно стать изучение зависимости эффекта СМК от температуры. Возможно, критично и время, прошедшее от очередного разбавления до обнаружения эффекта.
Во всем сказанном можно выделить главное: мысль человеческая ничуть не менее изобретательна, чем природа, которая ее породила, и именно потому мы способны к познанию природы. Изучение самого факта существования обсуждаемого эффекта до сих пор сдерживалось, по всей видимости, скорее консервативностью мысли исследователей, воспитанных на классической теории растворов, чем непознаваемостью самого явления.
Помните: А и Б сидели на трубе, А упало, Б пропало, что осталось на трубе? Осталось скромное и незаметное «и» — рабочий «фоновый» союз, почти неразличимый в обычной речи. Так и здесь: если само вещество действовать не может — его просто нет, но действие есть, то кто-то же должен действовать. И этот кто-то — вода — фон всего процесса. Заметим, что для обнаружения эффекта СМК, как правило, используется биоиндика-
ция — реакция живых организмов или их тканей (см. статью Тушмаловой и Лебедевой). Видимо, механизм эффекта понятен структуре живого, вышедшего из воды…
Людвиг фон Берталанфи на вопрос: «Что есть жизнь?» — дал весьма примечательный ответ: «Жизнь — это скорее процесс, чем структура». Видимо, прежде, чем мы поймем, что же такое жизнь, нам еще не раз придется отказаться от механистических схем и перейти к представлению о постоянно действующих в области живого (и не только) самоподдерживающихся явлениях.
Яркий пример этого — работа Стивена Роуза, исследовавшего механизм работы памяти. В своей книге «Устройство памяти — от молекул к сознанию» (М., «Мир». 1995) он пишет, что общим в его работе и трудах других исследователей явился вывод: «…память … не есть некая пассивная надпись на восковой табличке или кремниевых чипах мозга — она представляет собой активный процесс». Так же и разум не сумма знаний, но горящий светильник. И это только начало долгого разговора…
Зам. гл. редактора
журнала «Экология и жизнь»
А. Самсонов
mirznanii.com
