Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева

Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. В центре атома находится положительно заряженное ядро. Оно занимает ничтожную часть пространства внутри атома, в нём сосредоточены весь положительный заряд и почти вся масса атома.
Ядро состоит из элементарных частиц — протона и нейтрона; вокруг атомного ядра по замкнутым орбиталям движутся электроны.
Протон (р) — элементарная частица с относительной массой 1,00728 атомной единицы массы и зарядом +1 условную единицу. Число протонов в атомном ядре равно порядковому номеру элемента в Периодической системе Д.И. Менделеева.
Нейтрон (n) — элементарная нейтральная частица с относительной массой 1,00866 атомной единицы массы (а. е. м.).
Число нейтронов в ядре N определяют по формуле:
где А — массовое число, Z — заряд ядра, равный числу протонов (порядковому номеру).
Обычно параметры ядра атома записывают следующим образом: слева внизу от символа элемента ставят заряд ядра, а вверху — массовое число, например:
Эта запись показывает, что заряд ядра (следовательно, и число протонов) для атома фосфора равен 15, массовое число равно 31, а число нейтронов равно 31 – 15 = 16. Так как массы протона и нейтрона очень мало отличаются друг от друга, то массовое число приблизительно равно относительной атомной массе ядра.
Электрон ( е–) — элементарная частица с массой 0,00055 а. е. м. и условным зарядом –1. Число электронов в атоме равно заряду ядра атома (порядковому номеру элемента в Периодической системе Д.И. Менделеева).
Электроны движутся вокруг ядра по строго определённым орбиталям, образуя так называемое электронное облако.
Область пространства вокруг атомного ядра, где наиболее (90 и более %) вероятно нахождение электрона, определяет форму электронного облака.
Электронное облако s-электрона имеет сферическую форму; на s-энергетическом подуровне может максимально находиться два электрона.
Электронное облако p-электрона имеет гантелеобразную форму; на трёх p-орбиталях максимально может находиться шесть электронов.
Орбитали изображают в виде квадрата, сверху или снизу которого пишут значения главного и побочного квантовых чисел, описывающих данную орбиталь. Такую запись называют графической электронной формулой, например:
В этой формуле стрелками обозначают электрон, а направление стрелки соответствует направлению спина — собственного магнитного момента электрона. Электроны с противоположными спинами ↑↓ называют спаренными.
Электронные конфигурации атомов элементов можно представить в виде электронных формул, в которых указывают символы подуровня, коэффициент перед символом подуровня показывает его принадлежность к данному уровню, а степень у символа — число электронов данного подуровня.
В таблице 1 приведено строение электронных оболочек атомов первых 20 элементов Периодической системы химических элементов Д.И. Менделеева.

Химические элементы, в атомах которых s-подуровень внешнего уровня пополняется одним или двумя электронами, называют s-элементами. Химические элементы, в атомах которых заполняется p-подуровень (от одного до шести электронов), называют p-элементами.
Число электронных слоёв в атоме химического элемента равно номеру периода.
В соответствии с правилом Хунда электроны располагаются на однотипных орбиталях одного энергетического уровня таким образом, чтобы суммарный спин был максимален. Следовательно, при заполнении энергетического подуровня каждый электрон прежде всего занимает отдельную ячейку, а только после этого начинается их спаривание. Например, у атома азота все p-электроны будут находиться в отдельных ячейках, а у кислорода начнётся их спаривание, которое полностью закончится у неона.


Изотопами называют атомы одного и того же элемента, содержащие в своих ядрах одинаковое число протонов, но различное число нейтронов.
Изотопы известны для всех элементов. Поэтому атомные массы элементов в периодической системе являются средним значением из массовых чисел природных смесей изотопов и отличаются от целочисленных значений. Таким образом, атомная масса природной смеси изотопов не может служить главной характеристикой атома, а следовательно, и элемента. Такой характеристикой атома является заряд ядра, определяющий число электронов в электронной оболочке атома и её строение.
Рассмотрим несколько типовых заданий по этому разделу.
Пример 1. Атом какого элемента имеет электронную конфигурацию 1s22s22p63s23p64s1?
- Li
- Na
- K
- Cl
На внешнем энергетическом уровне у данного элемента находится один 4s-электрон. Следовательно, этот химический элемент находится в четвёртом периоде первой группе главной подгруппе. Этот элемент — калий.
К этому ответу можно прийти по-другому. Сложив общее количество всех электронов, получим 19. Общее число электронов равно порядковому номеру элемента. Под номером 19 в периодической системе находится калий.
Пример 2. Химическому элементу соответствует высший оксид RO2. Электронной конфигурации внешнего энергетического уровня атома этого элемента соответствует электронная формула:
- ns2np4
- ns2np2
- ns2np3
- ns2np6
По формуле высшего оксида (смотрите на формулы высших оксидов в Периодической системе) устанавливаем, что этот химический элемент находится в четвёртой группе главной подгруппы. У этих элементов на внешнем энергетическом уровне находятся четыре электрона — два s и два p. Следовательно, правильный ответ 2.
Тренировочные задания
1. Общее число s-электронов в атоме кальция равно
1) 20
2) 40
3) 8
4) 6
2. Число спаренных p-электронов в атоме азота равно
1) 7
2) 14
3) 3
4) 4
3. Число неспаренных s-электронов в атоме азота равно
1) 7
2) 14
3) 3
4) 4
4. Число электронов на внешнем энергетическом уровне атома аргона равно
1) 18
2) 6
3) 4
4) 8
5. Число протонов, нейтронов и электронов в атоме 94Be равно
1) 9, 4, 5
2) 4, 5, 4
3) 4, 4, 5
4) 9, 5, 9
6. Распределение электронов по электронным слоям 2; 8; 4 — соответствует атому, расположенному в(во)
1) 3-м периоде, IА группе
2) 2-м периоде, IVА группе
3) 3-м периоде, IVА группе
4) 3-м периоде, VА группе
7. Химическому элементу, расположенному в 3-м периоде VA группе соответствует схема электронного строения атома
1) 2, 8, 6
2) 2, 6, 4
3) 2, 8, 5
4) 2, 8, 2
8. Химический элемент с электронной конфигурацией 1s22s22p4 образует летучее водородное соединение, формула которого
1) ЭН
2) ЭН2
3) ЭН3
4) ЭН4
9. Число электронных слоёв в атоме химического элемента равно
1) его порядковому номеру
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
10. Число внешних электронов в атомах химических элементов главных подгрупп равно
1) порядковому номеру элемента
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
11. Два электрона находятся во внешнем электронном слое атомов каждого из химических элементов в ряду
1) He, Be, Ba
2) Mg, Si, O
3) C, Mg, Ca
4) Ba, Sr, B
12. Химический элемент, электронная формула которого 1s22s22p63s23p64s1, образует оксид состава
1) Li2O
2) MgO
3) K2O
4) Na2O
13. Число электронных слоев и число p-электронов в атоме серы равно
1) 2, 6
2) 3, 4
3) 3, 16
4) 3, 10
14. Электронная конфигурация ns2np4 соответствует атому
1) хлора
2) серы
3) магния
4) кремния
15. Валентные электроны атома натрия в основном состоянии находятся на энергетическом подуровне
1) 2s
2) 2p
3) 3s
4) 3p
16. Атомы азота и фосфора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковую конфигурацию внешнего электронного слоя
4) одинаковое число электронов
17. Одинаковое число валентных электронов имеют атомы кальция и
1) калия
2) алюминия
3) бериллия
4) бора
18. Атомы углерода и фтора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковое число электронных слоёв
4) одинаковое число электронов
19. У атома углерода в основном состоянии число неспаренных электронов равно
1) 1
3) 3
2) 2
4) 4
20. В атоме кислорода в основном состоянии число спаренных электронов равно
1) 2
3) 4
2) 8
4) 6
Ответы
himi4ka.ru
Тема №1 «Строение атома» | CHEM-MIND.com
Оглавление
Электроны
Понятие атом возникло еще в античном мире для обозначения частиц вещества. В переводе с греческого атом означает «неделимый».
Ирландский физик Стони на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами, сущеетвующими в атомах всех химических элементов. В 1891 г. Стони предложил эти частицы назвать электронами, что по-гречески означает «янтарь». Через несколько лет после того, как электрон получил свое название, английский физик Джозеф Томсон и французский физик Жан Перрен доказали, что электроны несут на себе отрицательный заряд. Это наименьший отрицательный заряд, который в химии принят за единицу (-1). Томсон даже сумел определить скорость движения электрона (скорость электрона на орбите обратно пропорциональна номеру орбиты n. Радиусы орбит растут пропорционально квадрату номера орбиты. На первой орбите атома водорода (n=1; Z=1) скорость равна ≈ 2,2·106 м/с, то есть примерно в сотню раз меньше скорости света с=3·108 м/с.) и массу электрона (она почти в 2000 раз меньше массы атома водорода).
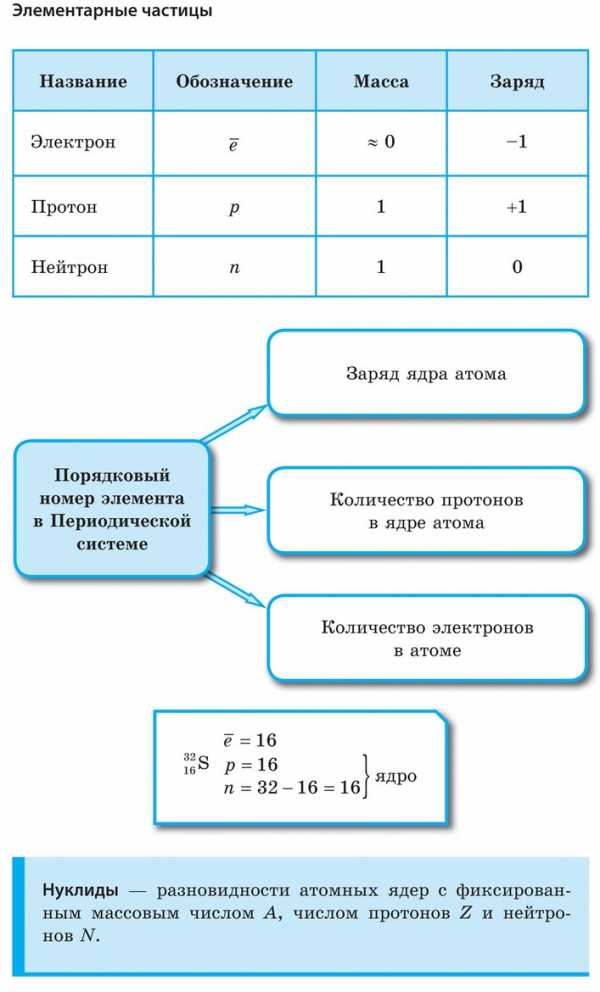
Состояние электронов в атоме
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и пространстве, в котором он находится. Электрон в атоме не имеет траектории движения, т. е. можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра.
 Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек.
При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек.
При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. В нем заключено приблизительно 90 % электронного облака, и это означает, что около 90 % времени электрон находится в этой части пространства. По форме различают 4 известных ныне типа орбиталей, которые обозначаются латинскими буквами s, p, d и f. Графическое изображение некоторых форм электронных орбиталей представлено на рисунке.

Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром. Электроны, обладающие близкими значениями энергии, образуют единый электронный слои, или энергетический уровень. Энергетические уровни нумеруют, начиная от ядра, — 1, 2, 3, 4, 5, 6 и 7.
Целое число n, обозначающее номер энергетического уровня, называют главным квантовым числом. Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня, электроны последующих уровней будут характеризоваться большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внешнего уровня.
Наибольшее число электронов на энергетическом уровне определяется по формуле:
N = 2n2,
где N — максимальное число электронов; n — номер уровня, или главное квантовое число. Следовательно, на первом, ближайшем к ядру энергетическом уровне может находиться не более двух электронов; на втором — не более 8; на третьем — не более 18; на четвертом — не более 32.
Начиная со второго энергетического уровня (n = 2) каждый из уровней подразделяется на подуровни (подслои), несколько отличающиеся друг от друга энергией связи с ядром. Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один подуровень; второй — два; третий — три; четвертый — четыре подуровня. Подуровни в свою очередь образованы орбиталями. Каждому значению n соответствует число орбиталей, равное n.
Подуровни принято обозначать латинскими буквами, равно как и форму орбиталей, из которых они состоят: s, p, d, f.

Протоны и нейтроны

Атом любого химического элемента сравним с крохотной Солнечной системой. Поэтому такую модель атома, предложенную Э. Резерфордом, называют планетарной.
Атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов — протонов и нейтронов.
Протоны имеют заряд, равный заряду электронов, но противоположный по знаку (+1), и массу, равную массе атома водорода (она принята в химии за единицу). Нейтроны не несут заряда, они нейтральны и имеют массу, равную массе протона.
Протоны и нейтроны вместе называют нуклонами (от лат. nucleus — ядро). Сумма числа протонов и нейтронов в атоме называется массовым числом. Например, массовое число атома алюминия:

13 + 14 = 27
число протонов 13, число нейтронов 14, массовое число 27
Так как массой электрона, ничтожно малой, можно пренебречь, то очевидно, что в ядре сосредоточена вся масса атома. Электроны обозначают e—.
Поскольку атом электронейтрален, то также очевидно, что число протонов и электронов в атоме одинаково. Оно равно порядковому номеру химического элемента, присвоенному ему в Периодической системе. Масса атома складывается из массы протонов и нейтронов. Зная порядковый номер элемента (Z), т. е. число протонов, и массовое число (А), равное сумме чисел протонов и нейтронов, можно найти число нейтронов (N) по формуле:

N = A — Z
Например, число нейтронов в атоме железа равно:
56 — 26 = 30
Изотопы
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами. Химические элементы, встречающиеся в природе, являются смесью изотопов. Так, углерод имеет три изотопа с массой 12, 13, 14; кислород — три изотопа с массой 16, 17, 18 и т. д. Обычно приводимая в Периодической системе относительная атомная масса химического элемента является средним значением атомных масс природной смеси изотопов данного элемента с учетом их относительного содержания в природе. Химические свойства изотопов большинства химических элементов совершенно одинаковы. Однако изотопы водорода сильно различаются по свойствам из-за резкого кратного увеличения их относительной атомной массы; им даже присвоены индивидуальные названия и химические знаки.

Элементы первого периода
Схема электронного строения атома водорода:

Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).

Графическая электронная формула атома водорода (показывает распределение электронов по энергетическим уровням и подуровням):
Графические электронные формулы атомов показывают распределение электронов не только по уровням и подуровням, но и по орбиталям.
В атоме гелия первый электронный слой завершен — в нем 2 электрона. Водород и гелий — s-элементы; у этих атомов заполняется электронами s-орбиталь.
Элементы второго периода
У всех элементов второго периода первый электронный слой заполнен, и электроны заполняют s- и р-орбитали второго электронного слоя в соответствии с принципом наименьшей энергии (сначала s, а затем р) и правилами Паули и Хунда.
В атоме неона второй электронный слой завершен — в нем 8 электронов.
Элементы третьего периода
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d- подуровни.
У атома магния достраивается 3s- электронная орбиталь. Na и Mg — s-элементы.
У алюминия и последующих элементов заполняется электронами 3р-подуровень.
У элементов третьего периода остаются незаполненными 3d-орбитали.
Все элементы от Al до Ar — р-элементы. s- и р-элементы образуют главные подгруппы в Периодической системе.

Элементы четвертого — седьмого периодов
У атомов калия и кальция появляется четвертый электронный слой, заполняется 4s-подуровень, т. к. он имеет меньшую энергию, чем 3d-подуровень.
К, Са — s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами 3d-подуровень. Это 3d-элементы. Они входят в побочные подгруппы, у них заполняется предвнешний электронный слой, их относят к переходным элементам.
Обратите внимание на строение электронных оболочек атомов хрома и меди. В них происходит «провал» одного электрона с 4s- на 3d-подуровень, что объясняется большей энергетической устойчивостью образующихся при этом электронных конфигураций 3d5 и 3d10:
В атоме цинка третий электронный слой завершен — в нем заполнены все подуровни 3s, 3р и 3d, всего на них 18 электронов. У следующих за цинком элементов продолжает заполняться четвертый электронный слой, 4р-подуровень.
Элементы от Ga до Кr — р-элементы.
У атома криптона внешний слой (четвертый) завершен, имеет 8 электронов. Но всего в четвертом электронном слое может быть 32 электрона; у атома криптона пока остаются незаполненными 4d- и 4f-подуровни.У элементов пятого периода идет заполнение по-дуровней в следующем порядке: 5s — 4d — 5р. И так-же встречаются исключения, связанные с « провалом» электронов, у 41Nb, 42Мо, 44Ru, 45Rh, 46Pd, 47Ag.
В шестом и седьмом периодах появляются f-элементы, т. е. элементы, у которых идет заполнение соответственно 4f- и 5f-подуровней третьего снаружи электронного слоя.
4f-элементы называют лантаноидами.
5f-элементы называют актиноидами.
Порядок заполнения электронных подуровней в атомах элементов шестого периода: 55Cs и 56Ва — 6s-элементы; 57La … 6s25dx — 5d-элемент; 58Се — 71Lu — 4f-элементы; 72Hf — 80Hg — 5d-элементы; 81Т1 — 86Rn — 6d-элементы. Но и здесь встречаются элементы, у которых «нарушается» порядок заполнения электронных орбиталей, что, например, связано с большей энергетической устойчивостью наполовину и полностью заполненных f-подуровней, т. е. nf
- s-элементы. Электронами заполняется s-подуровень внешнего уровня атома; к s-элементам относятся водород, гелий и элементы главных подгрупп I и II групп.
- p-элементы. Электронами заполняется р-подуровень внешнего уровня атома; к р-элементам относятся элементы главных подгрупп III— VIII групп.
- d-элементы. Электронами заполняется d-подуровень предвнешнего уровня атома; к d-элементам относятся элементы побочных подгрупп I—VIII групп, т. е. элементы вставных декад больших периодов, расположенных между s- и р-элементами. Их также называют переходными элементами.
- f-элементы. Электронами заполняется f-подуровень третьего снаружи уровня атома; к ним относятся лантаноиды и антиноиды.

Основное и возбужденное состояния
Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитали может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского — «веретено»), т. е. обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемый оси: по часовой или против часовой стрелки.

Этот принцип носит название принципа Паули. Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т. е. электроны с противоположными спинами. На рисунке показана схема подразделения энергетических уровней на подуровни и очередность их заполнения.


Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек — записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули и правило Ф. Хунда, согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины, при этом по принципу Паули будут уже противоположно направленными.
Правило Хунда и принцип Паули
Правило Хунда — правило квантовой химии, определяющее порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Другая формулировка: Ниже по энергии лежит тот атомный терм, для которого выполняются два условия.
- Мультиплетность максимальна
- При совпадении мультиплетностей суммарный орбитальный момент L максимален.
Разберём это правило на примере заполнения орбиталей p-подуровня p-элементов второго периода (то есть от бора до неона (в приведённой ниже схеме горизонтальными чёрточками обозначены орбитали, вертикальными стрелками — электроны, причём направление стрелки обозначает ориентацию спина).
При́нцип Па́ули (принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона (частицы с полуцелым спином) не могут одновременно находиться в одном и том же квантовом состоянии.
 Правило Хунда и принцип Паули
Правило Хунда и принцип Паули Правило Клечковского
Правило Клечковского — по мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра.
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречатреальной энергетической последовательности атомых орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место “провал” электрона с s-подуровня внешнего слояна d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, аименно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d,а не 4f, и только затем происходит заселение четырнадцатью электронами 4f орбиталей, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и дляорбиталей 7s, 6d и 5f.
Распределение элекронов в атоме хрома — согласно правилам(сверху) и реальное(снизу), согласно исключениям из правила Клечковского:

www.chem-mind.com
Строение атома | himiyaklas.ru
Содержание статьи:
- Почему у атомов разных веществ разные свойства?
- Из чего “сделан” атом?
- Чем отличаются друг от друга атомы разных химических элементов?
- Масса атома.
- Строение электронной оболочки (электронные орбитали, основное и возбужденное состояние, электронные конфигурации атома и электрона).
У каждого вещества есть свои свойства, которые отличают его от других веществ. Чем обусловлены эти свойства?
Тем, какой состав имеет молекула. То есть какими атомами образована молекула, в каком количестве, какими связями соединены эти атомы. Все это определяет свойство молекулы, и соответственно свойство вещества, которое эти молекулы образуют.
Например, свойства воды: прозрачность, текучесть, способность вызывать ржавчину обусловлено именно наличием двух атомов водорода и одного атома кислорода.
Поэтому прежде, чем приступить к изучению свойств молекул (то есть свойств веществ), нужно рассмотреть «кирпичики», которыми эти молекулы образованы. Разобраться в строении атома.
Как устроен атом?
Атомы – это частицы, которые, соединяясь друг с другом, образуют молекулы.
Сам атом состоит из положительно заряженного ядра (+) и отрицательно заряженной электронной оболочки (-). В целом атом электронейтрален. То есть заряд ядра равен по модулю заряду электронной оболочки.
Ядро образовано следующими частицами:
- Протоны. Один протон несет заряд +1. Масса его равна 1 а.е.м (атомная единица массы). Эти частицы обязательно присутствуют в ядре.
- Нейтроны. Нейтрон не имеет заряда (заряд = 0). Масса его равна 1 а.е.м. Нейтронов может не быть в ядре. Это не обязательный компонент атомного ядра.
Таким образом за общий заряд ядра отвечают протоны. Поскольку один нейтрон имеет заряд +1, то заряд ядра равен числу протонов.
Электронная оболочка, как видно из названия образована частицами, которые называются электронами. Если сравнивать ядро атома с планетой, то электроны – это ее спутники. Вращаясь вокруг ядра (пока представим, что по орбитам, а на самом деле по орбиталям), они образуют электронную оболочку.
- Электрон – это очень маленькая частица. Ее масса на столько мала, что принимается за 0. А вот заряд у электрона -1. То есть по модулю равен заряду протона, отличается знаком. Поскольку один электрон несет заряд -1, то общий заряд электронной оболочки равен числу электронов в ней.
Одно важное следствие, раз атом – частица, не имеющая заряда (заряд ядра и заряд электронной оболочки равны по модулю, но противоположены по знаку), то есть электронейтральная, следовательно, число электронов в атоме равно числу протонов.

Чем отличаются атомы разных химических элементов друг от друга?
Атомы разных химических элементов отличаются друг от друга зарядом ядра (то есть числом протонов, и, следовательно, числом электронов).
Как узнать заряд ядра атома элемента? Гениальный отечественный химик Д. И. Менделеев, открыв периодический закон, и разработав таблицу, названную его именем, дал нам возможность сделать это. Его открытие забегало далеко вперед. Когда еще не было известно о строении атома, Менделеев расположил элементы в таблице в порядке возрастания заряда ядра.
То есть порядковый номер элемента в периодической системе – это заряд ядра атома данного элемента. Например, у кислорода порядковый номер 8, соответственно заряд ядра атома кислорода равен +8. Соответственно число протонов равно 8, и число электронов равно 8.
Именно электроны в электронной оболочке определяют химические свойства атома, но об этом чуть позже.
Теперь поговорим о массе.
Один протон – это одна единица массы, один нейтрон – это тоже одна единица массы. Поэтому сумма нейтронов и протонов в ядре называется массовым числом. (Электроны на массу никак не влияют, так как мы пренебрегаем его массой и считаем ее равной нулю).
Атомная единица массы (а. е. м.) – специальная физическая величина для обозначения малых масс частиц, образующих атомы.



Все эти три атома – атомы одного химического элемента – водорода. Поскольку у них одинаковый заряд ядра.
Чем они будут отличаться? У этих атомов разные массовые числа (из-за разного числа нейтронов). У первого атома массовое число равно 1, у второго 2, у третьего 3.
Атомы одного элемента, различающиеся количеством нейтронов (и, следовательно, массовыми числами) называются изотопами.
У представленных изотопов водорода даже есть свои названия:
- Первый изотоп (с массовым числом 1) называется протий.
- Второй изотоп (с массовым числом 2) называется дейтерий.
- Третий изотоп (с массовым числом 3) называется тритий.
Теперь следующий резонный вопрос: почему если число нейтронов и протонов в ядре число целое, масса их по 1 а.е.м., то в периодической системе масса атома – дробное число. У серы, например: 32,066.
Ответ: у элемента есть несколько изотопов, они отличаются друг от друга массовыми числами. Поэтому атомная масса в периодической таблице – это среднее значение атомных масс всех изотопов элемента с учетом их встречаемости в природе. Эта масса, указанная в периодической системе, называется относительной атомной массой.
Для химических расчетов используются показатели именно такого «усредненного атома». Атомная масса округляется до целого.

Строение электронной оболочки.
Химические свойства атома определяются строением его электронной оболочки. Электроны вокруг ядра располагаются не абы как. Электроны локализуются на электронных орбиталях.
Электронная орбиталь – пространство вокруг атомного ядра, где вероятность нахождения электрона наибольшая.
У электрона есть один квантовый параметр, который называется спин. Если брать классическое определение из квантовой механики, то спин – это собственный момент импульса частицы. В упрощенном виде это можно представить, как направление вращения частицы вокруг своей оси.
Электрон – это частица с полуцелым спином, у электрона спин может быть либо +½ либо -½. Условно это можно представить, как вращение по часовой и против часовой.
На одной электронной орбитали могут находиться не более двух электронов с противоположенными спинами.
Общепринятым обозначением электронной обитали является клетка либо черточка. Электрон обозначается стрелкой: стрелка вверх ↑ – электрон с положительным спином +½, стрелка вниз ↓ – электрон с отрицательным спином -½.
Электрон, одинокий на орбитали называется неспаренным. Два электрона, располагающиеся на одной орбитали, называются спаренными.
Электронные орбитали подразделяются в зависимости от формы на четыре вида: s, p, d, f. Орбитали одинаковой формы формируют подуровень. Число орбиталей на подуровне определяется числом возможных вариантов расположения в пространстве.
- s-орбиталь.
s-орбиталь имеет форму шара:
В пространстве s-орбиталь может располагаться только одним способом:
Поэтому s-подуровнь формируется только одной s-орбиталью.
- р-орбиталь.
p-орбиталь имеет форму гантели:
В пространстве p-орбиталь может располагаться только тремя способами:
Поэтому p-подуровнь формируется тремя p-орбиталями.
- d-орбиталь.
d-орбиталь имеет сложную форму:
В пространстве d-орбиталь может располагаться пятью разными способами. Поэтому d-подуровнь формируется пятью d-орбиталями.
- f-орбиталь
f-орбиталь имеет еще более сложную форму. В пространстве f-орбиталь может располагаться семью разными способами. Поэтому f-подуровнь формируется семью f-орбиталями.
Электронная оболочка атома похожа на слоеное кондитерское изделие. В нем тоже есть слои. Электроны, находящиеся на разных слоях, имеют разную энергию: на слоях ближе ядру – меньше, на удаленных от ядра – бо̀льшую. Слои эти называются энергетическими уровнями.
Заполнение электронных орбиталей.
Первый энергетический уровень имеет только s-подуровень:

На втором энергетическом уровне есть s-подуровень и появляется p-подуровень:
На третьем энергетическом уровне есть s-подуровень, p-подуровень и появляется d-подуровень:
На четвертом энергетическом уровне, в принципе, прибавляется f-подуровень. Но в школьном курсе f-орбитали не заполняются, поэтому мы можем не изображать f-подуровень:
Число энергетических уровней в атоме элемента равно номеру периода. При заполнении электронных орбиталей нужно следовать следующим принципам:
- Каждый электрон старается занять в атоме то положение, где его энергия будет минимальной. То есть сначала идет заполнение первого энергетического уровня, потом второго и так далее.
Для описания строения электронной оболочки так же используется электронная формула. Электронная формула – это краткая запись в одну строку распределения электронов по подуровням.
- На подуровне сначала каждый электрон заполняет свободную орбиталь. И каждый имеет спин +½ (стрелка вверх).
И только после того как на каждой орбитали подуровня будет по одному электрону, следующий электрон становится спаренным – то есть занимает орбиталь, на которой уже есть электрон:
- d-подуровень заполняется по-особому.
Дело в том, что энергия d-подуровня выше, чем энергия s-подуровня СЛЕДУЮЩЕГО энергетического слоя. А как мы знаем, электрон старается занять то положение в атоме, где его энергия будет минимальной.
Поэтому после заполнения 3p-подуровня, заполняется сначала 4s-подуровень, после чего заполняется 3d-подуровень.



И только после того как 3d-подуровень заполнен полностью, заполняется 4p-подуровень.

Так же и с 4 энергетическим уровнем. После заполнения 4p-подуровня, следующим заполняется 5s-подуровень, после него 4d-подуровень. И после него только 5p.



- И есть еще один момент, одно правило касаемо заполнения d-подуровня.
То происходит явление, называемое провалом. При провале один электрон с s-подуровня следующего энергетического уровня, в прямом смысле проваливается на d-электрон.


Основное и возбужденное состояния атома.
Атомы, электронные конфигурации которых мы сейчас строили, называются атомами в основнóм состоянии. То есть, это обычное, естественное, если угодно, состояние.
Когда атом получает энергию извне, может произойти возбуждение.
Возбуждение – это переход спаренного электрона на пустую орбиталь, в пределах внешнего энергетического уровня.
Например, у атома углерода:
Возбуждение характерно для многих атомов. Это необходимо помнить, потому как возбуждение определяет способность атомов связываться друг с другом. Главное помнить условие, при котором может произойти возбуждение: спаренный электрон и пустая орбиталь на внешнем энергетическом уровне.

Есть атомы, у которых несколько возбужденных состояний:

Электронная конфигурация иона.
Ионы – это частицы, в которые превращаются атомы и молекулы, приобретая или теряя электроны. Эти частицы имеют заряд, так как у них либо «не хватает» электронов, либо их избыток. Положительно заряженные ионы называются катионами, отрицательные – анионами.
Атом хлора (не имеет заряда) приобретает электрон. У электрона заряд 1- (один минус), соответственно образуется частица, имеющая избыточный отрицательный заряд. Анион хлора:
Cl0 + 1e → Cl–

Атом лития (тоже не имеющий заряда) теряет электрон. У электрона заряд 1+ (один плюс), образуется частица, с недостатком отрицательного заряда, то есть заряд у нее положительный. Катион лития:
Li0 – 1e → Li+

Превращаясь в ионы, атомы приобретают такую конфигурация, что внешний энергетический уровень становится «красивым», то есть полностью заполненным. Такая конфигурация наиболее термодинамически стабильная, поэтому атомам есть резон превращаться в ионы.
И поэтому атомы элементов VIII-A группы (восьмой группы главной подгруппы), как сказано в следующем параграфе это благородные газы, такие химически малоактивны. У них в основном состоянии такое строение: внешний энергетический уровень полностью заполнен. Другие атомы, как бы стремятся приобрести конфигурацию этих самых благородных газов, поэтому и превращаются в ионы и образуют химические связи.
himiyaklas.ru
Основные сведения о строении атома: характеристики, особенности и формула
Атом – это мельчайшая частица химического вещества, которая способна сохранять его свойства. Слово «атом» происходит от древнегреческого «atomos», что означает «неделимый». В зависимости о того, сколько и каких частиц находится в атоме, можно определить химический элемент.

Кратко о строении атома
Как можно вкратце перечислить основные сведения о строении атома? Атом является частицей с одним ядром, которое заряжено положительно. Вокруг этого ядра расположено отрицательно заряженное облако из электронов. Каждый атом в своем обычном состоянии является нейтральным. Размер этой частицы полностью может быть определен размером электронного облака, которое окружает ядро.
Само ядро, в свою очередь, тоже состоит из более мелких частиц – протонов и нейтронов. Протоны являются положительно заряженными. Нейтроны не несут в себе никакого заряда. Однако протоны вместе с нейтронами объединяются в одну категорию и носят название нуклонов. Если необходимы основные сведения о строении атома кратко, то эта информация может быть ограничена перечисленными данными.

Первые сведения об атоме
О том же, что материя может состоять из мелких частиц, подозревали еще древние греки. Они полагали, что все существующее и состоит из атомов. Однако такое воззрение носило чисто философский характер и не может быть трактовано научно.
Первым основные сведения о строении атома получил английский ученый Джон Дальтон. Именно этот исследователь сумел обнаружить, что два химических элемента могут вступать в различные соотношения, и при этом каждая такая комбинация будет представлять собой новое вещество. Например, восемь частей элемента кислорода порождают собой углекислый газ. Четыре части кислорода – угарный газ.
В 1803 году Дальтон открыл так называемый закон кратных отношений в химии. При помощи косвенных измерений (так как ни один атом тогда не мог быть рассмотрен под тогдашними микроскопами) Дальтон сделал вывод об относительном весе атомов.

Исследования Резерфорда
Почти столетие спустя основные сведения о строении атомов были подтверждены еще одним английским химиком — Эрнестом Резерфордом. Ученый предложил модель электронной оболочки мельчайших частиц.
На тот момент названная Резерфордом «Планетарная модель атома» была одним из важнейших шагов, которые могла сделать химия. Основные сведения о строении атома свидетельствовали о том, что он похож на Солнечную систему: вокруг ядра по строго определенным орбитам вращаются частицы-электроны, подобно тому, как это делают планеты.
Электронная оболочка атомов и формулы атомов химических элементов
Электронная оболочка каждого из атомов содержит ровно столько электронов, сколько находится в его ядре протонов. Именно поэтому атом является нейтральным. В 1913 году еще один ученый получил основные сведения о строении атома. Формула Нильса Бора была похожа на ту, что получил Резерфорд. Согласно его концепции, электроны также вращаются вокруг ядра, расположенного в центре. Бор доработал теорию Резерфорда, внес стройность в ее факты.
Уже тогда были составлены формулы некоторых химических веществ. Например, схематически строение атома азота обозначается как 1s22s22p3, строение атома натрия выражается формулой 1s22s22p63s1. Через эти формулы можно увидеть, какое количество электронов движется по каждой из орбиталей того или иного химического вещества.

Модель Шредингера
Однако затем и эта атомная модель устарела. Основные сведения о строении атома, известные науке сегодня, во многом стали доступны благодаря исследованиям австрийского физика Э. Шредингера.
Он предложил новую модель его строения – волновую. К этому времени ученые уже доказали, что электрон наделен не только природой частицы, но обладает свойствами волны.
Однако у модели Шредингера и Резерфорда имеются и общие положения. Их теории сходны в том, что электроны существуют на определенных уровнях.
Такие уровни также называются электронными слоями. При помощи номера уровня может быть охарактеризована энергия электрона. Чем выше слой, тем большей энергией он обладает. Все уровни считаются снизу вверх, таким образом, номер уровня соответствует его энергии. Каждый из слоев в электронной оболочке атома имеет свои подуровни. При этом у первого уровня может быть один подуровень, у второго – два, у третьего – три и так далее (см. приведенные выше электронные формулы азота и натрия).

Еще более мелкие частицы
На данный момент, конечно, открыты еще более мелкие частицы, нежели электрон, протон и нейтрон. Известно, что протон состоит из кварков. Существуют и еще более мелкие частицы мироздания – например, нейтрино, который по своим размерам в сто раз меньше кварка и в миллиард раз меньше протона.
Нейтрино – это настолько мелкая частица, что она в 10 септиллионов раз меньше, чем, к примеру, тираннозавр. Сам тираннозавр во столько же раз меньших размеров, чем вся обозримая Вселенная.
Основные сведения о строении атома: радиоактивность
Всегда было известно, что ни одна химическая реакция не может превратить один элемент в другой. Но в процессе радиоактивного излучения это происходит самопроизвольно.
Радиоактивностью называют способность ядер атомов превращаться в другие ядра – более устойчивые. Когда люди получили основные сведения о строении атомов, изотопы в определенной мере могли служить воплощением мечтаний средневековых алхимиков.
В процессе распада изотопов испускается радиоактивное излучение. Впервые такое явление было обнаружено Беккерелем. Главный вид радиоактивного излучения – это альфа-распад. При нем происходит выброс альфа-частицы. Также существует бета-распад, при котором из ядра атома выбрасывается, соответственно, бета-частица.
Природные и искусственные изотопы
В настоящее время известно порядка 40 природных изотопов. Их большая часть расположена в трех категориях: урана-радия, тория и актиния. Все эти изотопы можно встретить в природе – в горных породах, почве, воздухе. Но помимо них, известно также порядка тысячи искусственно выведенных изотопов, которые получают в ядерных реакторах. Многие их таких изотопов используются в медицине, особенно в диагностике.

Пропорции внутри атома
Если представить себе атом, размеры которого будут сопоставимы с размерами международного спортивного стадиона, тогда можно визуально получить следующие пропорции. Электроны атома на таком «стадионе» будут располагаться на самом верху трибун. Каждый из них будет иметь размеры меньше, чем булавочная головка. Тогда ядро будет расположено в центре этого поля, а его размер будет не больше, чем размер горошины.
Иногда люди задают вопрос, как в действительности выглядит атом. На самом деле он в буквальном смысле слова не выглядит никак – не по той причине, что в науке используются недостаточно хорошие микроскопы. Размеры атома находятся в тех областях, где понятие «видимости» просто не существует.
Атомы обладают очень малыми размерами. Но насколько малы в действительности эти размеры? Факт состоит в том, что самая маленькая, едва различимая человеческим глазом крупица соли содержит в себе порядка одного квинтиллиона атомов.
Если же представить себе атом такого размера, который мог бы уместиться в человеческую руку, то тогда рядом с ним находились бы вирусы 300-метровой длины. Бактерии имели бы длину 3 км, а толщина человеческого волоса стала бы равна 150 км. В лежачем положении он смог бы выходить за границы земной атмосферы. А если бы такие пропорции были действительны, то человеческий волос в длину смог бы достигать Луны. Вот такой он непростой и интересный атом, изучением которого ученые продолжают заниматься и по сей день.
fb.ru
1.1.1. Строение электронных оболочек атомов химических элементов.
Химия — наука о веществах, их свойствах и превращениях.
Химическими веществами называют то, из чего состоит окружающий нас мир.
Свойства каждого химического вещества делятся на два типа: это химические, которые характеризуют его способность образовывать другие вещества, и физические, которые объективно наблюдаются и могут быть рассмотрены в отрыве от химических превращений. Так, например, физическими свойствами вещества являются его агрегатное состояние (твердое, жидкое или газообразное), теплопроводность, теплоемкость, растворимость в различных средах (вода, спирт и др.), плотность, цвет, вкус и т.д.
Превращения одних химических веществ в другие вещества называют химическими явлениями или химическими реакциями. Следует отметить, что существуют также и физические явления, которые, очевидно, сопровождаются изменением каких-либо физических свойств вещества без его превращения в другие вещества. К физическим явлениям, например, относятся плавление льда, замерзание или испарение воды и др.
О том, что в ходе какого-либо процесса имеет место химическое явление, можно сделать вывод, наблюдая характерные признаки химических реакций, такие как изменение цвета, образование осадка, выделение газа, выделение теплоты и (или) света.
Так, например, вывод о протекании химических реакций можно сделать, наблюдая:
— образование осадка при кипячении воды, называемого в быту накипью;
— выделение тепла и света при горении костра;
— изменение цвета среза свежего яблока на воздухе;
— образование газовых пузырьков при брожении теста и т.д.
Мельчайшие частицы вещества, которые в процессе химических реакций практически не претерпевают изменений, а лишь по-новому соединяются между собой, называются атомами.
Сама идея о существовании таких единиц материи возникла еще в древней Греции в умах античных философов, что собственно и объясняет происхождение термина «атом», поскольку «атомос» в буквальном переводе с греческого означает «неделимый».
Тем не менее, вопреки идее древнегреческих философов, атомы не являются абсолютным минимумом материи, т.е. сами имеют сложное строение.
Каждый атом состоит из так называемых субатомных частиц – протонов, нейтронов и электронов, обозначаемых соответственно символами p+, no и e−. Надстрочный индекс в используемых обозначениях указывает на то, что протон имеет единичный положительный заряд, электрон – единичный отрицательный заряд, а нейтрон заряда не имеет.
Что касается качественного устройства атома, то у каждого атома все протоны и нейтроны сосредоточены в так называемом ядре, вокруг которого электроны образуют электронную оболочку.
Протон и нейтрон обладают практически одинаковыми массами, т.е. mp ≈ mn , а масса электрона почти в 2000 раз меньше массы каждого из них, т.е. mp/me ≈ mn/me ≈ 2000.
Поскольку фундаментальным свойством атома является его электронейтральность, а заряд одного электрона равен заряду одного протона, из этого можно сделать вывод о том, что количество электронов в любом атоме равно количеству протонов.
Так, например, в таблице ниже представлен возможный состав атомов:
| атом1 | атом2 | атом3 | атом4 | |
| ядро | 1p+ | 1p+, 1n0 | 4p+, 3n0 | 4p+, 4n0 |
| оболочка | 1e− | 1e− | 4e− | 4e− |
Вид атомов с одинаковым зарядом ядер, т.е. с одинаковым числом протонов в их ядрах, называют химическим элементом. Таким образом, из таблицы выше можно сделать вывод о том, что атом1 и атом2 относятся в одному химическому элементу, а атом3 и атом4 — к другому химическому элементу.
Каждый химический элемент имеет свое название и индивидуальный символ, который читается определенным образом. Так, например, самый простой химический элемент, атомы которого содержат в ядре только один протон, имеет название «водород» и обозначается символом «Н», что читается как «аш», а химический элемент с зарядом ядра +7 (т.е. содержащий 7 протонов) — «азот», имеет символ «N» , который читается как «эн».
Как можно заметить из представленной выше таблицы, атомы одного химического элемента могут отличаться количеством нейтронов в ядрах.
Атомы, относящиеся к одному химическому элементу, но имеющие разное количество нейтронов и, как следствие массу, называют изотопами.
Так, например, химический элемент водород имеет три изотопа – 1Н, 2Н и 3Н. Индексы 1, 2 и 3 сверху от символа Н означают суммарное количество нейтронов и протонов. Т.е. зная, что водород – это химический элемент, который характеризуется тем, что в ядрах его атомов находится по одному протону, можно сделать вывод о том, что в изотопе 1Н вообще нет нейтронов (1-1=0), в изотопе 2Н – 1 нейтрон (2-1=1) и в изотопе 3Н – два нейтрона (3-1=2). Поскольку, как уже было сказано, нейтрон и протон имеют одинаковые массы, а масса электрона по сравнению с ними пренебрежимо мала, это значит, что изотоп 2Н практически в два раза тяжелее изотопа 1Н, а изотоп 3Н — и вовсе в три раза. В связи с таким большим разбросом масс изотопов водорода изотопам 2Н и 3Н даже были присвоены отдельные индивидуальные названия и символы, что не характерно больше ни для одного другого химического элемента. Изотопу 2Н дали название дейтерий и присвоили символ D, а изотопу 3Н дали название тритий и присвоили символ Т.
Если принять массу протона и нейтрона за единицу, а массой электрона пренебречь, фактически верхний левый индекс помимо суммарного количества протонов и нейтронов в атоме можно считать его массой, в связи с чем этот индекс называют массовым числом и обозначают символом А. Поскольку за заряд ядра любого атома отвечают протоны, а заряд каждого протона условно считается равным +1, количество протонов в ядре называют зарядовым числом (Z). Обозначив количество нейтронов в атоме буквой N, математически взаимосвязь между массовым числом, зарядовым числом и количеством нейтронов можно выразить как:
Согласно современным представлениям, электрон имеет двойственную (корпускулярно-волновую) природу. Он обладает свойствами как частицы, так и волны. Подобно частице, электрон имеет массу и заряд, но в то же время поток электронов, подобно волне, характеризуется способностью к дифракции.
Для описания состояния электрона в атоме используют представления квантовой механики, согласно которым электрон не имеет определенной траектории движения и может находиться в любой точке пространства, но с разной вероятностью.
Область пространства вокруг ядра, где наиболее вероятно нахождение электрона, называется атомной орбиталью.
Атомная орбиталь может обладать различной формой, размером и ориентацией. Также атомную орбиталь называют электронным облаком.
Графически одну атомную орбиталь принято обозначать в виде квадратной ячейки:
Квантовая механика имеет крайне сложный математический аппарат, поэтому в рамках школьного курса химии рассматриваются только лишь следствия квантово-механической теории.
Согласно этим следствиям, любую атомную орбиталь и находящийся на ней электрон полностью характеризуют 4 квантовых числа.
- Главное квантовое число – n — определяет общую энергию электрона на данной орбитали. Диапазон значений главного квантового числа – все натуральные числа, т.е. n = 1,2,3,4, 5 и т.д.
- Орбитальное квантовое число — l – характеризует форму атомной орбитали и может принимать любые целочисленные значения от 0 до n-1, где n, напомним, — это главное квантовое число.
Орбитали с l = 0 называют s-орбиталями. s-Орбитали имеют сферическую форму и не обладают направленностью в пространстве:
Орбитали с l = 1 называются p-орбиталями. Данные орбитали обладают формой трехмерной восьмерки, т.е. формой, полученной вращением восьмерки вокруг оси симметрии, и внешне напоминают гантель:
Орбитали с l = 2 называются d-орбиталями, а с l = 3 – f-орбиталями. Их строение намного более сложное.
3) Магнитное квантовое число – ml – определяет пространственную ориентацию конкретной атомной орбитали и выражает проекцию орбитального момента импульса на направление магнитного поля. Магнитное квантовое число ml соответствует ориентации орбитали относительно направления вектора напряженности внешнего магнитного поля и может принимать любые целочисленные значения от –l до +l, включая 0, т.е. общее количество возможных значений равно (2l+1). Так, например, при l = 0 ml = 0 (одно значение), при l = 1 ml = -1, 0, +1 (три значения), при l = 2 ml = -2, -1, 0, +1, +2 (пять значений магнитного квантового числа) и т.д.
Так, например, p-орбитали, т.е. орбитали с орбитальным квантовым числом l = 1, имеющие форму «трехмерной восьмерки», соответствуют трем значениям магнитного квантового числа (-1, 0, +1), что, в свою очередь, соответствует трем перпендикулярным друг другу направлениям в пространстве.
4) Спиновое квантовое число (или просто спин) — ms — условно можно считать отвечающим за направление вращения электрона в атоме, оно может принимать значения . Электроны с разными спинами обозначают вертикальными стрелками, направленными в разные стороны: ↓ и ↑.
Совокупность всех орбиталей в атоме, имеющих одно и то же значение главного квантового числа, называют энергетическим уровнем или электронной оболочкой. Любой произвольный энергетический уровень с некоторым номером n состоит из n2 орбиталей.
Множество орбиталей с одинаковыми значениями главного квантового числа и орбитального квантового числа представляет собой энергетический подуровень.
Каждый энергетический уровень, которому соответствует главное квантовое число n, содержит n подуровней. В свою очередь, каждый энергетический подуровень с орбитальным квантовым числом l, состоит из (2l+1) орбиталей. Таким образом, s-подуровень состоит из одной s-орбитали, p-подуровень – трех p-орбиталей, d-подуровень – пяти d-орбиталей, а f-подуровень — из семи f-орбиталей. Поскольку, как уже было сказано, одна атомная орбиталь часто обозначается одной квадратной ячейкой, то s-, p-, d- и f-подуровни можно графически изобразить следующим образом:
Каждой орбитали соответствует индивидуальный строго определенный набор трех квантовых чисел n, l и ml.
Распределение электронов по орбиталям называют электронной конфигурацией.
Заполнение атомных орбиталей электронами происходит в соответствии с тремя условиями:
- Принцип минимума энергии: электроны заполняют орбитали, начиная с подуровня с наименьшей энергией. Последовательность подуровней в порядке увеличения их энергий выглядит следующим образом: 1s<2s<2p<3s<3p<4s≤3d<4p<5s≤4d<5p<6s…;
Для того чтобы проще запомнить данную последовательность заполнения электронных подуровней, весьма удобна следующая графическая иллюстрация:
- Принцип Паули: на каждой орбитали может находиться не более двух электронов.
Если на орбитали находится один электрон, то он называется неспаренным, а если два, то их называют электронной парой.
- Правило Хунда: наиболее устойчивое состояние атома является такое, при котором в пределах одного подуровня атом обладает максимально возможным числом неспаренных электронов. Такое наиболее устойчивое состояние атома называется основным состоянием.
Фактически вышесказанное означает то, что, например, размещение 1-го, 2-х, 3-х и 4-х электронов на трех орбиталях p-подуровня будет осуществляться следующим образом:
Заполнение атомных орбиталей от водорода, имеющего зарядовое число равное 1, до криптона (Kr) с зарядовым числом 36 будет осуществляться следующим образом:
Подобное изображение порядка заполнения атомных орбиталей называется энергетической диаграммой. Исходя из электронных диаграмм отдельных элементов, можно записать их так называемые электронные формулы (конфигурации). Так, например, элемент с 15ю протонами и, как следствие, 15ю электронами, т.е. фосфор (P), будет иметь следующий вид энергетической диаграммы:
При переводе в электронную формулу атома фосфора примет вид:
15P = 1s22s22p63s23p3
Цифрами нормального размера слева от символа подуровня показан номер энергетического уровня, а верхними индексами справа от символа подуровня показано количество электронов на соответствующем подуровне.
Ниже приведены электронные формул первых 36 элементов периодической системы Д.И. Менделеева.
| период | № элемента | символ | название | электронная формула |
| I | 1 | H | водород | 1s1 |
| 2 | He | гелий | 1s2 | |
| II | 3 | Li | литий | 1s22s1 |
| 4 | Be | бериллий | 1s22s2 | |
| 5 | B | бор | 1s22s22p1 | |
| 6 | C | углерод | 1s22s22p2 | |
| 7 | N | азот | 1s22s22p3 | |
| 8 | O | кислород | 1s22s22p4 | |
| 9 | F | фтор | 1s22s22p5 | |
| 10 | Ne | неон | 1s22s22p6 | |
| III | 11 | Na | натрий | 1s22s22p63s1 |
| 12 | Mg | магний | 1s22s22p63s2 | |
| 13 | Al | алюминий | 1s22s22p63s23p1 | |
| 14 | Si | кремний | 1s22s22p63s23p2 | |
| 15 | P | фосфор | 1s22s22p63s23p3 | |
| 16 | S | сера | 1s22s22p63s23p4 | |
| 17 | Cl | хлор | 1s22s22p63s23p5 | |
| 18 | Ar | аргон | 1s22s22p63s23p6 | |
| IV | 19 | K | калий | 1s22s22p63s23p64s1 |
| 20 | Ca | кальций | 1s22s22p63s23p64s2 | |
| 21 | Sc | скандий | 1s22s22p63s23p64s23d1 | |
| 22 | Ti | титан | 1s22s22p63s23p64s23d2 | |
| 23 | V | ванадий | 1s22s22p63s23p64s23d3 | |
| 24 | Cr | хром | 1s22s22p63s23p64s13d5 здесь наблюдается проскок одного электрона с s на d подуровень | |
| 25 | Mn | марганец | 1s22s22p63s23p64s23d5 | |
| 26 | Fe | железо | 1s22s22p63s23p64s23d6 | |
| 27 | Co | кобальт | 1s22s22p63s23p64s23d7 | |
| 28 | Ni | никель | 1s22s22p63s23p64s23d8 | |
| 29 | Cu | медь | 1s22s22p63s23p64s13d10 здесь наблюдается проскок одного электрона с s на d подуровень | |
| 30 | Zn | цинк | 1s22s22p63s23p64s23d10 | |
| 31 | Ga | галлий | 1s22s22p63s23p64s23d104p1 | |
| 32 | Ge | германий | 1s22s22p63s23p64s23d104p2 | |
| 33 | As | мышьяк | 1s22s22p63s23p64s23d104p3 | |
| 34 | Se | селен | 1s22s22p63s23p64s23d104p4 | |
| 35 | Br | бром | 1s22s22p63s23p64s23d104p5 | |
| 36 | Kr | криптон | 1s22s22p63s23p64s23d104p6 |
Как уже было сказано, в основном своем состоянии электроны в атомных орбиталях расположены согласно принципу наименьшей энергии. Тем не менее, при наличии пустых p-орбиталей в основном состоянии атома, нередко, при сообщении ему избыточной энергии атом можно перевести в так называемое возбужденное состояние. Так, например, атом бора в основном своем состоянии имеет электронную конфигурацию и энергетическую диаграмму следующего вида:
5B = 1s22s22p1
А в возбужденном состояниии (*), т.е. при сообщении некоторой энергии атому бора, его электронная конфигурация и энергетическая диаграмма будут выглядеть так:
5B* = 1s22s12p2
В зависимости от того, какой подуровень в атоме заполняется последним, химические элементы делят на s, p, d или f.
Нахождение s, p, d и f-элементов в таблице Д.И. Менделеева:
- У s-элементов последний заполняемый s-подуровень. К данным элементам относятся элементы главных (слева в ячейке таблицы) подгрупп I и II групп.
- У p-элементов заполняется p-подуровень. К p-элементам относят последние шесть элементов каждого периода, кроме первого и седьмого, а также элементы главных подгрупп III-VIII групп.
- d-Элементы расположены между s – и p-элементами в больших периодах.
- f-Элементы называют лантаноидами и актиноидами. Они вынесены вниз таблицы Д.И. Менделеева.
scienceforyou.ru
3.Состав и строение атома. Электронное строение атома. Орбиталь.
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Атом состоит из ядра (оно имеет положительный заряд) и электронов (они имеют отрицательный заряд). В целом атом электронейтрален.
Положительный заряд ядра атома равен порядковому номеру химического элемента.
Ядро атома – сложная частица. В ядре сосредоточена почти вся масса атома.
Заряд ядра определяют протоны. Причем число протонов равно (по величине) заряду ядра атома, т.е. порядковому номеру.
Число нейтронов N определяют по разности между величинами: «масса ядра» А и «порядковый номер» Z.
электроны, имеющие приблизительно равный запас энергии, находятся на приблизительно равном расстоянии от ядра и образуют энергетический уровень.
Изотопами называют атомы одного и того же химического элемента (одинаковое число протонов), различающиеся массой (разное число нейтронов).
Изотопы и их химические соединения отличаются друг от друга по физическим свойствам, но химические свойства у изотопов одного химического элемента одинаковы.
Форма атома — сферическая. Радиус ядра примерно в 100000 раз меньше радиуса атома.
Химический элемент — вид атомов (совокупность атомов) с одинаковым зарядом ядра (с одинаковым числом протонов в ядре).
Изотоп — совокупность атомов одного элемента с одинаковым числом нейтронов в ядре (или вид атомов с одинаковым числом протонов и одинаковым числом нейтронов в ядре).
Разные изотопы отличаются друг от друга числом нейтронов в ядрах их атомов.
Строение электронной оболочки атома
Атомная орбиталь — состояние электрона в атоме. Условное обозначение орбитали — . Каждой орбитали соответствует электронное облако.
Орбитали реальных атомов в основном состоянии бывают четырех типов: s, p, d и f.
Электронное облако — часть пространства, в которой электрон можно обнаружить с вероятностью 90 (или более) процентов.
Примечание: иногда понятия «атомная орбиталь» и «электронное облако» не различают, называя и то, и другое «атомной орбиталью».
Электронная оболочка атома слоистая. Электронный слой образован электронными облаками одинакового размера. Орбитали одного слоя образуют электронный («энергетический») уровень, их энергии одинаковы у атома водорода, но различаются у других атомов.
Однотипные орбитали одного уровня группируются в электронные (энергетические) подуровни:
s-подуровень (состоит из одной s-орбитали), условное обозначение — .
p-подуровень (состоит из трех p-орбиталей), условное обозначение — .
d-подуровень (состоит из пяти d-орбиталей), условное обозначение — .
f-подуровень (состоит из семи f-орбиталей), условное обозначение — .
Энергии орбиталей одного подуровня одинаковы.
Порядок заполнения электронами орбиталей атома определяется тремя законами природы (формулировки даны упрощенно):
1. Принцип наименьшей энергии — электроны заполняют орбитали в порядке возрастания энергии орбиталей.
2. Принцип Паули — на одной орбитали не может быть больше двух электронов.
3. Правило Хунда — в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары.
Общее число электронов на электронном уровне (или в электронном слое) равно 2n2.
Распределение подуровней по энергиям выражается рядом (в прядке увеличения энергии):
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p .
Валентные электроны — электроны атома, которые могут принимать участие в образовании химических связей. У любого атома это все внешние электроны плюс те предвнешние электроны, энергия которых больше, чем у внешних. Например: у атома Ca внешние электроны — 4s2, они же и валентные; у атома Fe внешние электроны — 4s2, но у него есть 3d6, следовательно у атома железа 8 валентных электронов. Валентная электронная формула атома кальция — 4s2, а атома железа — 4s23d6.
Орбиталь – пространство вокруг ядра, в котором наиболее вероятно нахождение электрона. Применительно к электрону можно сказать, что он ведет себя и как частица, и как волна, т. е. обладает, как и другие микрочастицы, корпускулярно-волновым дуализмом (двойственностью). С одной стороны, электроны как частицы производят давление, с другой стороны, движущийся поток электронов обнаруживает волновые явления, например дифракцию электронов.
studfiles.net
Строение атома. Изотопы | АЛХИМИК
В 1913 г. английский физик Г. Мозли установил, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д. И. Менделеева.
Каждый протон имеет заряд +1, поэтому заряд ядра равен числу протонов. Атом является электронейтральной частицей, поэтому число протонов равно числу электронов. Следовательно:
Например, элемент железо Fe имеет порядковый номер 26. Следовательно, заряд ядра атома железа равен +26, т. е. ядро содержит 26 протонов, а вокруг ядра движутся 26 электронов.
Элементарные частицы имеют следующие абсолютные и относительные массы:
Данные этой таблицы показывают, что масса протона, как и масса нейтрона, приблизительно в 1840 раз больше массы электрона. Протоны и нейтроны находятся в ядре, поэтому масса атома почти равна массе ядра. Масса ядра, как и масса атома, определяется суммой числа протонов и числа нейтронов. Эта сумма называется массовым числом атома.
Атомы одного элемента, которые имеют разные массовые числа, называются изотопами.
Атомы изотопов одного элемента имеют одинаковое число протонов (Z) и отличаются друг от друга числом нейтронов (N).
Изотопы обозначаются символами соответствующих элементов, слева от которых вверху записывают массовое число изотопа, а внизу — порядковый номер (заряд ядра атома) элемента. Например:
126C — изотоп углерода с массовым числом 12;
188О — изотоп кислорода с массовым числом 18.
Иногда в символах изотопов записывают только массовые числа ( 12С, 18 О, 27Al и т. д.)
Элемент водород имеет три изотопа, каждый из которых имеет свое название:
В названиях изотопов других элементов указываются их массовые числа. Например: 126С — углерод-12; 35 17Cl — хлор-35 и т. д.
В природе различные элементы имеют разное число изотопов с разным процентным содержанием каждого из них.
Относительная атомная масса элемента Аr, которая приводится в периодической системе, — это средняя величина массовых чисел природных изотопов этого элемента с учетом процентного содержания каждого изотопа.
Например, в природе все атомы хлора представляют собой два вида изотопов: 35 Cl (процентное содержание 75,5%) и 37 Cl (24,5%). Относительная атомная масса хлора
Химические свойства всех изотопов одного элемента одинаковы. Следовательно, химические свойства элемента зависят не от атомной массы, а от заряда ядра.
Поэтому современная формулировка периодического закона читается так:
Свойства элементов и их соединений находятся в периодической зависимости от заряда ядра атома, или порядкового номера элемента.
Формулировка периодического закона Д. И. Менделеевым и современная формулировка не противоречат друг другу, потому что для большинства элементов при увеличении заряда ядра относительная атомная масса тоже увеличивается. Существуют лишь немногие исключения из этого правила. Например, элемент № 18 аргон Ar имеет большую атомную массу, чем элемент № 19 калий K.
Скачать:
Скачать бесплатно реферат на тему:«Строение атома и атомного ядра» СТРОЕНИЕ-АТОМА-И-АТОМНОГО-ЯДРА.docx (7 Загрузок)
Рефераты по другим темам можно скачать здесь
Читайте также
Похожее
al-himik.ru
