Аденозинтрифосфат — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 февраля 2018; проверки требуют 4 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 февраля 2018; проверки требуют 4 правки. Перейти к навигации Перейти к поиску| Аденозинтрифосфат | |
|---|---|
| Общие | |
| Сокращения | АТФ (англ. ATP) |
| Хим. формула | C₁₀H₁₆N₅O₁₃P₃ |
| Физические свойства | |
| Молярная масса | 507,18 г/моль |
| Термические свойства | |
| 144 градус Цельсия[1] | |
| Химические свойства | |
| Растворимость в воде | растворимость в воде (20 °C) — 5 г/100 мл |
| Классификация | |
ru.wikipedia.org
Синтез атф в хлоропластах
Синтез АТФ в хлоропластах – это биохимический процесс, проводимый в мембранах тилакоидов, где происходят также реакции фотосинтеза и перенос протонов для транспортировки энергии. Хлоропласты для воспроизводства процессов перекачивают через себя протоны, используемые для преобразования световой энергии в движущую силу для проведения синтеза в клетке растения.
Фотосинтез и производство кислорода
Для проведения фотосинтеза в водорослях и листьях растений имеются специальные структурные образования – хлоропласты с мелкими отсеками-тилакоидами, используемые для воспроизводства кислорода. Хлоропласт – это энергетическая станция, вырабатывающая энергию для проведения реакций, переносов протонов, формирования АТФ (аденозинтрифосфата) и фотосинтеза.
Основные процессы протекают в мембранах тилакоидов, которые выполняют следующие функции:
- Расщепление молекул воды для выделения кислорода – фотосинтез.
- Транспортировку протонов, переносящих энергию.
- Синтез атф в хлоропластах – универсального энергетического поставщика, участвующего в проведении биохимических реакций.
Тилакоиды располагаются не только в хлоропластах растений, но и присутствуют в цианобактериях, не имеющих ядра и внутреннего разделения на клетки. По мнению учёных, в появлении хлоропластов сыграли немаловажную роль цианобактерии. У них схожее строение, мембрана из двух оболочек, присутствует РНК, ДНК и возможен синтез белка.
Цианобактерии являются самыми древними представителями жизни на планете, и именно им принадлежит первенство в переработке углекислого газа в кислород и воспроизводство
«Фармконтракт-Синтез» является инжиниринговым подразделением ГК «Фармконтракт», занимается разработкой и внедрением проектов для проведения биохимических исследований и лабораторных испытаний в максимально приближенных к естественным условиям. Мы осуществляем поставку комплексов и систем для наблюдения за фотосинтезом, расщеплением клеток или образованием молекул. Нами осуществляется доставка и установка оборудования, валидация методов исследования, квалификационные испытания, модернизацию действующих систем или внедрение автоматики.
phct-synthesis.ru
Биоэнергетические процессы в клетке (Атомная энергетика клетки).
Жизнедеятельность клеток требует энергетических затрат. Живые системы( организмы) получают ее из внешних источников, например, от Солнца( фототрофы, каковыми являются растения, некоторые виды простейших и микроорганизмы), или производят ее сами( аэробные аутотрофы) в результате окисления различных веществ(субстратов).В обоих случаях клетки синтезируют универсальную высокоэнергетичную молекулу АТФ( аденозинтрифосфорную кислоту),при разрушении которой выделяется энергия. Эта энергия расходуется для выполнения всех видов функций- активного транспорта веществ, синтетических процессов, механической работы и т.д.
Сама по себе молекула АТФ достаточно проста и представляет собой нуклеотид, состоящий из аденина, сахара рибозы и трех остатков фосфорной кислоты.( Рис). Молекулярная масса АТФ невелика и составляет 500 дальтон. АТФ является универсальным переносчиком и хранителем энергии в клетке, которая заключена в высокоэнергетичных связях между тремя остатками фосфорной кислоты.
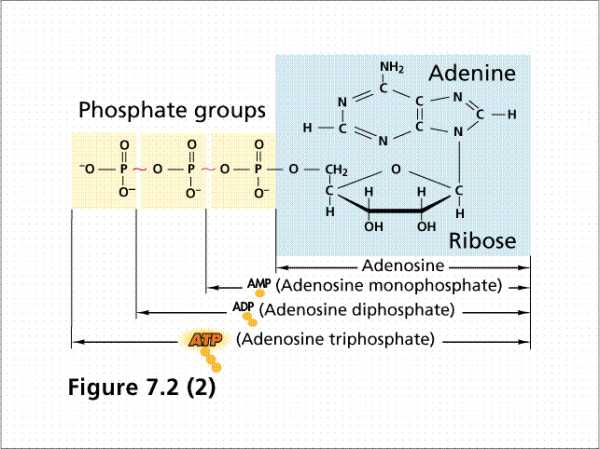

структурная формула пространственная формула
Рис 37. Аденозин-трифосфорная кислота ( АТФ)
Цвета для обозначения молекул(пространственная формула):белый –водород,красный – кислород, зеленый –углерод, голубой –азот,темно-красный — фосфор
Отщепление одного лишь остатка фосфорной кислоты от молекулы АТФ сопровождается высвобождением значительной порции энергии – около 7,3 ккал.
Как же происходит процесс запасания энергии в виде АТФ? Рассмотрим это на примере окисления( сгорания) глюкозы – распространенного источника энергии для перевода в энергию химических связей АТФ.
НОСН2
С ОН Н Н
С С
ОН ОН Н
С С ОН
Н ОН
Рис 38. Структурная формула
глюкозы ( содержание в крови человека- 100 мг%)
Окисление одного моля глюкозы( 180 г) сопровожда-
ется выделением около 690 ккал свободной энергии.
С6Н12О6+ 6О2 6СО2+6Н2О + Е( около 690 ккал)
В живой клетке это огромное количество энергии высвобождается не сразу, а постепенно в виде ступенчатого процесса и регулируется целым рядом окислительных ферментов. При этом, высвобождаемая энергия переходит не в тепловую энергию, как при горении, а запасается в виде химических связей в молекуле АТФ( макроэргические связи) в процессе синтеза АТФ из АДФ и неорганического фосфата. Этот процесс можно сравнить с работой аккумулятора, который заряжается от различных генераторов и может обеспечивать энергией множество машин и аппаратов. В клетке роль унифицированного аккумулятора выполняет система аденозин-ди и три-фосфорных кислот. Зарядка аденилового аккумулятора состоит в соединении АДФ с неорганическим фосфатом ( реакция фосфорилирования) и образовании АТФ:
АДФ + ФнеоргАТФ + Н2О
Для образования всего 1 молекулы АТФ требуется затрата энергии извне в количестве 7,3 ккал. И наоборот, при гидролизе АТФ( разрядке аккумулятора) это же количество энергии выделяется. Оплата этого энергетического эквивалента, называемого в биоэнергетике “ квантом биологической энергии “ происходит из внешних ресурсов – то есть за счет пищевых веществ. Роль АТФ в жизнедеятельности клетки может быть представлена так:
АТФ
Энергети- Система Система Функции
ческие ре- аккумуляции использова- клетки
сурсы энергии ния энергии
АДФ + Фн
Рис.39 Общий план энергетики клетки
Синтез молекул АТФ происходит не только за счет расщепления углеводов( глюкозы), но и белков( аминокислот) и жиров( жирных кислот). Общая схема каскадов биохимических реакций такова( Рис ).
1.Начальные этапы окисления происходят в цитоплазме клеток и не требуют участия кислорода. Эта форма окисления называется анаэробным окислением , или проще – гликолизом.Основной субстрат при анаэробном окислении –гексозы, преимущественно глюкоза. В процессе гликолиза происходит неполное окисление субстрата: глюкоза распадается до триоз ( две молекулы пировиноградной кислоты). При этом, для осуществления реакции в клетке затрачивается две молекулы АТФ, но и синтезируется 4 молекулы АТФ. То есть, методом гликолиза клетка “ зарабатывает” всего две молекулы АТФ при окислении 1 молекулы глюкозы. С точки зрения эффективности энергетики это
маловыгодный процесс.При гликолизе высвобождается всего 5% энергии химических связей молекулы глюкозы.
С6 Н12 О6+ 2Фнеорг+2АДФ 2 С3Н4О3+2АТФ + 2Н2О
Глюкоза пируват
Несмотря на низкую эффективность, гликолиз широко используется в природе: у микроорганизмов, у паразитических кишечных анаэробных простейших, у многих опухолевых клеток.Эритроциты млекопитающих, например, получают энергию за счет гликолиза и у них отсутствуют митохондрии.
2. Образовавшиеся в процессе гликолиза триозы ( в основном-пировиноградная кислота, пируват) использу-
ются для дальнейшего более эффективного окисления, но уже в органеллах клетки – митохондриях. При этом, высвобождается энергия расщепления всех химических связей, что приводит к синтезу большого количества АТФ и потреблению кислорода.
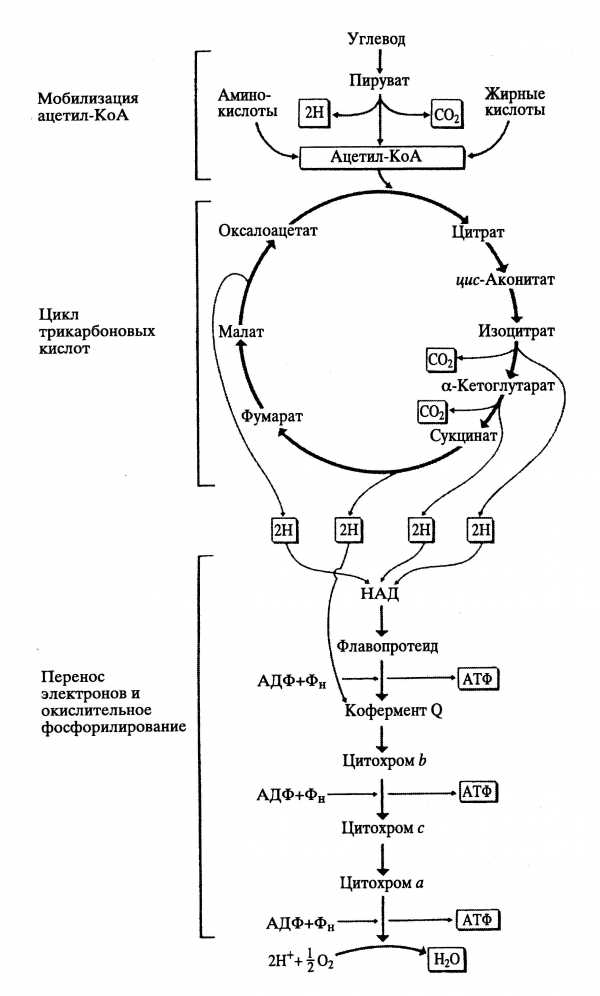
Рис.40 Схема цикла Кребса( трикарбоновых кислот) и окислительного фосфорилирования( дыхательной цепи)
Эти процессы связаны с окислительным циклом трикарбоновых кислот (синонимы:циклом Кребса, циклом лимонной кислоты) и с цепью переноса электронов с одного фермента на другой ( дыхательная цепь), когда из АДФ образуется АТФ путем присоединения одного остатка фосфорной кислоты( окислительное фосфорилирование).
Понятием “окислительное фосфорилирование“ определяют синтез АТФ из АДФ и фосфата за счет энергии окисления субстратов ( питательных веществ).
Под окислением
Какова роль окислительного фосфорилирования у человека? Представление об этом может дать следующий грубый расчет:
Взрослый человек при сидячей работе потребляет в день около 2800 ккал энергии с пищей. Для того, чтобы такое количество энергии было получено методом гидролиза АТФ, потребуется 2800/7,3 = 384 моль АТФ, или 190 кг АТФ. Тогда как известно, что в организме человека содержится около 50 г АТФ. Поэтому ясно, что для удовлетворения потребности в энергии в организме эти 50 г АТФ должны тысячи раз расщепиться и заново синтезироваться. Кроме того, сама скорость обновления АТФ в организме меняется в зависимости от физиологического состояния – минимальная во время сна и максимальная – при мышечной работе. А это означает, что окислительное фосфорилирование – не просто непрерывный процесс, но и регулируемый в широких пределах.
Суть окислительного фосфорилирования заключается в сопряжении двух процессов, когда окислительная реакция с привлечением энергии извне( экзэргическая реакция) увлекает за собой другую, эндэргическую реакцию фосфорилирования АДФ неорганическим фосфатом:
Ав АДФ + Фн
окислениефосфорилирование
Ао АТФ
Здесь Ав–восстановленная форма вещества, подвергающегося фосфорилирующему окислению,
Ао – окисленная форма вещества.
В цикле Кребса образовавшийся в результате гликолиза пируват ( СН3СОСООН) окисляется до ацетата и соединяется с коферментом А, образуя ацетил-коА. После нескольких этапов окисления образуется шестиуглеродное соединение лимонная кислота( цитрат), также окисляющееся до оксал-ацетата; затем цикл повторяется(Cхема цикла трикарб. Кислот). При этом окислении выделяются две молекулы СО2и электроны, которые переносятся на акцепторные( воспринимающие) молекулы ко-ферментов( НАД – никотинамиддинуклеотид) и затем вовлекаются в цепь переноса электронов с одного субстрата( фермента) на другой.
При полном окислении одного моля глюкозы до СО2и Н2О в цикле гликолиза и трикарбоновых кислот образуется 38 молекул АТФ с энергией химических связей 324 ккал, а общий выход свободной энергии этого превращения , как отмечалось ранее, составляет 680 ккал. Эффективность выхода запасенной энергии в АТФ составляет 48%( 324/680 х100%= 48%).
Cуммарное уравнение окисления глюкозы в цикле Кребса и гликолитическом цикле:
C6Н12О6 +6О2+36 АДФ +Фн 6СО2+36АТФ + 42Н2О
3. Освободившиеся в результате окисления в цикле Кребса электроны соединяются с ко-ферментом и транспортируются в цепь переноса электронов( дыхательную цепь) с одного фермента на другой, где в процессе переноса и происходит сопряжение( трансформация энергии электронов в энергию химических связей) с синтезом молекул АТФ.
Существует три участка дыхательной цепи, в которых энергия процесса окисления-восстановления трансформируется в энергию связей молекул в АТФ. Эти участки называются пунктами фосфорилирования:
1.Участок переноса электронов от НАД-Н к флавопротеиду, синтезируется 10 молекул АТФ за счет энергии окисления одной молекулы глюкозы,
2.Перенос электронов на участке от цитохрома б к цитохрому с1, фосфорилируется 12 молекул АТФ на одну молекулу глюкозы,
3. Перенос электронов на участке цитохром с – молекулярный кислород, синтезируется 12 молекул АТФ.
Итого, на этапе дыхательной цепи происходит синтез( фосфорилирование) 34 молекул АТФ. А общий выход АТФ в процессе аэробного окисления одной молекулы глюкозы составляет 40 единиц.
Таблица 1
Энергетика окисления глюкозы
|
Механизм накопления энергии |
Выход АТФ на одну молекулу глюкозы |
|
Гликолиз Цикл Кребса( трикарбо- новых кислот) Дыхательная цепь |
4 2 34 Итого: 40 С вычетом энергозатрат на запуск гликолиза 38 АТФ |
На каждую пару электронов, передающихся по цепи от НАД –Н+к кислороду, синтезируется три молекулы АТФ
Дыхательная цепь представляет собой ряд белковых комплексов, встроенных во внутреннюю мембрану митохондрий( Рис 41 ).
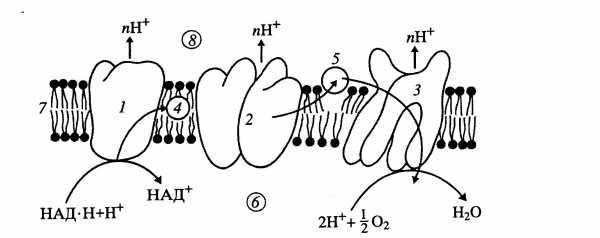
Рис.41 Схема расположения ферментов дыхательной цепи во внутренней мембране митохондрий:
1-НАД-Н-дегидрогеназный комплекс, с1-комплекс, 3-цитохром-оксидазный комплекс, 4-убихинон, 5-цито-
хром-с, 6-матрикс митохондрии, внутренняя мембрана митохондрии,8- межмембранное пространство.
Итак, полное окисление исходного субстрата завершается высвобождением свободной энергии, значительная часть которой ( до 50%) расходуется на синтез молекул АТФ, образованием СО2и воды.Другая половина свободной энергии окисления субстратов идет на следующие нужды клетки:
1. Для биосинтеза макромолекул( белков, жиров, углеводов),
2. Для процессов движения и сокращения,
3. Для активного транспорта веществ через мембраны,
4.Для обеспечения передачи генетической информации.
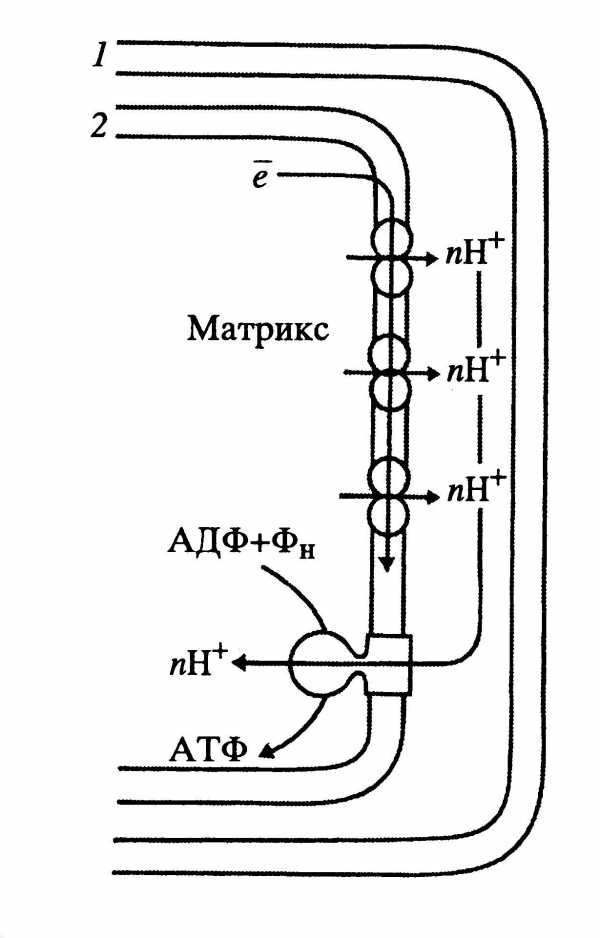
3
Рис.42 Общая схема процесса окислительного фосфорилирования в митохондриях.
1- наружная мембрана митохондрии, 2- внутренняя мембрана, 3- встроенный во внутреннюю мембрану фермент АТФ-синтетаза.
Синтез молекул АТФ
Синтез АТФ происходит во внутренней мембране митохондрий, смотрящей в матрикс( Рис 42 выше).В нее встроены специализировавнные белки-ферменты, занимающиеся исключительно синтезом АТФ из АДФ и неорганического фосфата Фн—АТФ-синтетазы( АТФ-С). В электронном микроскопе эти ферменты имеют весьма характерный вид, за что и были названы “грибовидными тельцами”( Рис). Эти структуры сплошь выстилают внутреннюю поверхность мембраны митохондрии,направленную в матрикс.По образному
выражению известного исследователя биоэнергетики проф. Тихонова А.Н.,АТФ-С является “самым миниатюрным и совершенным мотором в природе”.
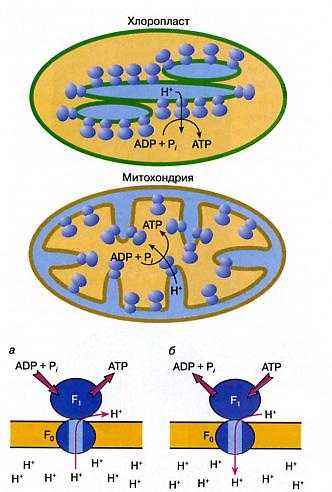
Рис.43 Локализация
АТФ-синтетаз в мембране мито-
хондрий( клетки животных) и хлоропластов( клетки растений).
Голубые участки -области с повышенной концентрацией Н+( кислотная зона),оранжевые участки –области с низкой концентрацией Н+.
Внизу: перенос ионов водорода Н+ через мембрану при синтезе(а) и гидролизе(б) АТФ
Эффективность работы этого фермента такова, что одна молекула способна осуществить 200 циклов ферментативной активации в секунду, при этом синтезируется 600 молекул АТФ.
Интересная подробность работы этого мотора в том, что он содержит вращающиеся детали и состоит из роторной части и статора, причем, вращение ротора происходит против часовой стрелки.( Рис. 44)
Мембранная часть АТФ-С, или фактор сопряжения F0,представляет собой гидрофобный белковый комплекс. Второй фрагмент АТФ-С – фактор сопряженияF1— выступает из мембраны в виде грибовидного образования. В митохондриях животных клеток АТФ-С встроена во внутреннюю мембрану, а комплексF1обращен в сторону матрикса.
Образование АТФ из АДФ и Фн происходит в каталитических центрах фактора сопряжения F1. Этот белок можно легко выделить из мембраны митохондрий, при этом он сохраняет способность гидролизовать молекулу АТФ, но теряет способность синтезировать АТФ. Способность синтезировать АТФ – это свойство единого комплексаF0F1в мембране митохондрии( рис1 а)Это связано с тем, что синтез АТФ в помошью АТФ-С сопряжен с транспортом через нее протонов Н+в направлении отF0rF1( рис 1 а). Движущей силой для работы АТФ-С является протонный потенциал, создаваемый дыхательной цепью транспорта электронов е—.
АТФ-С – это обратимая молекулярная машина, катализирующая как синтез, так и гидролиз АТФ. В режиме синтеза АТФ работа фермента осуществляется за счет энергии протонов Н+, переносимых под действием разности протонных потенциалов. В то же время, АТФ-С работает и как протонная помпа – за счет энергии гидролиза АТФ она перекачивает протоны из области с низким протонным потенциалом в область с высоким потенциалом ( рис 1б). Сейчас уже известно, что каталитическая активность АТФ-С непосредственно связана с вращением ее роторной части. Было показано, что молекулаF1 вращает роторный фрагмент дискретными скачками с шагом в 1200. Один оборот на 1200сопровождается гидролизом одной молекулы АТФ.
Замечательным качеством вращающегося мотора АТФ-С является его исключительно высокая КПД. Было показано, что работа, которую совершает мотор при повороте роторной части на 1200, почти точно совпадает с величиной энергии, запасенной в молекуле АТФ, т.е. КПД мотора близок к 100%.
В таблице приведены сравнительные характеристики нескольких типов молекулярных моторов, работающих в живых клетках. Среди них АТФ-С выделяется своими наилучшими свойствами. По эффективности работы и развиваемой ею силе она значительно превосходит все известные в природе молекулярные моторы и уж конечно – все созданные человеком.
Таблица 2 Сравнительные характеристики молекулярных моторов клеток( по: Kinoshitaetal, 1998).
|
Мотор/ Путь |
Шаг |
Макс.сила |
Макс. КПД |
Способ движения |
|
Миозин/ актин Кинезин/ микротру- бочка РНКполи- Мераза F1-комплекс АТФ-С |
Перемен Ный Смещение На 8 нм Смещение на 0.34 нм Поворот На 1200 |
3-5 пН 5 пН 14 пН 40 пН .нм |
Около 20% Ок 50% Ок. 20% Ок 100% |
Шаги, прыжки Бег Шаги Ползание вращение |
Молекула F1комплекса АТФ-С примерно в 10 раз сильнее акто-миозинового комплекса – молекулярной машины, специализирующейся на выполнении механической работы. Таким образом, за многие миллионы лет эволюции до того, как появился человек,придумавший колесо, преимущества вращательного движения были уже реализованы природой на молекулярном уровне.
Объем работы, которую производит АТФ-С, поражает грандиозностью. Общая масса молекул АТФ синтезируемых в организме взрослого человека за сутки cоставляет около 100 кг. В этом нет ничего удивительного, поскольку в организме идут многочисленные
биохимические процессы с использованием АТФ. Поэтому, чтобы организм мог жить, его АТФ-С должны постоянно крутиться, своевременно восполняя запасы АТФ.
Яркий пример молекулярных электромоторов – работа жгутиков бактерий. Бактерии плавают со средней скоростью 25 мкм/с , а некоторые из них – со скоростью более 100 мкм/с. Это означает, что за одну секунду бактерия перемещается на расстояние в 10 и более раз большее, чем собственные размеры. Если бы пловец преодолевал за одну секунду расстояние, в десять раз больше его собственного роста б , то 100-метровую дорожку он проплывал бы за 5 секунд!
Скорость вращения электромоторов бактерий колеблется от 50-100 об/ сек до 1000 об/ сек, при этом они очень экономичны и расходуют не более 1% энергетических ресурсов клетки.
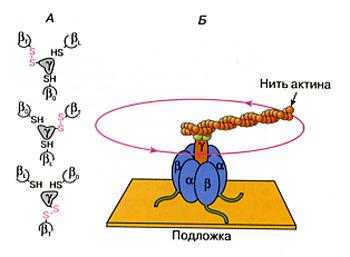
Рис 44. Схема вращения роторной субъединицы АТФ-синтетазы.
Таким образом, во внутренней мембране митохондрий локализованы как ферменты дыхательной цепи, так и синтеза АТФ.
Помимо синтеза АТФ, выделяющаяся при транспортировке электронов энергия запасается еще и в виде градиента протонов на мембране митохондрий.При этом, между наружной и внутренней мембранами возникает повышенная концентрация ионов Н+( протонов). Возникший протонный градиент из матрикса в межмембранное пространство служит движущей силой при синтезе АТФ( Рис.42). По существу,внутренняя мембрана митохондрий с встроенными АТФ-синтетазами является совершенной электростанцией на протонах, поставляющей с высокой эффективностью энергию для жизнедеятельности клетки.
При достижении определенной разности потенциалов ( 220 мВ) на мембране,АТФ-синтетаза начинает транспортировать протоны обратно в матрикс; при этом происходит превращение энергии протонов в энергию синтеза химических связей АТФ. Так осуществляется сопряжение окислительных процессов с синтетически-
ми в процессе фосфорилирования АДФ до АТФ.
Энергетика окислительного фосфорилирования
жиров
Еще более эффективным оказывается синтез АТФ при окислении жирных кислот и липидов. При полном окислении одной молекулы жирной кислоты, например, пальмитиновой, образуется 130 молекул АТФ. Изменение свободной энергии окисления кислоты составляет ∆G= -2340 ккал, а аккумулированная в АТФ энергия при этом составляет около 1170 ккал.
Энергетика окислительного расщепления аминокислот
Большую часть метаболической энергии, вырабатываемой в тканях, обеспечивают процессы окисления углеводов и особенно жиров; у взрослого человека до 90% всей потребности в энергии покрывается из этих двух источников. Остальную энергию ( в зависимости от рациона от 10 до 15%) поставляет процесс окисления аминокислот( рис цикла Кребса ).
Было подсчитано, что клетка млекопитающих содержит в среднем около 1 миллиона ( 106) молекул АТФ. В пересчете на все клетки тела человека ( 1016 –1017 ) это составляет 1023 молекул АТФ. Суммарная энергия, заключенная в этой массе АТФ, может достигать значений 1024 ккал! ( 1 Дж= 2,39х 10-4ккал). У человека весом 70 кг общее количество АТФ составляет 50 г, большая часть которого ежедневно расходуется и вновь синтезируется.
studfiles.net
Аэробное дыхание. Синтез АТФ. Цепи.
ПВК, окисляется с участием коэнзима А до ацетил-КоА. В данном процессе работают ферменты пируватдегидрогеназы: Ch4–CO–COOH + KoA–SH + HAД+ = Ch4–CO~KoA + НАД · Н2 + CO2
Ацетил-КоА является исходным субстратом цикла трикарбоновых кислот (ЦТК), или цикла Кребса.
В цикл Кребса включается одна молекула ацетил-КоА, которая в реакции с оксалоацетатом, катализируемой цитратсинтетазой, приводит к образованию лимонной кислоты и свободн. коэнзимаА. Лимонная кислота с помощью фермента аконитазы превращается в цис-акотиновую и изолимонную кислоты. Изолимонная кислота через щавелевоянтарную кислоту превращается в а-кетоглутаровую кислоту, которая подвергается дальнейшему декарбоксилированию.
В конечном итоге — двух молекул СО2, одной молекулы АТФ и 8 атомов водорода, из которых шесть атомов связаны в молекулах пиридиннуклеотидов и два атома – в молекулах флавопротеинов.
У некоторых бактерий цикл трикарбоновых кислот «разорван». Наиболее часто отсутствует этап превращения а-кетоглутаровой кислоты в янтарную. В таком виде ЦТК не может функционировать в системе энергодающих реакций клетки. Основная функция «разорванного» ЦТК – биосинтетическая.
Образовавшиеся на разных этапах окисления органических веществ НАДН2 и ФАДН2, поступают в дыхательную цепь, которая у бактерий находится в цитоплазматической мембране. Они вновь окисляются до НАД и ФАД, а отщепившийся от них водород передается не менее чем через пять переносчиков на заключительный участок цепи, где соединяется с молекук.кислородом, образуя воду.
Транспорт водорода сопровождается протеканием ряда окислительно-восстановительных реакции- образ.АТФ — окислительного фосфорилирования.
Флавопротеины – коферменты, в состав которых входит витамин В2, а в качестве простетических групп в них выступают флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД). Флавопротеины осуществляют перенос атомов водорода, т. е. являются дегидрогеназами. Дегидрогеназа, содержащая в качестве простетической группы ФМН, яв- ляется НАДФН2-дегидрогеназой. Это стартовый переносчик в дыхательной цепи, осуществляющей перенос водорода с НАДФН2 на следующие компоненты дыхательной цепи. Дегидрогеназа, содержащая в качестве простетической группы ФАД, действует как сукцинатдегидрогеназа. Она катализирует окисление янтарной кислоты в фумаровую в ЦТК. Атомы водорода от ФАДН2 поступают сразу на хиноны, локализ. на последних этапах электронтрансп.ц.
Железосерные белки (FeS-белки) содержат железосероцентры, в которых атомы железа связаны, с одной стороны, с серой аминокислоты цистеина, а с другой – с неорганической сульфидной серой.
Железосероцентры входят в состав некоторых флавопротеинов или же служат в качестве единственных простетических групп белков. Железосероцентры в зависимости от строения могут осуществлять одновременный перенос одного или двух электронов, что связано с изменением валент. атомов железа.
Хиноны – жирорастворимые соединения. У грамотрицательных бактерий они представлены убихиноном (кофермент Q) или менахиноном
Хиноны липофильны, и поэтому локализуются в липидной фазе мембраны. Они переносят атомы водорода. Они служат «сборщиками» водорода, поставляемого различными коферментами и простетическими группами в дыхательной цепи, и передают его цитохромам.
Цитохромы принимают участие на заключительном этапе в цепи переноса электронов. К ним электроны поступают от хинонов. В качестве простетической группы цитохромы содержат гем. Цитохромы окра-
шены; они отличаются друг от друга спектрами поглощения и окислительно-восстановительными потенциалами. Широко распространен цитохром с. Конечные (терминальные) цитохромы дыхательной цепи – это цитохромы а + а3 или цитохромоксидаза. Они передают электроны на молекулярный
кислород, т. е. катализируют восстановление молекулярного кислорода до воды. В реакционном центре цитохромоксидазы, помимо двух гемов, содержатся два атома меди.
Флавопротеины и хиноны осуществляют перенос атомов водорода, а FeS-белки и цитохромы – электронов.
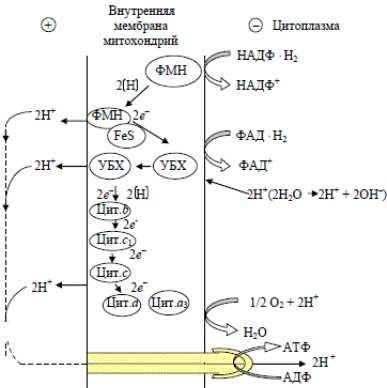 у дрожжей: • комплекс 1 – НАД Н2-дегидрогеназа; в него входят ФМН и железосерные белки; НАД Н2-дегидрогеназа переносит водород от НАДН2 к коферменту Q; • комплекс 2 – сукцинатдегидрогеназа, содержащая ФАД. Она отдает водород в дыхательную цепь на уровне кофермента Q; • комплекс 3 – цитохром b и цитохром с1, принимающие электроны от кофермента Q и передающие их на цитохром с; • комплекс 4 –цитохромоксидаза, осуществляющая перенос электронов на молекулярный кислород.
у дрожжей: • комплекс 1 – НАД Н2-дегидрогеназа; в него входят ФМН и железосерные белки; НАД Н2-дегидрогеназа переносит водород от НАДН2 к коферменту Q; • комплекс 2 – сукцинатдегидрогеназа, содержащая ФАД. Она отдает водород в дыхательную цепь на уровне кофермента Q; • комплекс 3 – цитохром b и цитохром с1, принимающие электроны от кофермента Q и передающие их на цитохром с; • комплекс 4 –цитохромоксидаза, осуществляющая перенос электронов на молекулярный кислород.
Дых. цепь бактерий E. coli: — в нее не входит цитохром с; — дых. цепь у E. coli разветвлена.
В клетках, растущих в условиях достаточной аэрации, восстановительные эквиваленты передаются к кислороду преимущественно через кофермент Q, цитохром b556 и цитохром о. При ограниченном снабжении кислородом клетки используют в качестве переносчиков электронов менахинон или убихинон и цитохромы b558 и d. В последнем случае обр-ся меньшее АТФ.
У дрожжей существуют 3 пункта фосфорилирования, которые соответствуют участкам
выхода протонов во внешнюю среду. Первый участок локализован в на-чале дыхательной цепи и связан с функционированием НАДФН2-дегидрогеназы. Второй определяется способностью убихинона переносить водород. Последний локализован в конце цепи и связан с активностью цитохромоксидазы.
Так как внутренняя мембрана митохондрий и цитоплазматическая мембрана бактерий непроницаемы для ионов, в том числе и для Н+, и ОН–, то создается трансмембранный электрохимический, или протонный градиент между наружной и внутренней их сторонами. Протоны могут обратно поступать
через мембрану только в определенных местах. В них располагаются АТФ-синтазы.
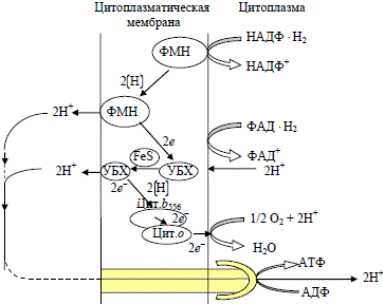 Установлено, что синтез молекулы АТФ связан с переносом двух протонов через комплекс АТФ-синтазы. При окислении НАДН2 молек. кислородом выделяется 6 протонов,макс.выход АТФ =3.
Установлено, что синтез молекулы АТФ связан с переносом двух протонов через комплекс АТФ-синтазы. При окислении НАДН2 молек. кислородом выделяется 6 протонов,макс.выход АТФ =3.
• в процессе гликолиза образуются 2 АТФ, 2 НАДН2 и 2пирувата; • при окислительном декарбоксилировании 2 пирувата образуются 2 ацетил-КоА и 2 НАДН2; • окисление 2 ацетил-КоА в цикле Кребса приводит к образованию 6 НАДН2, 2 ФАДН2 и 2 АТФ. НАДН2 — 3 АТФ, ФАДН2 – 2 АТФ.Суммарный энергетический выход С6Н12О6 + 6О2 + 38АДФ + 38Н3РО4 6СО2 + 38АТФ + 44Н2О
E. coli. Имеются только два пункта, в которых происходит «выброс» протонов.Следовательно, при окислении одной молекулы НАДН2 образуются только 2 АТФ, а при окисл. молекулы ФАДН2 – 1 АТФ. E. coli 26 молекул АТФ: • 2 АТФ синтезируются в гликолизе; • 2 АТФ синтезируются в двух оборотах цикла Кребса; • 10 молекул НАДН2 приводят к синтезу 20 молекул АТФ; • 2 ФАДН2=2 АТФ.
Corynebacterium diphtheriae имеется только один пункт «выброса» протонов. У Mycobacterium phlei – 3.
students-library.com
синтез атф в клетке происходит в процессе
синтез атф в клетке происходит в процессе
В разделе Школы на вопрос синтез молекулы АТФ происходит заданный автором роскошь лучший ответ это 4) На кислородном этапе энергетического обмена.
Энергетический обмен в клетках растений и животных, его значение. Роль митохондрий в нем.
1. Энергетический обмен — совокупность реакций окисления органических веществ в клетке, синтеза молекул АТФ за счет освобождаемой энергии. Значение энергетического обмена — снабжение клетки энергией, которая необходима для жизнедеятельности.
2. Этапы энергетического обмена : подготовительный, бескислородный, кислородный.
1) Подготовительный — расщепление в лизосо-мах полисахаридов до моносахаридов, жиров до глицерина и жирных кислот, белков до аминокислот, нуклеиновых кислот до нуклеотидов. Рассеивание в виде тепла небольшого количества освобождаемой при этом энергии;
2) бескислородный — окисление веществ без участия кислорода до более простых, синтез за счет освобождаемой энергии двух молекул АТФ. Осуществление процесса на внешних мембранах митохондрий при участии ферментов;
3) кислородный — окисление кислородом воздуха простых органических веществ до углекислого газа и воды, образование при этом 36 молекул АТФ. Окисление веществ при участии ферментов, расположенных на кристах митохондрий. Сходство энергетического обмена в клетках растений, животных, человека и грибов — доказательство их родства.
3. Митохондрии — «силовые станции» клетки, их отграничение от цитоплазмы двумя мембранами — внешней и внутренней. Увеличение поверхности внутренней мембраны за счет образования складок — крист, на которых расположены ферменты. Они ускоряют реакции окисления и синтеза молекул АТФ. Огромное значение митохондрий — причина большого количества их в клетках организмов почти всех царств.
Обобщенная реакция кислородного этапа окисления:
2С3Н403 + 4Н + 602 -> 6С02 + 6Н20; 36АДФ -> 36АТФ.
ссылка
Привет! Вот подборка тем с ответами на Ваш вопрос: синтез молекулы АТФ происходит
Ответ от 2 ответа[гуру]Привет! Вот еще темы с нужными ответами:
Аденозинтрифосфат на Википедии
Посмотрите статью на википедии про Аденозинтрифосфат
Биосинтез белка на Википедии
Посмотрите статью на википедии про Биосинтез белка
Ответить на вопрос:
22oa.ru
Какое количество АТФ содержится в организме?
⇐ ПредыдущаяСтр 15 из 31Следующая ⇒
Судя по всему выше изложенному, требуется колоссальное количество АТФ. В скелетных мышцах при их переходе от состояния покоя к сократительной активности — в 20 раз (или даже в несколько сотен раз) резко одномоментно повышается скорость расщепления АТФ.
Однако, запасы АТФ в мышцах сравнительно ничтожны (около 0,75 % от ее массы) и их может хватить лишь на 2-3 секунды интенсивной работы.
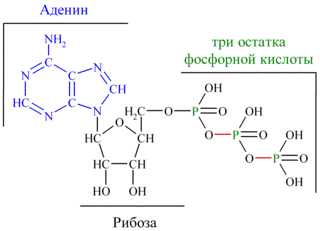
Рис.15. Аденозинтрифосфат (АТФ, ATP). Молярная масса 507.18г/моль
Это происходит потому, что АТФ — крупная тяжелая молекула (рис.15). АТФ представляет собой нуклеотид, образованный азотистым основанием аденином, пятиуглеродным сахаром рибозой и тремя остатками фосфорной кислоты. Фосфатные группы в молекуле АТФ соединены между собой высокоэнергетическими (макроэргическими) связями. Подсчитано, что если бы в организме содержалось количество АТФ, достаточное для использования в течение одного дня, то вес человека, даже ведущего сидячий образ жизни, был бы на 75% больше.
Чтобы поддерживать длительное сокращение, молекулы АТФ должны образовываться в процессе метаболизма с такой же скоростью, с какой они расщепляются во время сокращения. Поэтому АТФ является одним из самых часто обновляемых веществ, так у человека продолжительность жизни одной молекулы АТФ менее 1 мин. В течение суток одна молекула АТФ проходит в среднем 2000—3000 циклов ресинтеза (человеческий организм синтезирует около 40 кг АТФ в день, но содержит в каждый конкретный момент примерно 250 г), то есть запаса АТФ в организме практически не создаётся, и для нормальной жизнедеятельности необходимо постоянно синтезировать новые молекулы АТФ.
Таким образом, для поддержания активности мышечной ткани на определенном уровне необходим быстрый ресинтез АТФ с той же скоростью, с какой он расходуется.Это происходит в процессе рефосфорилирования, при соединении АДФ и фосфатов
Синтез АТФ —фосфорилирование АДФ
В организме АТФ образуется из АДФ и неорганического фосфата за счет энергии, освобождающейся при окислении органических веществ и в процессе фотосинтеза. Этот процесс называется фосфорилированием. При этом должно быть затрачено не менее 40 кДж/моль энергии, которая аккумулируется в макроэргических связях:
АДФ + H3PO4 + энергия → АТФ + H2O
Фосфорилирование АДФ
Субстратное фосфорилирование АТФ Окислительное фосфорилирование АТФ
Фосфорилирование АДФ возможно двумя способами: субстратное фосфорилирование и окислительное фосфорилирование (используя энергию окисляющихся веществ). Основнаямасса АТФ образуется на мембранах митохондрий в ходе окислительного фосфорилирования Н-зависимой АТФ – синтазой.. Субстратное фосфорилирование АТФ не требует участия мембранных ферментов, оно происходит в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений..
Реакции фосфорилирования АДФ и последующего использования АТФ в качестве источника энергии образуют циклический процесс, составляющий суть энергетического обмена.
Существуют три способа образования АТФ во время сокращения мышечного волокна.
Три основных пути ресинтеза АТФ:
1 — креатинфосфатная (КФ) система
2 — гликолиз
3 — окислительное фосфорилирование
Креатинфосфатная (КФ) система –
— фосфорилирование АДФ путем переноса фосфатной группы от креатинфосфата
— анаэробный креатинфосфатный ресинтез АТФ.
Рис.16. Креатинфосфатная(КФ)система ресинтеза АТФ в организме
Для поддержания активности мышечной ткани на определенном уровне необходим быстрый ресинтез АТФ. Это происходит в процессе рефосфорилирования, при соединении АДФ и фосфатов. Наиболее доступным веществом, которое используется для ресинтеза АТФ, в первую очередь является креатинфосфат (рис.16), легко передающий свою фосфатную группу на АДФ:
КрФ + АДФ → Креатин + АТФ
КрФ – это соединение азотосодержащего вещества креатинина с фосфорной кислотой. Концентрация его в мышцах составляет примерно 2–3 %, т. е. в 3–4 раза больше по сравнению с АТФ. Умеренное (на 20–40 %) снижение содержания АТФ сразу же ведет к использованию КрФ. Однако при максимальной работе запасы креатинфосфата также быстро истощаются. Благодаря фосфорилированию АДФ креатинфосфатом обеспечивается очень быстрое образование АТФ в самом начале сокращения.
В течение периода покоя концентрация креатинфосфата в мышечном волокне возрастает до уровня, примерно в пять раз превышающего содержание АТФ. В начале сокращения, когда начинаются снижение концентрации АТФ и увеличение концентрации АДФ вследствие расщепления АТФ под действием АТФазы миозина, реакция сдвигается в сторону образования АТФ за счет креатинфосфата. При этом переход энергии совершается с такой большой скоростью, что в начале сокращения концентрация АТФ в мышечном волокне изменяется мало, в то время как концентрация креатинфосфата падает быстро.
Хотя АТФ образуется за счет креатинфосфата очень быстро, посредством единственной ферментативной реакции (рис.16), количество АТФ лимитировано исходной концентрацией креатинфосфата в клетке. Чтобы мышечное сокращение могло продолжаться дольше нескольких секунд, необходимо участие двух других, упоминавшихся выше, источников образования АТФ. После начала сокращения, обеспечиваемого за счет использования креатинфосфата, подключаются более медленные, требующие участия многих ферментов пути окислительного фосфорилирования и гликолиза, благодаря которым скорость образования АТФ увеличивается до уровня, соответствующего скорости расщепления АТФ.
Какая система синтеза АТФ самая быстрая?
Система КФ (креатинфосфата) — это самая быстрая система ресинтеза АТФ в организме, поскольку она включает в себя только одну ферментативную реакцию. Она осуществляет перенос высокоэнергетического фосфата прямо с КФ на АДФ с образованием АТФ. Однако способность этой системы ресинтезировать АТФ ограничена, так как запасы КФ в клетке невелики. Поскольку эта система не использует для синтеза АТФ кислород, ее считают анаэробным источником АТФ.
Сколько КФ хранится в организме?
Общих запасов КФ и АТФ в организме хватило бы менее чем на 6 секунд интенсивной физической нагрузки.
В чем заключается преимущество анаэробной выработки АТФ с использованием КФ?
Система КФ/АТФ используется во время кратковременной интенсивной физической нагрузки. Она расположена на головках молекул миозина, т. е. непосредственно в месте потребления энергии. Система КФ/АТФ используется, когда человек совершает быстрые движения, например, быстро поднимается в гору, выполняет высокие прыжки, бежит стометровку, быстро поднимается с кровати, убегает от пчелы или отскакивает в сторону от грузовика при переходе улицы.
Гликолиз
— фосфорилирование АДФ в цитоплазме
— расщепление гликогена и глюкозы в анаэробных условиях с образованием молочной кислоты и АТФ.
Для восстановления АТФ с целью продолжения интенсивной мышечной деятельности в процесс включается следующий источник энергообразования – ферментативное расщепление углеводов в бескислородных (анаэробных) условиях.
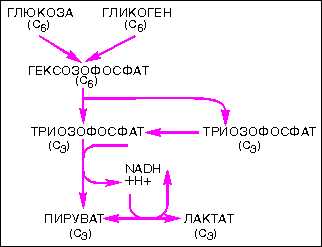
Рис.17. Общая схема гликолиза
Процесс гликолиза схематично представлен следующим образом (рис.17).
Появление в процессе гликолиза свободных фосфатных групп делает возможным ре-синтез АТФ из АДФ. Однако при этом кроме АТФ образуются две молекулы молочной кислоты.
Процесс гликолиза более медленный по сравнению с креатинфосфатным ресинтезом АТФ. Длительность работы мышц в анаэробных (бескислородных) условиях ограничена в связи с исчерпыванием запасов гликогена или глюкозы и в связи с накоплением молочной кислоты.
Анаэробное образование энергии путем гликолиза производится неэкономно с большим расходом гликогена, так как используется только часть содержащейся в нем энергии (молочная кислота при гликолизе не используется, хотя содержит значительные запасы энергии).
Конечно, уже на этом этапе часть молочной кислоты окисляется некоторым количеством кислорода до углекислого газа и воды:
С3Н6О3 + 3О2 = 3СО2 + 3Н2О 41
Образующаяся при этом энергия идет на ресинтез углевода из других частей молочной кислоты. Однако ограниченное количество кислорода при очень интенсивной физической нагрузке оказывается недостаточным для поддержания реакций, направленных на преобразование молочной кислоты и ресинтез углеводов.
Откуда берется АТФ для физической активности, продолжающейся более 6 секунд?
При гликолизе АТФ образуется без использования кислорода (анаэробно). Гликолиз происходит в цитоплазме мышечной клетки. В процессе гликолиза углеводы окисляются до пирувата или лактата и выделяются 2 молекулы АТФ (3 молекулы, если начинать расчет с гликогена). При гликолизе АТФ синтезируется быстро, но медленнее, чем в системе КФ.
Что является конечным продуктом гликолиза — пируват или лактат?
Когда гликолиз протекает медленно, и митохондрии адекватно акцептируют восстановленный НАДН, конечным продуктом гликолиза является пируват. Пируват превращается в ацетил-КоА (реакция, требующая НАД) и подвергается полному окислению в цикле Кребса и ЦПЭ. Когда митохондрии не могут обеспечить адекватное окисление пирувата или регенерацию акцепторов электронов (НАД или ФАДН), пируват превращается в лактат. Превращение пирувата в лактат уменьшает концентрацию пирувата, что предотвращает ингибирование реакции конечными продуктами, и гликолиз продолжается.
В каких случаях основным конечным продуктом гликолиза оказывается лактат?
Лактат образуется в том случае, когда митохондрии не могут адекватно окислять пируват или регенерировать достаточное количество акцепторов электронов. Это происходит при низкой ферментативной активности митохондрий, при недостаточном кислородном обеспечении, при высокой скорости гликолиза. В целом, образование лактата усиливается во время гипоксии, ишемии, при кровотечении, после употребления углеводов, при высокой концентрации гликогена в мышцах, при гипертермии, вызванной физической нагрузкой.
Какими другими способами может метаболизироваться пируват?
Во время физических упражнений или при недостаточно калорийном питании пируват превращается в заменимую аминокислоту аланин. Синтезированный в скелетных мышцах аланин с током крови попадает в печень, где превращается в пируват. Затем пируват превращается в глюкозу, которая поступает в кровоток. Этот процесс аналогичен циклу Кори и называется аланиновым циклом.
Рекомендуемые страницы:
lektsia.com
АТФ и ее роль в обмене веществ
Любой организм может существовать до тех пор, пока происходит поступление питательных веществ из внешней среды и пока продукты его жизнедеятельности выделяются в эту среду. Внутри клетки происходит непрерывный очень сложный комплекс химических превращений, благодаря которым из питательных веществ образуются компоненты тела клетки. Совокупность процессов превращения материи в живом организме, сопровождающихся постоянным ее обновлением, и называется обменом веществ.
Часть общего обмена, которая состоит в поглощении, усвоении питательных веществ и создании за их счет структурных компонентов клетки, называется ассимиляцией — это конструктивный обмен. Вторую часть общего обмена составляют процессы диссимиляции, т.е. процессы разложения и окисления органических веществ, в результате которых клетка получает энергию, — это энергетический обмен. Конструктивный и энергетический обмен составляют единое целое.
В процессе конструктивного обмена клетка из довольно ограниченного числа низкомолекулярных соединений синтезирует биополимеры своего тела. Биосинтетические реакции протекают при участии разнообразных ферментов и требуют затрат энергии.
Живые организмы могут использовать только химически связанную энергию. Каждое вещество обладает определенным запасом потенциальной энергии. Главными материальными носителями ее являются химические связи, разрыв или преобразование которых приводит к освобождению энергии. Энергетический уровень одних связей имеет величину 8—10 кДж — эти связи называются нормальными. В других связях заключена значительно большая энергия — 25—40 кДж — это так называемые макроэргические связи. Почти все известные соединения, обладающие такими связями, имеют в своем составе атомы фосфора или серы, по месту которых в молекуле и локализованы эти связи. Одним из соединений, играющих важнейшую роль в жизнедеятельности клетки, является аденозинтрифосфорная кислота (АТФ).
Аденозинтрифосфорная кислота (АТФ) состоит из органического основания аденина (I), углевода рибозы (II) и трех остатков фосфорной кислоты (III). Соединение аденина и рибозы называется аденозином. Пирофосфатные группы имеют макроэргические связи, обозначенные значком ~. Разложение одной молекулы АТФ с участием воды сопровождается отщеплением одной молекулы фосфорной кислоты и выделением свободной энергии, которая равна 33—42 кДж/моль. Все реакции с участием АТФ регулируются ферментными системами.
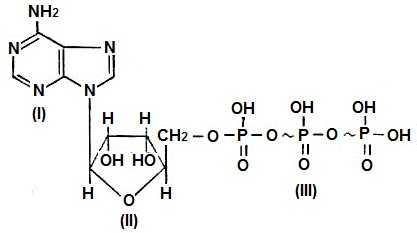
Рис.1. Аденозинтрифосфорная кислота (АТФ)
Энергетический обмен в клетке. Синтез АТФ
Синтез АТФ происходит в мембранах митохондрий в процессе дыхания, поэтому все ферменты и кофакторы дыхательной цепи, все ферменты окислительного фосфорилирования локализованы в данных органеллах.
Синтез АТФ происходит таким образом, что два иона Н+ отщепляются от АДФ и фосфата (Р) с правой стороны мембраны, компенсируя потерю двух Н+ при восстановлении вещества В. Один из кислородных атомов фосфата переносится на другую сторону мембраны и, присоединив два иона Н+ из левого отсека, образует Н2О. Остаток фосфорила присоединяется к АДФ, образуя АТФ.
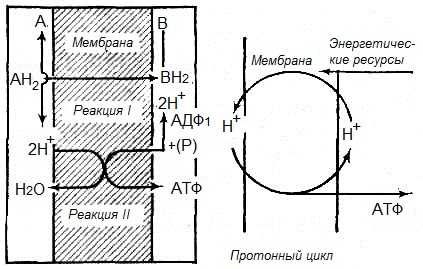
Рис.2. Схема окисления и синтеза АТФ в митохондриальных мембранах
В клетках организмов изучено много биосинтетических реакций, использующих энергию, заключенную в АТФ, в ходе которых происходят процессы карбоксилирования и декарбоксилирования, синтеза амидных связей, образования макроэргических соединений, способных переносить энергию от АТФ к анаболическим реакциям синтеза веществ. Эти реакции играют важную роль в процессах обмена веществ растительных организмов.
С участием АТФ и других макроэргических нуклеозидполифосфатов (ГТФ, ЦТФ, УГФ) может происходить активирование молекул моносахаридов, аминокислот, азотистых оснований, ацилглицеринов путем синтеза активных промежуточных соединений, являющихся производными нуклеотидов. Так, например, в процессе синтеза крахмала с участием фермента АДФ-глюкозо-пирофосфорилазы образуется активированная форма глюкозы — аденозиндифосфатглюкоза, которая легко становится донором глюкозных остатков при формировании структуры молекул этого полисахарида.
Синтез АТФ происходит в клетках всех организмов в процессе фосфорилирования, т.е. присоединения неорганического фосфата к АДФ. Энергия для фосфорилирования АДФ образуется в ходе энергетического обмена. Энергетический обмен, или диссимиляция, представляет собой совокупность реакций расщепления органических веществ, сопровождающихся выделением энергии. В зависимости от среды обитания диссимиляция может протекать в два или три этапа.
У большинства живых организмов — аэробов, живущих в кислородной среде, — в ходе диссимиляции осуществляется три этапа: подготовительный, бескислородный и кислородный, в процессе которых органические вещества распадаются до неорганических соединений. У анаэробов, обитающих в среде, лишенной кислорода, или у аэробов при его недостатке диссимиляция протекает лишь в два первых этапа с образованием промежуточных органических соединений, еще богатых энергией.
Первый этап — подготовительный — заключается в ферментативном расщеплении сложных органических соединений на более простые (белков — на аминокислоты, жиров — на глицерин и жирные кислоты, полисахаридов — на моносахариды, нуклеиновых кислот — на нуклеотиды). Распад органических субстратов пищи осуществляется на разных уровнях желудочно-кишечного тракта многоклеточных организмов. Внутриклеточное расщепление органических веществ происходит под действием гидролитических ферментов лизосом. Высвобождающаяся при этом энергия рассеивается в виде теплоты, а образующиеся малые органические молекулы могут подвергнуться дальнейшему расщеплению или использоваться клеткой как «строительный материал» для синтеза собственных органических соединений.
Второй этап — неполное окисление (бескислородный) — осуществляется непосредственно в цитоплазме клетки, в присутствии кислорода не нуждается и заключается в дальнейшем расщеплении органических субстратов. Главным источником энергии в клетке является глюкоза. Бескислородное, неполное расщепление глюкозы называют гликолизом.
Гликолиз — многоступенчатый ферментативный процесс превращения шестиуглеродной глюкозы в две трехуглеродные молекулы пировиноградной кислоты (пирувата, ПВК) С3Н4О3. В ходе реакций гликолиза выделяется большое количество энергии — 200 кДж/моль. Часть этой энергии (60%) рассеивается в виде теплоты, остальное (40%) используется на синтез АТФ.
В результате гликолиза одной молекулы глюкозы образуется по две молекулы ПВК, АТФ и воды, а также атомы водорода, которые запасаются клеткой в форме НАД • Н, т.е. в составе специфического переносчика — никотинамидадениндинуклеотида. Дальнейшая судьба продуктов гликолиза — пирувата и водорода в форме НАД • Н — может складываться по-разному. У дрожжей или в клетках растений при недостатке кислорода происходит спиртовое брожение — ПВК восстанавливается до этилового спирта:
В клетках животных, испытывающих временный недостаток кислорода, например в мышечных клетках человека при чрезмерной физической нагрузке, а также у некоторых бактерий происходит молочнокислое брожение, при котором пируват восстанавливается до молочной кислоты. При наличии в среде кислорода продукты гликолиза претерпевают дальнейшее расщепление до конечных продуктов.
Третий этап — полное окисление (дыхание) — протекает при обязательном участии кислорода. Аэробное дыхание представляет собой цепь реакций, контролируемых ферментами внутренней мембраны и матрикса митохондрии. Попав в митохондрию, ПВК взаимодействует с ферментами матрикса и образует: диоксид углерода, который выводится из клетки; атомы водорода, которые в составе переносчиков направляются к внутренней мембране; ацетилкофермент А (ацетил-КоА), который вовлекается в цикл трикарбоновых кислот (цикл Кребса). Цикл Кребса — это цепь последовательных реакций, в ходе которых из одной молекулы ацетил-КоА образуются две молекулы СО2, молекула АТФ и четыре пары атомов водорода, передаваемые на молекулы-переносчики — НАД и ФАД (флавинадениндинуклеотид). Суммарную реакцию гликолиза и цикла Кребса можно представить в следующем виде:
Итак, в результате бескислородного этапа диссимиляции и цикла Кребса молекула глюкозы расщепляется до неорганического диоксида углерода (СО2), а высвободившаяся при этом энергия частично расходуется на синтез АТФ, но в основном сберегается в нагруженных электронами переносчиках НАД Н2 и ФАД Н2. Белки-переносчики транспортируют атомы водорода к внутренней мембране митохондрий, где передают их по цепи встроенных в мембрану белков. Транспорт частиц по цепи переноса осуществляется таким образом, что протоны остаются на внешней стороне мембраны и накапливаются в межмембранном пространстве, превращая его в Н+-резервуар, а электроны передаются на внутреннюю поверхность внутренней митохондриальной мембраны, где соединяются в конечном итоге с кислородом.
В результате деятельности ферментов цепи переноса электронов внутренняя мембрана митохондрий изнутри заряжается отрицательно, а снаружи — положительно (за счет Н ), так что между ее поверхностями создается разность потенциалов. Известно, что во внутреннюю мембрану митохондрий встроены молекулы фермента АТФ-синтетазы, обладающие ионным каналом. Когда разность потенциалов на мембране достигает критического уровня (200 мВ), положительно заряженные частицы Н+ силой электрического поля начинают проталкиваться через канал АТФазы и, оказавшись на внутренней поверхности мембраны, взаимодействуют с кислородом, образуя воду.
Нормальное протекание метаболических реакций на молекулярном уровне обусловлено гармоничным сочетанием процессов катаболизма и анаболизма. При нарушении катаболических процессов прежде всего возникают энергетические трудности, нарушаются регенерация АТФ, а также поступление необходимых для биосинтетических процессов исходных субстратов анаболизма. В свою очередь, первичное или связанное с изменениями процессов катаболизма повреждение анаболических процессов ведет к нарушению воспроизведения функционально важных соединений — ферментов, гормонов и др.
Нарушение различных звеньев метаболических цепей неравнозначно по своим последствиям. Наиболее существенные, глубокие патологические изменения катаболизма происходят при повреждении системы биологического окисления при блокаде ферментов тканевого дыхания, гипоксии и др. или повреждении механизмов сопряжения тканевого дыхания и окислительного фосфорилирования (например, разобщение тканевого дыхания и окислительного фосфорилирования при тиреотоксикозе). В этих случаях клетки лишаются основного источника энергии, почти все окислительные реакции катаболизма блокируются или теряют способность аккумулировать освобождающуюся энергию в молекулах АТФ. При ингибировании реакций цикла трикарбоновых кислот выработка энергии в процессе катаболизма сокращается примерно на две трети.
biofile.ru
