Синтез углеводов происходит при фотосинтезе
Синтез углеводов происходит при фотосинтезе и сопровождается формированием не только простых моносахаридов, но и молекул сложных сахаров – крахмала, сахарозы и клетчатки. В растениях происходит разложение углеводов до простых составляющих, и их перетекание в органы, нуждающиеся в питании. Уже здесь происходит новое образование сложных углеводов, регулирующих процессы прорастания, распада или увеличения корневой системы.
Процессы перехода углеводов из одной формы в другую проходят при участии фосфорных эфиров полисахаридов или их уридиндифосфатов (УДФ-доноры), которые представляют собой определённый полисахарид, соединённый с уридином при помощи двух фосфорных остатков.
Сахароза. Синтез углевода происходит при фотосинтезе из фруктозы и глюкозы. Сначала молекула глюкозы фосфилируется в присутствии АТФ до образования глюкозы-6-фосфата и молекулы АДФ (аденозиндифосфат) – переносчика фосфатной группы. Далее, он переходит в глюкозо-1-фосфат, который соединяется с уридиндифосфорной кислотой (УДФ) и образует уридиндифосфатглюкозу (УДФ-глюкозу).
Одновременно проходит похожая реакция с участием фруктозы и образованием фруктозо-6-фосфата, соединяемого с УДФ-глюкозой в присутствии фермента сахарозофосфат-УДФ-глюкозилтрансферазы. Образуется сахарозо-6-фосфат, который под воздействием фосфатазы, контролирующей гидролиз, переходит в свободную сахарозу.
Крахмал. Синтезируемый углевод состоит из амилозы и амилопектина – двух полисахаридов. Амилоза образуется удлинением глюкозных остатков уридиндифосфатглюкозы (УДФК) с помощью акцептора в присутствии фермента крахмалглюкозилтрансферазы. Аналогичная реакция происходит при синтезе амилопектина, только в качестве носителей глюкозных остатков используют аденозиндифосфатглюкозу.
Целлюлоза. Синтез углевода происходит при фотосинтезе, и молекула состоит из остатков β-глюкозы. В качестве исходного материала используется гуанозиндифосфатглюкоза, преобразующаяся в присутствии фермента целлюлозосинтетазы в целлюлозу.
Фармконтракт-Синтез является структурным подразделением ГК «Фармконтракт», разрабатывает и реализует проекты биохимического синтеза органических соединений, ферментов и молекул при помощи высокоточных систем в условиях приближённых к натуральным. Мы самостоятельно устанавливаем приборы и комплексы, обеспечиваем сервисное обслуживание и быструю доставку оборудования.
phct-synthesis.ru
Синтез липидов, углеводов в клетке
Синтез углеводов в клетке и образование липидов обеспечивают организм человека необходимым количеством энергии для жизнедеятельности и метаболизма. В первую очередь расходуется энергия глюкозы, получаемой в процессе распада углеводов. Потом клетки задействуют энергию заранее сформированных липидов, а потом переходит к расходованию накопленных жиров.
Процесс распределения углеводов
Поступающие для обеспечения организма энергией углеводы распределяются следующим образом:
- аккумулируются в гликогене, в виде которого делаются запасы глюкозы;
- избыток откладывается в виде жиров, содержащихся в клетках- адипоцитах.
Поступающий с пищей жир под действием ферментов и желез внутренней секреции подвергается распаду до длинных и коротких жирных кислот, и спирта гицерола. Короткие жирные кислоты усваиваются без дополнительного связывания, а длинные вместе с глицеролом участвуют в синтезе липидов, отвечающих за транспортировку энергии к тканям и органам для нормального функционирования. Лишняя энергия скапливается в молекулах АТФ (аденозинтрифосфат).
Синтезирование углеводов в клетке
Основную часть глюкозы организм получает с пищей извне, но при необходимости углеводы могут синтезироваться из неуглеводных соединений. В качестве исходных компонентов используется лактат (молочная кислота) или пируват (пировиноградная кислота), глицерин и аминокислоты. Процесс синтеза углеводов в клетке требует больших затрат энергии и набора ферментов – глюкозо-фосфотаз.
Синтезируемые липиды не окисляются, если в организме совсем отсутствует глюкоза. Расход энергии, заключённый в жирных кислотах липидов, начинается при недостатке глюкозы, которая исключает накопление в клетке ацетона, возникающего из-за неполного их распада. Расход липидов начинается при физических нагрузках, после ночного сна или долгого отсутствия приёма пищи.
Инжиринговое подразделение «Фармконтракт-Синтез» занимается разработкой и реализацией проектов, обеспечивающих воспроизведение условий для наблюдения и регулирования процессов, происходящих в клетках. С помощью нашего оборудования, вы сможете отслеживать и формировать новые процессы, проводить научные исследования и контролировать действие препаратов. С нами работает более сотни производителей, давно зарекомендовавших себя на рынке биотехнологического оснащения.
Синтез липидов и углеводов в клетке
Количество просмотров публикации Синтез липидов и углеводов в клетке — 882
Липиды имеют очень большое значение в метаболизме клетки. Все липиды — ϶ᴛᴏ органические водонерастворимые соединения, присутствующие во всех живых клетках. Необходимо отметить, что по своим функциям липиды разделяются на три группы:
— структурные и рецепторные липиды клеточных мембран
— энергетическое ʼʼдепоʼʼ клеток и организмов
— витамины и гормоны ʼʼлипиднойʼʼ группы
Основу липидов составляют жирные кислоты (насыщенные и ненасыщенные) и органический спирт – глицерол. Основную массу жирных кислот мы получаем из пищи (животной и растительной). Животные жиры — ϶ᴛᴏ смесь насыщенных (40-60%) и ненасыщенных (30-50%) жирных кислот. Растительные жиры наиболее богаты (75-90%) ненасыщенными жирными кислотами и наиболее полезны для нашего организма.
Основная масса жиров используется для энергетического обмена, расщепляясь специальными ферментами – липазами и фосфолипазами. В результате получаются жирные кислоты и глицерин, которые в дальнейшем используются в реакциях гликолиза и цикла Кребса.С точки зрения образования молекул АТФ — жиры составляют основу энергетического запаса животных и человека.
Эукариотическая клетка получает жиры с пищей, хотя сама может синтезировать большинство жирных кислот (за исключением двух незаменимых– линолевой и линоленовой). Синтез начинается в цитоплазме клеток с помощью сложного комплекса ферментов и заканчивается в митохондриях или гладком эндоплазматическом ретикулуме.
Исходным продуктом для синтеза большинства липидов (жиров, стероидов, фосфолипидов) служит ʼʼуниверсальнаяʼʼ молекула – ацетил-Коэнзим А (активированная уксусная кислота), являющаяся промежуточным продуктом большинства реакций катаболизма в клетке.
Жиры есть в любой клетке, но особенно много их в специальных жировых клетках – адипоцитах, образующих жировую ткань. Контролируется жировой обмен в организме специальным гормонами гипофиза, а также инсулином и адреналином.
Углеводы (моносахариды, дисахариды, полисахариды) являются важнейшими соединениями для реакций энергетического обмена. В результате распада углеводов клетка получает большую часть энергии и промежуточные соединения для синтеза других органических соединений (белков, жиров, нуклеиновых кислот).
Основную массу сахаров клетка и организм получает извне – из пищи, но может синтезировать глюкозу и гликоген из неуглеводных соединений. Субстратами для разного вида углеводного синтеза выступают молекулы молочной кислоты (лактат) и пировиноградной кислоты (пируват), аминокислоты и глицерин. Эти реакции идут в цитоплазме при участии целого комплекса ферментов – глюкозо-фосфотаз. Для всех реакций синтеза требуется энергия – синтез 1 молекулы глюкозы требует 6 молекул АТФ!
Основной объём собственного синтеза глюкозы протекает в клетках печени и почек, но не идет в сердце, мозге и мышцах (там нет необходимых ферментов). По этой причине нарушения углеводного обмена в первую очередь сказываются на работе этих органов. Углеводный обмен контролируется группой гормонов: гормонами гипофиза, глюкокортикостероидными гормонами надпочечников, инсулином и глюкагоном поджелудочной железы. Нарушения гормонального баланса углеводного обмена приводит к развитию диабета.
Мы кратко рассмотрели основные части пластического обмена. Можно сделать ряд общих выводов:
referatwork.ru
Где происходит синтез углеводов — Про холестерин
Холестерин в крови от 3 до 3.9 ммоль/л: что это значит
Точной цифры нормы для холестерина нет. Она своя у каждого человека. Но существуют возрастные пределы этого показателя крови.
Сейчас мы разберёмся в некоторых вопросах, касающихся холестерина. Что он собой представляет. В каких продуктах содержится. Какие его нижние нормы у мужчин и женщин в разном возрасте. Какие последствия холестерола 3,0–3,3 ммоль/л у людей после 40–50 лет. Что нужно предпринять в таком случае.
- Какие продукты содержат высокий холестерин
- Норма нижней границы общего холестерина
- Интерпретация уровня холестерина
- Возможные последствия этого уровня холестерина после 40 лет
- Лечение
Какие продукты содержат высокий холестерин
Жироподобное вещество холестерин циркулирует в крови в виде двух соединений – липопротеидов высокой (ЛПВП) и низкой плотности (ЛПНП). Организм человека нуждается в обеих фракциях. Без хорошего холестерина невозможен обмен жиров, белков и углеводов. Плохие ЛПНП синтезируют женские и мужские половые гормоны. Они же формируют плаценту – тот орган, с которого начинается жизнь. Без них не обходится синтез витамина D и всех остальных. Из них же состоит оболочка всех клеток нашего тела. При нарушении соотношения обеих фракций развиваются заболевания.
Холестерин вырабатывается печенью, но 20% поступает с мясными и молочными продуктами. Больше всего его содержится в таких продуктах:
- трансжиры – маргарин, кулинарный жир;
- сметана, сливочное масло, сливки;
- печень, почки, мозги;
- жирная говядина, баранина, свинина;
- яичный желток;
- фастфуд;
- креветки.
- переработанное мясо – окорок, ветчина, колбаса, сосиски, консервы мясные и рыбные.
Здоровый человек может и должен употреблять все эти продукты, но в количестве 300–400 мг холестерина в сутки.
Эти продукты ограничивают при повышенном холестерине и ожирении. Не рекомендуется их употребление при снижении возрастной нормы холестерола крови.
Норма нижней границы общего холестерина
- 20–25 лет не меньше 3,16/3,16;
- 25–30 лет 3,44/3,32;
- 30–40 лет 3, 57/3,63;
- 40– 50 лет не ниже 4,09/3,94;
- 50–60 лет не меньше 4,09/4,46;
- 60–70 лет – 4,12/4,43;
- 70 лет и старше – не меньше 3,73/4,43.
Уровень холестерола очень важно поддерживать в норме. Для того чтобы вовремя диагностировать заболевание, анализ крови на общий холестерол нужно начинать сдавать с 20 лет.
Интерпретация уровня холестерина
Оптимальное содержание холестерина 3.3–5,2 ммоль/литр. Не существует точной цифры нормы. Уровень общего холестерола для каждого человека отличается в зависимости от пола и возраста. Для женщин от 20 до 35 лет холестерол 3,0–3,3 ммоль/л является нормой. Для мужчин этот диапазон считается нормальным до 30 лет.
Для женщин в период вынашивания плода холестерол на уровне 3,0–3,3 ммоль/л интерпретируется как сниженный, потому, что физиологически во время беременности холестерин повышается. Он необходим для формирования плаценты и развития мозга плода. Недостаток этого вещества у женщины негативно отражается на течении беременности и развитии ребёнка.
Для мужчин после 30-летнего возраста холестерол в пределах 3,0–3,3 ммоль/л может отразиться на репродуктивной функции. Сперматозоиды снижают двигательную активность, что негативно отражается на мужском зачатии.
Для женщин после 40 лет, а мужчин после 35-летнего возраста уровень холестерола 3,0–3,3 ммоль/л настораживает. Причинами могут быть такие факторы:
- заболевания печени;
- табакокурение;
- алкоголизм;
- голодание;
- неразумное вегетарианство;
- недостаточное поступление жиров с пищей при изнуряющих диетах для похудения;
- психические расстройства – суицидальное поведение, агрессивное состояние;
- старческий маразм.
В некоторых случаях причиной может быть генетическая предрасположенность, а также стрессовые ситуации.
Возможные последствия этого уровня холестерина после 40 лет
Если у лиц после 40–50 лет холестерин 3 ммоль/л или меньше, то это означает сбои в работе организме. При содержании холестерола от 3,0 до 3,33 ммоль/л у людей после 40–50 лет могут развиваться следующие симптомы:
- Снижение пористости костей происходит, потому что без холестерина невозможен синтез витамина D, который обусловливает всасывание кальция и поступление его в кости.
- Ухудшение эластичности сосудов, которое напрямую связано с уровнем ЛПВП. Это приводит к нарушению мозгового кровообращения различной степени тяжести.
- Снижение сексуальной активности и либидо, потому что выработку половых гормонов обеспечивают ЛПНП.
- Вследствие понижения устойчивости организма к инсулину может спровоцировать развитие сахарного диабета.
- Без холестерина плохо усваиваются жирорастворимые витамины A и E, что обусловливает ухудшение зрения, выпадение волос, сухость кожи.
- Может вызвать неадекватное поведение – депрессию или агрессивное состояние, а в пожилом возрасте повышает вероятность развития болезни Альцгеймера.
- Развитие синдрома кишечной мальабсорбции. Продукты распада в кишечнике плохо выводятся из организма. Всасываемость же полезных веществ ограничивается.
После 40–50 лет нельзя допускать уровень холестерина до 3–3,33 ммоль/л. Если не предпринять лечение, холестерин понизится до опасного уровня.
Лечение
При уровне общего холестерола 3–3,33 ммоль/л после 40–50 лет пациенты попадают к различным специалистам в зависимости от появившейся проблемы. Это может быть эндокринолог, невролог, гинеколог и сексолог. Врач назначает лечебное питание в зависимости от возрастной нормы. В меню включают продукты, содержащие насыщенные и полиненасыщенные жиры, клетчатку, белки.
Диета состоит из следующих продуктов питания:
- Печень, мозги, почки, печень.
- Мясо говяжье, куриное.
- Молочные продукты 9% жирности, голландский сыр, сливки, сметана.
- Жирная рыба лососёвых пород, икра.
- Оливковое, рапсовое масло.
- Грецкие орехи, семечки.
- Яйца в любом виде.
Такую диету нужно обязательно разнообразить клетчаткой. Она содержится в овощах, фруктах, бобовых. Антиоксидант витамин C, содержащийся в цитрусах, уменьшает воздействие липопротеинов высокой плотности. Несмотря на разнообразие диеты, в ней всё-таки имеются ограничения в употреблении легкоусвояемых углеводов – сахара, сдобы и макарон. Лечебное питание необходимо поддерживать до коррекции соотношения ЛПНП и ЛПВП.
В заключение подчеркнём. Холестерол в пределах 3,0–3,33 ммоль/л является нормой для женщин до 35, а мужчин – до 30 лет. Однако для лиц обоего пола после 40–50 лет это сопряжено с тенденцией снижения и может привести к опасным последствиям. Поэтому в зависимости от возрастных норм врачи применяют лечебное питание до коррекции ЛПНП и ЛПВП. Для этого в меню включают жиры животного происхождения и клетчатку.
Узнаем, почему повышенны триглицериды и что делать
Сдав кровь на биохимию и получив результаты, человек обнаруживает, что в крови повышены триглицериды. Что это значит? Скорее всего, у пациента есть проблемы с сердечно-сосудистой системой, высокий риск инфаркта. Повышенный уровень свидетельствует о начале атеросклероза. Триглицериды — это нейтральные жиры, поступающие в организм с пищей. Они служат источником энергии, излишек которой, откладывается в жировых клетках.
Что это такое?
С химической точки зрения триглицериды — комплекс трехатомного спирта, который соединен с молекулами жирных кислот. ТГ попадают в организм с пищей и расщепляются с помощью кислоты, содержащейся в желудочном соке. Затем расщепленные ТГ всасываются в тонком кишечнике, где происходит их обратный синтез. Там они соединяются с белками, образуя липопротеиды, после попадают в кровь. С помощью крови липопротеиды доставляются во все органы и ткани.
Таким образом, триглицериды — это основная составляющая мембраны клетки.
Посмотрите видео про триглицериды
Нормы
Спроси гематолога!
Не стесняйтесь, задавайте свои вопросы штатному гематологу прямо на сайте в комметариях. Мы обязательно ответим.Задать вопрос>>
Уровень триглицеридов в биохимическом анализе крови является важным показателем здоровья. Что значит, если они повышены? Повышенный уровень не говорит напрямую о болезнях, а указывает на высокую вероятность инфаркта, инсульта, ишемии и других заболеваний сердечно-сосудистой системы. Анализ уровня ТГ проводят совместно с анализом жирового спектра. То есть оценивают уровень ТГ, плохого и хорошего холестерина.
Для того, чтобы понять, что значит «триглицериды повышены», нужно знать их допустимую норму. Норма зависит от пола, возраста пациента, общего состояния здоровья. У людей более старшего возраста наблюдается более повышенный уровень триглицеридов в крови, чем у молодых, и это не считается отклонением.

Измеряют ТГ в миллимолях на литр.
У мужчин триглицериды считаются повышенными , если показатели больше следующих значений:
- 10-20 лет — 0,35- 1,8;
- 20-30 лет — 0,45-2,75;
- 30-50 лет — 0,6-3,6;
- 50-60 лет — 0,55-3,2;
- 60-70 лет — 0,5- 2,9.
Триглицериды повышены у женщин, если они превышают следующие показатели:
- 10-20 лет — 0,4-1,5;
- 20-30 лет — 0,5 -1,64;
- 30-50 лет — 0,4-2,44;
- 50-60 лет — 0,6-2,95;
- 60-70 лет — 0,6-2,7.
Норма для детей до 10 лет — 0,33-1,12 и 0,4-1,23 у мальчиков и девочек соответственно.
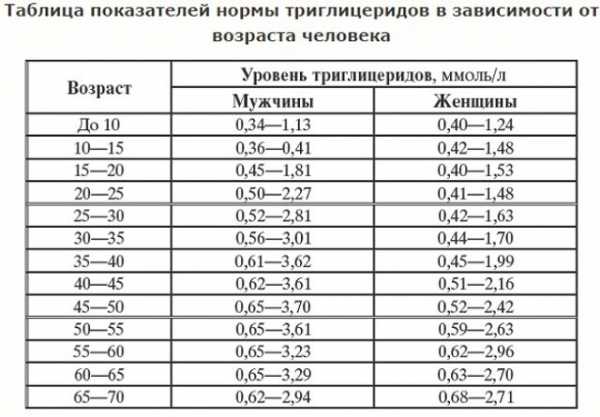
У беременных допускается незначительное отклонение от нормы в большую сторону. На это влияет изменение гормонального фона или переедание. Обычно при отсутствии серьезных сопутствующих патологий все нормализуется после родов.
Как проводят анализ
Анализ на уровень ТГ нужно проводить с профилактической целью раз в 3-4 года после 10 лет. В старшем возрасте такой анализ рекомендуют проходить ежегодно. Помимо этого, врач назначает исследование на триглицериды при различных заболеваниях сердца и сосудов, чтобы назначить корректную терапию. Обязательным регулярное исследование является для больных сахарным диабетом.
Материалом для исследования является кровь из вены. Ее берут утром натощак. Последний прием пищи должен быть за 12 часов до анализа.
Также накануне следует отказаться от физических нагрузок и употребления табака за час до забора крови.
Особенности повышения у детей
У детей триглицериды в крови бывают повышены в следующих случаях:
- Избыточный вес.
- Употребление продуктов с повышенной жирностью (чипсы, гамбургеры).
- Плохое питание с маленьким количеством клетчатки.
- Врожденные аномалии развития (синдром Дауна).
- Эндокринные заболевания (гипотиреоз).
В некоторых случаях снизить уровень триглицеридов у ребенка удается с помощью корректирвки питания.
Если причиной стали врожденные аномалии, то бороться с ними очень сложно.
Причины высоких показателей
В медицине обозначают несколько причин, по которым триглицериды могут быть повышены:
- Неправильное питание. Здесь имеет значение общее число калорий и несбалансированность по белкам, жирам и углеводам.
- Избыточный вес.
- Наследственный фактор нарушения обмена веществ.
- Маленькая физическая активность.
- Прием лекарственных средств: диуретиков, стероидных гормонов.
- Длительное употребление противозачаточных таблеток.
Также повысить уровень триглицеридов может прием больших доз алкоголя.

Малые порции красного вина, наоборот, способствуют нормализации количества ТГ.
Симптомы и опасность
Постоянно повышенный уровень ТГ в крови может спровоцировать развитие серьезных патологий: инфаркт, инсульт, панкреатит, диабет. Это далеко не полный перечень недугов. Также высокий уровень свидетельствует об уже имеющихся заболеваниях. Это такие болезни, как:
- Атеросклероз.
- Ишемия.
- Гипертония.
- Диабет.
- Подагра.
- Панкреатит.
- Гепатит.
- Цирроз печени.
- Заболевания почек.
- Гипотиреоз.
Заподозрить у себя повышение ТГ пациент может по следующим симптомам:
- Повышенное давление.
- Боли в сердце.
- Головные боли.
- Одышка.
- Повышение веса.
- Боли в области печени или поджелудочной.
При возникновении подобных симптомов следует обратиться к врачу и пройти обследование.
Как нормализовать уровень?
Существует несколько способов понизить триглицериды. Выбор зависит от степени повышения и наличия сопутствующего заболевания.
Как понизить с помощью диеты?
Первый шаг — это отказ от алкоголя. Особенно вредными в этом отношении являются пиво и крепкие напитки.
Разрешено употребление небольших порций красного сухого вина (до 100 мл в день).
Далее следует рассчитать допустимый дневной калораж с учетом возраста, веса и двигательной активности.
Рацион питания должен быть сбалансирован по жирам, белкам и углеводам.
Можно употреблять не более 0,9 г жиров на килограмм веса.
Категорически под запретом находятся следующие продукты:
- жирное мясо;
- колбасные изделия;
- сахар;
- сладости из рафинированного сахара;
- выпечка;
- консервы;
- маргарин;
- сало;
- бобовые.
Также следует ограничить употребление белого хлеба, картофеля, макарон, соусов.
Продукты, снижающие триглицериды:
- Каши на воде.
- Цельнозерновой хлеб.
- Свежая зелень.
- Овощи.
- Фрукты.
- Нежирное мясо.
- Рыба.
- Нежирные кисломолочные продукты.
- Растительные масла: оливковое, льняное, подсолнечное.
- Орехи.
Примерное меню для снижения ТГ
Вариант 1
- Завтрак: каша овсяная, фруктовый сок.
- Ланч: яблоко.
- Обед: куриный суп, рыба овощи гриль.
- Полдник: творожный пудинг.
- Ужин: куриная грудка, овощное рагу.
Вариант 2
- Завтрак: омлет, зеленый чай.
- Ланч: фруктовый салат.
- Обед: гречневые котлеты, салат из свежих овощей, заправленный оливковым маслом.
- Полдник: ягоды.
- Ужин: вегетарианские голубцы, немного риса.
Вариант 3
- Завтрак: творог обезжиренный с ягодами, кофе без сахара.
- Ланч: орехи, чай.
- Обед: рыбная котлета, зеленый салат.
- Полдник: фрукт.
- Ужин: тыквенное рагу, куриная грудка на пару.
В течение дня следует соблюдать питьевой режим, выпивать не менее 1,5л чистой воды.
Как снизить с помощью лекарств?
Корректировать уровень ТГ лекарственными средствами следует, учитывая наличие основного заболевания. При диабете, гипотиреозе нужно принимать лекарственные средства, назначенные лечащим врачом.
Для нормализации триглицеридов применяют следующие препараты:
Фибраты
Это лекарства с органическим составом, они притягивают молекулы ТГ, стимулируют выработку печенью компонента, который перерабатывает триглицериды.
Статины
Статины — препараты, снижающие уровень «плохого» холестерина — главного виновника повышенных ТГ.
Омега-3 жирные кислоты
Во время приема препаратов необходимо регулярно проводить анализ крови на триглицериды, чтобы отслеживать динамику и по необходимости корректировать дозировку.
Народные средства
Если у больного есть противопоказания к приему лекарств, то на помощь придут средства народной медицины. Их применение следует обсудить с лечащим врачом.
- Облепиховое масло. Способствует уменьшению концентрации ТГ. Принимают по чайной ложке 2 раза в день за 30 минут до еды.
- Свекольный сок. Снижает «плохой» холестерин. Принимают по 200гр в день в течение 15 дней.
- Лимонный сок. Разводят в воде и пьют в течение дня. Также используют для заправки салатов.
- Две столовых ложки овсяных хлопьев размешать в стакане воды и настаивать несколько часов. Выпивать натощак. Такое напиток способствует абсорбации жиров и снижению ТГ.
- Полезно каждый день съедать по зубчику чеснока.
Физическая активность
Одна из причин повышения триглицеридов — гиподинамия. Поэтому умеренные физические упражнения способствуют улучшению метаболизма, ускорению липидного обмена.
Для этих целей подойдут: легкий бег, ходьба, игровые виды спорта, занятия на велотренажере и беговой дорожке, танцы.
Профилактика
Любой недуг всегда легче предупредить. Для того, чтобы показатели ТГ в крови оставались в норме, следует соблюдать меры профилактики:
- Здоровый образ жизни.
- Физическая активность.
- Правильное питание.
- Регулярные профилактические осмотры и сдача анализов крови.
Эти нехитрые рекомендации позволят сохранить здоровье и предотвратить заболевания сердца и сосудов.
Липопротеины (липопротеиды) высокой и низкой плотности в крови: что это, норма, повышение
Липопротеины — сложные белково-липидные комплексы, входящие в состав всех живых организмов и являющиеся необходимой составной частью клеточных структур. Липопротеины выполняют транспортную функцию. Их содержание в крови — важный диагностический тест, сигнализирующий о степени развития заболеваний систем организма.
Это класс сложных молекул, в состав которых могут одновременно входить свободные триглицериды, жирные кислоты, нейтральные жиры, фосфолипиды и холестерин в различных количественных соотношениях.
Липопротеины доставляют липиды в различные ткани и органы. Они состоят из неполярных жиров, расположенных в центральной части молекулы — ядре, которое окружено оболочкой, образованной из полярных липидов и апобелков. Подобным строением липопротеинов объясняются их амфифильные свойства: одновременная гидрофильность и гидрофобность вещества.
Функции и значение
Липиды играют важную роль в организме человека. Они содержатся во всех клетках и тканях и участвуют во многих обменных процессах.
- Липопротеины — основная транспортная форма липидов в организме. Поскольку липиды являются нерастворимыми соединениями, они не могут самостоятельно выполнять свое предназначение. Липиды связываются в крови с белками — апопротеинами, становятся растворимыми и образуют новое вещество, получившее название липопротеид или липопротеин. Эти два названия являются равноценными, сокращенно — ЛП.
Липопротеины занимают ключевое положение в транспорте и метаболизме липидов. Хиломикроны транспортируют жиры, поступающие в организм вместе с пищей, ЛПОНП доставляют к месту утилизации эндогенные триглицериды, с помощью ЛПНП в клетки поступает холестерин, ЛПВП обладают антиатерогенными свойствами.
- Липопротеины повышают проницаемость клеточных мембран.
- ЛП, белковая часть которых представлена глобулинами, стимулируют иммунитет, активизируют свертывающую систему крови и доставляют железо к тканям.
Классификация
ЛП плазмы крови классифицируют по плотности (с помощью метода ультрацентрифугирования). Чем больше в молекуле ЛП содержится липидов, тем ниже их плотность. Выделяют ЛПОНП, ЛПНП, ЛПВП, хиломикроны. Это самая точная из всех существующих классификаций ЛП, которая была разработана и доказана с помощью точного и довольно кропотливого метода — ультрацентрифугирования.

По размерам ЛП также неоднородны. Самыми крупными являются молекулы хиломикронов, а затем по уменьшению размера — ЛПОНП, ЛПСП, ЛПНП, ЛПВП.
Электрофоретическая классификация ЛП пользуется большой популярностью у клиницистов. С помощью электрофореза были выделены следующие классы ЛП: хиломикроны, пре-бета-липопротеины, бета-липопротеины, альфа-липопротеины. Данный метод основан на введении в жидкую среду активного вещества с помощью гальванического тока.
Фракционирование ЛП проводят с целью определения их концентрации в плазме крови. ЛПОНП и ЛПНП осаждают гепарином, а ЛПВП остаются в надосадочной жидкости.
Виды
В настоящее время выделяют следующие виды липопротеинов:
ЛПВП (липопротеины высокой плотности)
ЛПВП обеспечивают транспорт холестерина от тканей организма к печени.
ЛПВП содержат фосфолипиды, которые поддерживают холестерин во взвешенном состоянии и предупреждают его выход из кровяного русла. ЛПВП синтезируются в печени и обеспечивают обратный транспорт холестерина из окружающих тканей к печени на утилизацию.
- Увеличение ЛПВП в крови отмечают при ожирении, жировом гепатозе и билиарном циррозе печени, алкогольной интоксикации.
- Снижение ЛПВП происходит при наследственной болезни Танжера, обусловленной скоплением холестерина в тканях. В большинстве прочих случаев снижение концентрации ЛПВП в крови — признак атеросклеротического повреждения сосудов.
Норма ЛПВП отличается у мужчин и женщин. У лиц мужского пола значение ЛП данного класса колеблется в пределах от 0,78 до 1,81 ммоль/л, норма у женщин ЛПВП — от 0,78 до 2,20, в зависимости от возраста.
ЛПНП (липопротеины низкой плотности)
ЛПНП являются переносчиками эндогенного холестерина, триглицеридов и фосфолипидов от печени к тканям.
Данный класс ЛП содержит до 45% холестерина и является его транспортной формой в крови. ЛПНП образуются в крови в результате действия на ЛПОНП фермента липопротеинлипазы. При его избытке на стенках сосудов появляются атеросклеротические бляшки.
В норме количество ЛПНП составляет 1,3-3,5 ммоль/л.
- Уровень ЛПНП в крови повышается при гиперлипидемии, гипофункции щитовидной железы, нефротическом синдроме.
- Пониженный уровень ЛПНП наблюдается при воспалении поджелудочной железы, печеночно-почечной патологии, острых инфекционных процессах, беременности.
ЛПОНП (липопротеины очень низкой плотности)
ЛПОНП образуются в печени. Они переносят эндогенные липиды, синтезируемый в печени из углеводов, в ткани.
Это самые крупные ЛП, уступающие по размерам лишь хиломикронам. Они более, чем на половину состоят из триглицеридов и содержат небольшое количество холестерина. При избытке ЛПОНП кровь становится мутной и приобретает молочный оттенок.
ЛПОНП — источник «плохого» холестерина, из которого на эндотелии сосудов образуются бляшки. Постепенно бляшки увеличиваются, присоединяется тромбоз с риском острой ишемии. ЛПОНП повышены у больных с сахарным диабетом и болезнями почек.
Хиломикроны
Хиломикроны отсутствуют в крови у здорового человека и появляются только при нарушении обмена липидов. Хиломикроны синтезируются в эпителиальных клетках слизистой оболочки тонкого кишечника. Они доставляют экзогенный жир из кишечника в периферические ткани и печень. Большую часть транспортируемых жиров составляют триглицериды, а также фосфолипиды и холестерин. В печени под воздействием ферментов триглицериды распадаются, и образуются жирные кислоты, часть которых транспортируется в мышцы и жировую ткань, а другая часть связывается с альбуминами крови.
ЛПНП и ЛПОНП являются высокоатерогенными — содержащими много холестерина. Они проникают в стенку артерий и накапливаются в ней. При нарушении метаболизма уровень ЛПНП и холестерина резко повышается.
Наиболее безопасными в отношении атеросклероза являются ЛПВП. Липопротеины этого класса выводят холестерин из клеток и способствуют его поступлению в печень. Оттуда он вместе с желчью попадает в кишечник и покидает организм.
Представители всех остальных классов ЛП доставляют холестерин в клетки. Холестерин — это липопротеид, входящий в состав клеточной стенки. Он участвует в образовании половых гормонов, процессе желчеобразования, синтезе витамина Д, необходимого для усвоения кальция. Эндогенный холестерин синтезируется в печеночной ткани, клетках надпочечников, стенках кишечника и даже в коже. Экзогенный холестерин поступает в организм вместе с продуктами животного происхождения.
Дислипопротеинемия — диагноз при нарушении обмена липопротеинов
Дислипопротеинемия развивается при нарушении в организме человека двух процессов: образования ЛП и скорости их выведения из крови. Нарушение соотношения ЛП в крови — не патология, а фактор развития хронического заболевания, при котором уплотняются артериальные стенки, суживается их просвет и нарушается кровоснабжение внутренних органов.
При повышении уровня холестерина в крови и снижении уровня ЛПВП развивается атеросклероз, приводящий к развитию смертельно опасных заболеваний.
Этиология
Первичная дислипопротеинемия является генетически детерминированной.

Причинами вторичной дислипопротеинемии являются:
- Гиподинамия,
- Сахарный диабет,
- Алкоголизм,
- Дисфункция почек,
- Гипотиреоз,
- Печеночно-почечная недостаточность,
- Длительный прием некоторых лекарств.
Понятие дислипопротеинемия включает 3 процесса — гиперлипопротеинемию, гиполипопротеинемию, алипопротеинемию. Дислипопротеинемия встречается довольно часто: у каждого второго жителя планеты отмечаются подобные изменения в крови.
Гиперлипопротеинемия — повышенное содержание ЛП в крови, обусловленное экзогенными и эндогенными причинами. Вторичная форма гиперлипопротеинемии развивается на фоне основной патологии. При аутоиммунных заболеваниях ЛП воспринимаются организмом как антигены, к которым вырабатываются антитела. В результате образуются комплексы антиген — антитело, обладающие большей атерогенностью, чем сами ЛП.
- Гиперлипопротеинемия 1 типа характеризуется образованием ксантом — плотных узелков, содержащих холестерин и расположенных над поверхностью сухожилий, развитием гепатоспленомегалии, панкреатита. Больные жалуются на ухудшение общего состояния, подъем температуры, потерю аппетита, приступообразную боль в животе, усиливающуюся после приема жирной пищи.
- При 2 типе образуются ксантомы в области сухожилий стоп и ксантелазмы в периорбитальной зоне.
- 3 тип — симптомы нарушения сердечной деятельности, появление пигментации на коже ладони, мягких воспаленных язвочек над локтями и коленями, а также признаков поражения сосудов ног.
- При 4 типе увеличивается печень, развивается ИБС и ожирение.
Алипопротеинемия — генетически обусловленное заболевание с аутосомно-доминантным типом наследования. Заболевание проявляется увеличением миндалин с оранжевым налетом, гепатоспленомегалией, лимфаденитом, мышечной слабостью, снижением рефлексов, гипочувствительностью.
Гиполипопротеинемия — низкое содержание в крови ЛП, часто протекающее бессимптомно. Причинами заболевания являются:
- Наследственность,
- Неправильное питание,
- Сидячий образ жизни,
- Алкоголизм,
- Патология пищеварительной системы,
- Эндокринопатия.
Дислипопротеинемии бывают: органными или регуляторными, токсигенными, базальными — исследование уровня ЛП натощак, индуцированными — исследование уровня ЛП после приема пищи, препаратов или физической нагрузки.
Диагностика
Известно, что для организма человека избыток холестерина очень вреден. Но и недостаток этого вещества может привести к дисфункции органов и систем. Проблема кроется в наследственной предрасположенности, а также в образе жизни и особенностях питания.

Диагностика дислипопротеинемии основывается на данных анамнеза болезни, жалобах больных, клинических признаках — наличии ксантом, ксантелазм, липоидной дуги роговицы.
Основным диагностическим методом дислипопротеинемии является анализ крови на липиды. Определяют коэффициент атерогенности и основные показатели липидограммы — триглицериды,общий холестерин, ЛПВП, ЛПНП.
Липидограмма – метод лабораторной диагностики, который выявляет нарушения липидного обмена, приводящие к развитию заболеваний сердца и сосудов. Липидограмма позволяет врачу оценить состояние пациента, определить риск развития атеросклероза коронарных, мозговых, почечных и печеночных сосудов, а также заболеваний внутренних органов. Кровь сдают в лаборатории строго натощак, спустя минимум 12 часов после последнего приема пищи. За сутки до анализа исключают прием алкоголя, а за час до исследования — курение. Накануне анализа желательно избегать стресса и эмоционального перенапряжения.
Ферментативный метод исследования венозной крови является основным для определения липидов. Прибор фиксирует предварительно окрашенные специальными реагентами пробы. Данный диагностический метод позволяет провести массовые обследования и получить точные результаты.
Сдавать анализы на определение липидного спектра с профилактической целью, начиная с юности необходимо 1 раз в 5 лет. Лицам, достигшим 40 лет, делать это следует ежегодно. Проводят исследование крови практически в каждой районной поликлинике. Больным, страдающим гипертонией, ожирением, заболеваниями сердца, печени и почек, назначают биохимический анализ крови и липидограмму. Отягощенная наследственность, имеющиеся факторы риска, контроль эффективности лечения — показания для назначения липидограммы.
Результаты исследования могут быть недостоверны после употребления накануне пищи, курения, перенесенного стресса, острой инфекции, при беременности, приеме некоторых лекарственных препаратов.
Диагностикой и лечение патологии занимается эндокринолог, кардиолог, терапевт, врач общей практики, семейный врач.
Лечение
Диетотерапия играет огромную роль в лечении дислипопротеинемии. Больным рекомендуют ограничить потребление животных жиров или заменить их синтетическими, принимать пищу до 5 раз в сутки небольшими порциями. Рацион необходимо обогащать витаминами и пищевыми волокнами. Следует отказаться от жирной и жареной пищи, мясо заменить морской рыбой, есть много овощей и фруктов. Общеукрепляющая терапия и достаточная физическая нагрузка улучшают общее состояние больных.
Гиполипидемическая терапия и антигиперлипопротеинемические препараты предназначены для коррекции дислипопротеинемии. Они направлены на снижение уровня холестерина и ЛПНП в крови, а также на повышение уровня ЛПВП.
Из препаратов для лечения гиперлипопротеинемии больным назначают:
- Статины – «Ловастатин», «Флувастатин», «Мевакор», «Зокор», «Липитор». Эта группа препаратов уменьшает выработку холестерина печенью, снижает количество внутриклеточного холестерина, разрушает липиды и оказывает противовоспалительное действие.
- Секвестранты снижают синтез холестерина и выводят его из организма — «Холестирамин», «Колестипол», «Холестипол», «Холестан».
- Фибраты снижаю уровень триглицеридов и повышают уровень ЛПВП — «Фенофибрат», «Ципрофибрат».
- Витамины группы В.
Гиперлипопротеинемия требует лечения гиполипидемическими препаратами «Холестерамином», «Никотиновой кислотой», «Мисклероном», «Клофибратом».
Лечение вторичной формы дислипопротеинемии заключается в устранении основного заболевания. Больным сахарным диабетом рекомендуют изменить образ жизни, регулярно принимать сахаропонижающие препараты, а также статины и фибраты. В тяжелых случаях требуется проведение инсулинотерапии. При гипотиреозе необходимо нормализовать функцию щитовидной железы. Для этого больным проводят гормональную заместительную терапию.
Больным, страдающим дислипопротеинемией, рекомендуют после проведения основного лечения:
- Нормализовать массу тела,
- Дозировать физические нагрузки,
- Ограничить или исключить употребление алкоголя,
- По возможности избегать стрессов и конфликтных ситуаций,
- Отказаться от курения.
Видео: липопротеины и холестерин — мифы и реальность
Видео: липопротеины в анализах крови — программа «Жить здорово!»
Шаг 2: после оплаты задайте свой вопрос в форму ниже ↓ Шаг 3: Вы можете дополнительно отблагодарить специалиста еще одним платежом на произвольную сумму ↑
krov.holesterin-lechenie.ru
7.3. Биосинтез углеводов
196 | 7. Обмен углеводов |
Впроцессе метаболизма углеводов происходит не только их катаболизм, но и взаимопревращение углеводов, биосинтез углеводов из неуглеводных предшественников и синтез полисахаридов из моносахаридов.
Общим центральным путем биосинтеза углеводов из неуглеводных предшественников является синтез глюкозы из пировиноградной кислоты, реализующийся путём обращения большинства реакций гликолиза . При этом для трех практически необратимых реакций(гексокиназной реакции, фосфофруктокиназной реакции и пируваткиназной реакции) существуют обходные ферментативные пути, обеспечивающие обратное превращение. В частности, внутри митохондрий пировиноградная кислота не может превратиться фосвфоенолпировиноградную кислоту путём обращения пируваткиназной реакции,
ипоэтому в начале под влиянием митохондриальной пируваткарбоксилазы пировиноградная кислота карбоксилируется в щавелево-уксуснуюкислоту. Реакция идёт при участии АТФ и положительного модулятора( ктиватора) фермента пируваткарбоксилазы –ацетил-КоА.Пируваткарбоксилаза является регуляторным ферментом. Реакция протекает в митохондриях.
Ch4 |
| COOH |
| ||
|
| пируваткарбоксилаза |
|
| |
| CO + CO + H O + АТФ |
|
| Ch3 | + АДФ +Ф |
|
|
| |||
| 2 | ацетил-КоА |
|
| |
| COOH |
|
| CO |
|
пировиноградная
кислота | COOH | |
щавелевоуксусная | ||
| ||
| кислота (оксалоацетат) |
Оксалоацетат восстанавливается затем в митохондриях в малат:
| COOH |
| митохондриальная |
|
| COOH |
|
|
|
|
|
| |||
| CH |
| малатдегидрогеназа |
| Ch3 | +НАД | |
| 2 | + НАД.Н 2 |
|
|
| CHOH | |
CO |
|
|
| ||||
| COOH |
|
|
|
| COOH |
|
|
|
|
|
| |||
оксалоацетат |
|
| малат |
| |||
(яблочная кислота)
Малат переходит из митохондрий в цитоплазму (с помощью пермиаз), где окисляется цитоплазматической малатдегидрогеназой до оксалоацетата:
| COOH |
| цитоплазматическая | COOH |
| |
|
|
|
|
|
| |
| Ch3 |
| малатдегидрогеназа |
| CH |
|
| CHOH | +НАД |
|
| 2 | + НАД.Н 2 |
|
| CO | ||||
| COOH |
|
|
| COOH |
|
|
|
|
|
| ||
малат |
|
| оксалоацетат | |||
7. Обмен углеводов | 197 |
Под действием фосфоенолпируваткарбоксикиназы (фосфопируваткарбоксилазы) далее происходит превращение оксалоацетата в фосфоенолпируват. При этом донором фосфата служит гуанозинтрифосфат(ГТФ) или инозинтрифосфат (ИТФ):
COOH |
| фосфоенолпируват- |
| Ch3 |
|
|
| ||||
| карбоксикиназа |
|
| OH | |||||||
|
|
|
|
| |||||||
Ch3 |
| Mg++ |
|
|
|
|
|
|
|
| |
+ ГТФ | C |
| O | P |
| O + CO 2 + ГДФ | |||||
|
| ||||||||||
|
|
|
|
| |||||||
|
|
|
|
|
|
| |||||
| CO |
| |||||||||
|
|
| COOH |
| OH | ||||||
|
|
|
| фосфоенолпируват | |||||||
COOH |
|
| |||||||||
оксалоацетат
Далее фосфоенолпируват в силу обратимости реакций гликолиза легко превращается в фруктозо-1,6-дифосфат.Обратное превращениефруктозо-1,6-дифосфата вфруктозо-6-фосфати далееглюкозо-6-фосфатав глюкозу обеспечивается соответствующими специфическими фосфатазами – дифосфофруктозофосфатазой иглюкозо-6-фосфатазой.Первая из них является регуляторным ферментом. Субстратами для синтеза глюкозы могут служить не только пируват, но и все вещества неуглеводной природы, способные превращаться в пируват или в один из метаболитов гликолиза или оксалоацетат. К таким веществам относится глицерин, который черезα-глицерофосфати фосфодиоксиацетон способен превращаться в фосфоглицериновый альдегид, т.е. в метаболит гликолиза, а также лактат. К этим веществам относятся и промежуточные продукты лимоннокислого цикла постольку, поскольку они могут превращаться в оксалоацетат. Однако главным источником новообразования глюкозы являются аминокислоты, превращающиеся в пируват и в оксалоацетат. Синтез глюкозы из неуглеводных источников получил название глюконеогенеза.
Ни ацетил-КоА,ни СО2 не могут превращаться в глюкозу в тканях животных. Кроме того, в животных тканяхацетил-КоАне может непосредственно превращаться ни в пируват, ни в сукцинат. У высших животных отсутствует метаболический путь превращения атомов углерода жирных кислот в углеводы. В отличии от этого, растения и многие микроорганизмы могут синтези-
ровать углеводы из жирных кислот через ацетил-КоАпри помощи реакций глиоксилатного цикла.
В процессе метаболизма углеводов происходит перестройка одного моносахарида в другой. Причем, многие биологически важные сахара могут образовываться не только в процесса апотомического распада углеводов, но и другим путем. Особенно реакционно-способнымиформами моносахаридов, наряду с их фосфорными эфирами, являются их соединения с пиримидиновыми нуклеотидами, в частности, с уридиндифосфатом. Моносахариды в соединении с уридиндифосфатом легко подвергаются изомеризации и гликозилтрансферазным реакциям. При участии уридиндифосфата осуществляются синтезы
198 | 7. Обмен углеводов |
дисахаридов. Уридиндифосфат принимает также участие в синтезе гликогена из глюкозы.
Как уже говорилось ранее, практически вся всосавшаяся из пищеварительного тракта глюкоза поступает в печень, где быстро при участии АТФ подвергается реакции фосфорилирования, катализируемой гексокиназой и далее может не только распадаться, но и участвовать в синтезе гликогена. В этом случае образовавшийся глюкозо-6-фосфатпод влиянием фермента фосфоглюкомутазы переходит вглюкозо-1-фосфат.Образовавшийсяглюкозо-1-фосфатуже непосредственно вовлекается в синтез гликогена.
Этот синтез, согласно Лелуару, осуществляется следующим путем. Глю- козо-1-фосфатв присутствии особого фермента(гликозилтрансферазы) вступает во взаимодействие с уридинтрифосфатом (УТФ) с образованием уридиндифосфоглюкозы(УДФ-Глюк.)и пирофосфата. Последний под влиянием пирофосфатазы немедленно подвергается гидролизу.
гексокиназа + АТФ
АДФ
|
|
|
|
|
|
| OH |
|
|
| |
|
| Ch3 | O P |
| O |
|
|
| |||
|
|
|
|
|
| ||||||
|
|
|
|
|
| ||||||
H |
| O |
|
| OH |
|
|
| |||
| H | фосфоглюкомутаза | |||||||||
| H |
|
|
|
|
|
| ||||
| OH | H |
|
|
|
|
|
|
| ||
|
|
|
|
|
|
| |||||
HO |
|
|
|
|
|
|
|
|
|
| |
|
| OH |
|
|
| ||||||
|
|
|
|
|
|
|
|
|
| ||
| H | OH |
|
|
| ||||||
| глюкоза |
|
| глюкозо-6-фосфат |
| |||||
|
| Ch3OH |
|
|
|
|
| |||
H |
| O H |
|
| гликозилтрансфераза + УТФ |
| ||||
| H |
|
|
|
| OH | УДФГ | |||
| OH | H |
|
|
|
| ||||
HO |
|
|
|
|
| P O |
|
| уридиндифосфоглюкоза | |
| O |
|
| ФФ | ||||||
|
|
|
| |||||||
| H |
| OH |
| OH |
|
|
| ||
глюкозо-1-фосфат | Ф | Ф |
| |||||||
Далее в присутствии особой трансферазы, получившей название гликогенсинтетазы и «затравочного» количества гликогена (полиглюкозы, имеющей не менее четырех остатков глюкозы) происходит своеобразный ферментативный процесс – удлинение цепочки гликогена с невосстанавливающего конца с образованием 1-4связи за счет присоединения остатков глюкозы, входящих в составУДФ-глюкозы.
|
|
|
|
|
|
|
|
|
|
|
| 7. Обмен углеводов |
|
|
|
|
|
|
|
|
| 199 | |||||
|
|
|
|
| Ch3OH |
|
|
|
|
|
|
|
|
|
|
| Ch3OH |
|
|
|
| ||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| H |
| O H |
|
|
|
| ||||||
|
|
| H |
| O | H |
|
|
| гликогенсинтетаза |
|
|
|
|
|
|
|
| |||||||||
|
|
|
|
|
|
|
| +УДФГ |
|
|
|
| H |
|
|
|
|
|
| + УДФ | |||||||
|
|
|
| H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| OH | H |
|
|
|
| |||||||
|
|
|
| OH | H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
| O |
|
|
|
|
|
|
|
| |||||
|
|
| O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| O |
|
|
|
| ||||
|
|
|
|
|
| O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| H |
| OH |
|
|
| n+1 | ||
|
|
|
| H | OH |
|
| n | |||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||
полиглюкоза
Образовавшийся УДФ затем вновь фосфорилируется за счет АТФ до УТФ и, таким образом, весь цикл превращения глюкозо-1-фосфатаможет начинаться сначала. Ветвление синтезируемой молекулы гликогена, как было показано А.Н. Петровой, осуществляется при участии особого фермента, катализирующего замыкание связей между 1 и 6 углеродными атомами остатков глюкозыамилотрансгликозилазы.
7.4. Нейрогуморальная регуляция углеводного обмена. Роль печени в углеводном обмене
Существенная роль в углеводном обмене принадлежит печени. Синтезируемый гликоген с его огромным молекулярным весом (от нескольких сот до нескольких миллионов) может накапливаться в печени в значительных количествах (у человека около 150 г) без изменения осмотических условий в клетках, и, следовательно, является удобной формой депонирования глюкозы. Повидимому, в этой связи печень играет важнейшую роль в поддержании постоянства содержания глюкозы в крови.
Наряду с печенью, значительное место в регуляции обмена углеводов принадлежит периферическим органам и прежде всего мышцам, усиленно потребляющим глюкозу. Однако в первую очередь печень сглаживает колебания уровня сахара, возникающие из-занеравномерного поступления его в кровь. При повышении концентрации сахара в крови печень забирает глюкозу и фиксирует её в виде гликогена, при снижении она «мобилизует» гликоген, переводя его черезглюкозо-1-фосфатвглюкозо-6-фосфати далее с помощью фермента фосфатазы(глюкозо-6-фосфатазы)в свободную глюкозу и фосфорную кислоту. При этом не образуется декстринов и мальтозы, что характерно для гидролитического расщепления гликогена. Одновременно в печени усиливается глюконеогенез, т.е. образование глюкозы главным образом из безазотистых остатков некоторых аминокислот. При помощи этих противоположных процессов печень поддерживает постоянство уровня сахара в крови. Процесс синтеза и распада гликогена в печени осуществляется при регулирующем воздействии гормонов на аденилат – и гуанилатциклазные механизмы гепатоцитов, с
200 | 7. Обмен углеводов |
помощью которых меняется активность внутриклеточных ферментов, принимающих участив в углеводном обмене(фосфорилаза, гликогенсинтетаза). В фиксировании глюкозы в печени на первом месте по значению стоит гексокиназа (глюкокиназа), катализирующая фосфорилирование глюкозы в глюкозо- 6-фосфати тем самым снижающая уровень свободной глюкозы в крови. Уровень сахара в крови (норма80-120мг%;3,33-5,55ммоль/л) влияет на скорость образованияглюкозо-6-фосфатапутем изменения активности гексокиназы. При гипергликемии (т.е. содержании глюкозы в крови выше нормы) активность гексокиназы увеличивается; при гипогликемии (т.е. содержании глюкозы в крови ниже нормы) она, наоборот, понижается.
Таким образом, ферменты обмена углеводов выполняют регуляторные функции по поддержанию постоянства уровня глюкозы в крови, меющего важное физиологическое значение. Гипогликемия создает острую опасность нарушения снабжения центральной нервной системы глюкозой, что приводит к глубокому обмороку и смерти. Гипергликемия ведет к потере глюкозы с мочой. Гипо- и гипергликемия, особенно гипергликемия, в ряде случаев является признаком патологического состояния организма.
Помимо механизмов внутриклеточной регуляции процессы обмена углеводов у человека и животных регулируются нервной системой и гормонами.
Установлено, что важную роль в регуляции углеводного обмена занимает продолговатый мозг и гипоталамическая область. Большое значение в регуляции углеводного обмена принадлежит коре больших полушарий головного мозга. Хорошо известно, что факторы психогенного характера приводят к усилению сахарообразования в печени и гипергликемии. Гипергликемия может быть вызвана условнорефлекторным путем, что также указывает на участие коры больших полушарий в регуляции углеводного обмена. Импульсы от высших метаболических центров, расположенных в гипоталамической области, распространяются по симпатическим нервам и приводят к усилению -инкреции мозговым веществом надпочечников адреналина, стимулирующего процесс глюкозообразования из гликогена в печени и повышения сахара в крови. С другой стороны, в блуждающих нервах содержатся волокна, возбуждающие инкрецию инсулинабета-клеткамиостровков Лангерганса поджелудочной железы, что ведет к снижению уровня сахара крови.
Таким образом, регулирующее действие нервной системы на обмен углеводов осуществляется, главным образом, через воздействие на инкрецию эндокринных желез, которые с помощью гормонов регулируют активность ферментов.
Особенно важны для регуляции углеводного обмена такие эндокринные железы, как поджелудочная железа, кора и мозговое вещество надпочечников, передняя доля гипофиза, щитовидная железа.
7. Обмен углеводов | 201 |
Инсулин – гормон β-клетокподжелудочной железы– единственный гормон, снижающий уровень сахара в крови. Его действие распространяется на мышечную и жировую ткани, а также на печень. Инсулин в печени в присутствии углеводов обладает гликогеностатическим действием. При недостаточности инсулина наблюдается повышение уровня глюкозы в крови(гипергликемия), избыточное выделение глюкозы с мочой (глюкозурия) и понижение содержания гликогена в печени. Мышечная и печеночная ткани утрачивают способность усваивать глюкозу. Одновременно подавляется биосинтез жирных кислот из глюкозы и ацетата и биосинтез белков. Недостаточность инсулина приводит к резкому снижению активности глюкокиназы и уридиндифосфотрансгликозидазы в печени. Наблюдается усиленный синтез ферментов, участвующих в глюконеогенезе из аминокислот и последний возрастает. Описанная картина недостаточности инсулина особенно сильно выражена при перерождении островков Лангерганса поджелудочной железы, вβ-клеткахкоторых вырабатывается инсулин. Это заболевание получило название диабета или сахарного мочеизнурения.
Если в печени действие инсулина на углеводный обмен развивается медленно, то в мышцах проявляется сравнительно быстро. Здесь этот гормон ускоряет метаболизм глюкозы. Он повышает окисление глюкозы и образование гликогена. Тонкий механизм действия инсулина в мышцах связывается прежде всего с повышением проницаемости клеточных мембран для глюкозы. При недостаточности инсулина замедленное поступление глюкозы в мышечную клетку, вероятно, лимитирует ее метаболизм. С повышением проницаемости мембран, вызванной инсулином, возрастает поступление глюкозы в мышечные клетки и одновременно увеличивается скорость ее окисления. Полагают, что инсулин участвует в регуляции синтеза мембранных систем переноса глюкозы и других метаболитов, увеличивая скорость образования специфических информационных РНК на рибосомах, кодирующих эти ферментные системы.
Гормоны коркового слоя надпочечников, влияющие на углеводный обмен (глюкокортикоидные гормоны: гидрокортизон, кортизон, кортикостерон), также действуют в печени и мышцах. Эти гормоны служат как бы антагонистами инсулина, их повышающее действие на уровень сахара крови основано на: увеличении скорости глюконеогенеза в печени и замедлении обмена глюкозы в периферических органах. Глюкокортикоидные гормоны повышают катаболизм белков в печени и тем самым способствуют образованию глюкозы из безазотистых фрагментов аминокислот(глюконеогенез). Под влиянием этих гормонов происходит также активирование фосфатазы(глюкозо-6-фосфа-тазы), благодаря чему изглюкозо-6-фосфатаусиливается образование свободной глюкозы и ее выход из печени. На периферии, т.е. в мышцах, глюкокортикоидные гормоны замедляют окисление глюкозы и препятствуют образованию гликогена.По-видимому,это связано со способностью гормонов влиять на
studfiles.net
Где происходит синтез углеводов в клетке
Сдав кровь на биохимию и получив результаты, человек обнаруживает, что в крови повышены триглицериды. Что это значит? Скорее всего, у пациента есть проблемы с сердечно-сосудистой системой, высокий риск инфаркта. Повышенный уровень свидетельствует о начале атеросклероза. Триглицериды — это нейтральные жиры, поступающие в организм с пищей. Они служат источником энергии, излишек которой, откладывается в жировых клетках.
С химической точки зрения триглицериды — комплекс трехатомного спирта, который соединен с молекулами жирных кислот. ТГ попадают в организм с пищей и расщепляются с помощью кислоты, содержащейся в желудочном соке. Затем расщепленные ТГ всасываются в тонком кишечнике, где происходит их обратный синтез. Там они соединяются с белками, образуя липопротеиды, после попадают в кровь. С помощью крови липопротеиды доставляются во все органы и ткани.
Таким образом, триглицериды — это основная составляющая мембраны клетки.
Уровень триглицеридов в биохимическом анализе крови является важным показателем здоровья. Что значит, если они повышены? Повышенный уровень не говорит напрямую о болезнях, а указывает на высокую вероятность инфаркта, инсульта, ишемии и других заболеваний сердечно-сосудистой системы. Анализ уровня ТГ проводят совместно с анализом жирового спектра. То есть оценивают уровень ТГ, плохого и хорошего холестерина.
Для того, чтобы понять, что значит «триглицериды повышены», нужно знать их допустимую норму. Норма зависит от пола, возраста пациента, общего состояния здоровья. У людей более старшего возраста наблюдается более повышенный уровень триглицеридов в крови, чем у молодых, и это не считается отклонением.
Спроси гематолога!Не стесняйтесь, задавайте свои вопросы штатному гематологу прямо на сайте в комметариях. Мы обязательно ответим.Задать вопрос>>
Измеряют ТГ в миллимолях на литр.
У мужчин триглицериды считаются повышенными , если показатели больше следующих значений:
- 10-20 лет — 0,35- 1,8;
- 20-30 лет — 0,45-2,75;
- 30-50 лет — 0,6-3,6;
- 50-60 лет — 0,55-3,2;
- 60-70 лет — 0,5- 2,9.
Триглицериды повышены у женщин, если они превышают следующие показатели:
- 10-20 лет — 0,4-1,5;
- 20-30 лет — 0,5 -1,64;
- 30-50 лет — 0,4-2,44;
- 50-60 лет — 0,6-2,95;
- 60-70 лет — 0,6-2,7.
Норма для детей до 10 лет — 0,33-1,12 и 0,4-1,23 у мальчиков и девочек соответственно.
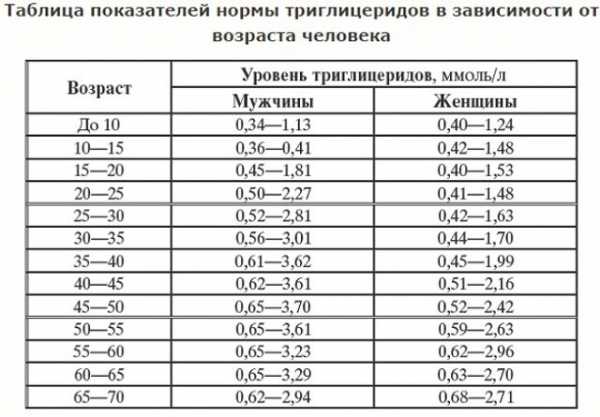
У беременных допускается незначительное отклонение от нормы в большую сторону. На это влияет изменение гормонального фона или переедание. Обычно при отсутствии серьезных сопутствующих патологий все нормализуется после родов.
Как проводят анализ
Анализ на уровень ТГ нужно проводить с профилактической целью раз в 3-4 года после 10 лет. В старшем возрасте такой анализ рекомендуют проходить ежегодно. Помимо этого, врач назначает исследование на триглицериды при различных заболеваниях сердца и сосудов, чтобы назначить корректную терапию. Обязательным регулярное исследование является для больных сахарным диабетом.
Материалом для исследования является кровь из вены. Ее берут утром натощак. Последний прием пищи должен быть за 12 часов до анализа.
Также накануне следует отказаться от физических нагрузок и употребления табака за час до забора крови.
Особенности повышения у детей
У детей триглицериды в крови бывают повышены в следующих случаях:
- Избыточный вес.
- Употребление продуктов с повышенной жирностью (чипсы, гамбургеры).
- Плохое питание с маленьким количеством клетчатки.
- Врожденные аномалии развития (синдром Дауна).
- Эндокринные заболевания (гипотиреоз).
В некоторых случаях снизить уровень триглицеридов у ребенка удается с помощью корректирвки питания.
Если причиной стали врожденные аномалии, то бороться с ними очень сложно.
Причины высоких показателей
В медицине обозначают несколько причин, по которым триглицериды могут быть повышены:
- Неправильное питание. Здесь имеет значение общее число калорий и несбалансированность по белкам, жирам и углеводам.
- Избыточный вес.
- Наследственный фактор нарушения обмена веществ.
- Маленькая физическая активность.
- Прием лекарственных средств: диуретиков, стероидных гормонов.
- Длительное употребление противозачаточных таблеток.
Также повысить уровень триглицеридов может прием больших доз алкоголя.

Малые порции красного вина, наоборот, способствуют нормализации количества ТГ.
Симптомы и опасность
Постоянно повышенный уровень ТГ в крови может спровоцировать развитие серьезных патологий: инфаркт, инсульт, панкреатит, диабет. Это далеко не полный перечень недугов. Также высокий уровень свидетельствует об уже имеющихся заболеваниях. Это такие болезни, как:
- Атеросклероз.
- Ишемия.
- Гипертония.
- Диабет.
- Подагра.
- Панкреатит.
- Гепатит.
- Цирроз печени.
- Заболевания почек.
- Гипотиреоз.
Заподозрить у себя повышение ТГ пациент может по следующим симптомам:
- Повышенное давление.
- Боли в сердце.
- Головные боли.
- Одышка.
- Повышение веса.
- Боли в области печени или поджелудочной.
При возникновении подобных симптомов следует обратиться к врачу и пройти обследование.
Как нормализовать уровень?
Существует несколько способов понизить триглицериды. Выбор зависит от степени повышения и наличия сопутствующего заболевания.
Как понизить с помощью диеты?
Первый шаг — это отказ от алкоголя. Особенно вредными в этом отношении являются пиво и крепкие напитки.
Разрешено употребление небольших порций красного сухого вина (до 100 мл в день).
Далее следует рассчитать допустимый дневной калораж с учетом возраста, веса и двигательной активности.
Рацион питания должен быть сбалансирован по жирам, белкам и углеводам.
Можно употреблять не более 0,9 г жиров на килограмм веса.
Категорически под запретом находятся следующие продукты:
- жирное мясо;
- колбасные изделия;
- сахар;
- сладости из рафинированного сахара;
- выпечка;
- консервы;
- маргарин;
- сало;
- бобовые.
Также следует ограничить употребление белого хлеба, картофеля, макарон, соусов.
Продукты, снижающие триглицериды:
- Каши на воде.
- Цельнозерновой хлеб.
- Свежая зелень.
- Овощи.
- Фрукты.
- Нежирное мясо.
- Рыба.
- Нежирные кисломолочные продукты.
- Растительные масла: оливковое, льняное, подсолнечное.
- Орехи.
Примерное меню для снижения ТГ
Вариант 1
- Завтрак: каша овсяная, фруктовый сок.
- Ланч: яблоко.
- Обед: куриный суп, рыба овощи гриль.
- Полдник: творожный пудинг.
- Ужин: куриная грудка, овощное рагу.
Вариант 2
- Завтрак: омлет, зеленый чай.
- Ланч: фруктовый салат.
- Обед: гречневые котлеты, салат из свежих овощей, заправленный оливковым маслом.
- Полдник: ягоды.
- Ужин: вегетарианские голубцы, немного риса.
Вариант 3
- Завтрак: творог обезжиренный с ягодами, кофе без сахара.
- Ланч: орехи, чай.
- Обед: рыбная котлета, зеленый салат.
- Полдник: фрукт.
- Ужин: тыквенное рагу, куриная грудка на пару.
В течение дня следует соблюдать питьевой режим, выпивать не менее 1,5л чистой воды.
Как снизить с помощью лекарств?
Корректировать уровень ТГ лекарственными средствами следует, учитывая наличие основного заболевания. При диабете, гипотиреозе нужно принимать лекарственные средства, назначенные лечащим врачом.
Для нормализации триглицеридов применяют следующие препараты:
Фибраты
Это лекарства с органическим составом, они притягивают молекулы ТГ, стимулируют выработку печенью компонента, который перерабатывает триглицериды.
Статины
Статины — препараты, снижающие уровень «плохого» холестерина — главного виновника повышенных ТГ.
Омега-3 жирные кислоты
Во время приема препаратов необходимо регулярно проводить анализ крови на триглицериды, чтобы отслеживать динамику и по необходимости корректировать дозировку.
Народные средства
Если у больного есть противопоказания к приему лекарств, то на помощь придут средства народной медицины. Их применение следует обсудить с лечащим врачом.
- Облепиховое масло. Способствует уменьшению концентрации ТГ. Принимают по чайной ложке 2 раза в день за 30 минут до еды.
- Свекольный сок. Снижает «плохой» холестерин. Принимают по 200гр в день в течение 15 дней.
- Лимонный сок. Разводят в воде и пьют в течение дня. Также используют для заправки салатов.
- Две столовых ложки овсяных хлопьев размешать в стакане воды и настаивать несколько часов. Выпивать натощак. Такое напиток способствует абсорбации жиров и снижению ТГ.
- Полезно каждый день съедать по зубчику чеснока.
Физическая активность
Одна из причин повышения триглицеридов — гиподинамия. Поэтому умеренные физические упражнения способствуют улучшению метаболизма, ускорению липидного обмена.
Для этих целей подойдут: легкий бег, ходьба, игровые виды спорта, занятия на велотренажере и беговой дорожке, танцы.
Профилактика
Любой недуг всегда легче предупредить. Для того, чтобы показатели ТГ в крови оставались в норме, следует соблюдать меры профилактики:
- Здоровый образ жизни.
- Физическая активность.
- Правильное питание.
- Регулярные профилактические осмотры и сдача анализов крови.
Эти нехитрые рекомендации позволят сохранить здоровье и предотвратить заболевания сердца и сосудов.
Аритмия и алкоголь — последствия для организма
Сердце – это важнейший орган в человеческом организме, который способен ритмично сокращаться под воздействием определенных импульсов.Оно способно обеспечивать кровью все органы даже вследствие сбоя в нервной системе. Однако под воздействием определенных факторов возникает аритмия – нарушение ритма сокращений сердечной мышцы.
Алкоголь оказывает губительное воздействие на весь организм человека, особенно на сердечно-сосудистую систему. Одним из наиболее опасных и серьезных последствий чрезмерного пристрастия к алкогольным напиткам является нарушение сердечного ритма.
Аритмия считается одним из самых опасных заболеваний сердечной системы человека. Эта болезнь может вызвать тромбоэмболические осложнения или перейти в хроническую сердечную недостаточность.Последние исследования ученых доказали, что под воздействием алкоголя недомогание возникает намного чаще, чем в обычных условиях.

Последствия употребления алкогольных напитков при нарушении ритма сокращения сердечной мышцы
Можно ли пить спиртное в случае наличия аритмии? Этот вопрос очень часто задают люди, у которых существуют заболевания сердца или сосудистой системы.
Аритмия сердца и алкоголь тесно связаны друг с другом. Употребление спиртосодержащих напитков способствует опасным сбоям в работе одного из важнейших органов. Пьянство вызывает разнообразные неполадки в работе сердечной мышцы. Если у человека присутствует боль, покалывание или тяжесть в груди, и он употребляет спиртные напитки, высока вероятность того, что из-за нездорового образа жизни болезнь усугубится. Обострение заболевания сопровождается учащением сердцебиения или наоборот, замиранием ударов мышцы.
Чрезмерное пристрастие к выпивке может стать причиной плохого самочувствия даже у людей со здоровым сердцем. Этиловый спирт пагубно воздействует на орган, особенно на электрическую проводимость сердечной мышцы.
На клеточном уровне спирт отлично растворяется в жирах и воде, что приводит к дестабилизации мембран клеток. Связывание рецепторов клеток спиртным способствует нарушению обмена информацией с окружающей средой. Это приводит к сбою в распространении электрических импульсов между клеточными мембранами. Чувствительность рецепторов значительно снижается, что способствует серьезному ухудшению в прохождении электрического сигнала. Подавление вследствие воздействия алкоголя различных сигналов, дисбаланс клеток влечет к возникновению аритмии.
Употребление спиртного даже в умеренных дозах может вызвать большие проблемы в функционировании сердца.
Боль в груди с похмелья
Чрезмерное пристрастие к вину, пиву, крепким напиткам влечет за собой весьма неприятный фактор – возникновение аритмии. Учащенный пульс в сочетании с резкими перепадами кровяного давления приводят к ухудшению работы всех разделов головного мозга.
Доза алкоголя, которая может вызвать симптомы заболевания, зависит от индивидуальной переносимости спиртного человеком.

Аритмия, возникающая после употребления крепких напитков, обычно проходит через несколько часов при условии, что у человека все в порядке со здоровьем. Но в случае наличия предпосылок к заболеванию очередная доза спиртного может быть весьма опасной и вызвать значительное ухудшение сердечной деятельности. Как правило, это проявляется при похмельном синдроме, когда проявляются следующие признаки:
- Значительная слабость, возникающая у человека через несколько часов после принятия алкогольных напитков.
- Обморок или полуобморочное состояние.
- Резкое возникновение у человека панического необъяснимого страха.
- Сильное головокружение.
- Покалывание, резкая или тянущая боль в груди.
- Затруднение дыхания или одышка.
Мерцательная аритмия – одна из распространенных форм нарушения нормального функционирования сердца
Медицинские статистические исследования показали, что употребление водки, коньяка и вина на 100% провоцирует возникновение сбоев в работе одного из самых важных человеческих органов. Одной из наиболее распространенных патологий, которая развивается вследствие этой пагубной привычки, является именно мерцательная аритмия. Эта болезнь влечет за собой резкое увеличение ритма работы сердечной мышцы.Существенно возрастает нагрузка на мышечную ткань сердца при недостаточном количестве кислорода в крови. При этом недомогании также наблюдается несоответствие количества сокращений желудочков и предсердий.
Основные симптомы недомогания:
- учащенное биение сердца;
- головокружение;
- затрудненное дыхание;
- внезапная потливость;
- ощущение дискомфорта в груди, тяжести, боли или покалывания;
- спутанное сознание;
- резкие скачки артериального давления;
- внутренняя дрожь, чувство паники.
При возникновении мерцательной аритмии выпивка категорически противопоказана. У большинства людей приступы и сбои в работе сердечно-сосудистой системы происходят именно после употребления не только крепких напитков, но и даже пива.
Вещества, содержащие этиловый спирт, нарушают в человеческом организме синтез белков, углеводов и липидов. Это влечет за собой изменение ионной структуры клеток и проницательности мембран, что негативно сказывается на работе мышцы миокарда.
Спиртное способствует ускорению сокращений сердца, что значительно повышает давление в артериях. Накопление крови в предсердиях является причиной возникновения тромбов. Попав в мозг, тромб вызывает инсульт.
В случае возникновения тахикардии, затруднении дыхания, ноющей боли в груди необходимо срочно обратиться к врачу или вызвать скорую медицинскую помощь.
При употреблении спиртного сердечно-сосудистой системе требуется большое количество кислорода, вследствие чего кровообращение ухудшается, и ритм сердца нарушается. Внезапная смерть вследствие инфаркта чаще всего наступает у пьющих людей.
Как, влияя на функцию печени, понизить уровень холестерина в крови
Холестерин является жизненно важным для организма человека соединением, участвующим в общем обмене, обеспечивающим образование гормонов, витаминов, желчных кислот. Без него невозможно построить клеточные мембраны, которые обладают столь уникальными свойствами.
- Образование
- Регуляция синтеза
- Роль печени
- Несколько следствий нарушения работы печени
- Как улучшить работу печени
- При повышении уровня холестерина
Около 80% холестерина синтезируется организмом самостоятельно и большей частью в печени, оставшиеся 20% человек, получает с пищей. Далее о том, что именно происходит в организме.
Образование
Синтез холестерина в организме происходит внутриклеточно, в печени. Структурной единицей его выступает ацетилкофермент А (ацетил-коА) ─ важное химическое соединение, образующееся в цикле Кребса, участвующее во многих метаболических реакциях живого организма.
В дальнейшем в синтезе холестерина ключевую роль играет фермент, называемый гидроксиметилглутарил-коА-редуктаза (ГМГ-коА-редуктаза), он же отвечает и за регуляцию его образования.
В сутки таким образом синтезируется около 1 г холестерина.
Регуляция синтеза
На интенсивность синтетических процессов влияет питание ─ когда уровень холестерина, получаемого с питанием достигает 2−3 г эндогенный синтез его в печени существенно тормозится, однако полной остановки выработки не происходит.
В свою очередь, вновь образованные молекулы также тормозят синтез холестерина по механизму отрицательной обратной связи. А именно происходит ингибирование образования ГМГ-коА-редуктазы, а также стимулирование появления таких ферментов, которые расщепляют ГМГ-коА-редуктазу.
Известно, что при введении в кровь инсулина или гормонов щитовидной железы активность ГМГ-коА-редуктазы повышается, а при повышении уровня глюкокортикостероидов ─ уменьшается. Таким образом, нарушение липидного обмена может быть спровоцировано:
- Неправильной работой тех или иных ферментов, участвующих в синтезе и регуляции обмена холестерина, в том числе как следствие наследственной патологии.
- Неадекватным лечением сахарного диабета (избыток инсулина).
- Заболевания щитовидной железы, протекающие с повышением в крови уровня тиреоидных гормонов.
- Обилие сладостей и углеводов в питании.
- Ожирение.
- Недостаток витамина Е, хрома.
- Опухоли надпочечников (нарушение синтеза глюкокортикостероидов).
Роль печени
Нормальная работа печени необходима для правильного обмена холестерина: достаточного его образования и выведения.
Этот орган отвечает за синтез белков, входящих в состав липопротеидов ─ специальных комплексов, обеспечивающих транспорт жиров по кровеносным сосудам. Нарушения указанной функции печени, вследствие различных факторов (инфекционные заболевания, токсические воздействия и другое) приводит к негативным изменениям липидного обмена и повышению уровня холестерина в крови.
Печень в ответе не только за синтез, но и за переработку и выведение холестерина из организма.
Организм человека может вывести не больше 1,5 г холестерина за сутки, превышение лимита приводит к нарушениям жирового обмена. Если по каким-то причинам печень не справляется со своими функциями ─ на фоне повышенного уровня холестерина начинают страдать сосуды ─ развивается атеросклероз.
Несколько следствий нарушения работы печени
Если происходит поломка на одном из этапов синтеза или регуляции образования холестерина, то одно из самых распространенных последствий ─ развитие атеросклероза. При этом системном заболевании происходит отложение холестерина в стенках артерий, что со временем ведет к их сужению или полной закупорке (с соответствующей клинической картиной, например, инсульта, инфаркта или перемежающейся хромоты).
Еще одним проявлением глубоких нарушений в регуляции синтеза и утилизации холестерина является желчекаменная болезнь (ЖКБ). Механизмом образования камней в желчном пузыре служит избыток синтеза холестерина со сниженным образованием желчных кислот, в связи с чем в желчь секретируется большое количество свободного холестерина. При этом он осаждается на стенках желчного пузыря, также может пропитываться билирубином, белками, солями. Таким образом получаются камни, состоящие исключительно из холестерина или его смеси с другими веществами.
Таким образом, здоровье печени оказывает прямое влияние на липидный спектр крови. Важно знать, что можно сделать, чтобы обеспечить идеальные условия для максимально эффективной работы печени.
Как улучшить работу печени
Влиять на функционирование печени, а тем самым и холестерина, можно и нужно. Но сделать так, чтобы влияния были исключительно позитивными уже сложнее.
Для оптимальной работы печени необходимо:
- Стараться придерживаться здорового питания, по возможности исключить жирные, соленые, копченые продукты и блюда. Заменить жирное мясо в своем рационе более полезной рыбой и морепродуктами.
- Увеличить потребление овощей и фруктов ─ они богаты клетчаткой, обезвреживают и выводят вредные вещества из организма.
- Повысить в рационе количество растительных масел, содержащих полиненасыщенные жирные кислоты (льняное).
- Избавиться от вредных привычек (курения, злоупотребления алкоголем).
- Избегать инфекционных заболеваний, в том числе тех, которые наносят вред непосредственно печени (гепатиты), помнить о возможных путях их передачи: не посещать тату-салоны, маникюрные салоны, в которых отсутствует необходимая обработка инструментов.
- Вовремя диагностировать и лечить заболевания эндокринной системы (сахарный диабет, тиреотоксикоз и другие) и другую соматическую патологию.
- Не допускать ожирение, при наличии избыточного веса приводить его в норму.
- Бороться с гиподинамией, вести активный образ жизни.
- Не допускать застоя желчи в желчном пузыре, используя диету или периодически принимая курс желчегонных средств.
При повышении уровня холестерина
При повышенном уровне холестерина в крови, особенно в возрасте после 35 лет у мужчин и 45 у женщин, нужно обратиться к врачу. Доктор проведет осмотр и назначит обследование:
- Соберет анамнез (исключит семейный анамнез повреждения того или иного звена жирового обмена, оценит факторы риска развития атеросклероза и его осложнений).
- Проведет лабораторные исследования (клинический и биохимический анализ крови, липидный спектр крови) и инструментальную диагностику (УЗИ брюшной полости), тем самым получив данные о состоянии жирового обмена и функции печени.
- При необходимости назначит медикаментозные препараты, которые вмешиваются в метаболизм жиров на том или ином уровне и нормализуют его.
Главное, не медлить с консультацией специалиста, чем раньше будет определена патология, тем легче будет с ней справиться.
zdor.holesterin-lechenie.ru
Биосинтез углеводов, ферменты углеводного обмена
В растениях в процессе фотосинтеза образуются не только фосфорные эфиры сахаров или простые сахара, но и более сложные формы углеводов — сахароза, крахмал, клетчатка. Распад сложных форм углеводов до простых протекает тоже очень быстро. Это наблюдается, например, при прорастании семян, старении вегетативных органов и др. Образующиеся при распаде простые сахара или их фосфорные эфиры оттекают в репродуктивные органы, где из них вновь синтезируются сложные углеводы. И, наконец, в растениях очень легко идут процессы взаимных превращений углеводов.
Взаимопревращение моносахаридов проходит через фосфорные эфиры сахаров или их уридиндифосфатпроизводные (УДФ-производные). УДФ-производные сахаров представляют собой тот или иной сахар, соединенный через два остатка фосфорной кислоты с уридином, например:

Рис.1. Уридиндифосфатглюкоза
Синтез сахарозы
Сахароза является наиболее важным из образующихся в растениях лигосахаридов, в форме которого связанный углерод и энергия транспортируются по всему растению. Она состоит из α-D-глюкозного остатка в его пиранозной форме, связанного гликозидной связью с β-D-фруктозой в фуранозной форме. Поскольку аномерный углеродный атом обоих моносахаридов участвует в образовании гликозидной связи, их полуацетальные группы заблокированы и ни одно из колец не может открыться. Таким образом, сахароза – это невосстанавливающий сахар (не восстанавливает реактивы Фелинга и Бенедикта), и за исключением ее чрезвычайной чувствительности к кислотному гидролизу, она химически инертна. При нагревании с кислотами, или под действием сахаразы (инвертазы) сахароза гидролизуется, образуя инвертный сахар – смесь глюкозы и фруктозы. Сахароза хорошо растворима в воде и обладает сладким вкусом.
Сахароза используется как продукт питания, а также в производстве
поверхностно-активных веществ (эфиры сахарозы с высшими кислотами). Основным
источником получения сахарозы является сахарная свекла, содержащая до 23 %
сахарозы, и сахарный тростник, стеб-ли которого содержат 10–18 % сахарозы. В
настоящее время установлено, что сахароза синтезируется не только в
хлоропластах, но и в цитоплазме фотосинтезирую-щих клеток из УДФ-глюкозы и
фруктозо-6-фосфата, возникшего из
дигидроксиацетонфосфата. Это вещество образуется при фотосинтезе в хлоропластах
и затем поступает в цитоплазму. В нефотосинтезирующих тканях (например, в
эндосперме прорастающих бобов клещевины) образование сахарозы из УДФ-глюкозы и
фруктозо-6-фосфата также происходит в цитоплазме клеток.
Сахароза (тростниковый, свекловичный сахар) – самый распространенный в природе дисахарид. В растениях он образуется из глюкозы и фруктозы. На первом этапе идет фосфорилирование глюкозы:
Глюкоза + АТФ → глюкоза-6-фосфат + АДФ,
затем глюкозо-6-фосфат изолируется в глюкозо-1-фосфат. Глюкозо-1-фосфат соединяется с УТФ, в результате чего отщепляется пирофосфатная кислота и образуется соединение глюкозы с уридиндифосфорной кислотой (УДФ) — уридиндифосфатглюкоза.
Одновременно идет фосфорилирование фруктозы под действием фермента фруктокиназы с участием АТФ:
фруктоза + АТФ → фруктозо-6-фосфат + АДФ.
После этого происходит взаимодействие УДФ-глюкозы с фруктозо-6-фосфатом с участием фермента сахарозофосфат-УДФ-глюкозилтрансферазы. Наконец, образовавшийся сахарозо-6-фосфат под действием фермента фосфатазы гидролизуется с образованием свободной сахарозы. Таким образом, для биосинтеза одной молекулы сахарозы необходимы 3 макроэргические фосфатные связи, эта реакция необратима. В нефотосинтезирующих тканях некоторых растений, например, в корнеплодах сахарной свеклы, клубнях картофеля и других сахароза может образоваться из свободной фруктозы:
УДФ-глюкоза + фруктоза ↔ сахароза + УДФ.
Реакция катализируется ферментом сахарозо-УДФ-глюкозилтрансферазой и в зависимости от условий может быть направлена как в сторону синтеза, так и в сторону расщепления сахарозы.
Синтез крахмала
Крахмал – запасной полисахарид растений, причем он может храниться в растении долго, или расходоваться достаточно быстро. На длительное время он запасается во многих семенах, клубнях и корневищах и используется только тогда, когда эти органы прорастают. На короткое время крахмал образуется в хлоропластах в период быстрого фотосинтеза, а в последующий темновой период он расходуется и оттекает из листьев в форме сахарозы. Крахмал всегда образуется и запасается в виде крахмальных зерен, находящихся в пластидах – хлоропластах либо амилопластах. Крахмальные зерна – это высокоорганизованные структуры, форма и размер которых очень разнообразны, но часто характерны для данного вида растения. Форма зерен может быть сферической, яйцевидной, чечевицеобразной или неправильной; размер может колебаться 1 до 100 мкм. Наиболее крупные крахмальные зерна у картофеля, а самые мелкие у риса и гречихи. Крахмальные зерна содержат до 20 % воды (из которых 10 % химически связано с крахмалом) и ряда концентрических слоев крахмала. Крахмальные зерна образуются путем наслаивания вновь образованных слоев на ранее существующие.
Содержание минеральных веществ в крахмале очень невелико – 0,2–0,7 %, они представлены в основном фосфорной кислотой. В крахмале найдены некоторые высокомолекулярные жирные кислоты (пальмитиновая, стеариновая и др.), содержание которых достигает 0,6 %. Крахмал представляет собой смесь двух полисахаридов – амилозы и амилопектина. Молекулы амилозы – это длинные неразветвленные цепи, содержащие от 100 до нескольких тысяч глюкопиранозных остатков, соединенных гликозидными связями. Изучение дифракции рентгеновских лучей показало, что молекулы амилозы имеют спиралевидную структуру диаметром 1,3 нм с шестью последовательными глюкозными остатками на один оборот спирали.
Молекулы амилозы растворимы в горячей воде, но образующийся раствор нестоек и затем происходит спонтанное осаждение амилозы, известное как ретроградация. Это происходит вследствие тенденции длинных и тонких амилозных молекул выстраиваться в линию рядом друг с другом и образовывать нерастворимые агрегаты с помощью водородных связей. Донором глюкозных остатков при биосинтезе амилозы может служить уридиндифосфатглюкоза-(УДФК). Для ее образования в реакционной среде необходимо наличие затравки, в качестве которой могут служить полисахариды, построенные всего лишь из 3—4 остатков глюкозы, соединенных α(1-4)-связями.
Остатки глюкозы переносятся на акцептор (затравку), где и происходит удлинение цепи. Реакция идет по схеме:
УДФГ + акцептор (Г)к —— УДФ + акцептор (Г)к + 1,
где Г — остатки глюкозы.
Фермент, катализирующий эту реакцию, называется УДФГ-крахмалглюкозилтрансферазой.
У большинства растений активным донором глюкозы является не УДФ-глюкоза, а аденозиндифосфатглкжозα(АДФГ). Реакция присоединения глюкозных остатков от АДФГ к низкомолекулярному акцептору идет аналогичным путем и катализируется ферментом АДФГ-крахмал-глюкозилтрансферазой. Синтез разветвленной молекулы амилопектина, имеющей α (1-6)-связи, происходит при помощи фермента α-глюкантрансферазы (Q-фермент). В синтезе крахмала участвуют и Д-фермент или глюкозилтрансфераза, образующий α(1-4)-связи и участвующий в образовании затравки.
Распад крахмала происходит при участии двух процессов — гидролиза и фосфоролиза.Гидролитический распад крахмала осуществляется под действием четырех ферментов класса гидролиз α-амилаза, катализирует расщепление α(1-4)-связи, причем связи разрываются беспорядочно. Конечный продукт такого распада — мальтоза, глюкоза, декстрины. Под действием β-амилазы происходит расщепление α (1-4)-связей с образованием остатков мальтозы. Фермент глюкоамилазы катализирует последовательное отщепление остатков глюкозы от молекулы крахмала. Амилопектин-1,6-глюкозидаза или R-фермент катализирует расщепление α(1-6)-связей в молекуле амилопектина, т. е. действует на точки ветвления.
Фосфоролиз — это присоединение фосфорной кислоты по месту разрыва глюкозидной связи между остатками моносахаридов в цепи полисахарида, при этом происходит образование глюкозо-1-фосфата. Эта реакция катализируется ферментомаглюконфосфорилазой, относящимся к классу трансфераз. Крахмал в растении может подвергаться очень быстрому распаду, так как ферменты распада находятся во всех органах растения.
Синтез целлюлозы
Целлюлоза не растворима в воде, она лишь набухает в ней. При кислотном гидролизе (кипячение в серной кислоте) превращается в глюкозу, при более слабом – в целлобиозу. С помощью рентгеноструктурного анализа установлено, что молекула целлюлозы имеет нитевидную форму. Эти нитевидные молекулы, благодаря водородным связям, соединяются пучками по 40–60 штук в мицеллу. В клеточных стенках растений мицеллы целлюлозы связаны во-дородными связями с различными гетерополисахаридами. Например, у белого клена ими являются соединенные между собой гликозидными связями ксилоглюкан, арабиногалактан, рамногалактурон. Кроме того, имеются данные о том, что в построении клеточной стенки растений принимает участие особый, богатый оксипролином гликопротеид экстензин.
Целлюлоза построена из остатков β-глюкозы. В биосинтезе целлюлозы принимает участие не свободная глюкоза, а ее ГДФ-производное — гуанозиндифосфатглюкоза при участии фермента целлюлозосинтетазы по схеме:
ГДФ — глюкоза + (глюкоза) к→ ГДФ + (глюкоза) к + 1
Распад целлюлозы идет преимущественно гидролитическим путем под действием фермента целлюлазы до дисахарида целлобиозы.
Транспорт углеводов осуществляется в виде сахарозы. В процессе фотосинтеза образуется много углеводов, и в этой связи большое значение имеет отток ассимилятов в другие части клетки из хлоропластов. Проникновение через мембрану хлоропластов фосфорилированных гексоз и сахарозы затруднено, наиболее легко через мембраны хлоропластов проникают триозофосфаты (ФГА и ФДА). Предполагается, что образующиеся сложные углеводы распадаются на триозофосфаты и в таком виде передвигаются в цитоплазму, где могут служить материалом для ресинтеза гексоз, сахарозы, крахмала.
Межклеточный паренхимный транспорт осуществляется двумя путями — по плазмодесмам (симпласту) или по свободному пространству (аппопласту). Сахароза, образовавшаяся в клетках мезофилла листа, десорбируется в аппопласт. Выходя из паренхимных клеток в аппопласт, сахароза расщепляется инвертазой на гексозы. Гексозы передвигаются по аппопласту к передаточным клеткам проводящих пучков по градиенту концентраций. При соприкосновении с передаточными клетками флоэмы они снова превращаются в сахарозу. Далее происходит загрузка ситовидных трубок, сахароза поступает против градиента концентраций, и требуется расход энергии (АТФ).
Предполагается, что сахароза преодолевает мембрану с помощью переносчика в комплексе с протоном. При этом благодаря работе Н+-АТФ-азы ионы Н+ выкачиваются из клеток флоэмы, а затем поступают обратно по градиенту рН, увлекая за собой сахарозу против градиента ее концентрации. Основной транспортной формой углеводов по флоэме служит сахароза (С12Н22О11). У некоторых видов наряду с сахарозой транспортной формой углеводов служат олигосахара (рафиноза, стахиоза), а также некоторые спирты.
biofile.ru
