Как получают синтетический метан — Автомобили
Изначально предполагалось, что это электричество, выработанное исключительно с помощью возобновляемых источников будет использоваться при производстве электрических автомобилей семейства e-tron, а также для их дальнейшего использования. В частности, председатель правления компании Руперт Штадлер в 2010 году неоднократно заявлял, что все электромобили «Audi» будут работать на электричестве, полученном экологически безопасным способом. Поэтому, собственно, на протяжении двух следующих лет этот топливный проект выглядел лишь как дополнение к проекту e-tron. Но кто бы мог подумать, что в итоге все это поставит под угрозу бизнес, например, Газпрома? Мечты Алексея Миллера явно выглядят иначе…
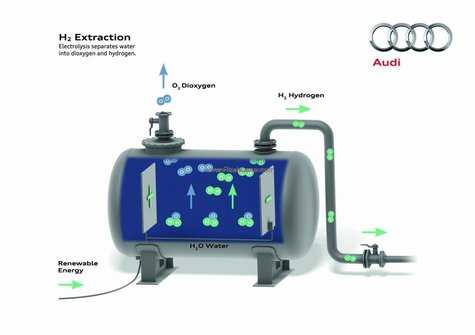
Выработка экологически чистого электричества действительно оказалась частью более крупной программы, но не совсем автомобильной. Инициатива со скромным названием Audi balanced mobility вплотную связана с машинами, но главной ее задачей является достижение нейтрального баланса по диоксиду углерода на протяжении всей жизни автомобиля, начиная с момента производства и заканчивая моментом утилизации. И одной из ключевых составляющих программы является проект Audi e-gas, а выработка электроэнергии в Северном море и ее транспортировка – лишь его составляющая. И это выглядит куда интереснее, чем повальное увлечение электромобилями и попытки создания эффективного гибрида.
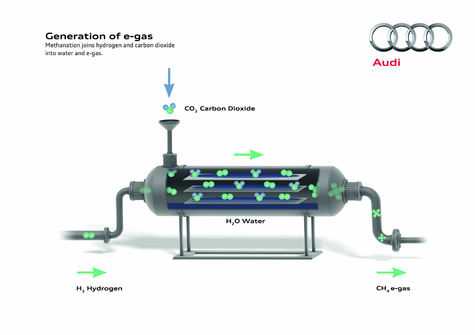
Дело в том, что e-gas отчасти можно считать углеводородом, так как речь идет о выработке синтетического… метана! Этот газ сам по себе является одним из самых быстровосполняемых углеводородов на планете. Однако искусственный метан, по мнению немцев, позволит еще и очистить Землю от парниковых газов. Суть в том, что при его выработке реакция происходит с использованием воды и диоксида углерода и, следовательно, предотвращает поступление последнего в атмосферу. В результате же мы получаем замкнутый, по сути, цикл оборота СО2. Единственным же выхлопом на первом этапе является кислород, а на втором – дистиллированная вода. Кроме того, гидролиз позволяет вырабатывать водород, который, в свою очередь также является источником энергии и в среднесрочной перспективе может использоваться на машинах с топливными ячейками.
Наряду с разработкой водородных машин, эта схема выглядит более чем перспективной, поскольку уж что-что, а запасы СО2 на планете не никогда иссякнут. Поэтому даже если для синтеза, в итоге, будет использоваться не «экологически чистое» электричество, она все равно окажется более реальной и эффективной, чем любое другое подобное начинание.
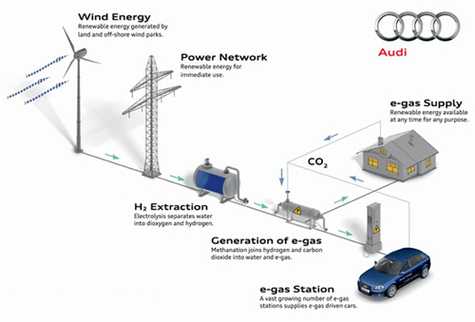
Дело в том, что установка, предназначенная для получения топлива может быть каких угодно размеров. Audi сейчас построила завод и ближайшем будущем собирается создать целую сеть подобных предприятий. Но кто мешает сделать сделать установку более компактной и обеспечить таким образом топливом, скажем, деревню? Или улицу? Или отдельно стоящий дом? Для гидролиза понадобится электричество, однако на этот случай есть ветряки. Разумеется, скажем, в Средней полосе России они не будут являться основным источником энергии, но почему им при этом не быть вспомогательным? В любом случае, вы производите дешевый метан, которым в последствии и топитесь, и машину заправляете.
А теперь сравните эту идею с «умным домом», который придумал «Nissan». После трагедии в Фукусиме японцы решили оградить соотечественников от длительных отключений электроэнергии: мол, ребята, ваш LEAF теперь умеет не только потреблять электричество, но и отдавать его – подключаете его к дому и можете пользоваться… Все отлично, если не одна мелочь: LEAF – аккумулятор, который, как известно, имеет свойство разряжаться, и в конце концов это произойдет. Для Японии, думаю, пять-шесть часов без энергии – нонсенс, у нас, как показывает практика, нормой считаются и несколько дней, так что программа e-gas в нашем случае – проект не только интересный, но и полезный, а для Европы еще и стратегический, так как в перспективе он позволит Старому Свету полностью слезть с российской газовой иглы. Учитывая, что эта схема давно и достаточно эффективно используется в химической промышленности, проблем с ее использованием быть не должно, единственная проблема, которую предстоит решить инженерам немецкой компании (в проекте также участвуют ETOGAS GmbH, MT-BioMethan GmbH, Центр по исследованию солнечной и водородной энергии (ZSW), Фрауэнхофский институт по ветроэнергетике и технологиям энергосистем (IWES) и EWE Energie AG) – возможность получения СО2 непосредственно из атмосферы, и если это случится мечты сбудутся у всех, а не только у менеджеров Газпрома.
Как это работает
Если упростить схему до школьного уровня, то она становится практически элементарной. Фактически технология состоит из трех этапов. Первый – выработка «зеленого» электричества. Второй – электролиз, в ходе которого вода расщепляется на кислород и водород. Третий – метанирование. Полученный в ходе гидролиза водород поступает в соответствующий резервуар, где в дальнейшем реагирует с СО2, образуя тот самый e-gas. В качестве же побочного продукта образуется дистиллированная вода.
Ветровые электростанции в Северном море

Электричество для проекта e-gas вырабатывают с помощью четырех энергетических установок, построенных на старых нефтяных платформах в Северном море. За счет постоянных ветров они примерно на 40% эффективнее наземных ветряков того же размера.
Каждая из турбин рассчитана на 3,6 мегаватт, то есть ежегодно они вырабатывают порядка 53 гигаватт энергии, которых вполне хватает для нужд среднего города. Притом, с повышением эффективности отдача ветряков будет только увеличиваться.
Топливный завод

В данном случае речь о громадном заводе по производству синтетического метана в немецком Верльте, который Audi с партнерами запустили 28 июня прошлого года. Его строительство началось в сентябре 2012 года, а закончено в декабре. Как заявили немцы, излишки тепла, образующиеся в ходе метанирования, используются на соседнем заводе по производству биогаза, а оттуда на предприятие поставляется высококонцентрированный CO2, использующийся как базовое сырье для производства e-gas. Последний момент и является основной технологической препоной для повсеместного внедрения подобных комплексов, поскольку иные составляющие – вода и электричество – по сути, есть где угодно.
Этот завод вписан в общую энергетическую и газораспределительную сети Германии со всеми отсюда вытекающими. Проще говоря, синтезируя с помощью «зеленого» электричества искусственный метан, немцы его, как минимум, сохраняют, поскольку он в последствии может быть использован в качестве топлива на газовых или тепловых электростанциях.
Стоит заметить, что e-gas практически идентичен природному газу. Предприятие в Верльте будет производить около 1000 тонн e-gas в год, химически связывая при этом около 2800 тонн двуокиси углерода. Примерно такое же количество СО2 за год поглощает буковый лес, состоящий из 220 000 деревьев.
Audi g-tron

В конце 2012 года менеджмент Audi объявил о том, что компания отказывается от выпуска R8 e-tron, обосновывая свое решение тем, что этот проект оказался слишком дорогим и неэффективным. В частности немцев не устроила стоимость аккумуляторов. В итоге те автомобили, которые уже были произведены, они планируют использовать для дальнейших испытаний. Нет существенных подвижек и в деле о запуске аналогичного А1. Машину обновили, но что с ней будет в дальнейшем пока неизвестно. В общем, реализацию концепции электромобиля в Ингольштадте, можно сказать, заморозили.
В то же время, не так давно оттуда пришло сообщение, что компания выпустит 1500 Audi A3 Sportback g-tron. В пятидверном хэтчбеке с двигателем 1.4 TFSI в качестве топлива может использоваться природный газ, биометан и Audi e-gas. Кроме того, двухтопливная концепция машины позволяет ей ездить и на бензине. Все это обеспечивает единовременный запас хода около 1300 километров.
Предполагается, что покупая Sportback g-tron клиент может заказать квоту на e-gas. С этого момента он будет включен в процесс учета топлива, гарантирующий, что весь газ, закачиваемый в баллон автомобиля на газозаправочной станции, поступил в газотранспортную сеть именно с завода Audi e-gas.
Audi утверждает, что A3 Sportback g-tron потребляет в среднем менее 3,5 кг e-gas на 100 км пути. Выбросы CО2 при этом не превышают 95 г/км по циклу NEDC, и что работа двигателя этого автомобиля является нейтральной с точки зрения влияния на климат, так как вся двуокись углерода, образующаяся во время эксплуатации автомобиля, ранее была изъята из атмосферы при производстве топлива. В итоге, даже при комплексном анализе wheel-to-well, который учитывает строительство и эксплуатацию завода, а также строительство и обслуживание ветрогенераторов, выбросы CO2 составляют лишь 20 г/км, что является рекордно низким показателем, который недавно был подтвержден сертификатом TÜV Nord.
www.avtovzglyad.ru
«Метан – в перспективе ценное сырье для химической промышленности»
Европейская Академия (Academia Europaea) – неправительственная организация, призванная объединить ученых всех европейских стран, была создана в 1988 г. В настоящее время в ее состав входят около 4000 ученых, в том числе 72 нобелевских лауреата. Россию представляют 75 членов. В 1992 году по инициативе одного из них, академика РАН, основателя и декана факультета биоинженерии и биоинформатики МГУ Владимира Скулачева, был образован Российский клуб Европейской Академии. В том же году клуб учредил ежегодную премию Европейской Академии для молодых российских ученых. Это достаточно престижная награда в научном сообществе, которая присуждается за фундаментальные научные исследования, выполненные в России и опубликованные в виде книг или статей в ведущих научных журналах. Одним из лауреатов по итогам 2017 года (вручение премии прошло этой весной) стал научный сотрудник группы ЯМР спектроскопии каталитических превращений углеводородов Института катализа СО РАН, к.х.н. Антон Габриенко. Он согласился поделиться с нашими читателями подробностями своей научной работы.
– Я представил на конкурс серию своих научных статей, посвященных общей теме: изучение механизмов активации и превращения метана на таких катализаторах, как металлсодержащие цеолиты.
– А превращать во что?
– В разные ценные, с точки зрения химической промышленности, продукты, такие, как метанол, карбоновые кислоты и ароматические углеводороды. В дальнейшем эти продукты используют при производстве полимеров, красителей и другого конечного продукта.
– Получается, метан – потенциально ценное сырье.
– Да, конечно. Метан — основной компонент природного и попутных нефтяных газов. Отсюда вытекают его основные достоинства, к которым можно отнести относительную доступность, большие запасы и низкую цену добычи. Но интерес к нему пока невысок, да и использование сложно назвать высокоэффективным.
Например, при нефтедобыче мы одновременно получаем большие объемы метана. Просто выпускать их в атмосферу нельзя, обратно закачать – тоже. В итоге, газ просто сжигают. Вы, возможно, видели эти «вечные» факелы возле нефтяных вышек. Или продают, как вид топлива. То есть, обычно, метан используют для получения тепловой энергии.
Но это не единственный вариант его применения. Как я уже сказал ранее, метан может быть ценным сырьем для каталитической промышленности.
– Но почему же тогда его не используют в качестве сырья предприятия химической отрасли?
– Потому что при сегодняшнем уровне технологий выгоднее перерабатывать с этими же целями нефть. Однако ресурсы нефти не безграничны, особенно той, что можно относительно недорого добывать. И когда они начнут истощаться, будет расти интерес к альтернативному сырью для химической промышленности, в том числе, к метану.
– Иначе говоря, вы работаете на перспективу.
– Вся фундаментальная наука в той или иной степени работает на перспективу. Работа нашей группы помогает лучше понять механизмы воздействия катализаторов определенного класса на метан. Применяя разные методы спектроскопии (ядерного магнитного резонанса, инфракрасную, рентгеновскую флуоресцентную и т.д.), мы построили достаточно полную, насколько это возможно, модель происходящих химических реакций. Это очень интересно и очень важно. Ведь, если мы говорим о промышленном применении катализаторов, то очень важно, чтобы он отработал не один цикл, а тысячи или даже миллионы. А это возможно только, если катализатор будет сам себя регенерировать в течение производственного процесса. Чтоб этого добиться, надо хорошо представлять, что происходит на поверхности катализатора во время реакций с метаном. На нашей модели мы видим, что происходит с молекулами метана и активными центрами на поверхности катализатора на разных этапах, как они взаимодействуют, почему процесс протекает так, а не иначе. И теперь с этой моделью можно работать, создавая новые, более эффективные катализаторы уже для промышленного использования. Пока же отсутствие таких катализаторов для селективного превращения метана – один из главных барьеров на пути его широкого использования в химической промышленности.
– Я правильно понимаю, что наша страна находится в числе мировых лидеров по имеющимся запасам метана?
– Да, это так. Все страны, обладающие большими запасами природного газа и нефти, одновременно имеют сопоставимые ресурсы по метану. И мы в этом отношении не исключение.
– А какое-то внимание к Вашей работе со стороны отечественных производителей, тех, кто выпускает катализаторы, есть?
– Знаете, пока как-то не замечали. Думаю, это вызвано тем, что пока на рынке нет соответствующей конъюнктуры. Но мы не сможем вечно выезжать на нефти, уже сейчас начались поиски возможной замены нефтепродуктам в разных сферах их применения. И это открывает интересные перспективы для прикладного использования полученных нами результатов.
– Вы несколько раз употребили слово – «интересный». А что самое интересное для Вас в таких исследованиях?
– В качестве примера, представьте, вы знаете, что если взять метан, добавить цеолит, замешать все это при высокой температуре, то на выходе вы получите бензол. А это уже совсем другое вещество.
И дальше вы начинаете детально разбираться, как это происходит, как одно вещество превращается в другое. Вот этот процесс выстраивания пути превращения, понимание того, как работает природа, получение новой информации о чем-то прежде неизвестном – это для меня самое интересное. На мой взгляд, наука так и работает.
– Последний вопрос – традиционный: Ваши планы?
– Наша группа работает в нескольких направлениях. Мы продолжаем копать эту тему, и чем дольше мы ею занимаемся, тем более интересные вещи мы находим. И одновременно мы пробуем проводить аналогичные исследования со схожими группами веществ. Моя кандидатская диссертация, которую я защитил в 2011 году, была посвящена цинк- и галлий-цеолитам. После мы попробовали цеолиты, содержащие серебро, индий. Сейчас мы пробуем работать с медьсодержащими цеолитами. Сейчас в научной литературе какой-то бум, связанный с этими системами, публикуется много новой информации, и мы хотим посмотреть, как они подходят для наших целей.
Наталья Тимакова
academcity.org
Ответы@Mail.Ru: как получить метан
Риторический вопрос….<br>То же самое касается вопроса, как получить водку, имея коньяк и отбеливатель :)<br>
Методом анального выпёрдывания.
Получение метана <br>Метан в лаборатории получают прокаливанием безводного ацетата натрия с натронной известью. Натронная известь представляет собой смесь гидроксида натрия с гидроксидом кальция. <br><br>Оборудование Натронная известь, ацетат натрия, пробирка с газоотводной трубкой, горелка, лучина <br> <br>Техника безопасности Опыт требует осторожного обращения с огнем. Проверка метана на чистоту аналогична проверке водорода на чистоту. <br> <br>Образовательный уровень базовый курс, самообразование <br> <br>Источники Постановка опыта и текст — к.п.н. Павел Беспалов <br><br>Описание опыта <br><br>Смешаем натронную известь с ацетатом натрия, тщательно перемешаем и поместим в пробирку. Закроем пробирку пробкой с газоотводной трубкой. Нагреем смесь. Через некоторое время начинает выделяться метан <br> <br>Ch4COONa + NaOH = Ch5 + Na2CO3 <br> <br>Поджигаем метан. Он горит почти бесцветным пламенем. При горении метана образуется углекислый газ и вода. <br> <br>Ch5 + 2О2 = СО2 + 2 Н2О <br><br>
метан-в значительном кол-ве содержится в попутном нефтяном газе (выделяющемся при добыче нефти), а также в коксовом газе. Выделяется со дна болот, прудов и стоячих вод, где он образуется при разложении растительных остатков без доступа воздуха. Метан постоянно скапливается в каменноугольных шахтах, где его называют рудничным газом. Смесь метана с воздухом крайне взрывоопасна (особенно в соотношении1:10)Ch4Cl+HCl-Ch5+Cl2.
Вообще, метан настолько распространенный в природе и в быту газ, что как-то никто не заморачивается с его получением. Бытовой газ (используемый в газовых плитах) почти на 99% состоит из метана. В промышленности метан иногда получают по реакции СО+Н2 —Ch5 + h3O, но делается это не ради получения метана, а чтобы очистить газ от СО (является ядом для катализатора, в следующей реакции (производство аммиака)) . Лабораторный способ получения чистого метана, уже описан, могу предложить более экзотический вид: восстановление формалина или метилового спирта в кислой среде. З. Ы. Любителем попукать: в ваших «газах» метана не присутствует. Вопреки общепринятому мнению метан (как и большинство инертных газов) запахом не обладает. Болотные газы действительно содержат метан, но пахнет не он, а сероорганические и азотоорганические соединения.
Открывать кран или конфорки газовой плиты бесполезно, там пропан или пропан-бутан. Пукать тоже — в кишечных газах нет метана, там водород и сероводород. Получить метан можно на болоте. Для этого возьмите емкость, заполните ее водой, опустите в болото горловиной вниз, вставьте в горловину воронку и под этой воронкой ткните палкой в дно болота. Выделяющийся при этом газ и будет метаном. Его надо улавливать воронкой. По мере заполнения газом бутыли вода из нее будет вытесняться.
touch.otvet.mail.ru
Что можно сделать из природного газа
Природный газ отлично вступает в химическую реакцию горения. Поэтому чаще всего из него получают энергию — электрическую и тепловую. Но на основе газа можно сделать еще удобрение, топливо, краску и многое другое.
Значительные объемы газа использует также металлургическая промышленность. Но и здесь природный газ также используется как источник энергии — для разогрева доменных печей.
Зеленое топливо
В России около половины поставок газа приходится на энергетические компании и коммунальное хозяйство. Даже если в доме нет газовой плиты или газового водонагревателя, все равно свет и горячая вода, скорее всего, получены с использованием природного газа.
Природный газ — самое чистое среди углеводородных ископаемых топлив. При его сжигании образуются только вода и углекислый газ, в то время как при сжигании нефтепродуктов и угля образуются еще копоть и зола. Кроме того, эмиссия парникового углекислого газа при сжигании природного газа самая низкая, за что он получил название «зеленое топливо». Благодаря своим высоким экологическим характеристикам природный газ занимает доминирующее место в энергетике мегаполисов.
На газе можно ездить
Природный газ может использоваться как моторное топливо. Сжатый (или компримированный) метан стоит в два раза дешевле 76-го бензина, продлевает ресурс двигателя и способен улучшить экологию городов. Двигатель на природном газе соответствует экологическому стандарту Евро-4. Газ можно использовать для обычных автомобилей, сельскохозяйственного, водного, воздушного и железнодорожного транспорта.
Компримированный газ получают на автомобильных газонаполнительных компрессорных станциях (АГНКС) путем сжатия природного газа, поступающего по газопроводу, до 20–25 МПа (200–250 атмосфер).
Еще из природного газа можно производить жидкие моторные топлива по технологии «газ-в-жидкость» (gas-to-liquid, GTL). Поскольку природный газ — достаточно инертный продукт, практически всегда при переработке на первом этапе его превращают в более реакционно-способную парогазовую смесь — так называемый синтез-газ (смесь СО и Н2).
Далее ее направляют на синтез для получения жидкого топлива. Это может быть так называемая синтетическая нефть, дизельное топливо, а также смазочные масла и парафины.
Впервые жидкие углеводороды из синтез-газа получили немецкие химики Франц Фишер и Ганс Тропш еще в 1923 году. Правда, тогда в качестве источника водорода они использовали уголь. В настоящее время различные варианты метода Фишера-Тропша используются во многих представленных на рынке процессах превращения газа в жидкие углеводороды.
Отбензинивание
Первичная переработка газа происходит на ГПЗ — газоперерабатывающих заводах.
Обычно в природном газе помимо метана содержатся разнообразные примеси, которые необходимо отделить. Это азот, углекислый газ, сероводород, гелий, пары воды.
Поэтому в первую очередь газ на ГПЗ проходит специальную обработку — очистку и осушку. Здесь же газ компримируют до давления, необходимого для переработки. На отбензинивающих установках газ разделяют на нестабильный газовый бензин и отбензиненный газ — продукт, который впоследствии и закачивают в магистральные газопроводы. Этот же уже очищенный газ идет на химических заводы, где из него производят метанол и аммиак.
А нестабильный газовый бензин после выделения из газа подается на газофракционирующие установки, где из этой смеси выделяются легкие углеводороды: этан, пропан, бутан, пентан. Эти продукты тоже становятся сырьем для дальнейшей переработки. Из них в дальнейшем получают, к примеру, полимеры и каучуки. А смесь пропана и бутана сама по себе является готовым продуктом — ее закачивают в баллоны и используют в качестве бытового топлива.
Краска, клей и уксус
По схеме, похожей на процесс Фишера-Тропша, из природного газа получают метанол (CH3OH). Он используется в качестве реагента для борьбы с гидратными пробками, которые образуются в трубопроводах при низких температурах. Метанол может стать и сырьем для производства более сложных химических веществ: формальдегида, изоляционных материалов, лаков, красок, клеев, присадок для топлива, уксусной кислоты.
Путем нескольких химических превращений из природного газа получают также минеральные удобрения. На первой стадии это аммиак. Процесс получения аммиака из газа похож на процесс gas-to-liquid, но нужны другие катализаторы, давление и температура.
Аммиак сам по себе является удобрением, а также используется в холодильных установках как хладагент и в качестве сырья для производства азотсодержащих соединений: азотной кислоты, аммиачной селитры, карбамида.
Как получается аммиак
Вначале природный газ очищают от серы, затем он смешивается с подогретым водяным паром и поступает в реактор, где проходит через слои катализатора. Эта стадия называется первичным риформингом, или парогазовой конверсией. Из реактора выходит газовая смесь, состоящая из водорода, метана, углекислого (СО2) и угарного газов (СО). Далее эта смесь направляется на вторичный риформинг (паровоздушная конверсия), где смешивается с кислородом из воздуха, паром и азотом в необходимом соотношении. На следующем этапе из смеси удаляют СО и СО2. После этого смесь водорода и азота поступает собственно на синтез аммиака.
www.gazprominfo.ru
Как из углерода получить метан 🚩 для получения метана 🚩 Естественные науки
Автор КакПросто!
Метан – простейший углеводород. Его химическая формула – СН4. Он гораздо легче воздуха, почти не растворяется в воде, представляет собою бесцветный газ, не имеющий запаха. Находит широкое применение – в качестве топлива, как сырье для производства многих органических веществ, таких, как ацетилен, метанол, формальдегид и т.д. Метан можно получить разными способами, в том числе из углерода.

Статьи по теме:
Инструкция
Перед вами стоит задача: получить углерод из метана. Сама формула метана может подсказать дальнейшие действия. Что надо сделать, чтобы из вещества С получить СН4? Разумеется, присоединить к углероду водород. То есть провести реакцию гидрирования. Она будет протекать по формуле: С + 2Н2 = СН4 Как это можно сделать? Просто так при нормальных условиях такая реакция не протекает. Для этого требуются особые условия. Метан из углерода получают одним из двух способов:- либо в пламени так называемой «электрической дуги» в атмосфере водорода. Реакция идет при температуре порядка 1200 градусов;- либо при более низкой температуре (порядка 400 – 500 градусов) и повышенном давлении. При этом в качестве инициатора и ускорителя реакции используется никелевый катализатор.Легко можно понять, что в лабораторной практике получить метан из углерода чрезвычайно тяжело. Поэтому в лабораториях применяют другие методы получения метана, например, путем воздействия воды на карбид алюминия, или при сплавлении едкого натра с ацетатом натрия. Да и в промышленных условиях синтезировать метан из углерода нерентабельно. Такие способы получения метана представляют чисто академический интерес.
Как ни странно это может прозвучать, но самый эффективный способ получения метана из углерода – с помощью так называемых «природных биологических реакторов». Иными словами, огромное количество метана образуется в желудочно-кишечном тракте травоядных животных, в процессе переваривания пищи, с помощью бактерий и ферментов, играющих роль катализатора. Сложные промежуточные процессы в итоге сводятся к той же самой схеме реакции: С + 2Н2 = СН4
Обратите внимание
По-другому метан часто называется болотным газом, а также рудничным газом, так как в изобилии образуется и при гниении растительности в стоячей воде, и в толще угольных пластов, при медленном превращении углерода без доступа воздуха. Именно поэтому случайное вскрытие полости угольного пласта, содержащей метан, грозит взрывом. При работе в шахтах, необходимо строго соблюдать меры безопасности!
Источники:
- из углерода получают
Совет полезен?
Распечатать
Как из углерода получить метан
Статьи по теме:
Не получили ответ на свой вопрос?
Спросите нашего эксперта:
www.kakprosto.ru
Переработка — метан — Большая Энциклопедия Нефти и Газа, статья, страница 3
Переработка — метан
Cтраница 3
Исходным сырьем для органического синтеза являются продукты термической переработки различных видов твердого топлива и нефти, а также углеводороды, получаемые из естественного газа. Большое сырьевое значение для производства ряда более сложных синтетических веществ имеет ацетилен, получающийся из карбида кальция или переработкой метана. [31]
Это особенно важно для России, которая обладает 34 % доказанных и около 40 % потенциальных запасов природного газа в мире. Такое положение дел стимулирует проведение серьезных исследований, направленных на поиски и разработку альтернативных, более экологически чистых и ресурсосберегающих способов переработки метана для получения водорода или синтез-газа. Это в полной мере относится и к способам получения водорода для питания топливных элементов. [32]
Все более отчетливо намечаются пути и методы энергетического и1 химического использования этого сырья; однако еще немного осуществлено в промышленности. Но если упорство и настойчивость ученых, и техников нашли пути химического связывания более инертного, чем метан азота, то есть ли основание сомневаться в блестящих перспективах широкой энерго-химической переработки метана. [33]
Чтобы предотвратить загрязнение получаемого водорода азотом, частичное окисление предпочтительно осуществлять чистым кислородом. Расход тепла при этом зависит от природы сырья. При переработке метана требуется столько же тепла, сколько и при его паровой конверсии, поскольку в обоих случаях протекают одинаковые реакции. [34]
Огромное значение в качестве сырья для пластических масс имеют природные и, в частности, попутные газы. Основную часть природных газов составляет метан, из которого в результате электрокрекинга и окислительного крекинга получают ацетилен, являющийся, в свою очередь, основным сырьем для производства ацетальдегида, уксусной кислоты, уксусного ангидрида и виниловых соединений, например хлористого винила и винил-ацетата. Другими важными методами переработки метана в сырье для полимеров являются хлорирование, окисление и некоторые другие процессы. [35]
Метан, который используется главным образом как топливо, добывают в виде природного газа или выделяют из газов нефтехимических и нефтеперерабатывающих заводов. Одной из самых важных областей применения метана является получение так называемого синтез-газа — смеси водорода с окисью углерода в различных пропорциях. Существует два основных метода переработки метана в синтез-газ: конверсия с водяным паром и неполное окисление. В обоих случаях исходным сырьем могут также служить высшие парафины. [36]
Фрейнд говорит о получении ацетилена из других углеводородов, помимо метана или этана. Большая часть моего доклада посвящена переработке метана. Фактически в настоящее время существуют 4 крупных промышленных установки, работающих на природном газе. Однако выбор природного газа определяется лишь экономическими соображениями, а не химическими, так как в районах; где находятся указанные установки, природный газ является наиболее дешевым сырьем. С химической точки зрения применение природного газа совершенно равноценно применению легких нефтяных газов или углеводородных паров, которые реагируют с кислородом точно так же, как природный газ. Проводившиеся нами полузаводские опыты по неполному окислению легких нефтяных газов давали одинаковые весовые выходы независимо от типа исходного углеводородного сырья. [37]
Выбор того или другого метода связан с проблемой сырья и вспомогательных продуктов, а также со стоимостью электроэнергии. С этой точки зрения для Румынской Народной Республики самым подходящим является метод окисления азотной кислотой. Получение аммиака и азотной кислоты при переработке метана и других лефтепродуктов делает применение азотной кислоты в качестве агента окисления дешевым. [38]
В начале нынешнего века в Норвегии, Швейцарии и Соединенных Штатах Америки на базе дешевой гидроэлектроэнергии был построен ряд заводов по получению азотной кислоты фиксацией в дуге атмосферного азота в виде NO. Процесс этот оказался, однако, нерентабельным и в настоящее время не используется. В настоящее время синильная кислота получается в качестве одного из побочных продуктов при переработке метана в электрической дуге. [39]
Страницы: 1 2 3
www.ngpedia.ru
Применение и получение предельных углеводородов
Л. А. Цветков
Применение углеводородов. Высокая теплота сгорания углеводородов обусловливает использование их в качестве топлива. Метан в составе природного газа находит все более широкое применение в быту и на производстве. Получило распространение применение пропана и бутана в виде «сжиженного газа», особенно в тех местностях, где нет подводки природного газа. Жидкие углеводороды используются как горючее для двигателей внутреннего сгорания в автомашинах, самолетах и т. д. Как весьма доступный углеводород, метан все в большей степени используется в качестве химического сырья.Реакции горения и разложения метана используются в производстве сажи, идущей на получение типографской краски и резиновых изделий из каучука. С этой целью в специальные печи вместе с метаном подают такое количество воздуха, чтобы сгорела лишь часть газа. Под действием развивающейся при горении высокой температуры другая часть разлагается, образуя тонкодисперсную сажу.
Метан — основной источник получения водорода в промышленности для синтеза аммиака и ряда органических соединений. Наиболее распространенный способ получения водорода из метана — взаимодействие его с водяным паром. Реакцию проводят в трубчатых печах при температуре около 400°C, давлении 2–3 МПа, в присутствии алюмоникелевого катализатора:CH4 + H2O —> 3H2 + CO
Для некоторых синтезов Используется непосредственно образующаяся смесь газов. Если же для последующих процессов нужен чистый водород (как в случае получения аммиака), оксид углерода (II) окисляют водяным паром, используя катализаторы.
Реакцией хлорирования получают хлорпроизводные метана. Все они находят практическое применение.
Хлорметан CH3Cl — газ. Как вещество, легко переходящее в жидкое состояние и поглощающее большое количество теплоты при последующем испарении, он применяется в качестве хладагента в холодильных установках.
Дихлорметан CH2Cl2, трихлорметан (хлороформ) CHCl3 и тетрахлорметан CCl4 — жидкости; они используются как растворители. Тетрахлорметан применяется, кроме того, при тушении огня (особенно в тех случаях, когда нельзя использовать воду), так как тяжелые негорючие пары этого вещества, образующиеся при испарении жидкости, быстро изолируют горящий предмет от кислорода воздуха.
При хлорировании метана образуется много хлороводорода. Растворяя его в воде, получают соляную кислоту.
В последнее время из метана получают ацетилен, необходимый для синтеза многих органических веществ.
Из гомологов метана при реакции изомеризации получают углеводороды разветвленного строения. Они используются в производстве каучуков и высококачественных сортов бензина. Высшие углеводороды служат исходными веществами для получения синтетических моющих средств.
Путем химической переработки предельные углеводороды часто превращают в непредельные углеводороды, химически более активные, из которых синтезируют многочисленные органические вещества.
Получение углеводородов. Предельные углеводороды в больших количествах содержатся в природном газе и нефти. Из этих природных источников и извлекают их для использования в качестве топлива и химического сырья.
В теоретическом отношении интересна реакция синтеза метана, так как она показывает возможность перехода от простых веществ к органическим соединениям. Реакция идет при нагревании углерода с водородом в присутствии порошкообразного никеля в качестве катализатора:
С + 2H2 —> CH4
Сопоставляя эту реакцию с термическим разложением метана, мы должны сделать вывод, что она обратима. Учитывая тепловой эффект реакции, можно записать следующее уравнение:
C + 2H2 <—> CH4 + 75 кДж
На основании данного уравнения можно высказать предположение о том, какие условия способствуют сдвигу равновесия в сторону получения метана, а какие будут вызывать его разложение. Так как синтез метана — реакция экзотермическая, то сильное нагревание не будет повышать выход продукта; равновесие сместится в сторону образования исходных веществ. При слабом нагревании будет недостаточна скорость образования метана. Поэтому оптимальная температура синтеза метана примерно 500°C, а для его разложения необходима температура свыше 1000°C.
На смещение равновесия влияет и изменение давления. Так как слева направо реакция идет с уменьшением объемов газов, то повышение давления будет способствовать образованию метана, а уменьшение — разложению его.
<<<
w-rabbit.narod.ru
