Формула белого фосфора в химии
Определение и формула белого фосфора
Метастабильный, при комнатной температуре мягкий как воск (режется ножом), на холоду – хрупкий. Плавится и кипит без разложения, летучий при слабом нагревании, перегоняется с водяным паром. Медленно окисляется на воздухе (цепная реакция с участием радикалов, хемилюминесценция), при слабом нагревании воспламеняется в присутствии кислорода. Хорошо растворяется в сероуглероде, аммиаке, оксиде серы (IV), плохо – в тетрахлориде углерода. Не растворяется в воде, хорошо сохраняется под слоем воды.
Рис. 1. Белый фосфор. Внешний вид.
Химическая формула белого фосфора
Химическая формула белого фосфора – P4. Она показывает, что в составе молекулы этого вещества находится четыре атома фосфора (Ar = 31 а.е.м.). По химической формуле можно вычислить молекулярную массу белого фосфора:
Mr(P4) = 2×Ar(P) = 4×31 = 124
Структурная (графическая) формула белого фосфора
Более наглядной является структурная (графическая) формула белого фосфора
Электронная формула
Электронная формула, показывающая распределение электронов в атоме по энергетическим подуровням показана ниже:
15P 1s22s22p63s23p3
Она также показывает, что фосфор относится к элементам р-семейства, а также число валентных электронов — на внешнем энергетическом уровне находится 5 электронов (3s23p3).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Белый фосфор Википедия
| Фосфор | |
|---|---|
| ← Кремний | Сера → | |
|
Белый, красный и фиолетовый фосфор |
|
| Название, символ, номер | Фосфор/ Phosphorus (P), 15 |
| Атомная масса (молярная масса) |
30,973762(2)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p3 |
| Радиус атома | 128 пм |
| Ковалентный радиус | 106 пм |
| Радиус иона | 35 (+5e) 212 (-3e) пм |
| Электроотрицательность | 2,19 [2] (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | 5, 3, 1, 0, −1, −3[3] |
| Энергия ионизации (первый электрон) |
1011,2(10,48) кДж/моль (эВ) |
| Плотность (при н. у.) | (белый фосфор)1,82 г/см³ |
| Температура плавления | 44,15 °C (317,3 K) |
| Температура кипения | 279,85 °C (553 K) |
| Уд. теплота плавления | 2,51 кДж/моль |
| Уд. теплота испарения | 49,8 кДж/моль |
| Молярная теплоёмкость | 21,6[4] (ромбич.) Дж/(K·моль) |
| Молярный объём | 17,0 см³/моль |
| Структура решётки | кубическая, объёмноцентрированная |
| Параметры решётки | 18,800 Å |
| Теплопроводность | (300 K) (0,236) Вт/(м·К) |
| Номер CAS | 7723-14-0 |
История
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень, а получил светящееся вещество. Бранд сфокусировался на опытах с человеческой мочой, так как полагал, что она, обладая золотистым цветом, может содержать золото или нечто нужное для его добычи. Первоначально его способ заключался в том, что сначала моча отстаивалась в течение нескольких дней, пока не исчезнет неприятный запах, а затем кипятилась до клейкого состояния. Нагревая эту пасту до высоких температур и доводя до появления пузырьков, он надеялся, что, сконденсировавшись, они будут содержать золото. После нескольких часов интенсивных кипячений получались крупицы белого воскоподобного вещества, которое очень ярко горело и к тому же мерцало в темноте. Бранд назвал это вещество

Несколько позже фосфор был получен другим немецким химиком — Иоганном Кункелем.
Независимо от Бранда и Кункеля фосфор был получен Р. Бойлем, описавшим его в статье «Способ приготовления фосфора из человеческой мочи», датированной 14 октября 1680 года и опубликованной в 1693 году.
Более усовершенствованный способ получения фосфора был опубликован в 1743 году Андреасом Маргграфом.
Существуют данные, что фосфор умели получать ещё арабские алхимики в XII в.
То, что фосфор — простое вещество, доказал Лавуазье.
Аморфную аллотропную модификацию фосфора — красный фосфор Pn — выделил, нагревая белый фосфор без доступа воздуха, А. Шрёттер в середине XIX в.
Происхождение названия
В 1669 году Хеннинг Бранд при нагревании смеси белого песка и выпаренной мочи получил светящееся в темноте вещество, названное сначала «холодным огнём». Вторичное название «фосфор» происходит от греческих слов «φώς» — свет и «φέρω» — несу. В древнегреческой мифологии имя Фосфор (или Эосфор, др.-греч. Φωσφόρος) носил страж Утренней звезды.
Получение
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре около 1600 °С:
- 2Ca3(PO4)2+10C+6SiO2→P4+10CO+6CaSiO3{\displaystyle {\mathsf {2Ca_{3}(PO_{4})_{2}+10C+6SiO_{2}\rightarrow P_{4}+10CO+6CaSiO_{3}}}} или Ca3(PO4)2 + 3SiO2+5C = 3CaSiO3+5CO+2P.
Образующиеся пары фосфора конденсируются в приёмнике под слоем воды в аллотропическую модификацию в виде белого фосфора. Вместо фосфоритов для получения элементарного фосфора можно восстанавливать углём и другие неорганические соединения фосфора, например, в том числе, метафосфорную кислоту:
- 4HPO3+10C→P4+2h3O+10CO{\displaystyle {\mathsf {4HPO_{3}+10C\rightarrow P_{4}+2H_{2}O+10CO}}}
Физические свойства
Элементарный фосфор при нормальных условиях существует в виде нескольких устойчивых аллотропических модификаций. Все существующие аллотропные модификации фосфора пока (2016 г.) до конца не изучены. Традиционно различают четыре его модификации: зеленовато-белый, красный, чёрный и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные описываемые модификации являются смесью этих четырёх. При стандартных условиях устойчивы только три аллотропических модификации фосфора (например, белый фосфор термодинамически неустойчив (квазистационарное состояние) и переходит со временем при нормальных условиях в красный фосфор). В условиях сверхвысоких давлений термодинамически устойчива металлическая форма элемента. Все модификации различаются по цвету, плотности и другим физическим и химическим характеристикам, особенно по химической активности. При переходе состояния вещества в более термодинамически устойчивую модификацию снижается химическая активность, например, при последовательном превращении белого фосфора в красный, потом красного в чёрный (металлический).
 Аллотропные модификации фосфора (белый, красный, чёрный, металлический)
Аллотропные модификации фосфора (белый, красный, чёрный, металлический)
Белый фосфор
Белый фосфор представляет собой белое вещество (из-за примесей может иметь желтоватый оттенок). По внешнему виду он очень похож на очищенный воск или парафин, легко режется ножом и деформируется от небольших усилий.
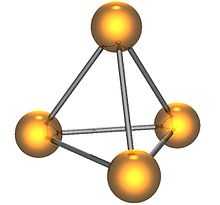 Молекула белого фосфора
Молекула белого фосфора
Белый фосфор имеет молекулярную кристаллическую решётку, формула молекулы белого фосфора — P4, причём атомы расположены в вершинах тетраэдра[6]. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствии воздуха под слоем очищенной воды или в специальных инертных средах.
Плохо растворяется в воде[6], но легкорастворим в органических растворителях. Растворимостью белого фосфора в сероуглероде пользуются для промышленной очистки его от примесей. Плотность белого фосфора из всех его модификаций наименьшая и составляет около 1823 кг/м³. Плавится белый фосфор при 44,1 °C. В парообразном состоянии происходит диссоциация молекул фосфора.
Химически белый фосфор чрезвычайно активен. Например, он медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение). Явление такого рода свечения вследствие химических реакций окисления называется хемилюминесценцией (иногда ошибочно фосфоресценцией). При взаимодействии с кислородом белый фосфор горит даже под водой[7].
Белый фосфор не только активен химически, но и весьма ядовит: летальная доза белого фосфора для взрослого человека составляет 0,05—0,15 г[4], а при хроническом отравлении поражает кости, например, вызывает омертвение челюстей[4]. При контакте с кожей легко самовоспламеняется, вызывая серьёзные ожоги[8]
Под действием света, при нагревании до не очень высоких температур в безвоздушной среде[6], а также под действием ионизирующего излучения[10] белый фосфор превращается в красный фосфор.
Жёлтый фосфор
Неочищенный белый фосфор обычно называют «жёлтый фосфор». Сильно ядовитое (ПДК в атмосферном воздухе 0,0005 мг/м³), огнеопасное кристаллическое вещество от светло-жёлтого до тёмно-бурого цвета. Плотность 1,83 г/см³, плавится при +43,1 °C, кипит при +280 °C. В воде не растворяется, на воздухе легко окисляется и самовоспламеняется. Горит ослепительным ярко-зёленым пламенем с выделением густого белого дыма — мелких частичек декаоксида тетрафосфора P4O10[11].
Так как фосфор реагирует с водой лишь при температуре свыше 500 °C, то для тушения фосфора используют воду в больших количествах (для снижения температуры очага возгорания и перевода фосфора в твёрдое состояние) или раствор сульфата меди (медного купороса), после гашения фосфор засыпают влажным песком. Для предохранения от самовозгорания жёлтый фосфор хранится и перевозится под слоем воды (раствора хлорида кальция)[12].
Красный фосфор
Красный фосфорКрасный фосфор — это более термодинамически стабильная модификация элементарного фосфора. Впервые он был получен в 1847 году в Швеции австрийским химиком А. Шрёттером при нагревании белого фосфора при 500 °С в атмосфере угарного газа (СО) в запаянной стеклянной ампуле.
Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления, красный фосфор имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком, имеет металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Растворить красный фосфор возможно лишь в некоторых расплавленных металлах (свинец и висмут), чем иногда пользуются для получения крупных его кристаллов. Так, например, немецкий физико-химик И. В. Гитторф в 1865 году впервые получил прекрасно построенные, но небольшие по размеру кристаллы (фосфор Гитторфа). Красный фосфор на воздухе не самовоспламеняется, вплоть до температуры 240—250 °С (при переходе в белую форму во время возгонки), но самовоспламеняется при трении или ударе, у него полностью отсутствует явление хемилюминесценции. Нерастворим в воде, а также в бензоле, сероуглероде и других веществах, растворим в трибромиде фосфора. При температуре возгонки красный фосфор превращается в пар, при охлаждении которого образуется в основном белый фосфор.
Ядовитость его в тысячи раз меньше, чем у белого, поэтому он применяется гораздо шире, например, в производстве спичек (составом на основе красного фосфора покрыта тёрочная поверхность коробков). Плотность красного фосфора также выше, и достигает 2400 кг/м³ в литом виде. При хранении на воздухе красный фосфор в присутствии влаги постепенно окисляется, образуя гигроскопичный оксид, поглощает воду и отсыревает («отмокает»), образуя вязкую фосфорную кислоту; поэтому его хранят в герметичной таре. При «отмокании» — промывают водой от остатков фосфорных кислот, высушивают и используют по назначению.
Чёрный фосфор
Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. Для проведения синтеза чёрного фосфора Бриджмен применил давление в 2⋅109 Па (20 тысяч атмосфер) и температуру около 200 °С. Начало быстрого перехода лежит в области 13 000 атмосфер и температуре около 230 °С.
Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Чёрный фосфор проводит электрический ток и имеет свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 1,8⋅106 Па.
Металлический фосфор
При 8,3⋅1010 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу с плотностью 3,56 г/см³, а при дальнейшем повышении давления до 1,25⋅1011 Па — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает до 3,83 г/см³. Металлический фосфор очень хорошо проводит электрический ток.
Химические свойства
Химическая активность фосфора значительно выше, чем у азота. Химические свойства фосфора во многом определяются его аллотропной модификацией. Белый фосфор очень активен, в процессе перехода к красному и чёрному фосфору химическая активность снижается. Белый фосфор в воздухе при окислении кислородом воздуха при комнатной температуре излучает видимый свет, свечение обусловлено фотоэмиссионной реакцией окисления фосфора.
В жидком и растворенном состоянии, а также в парах до 800 °С фосфор состоит из молекул Р4. При нагревании выше 800 °С молекулы диссоциируют: Р4 = 2Р2. При температуре выше 2000 °С молекулы распадаются на атомы.
Взаимодействие с простыми веществами
Фосфор легко окисляется кислородом:
- 4P+5O2→2P2O5{\displaystyle {\mathsf {4P+5O_{2}\rightarrow 2P_{2}O_{5}}}} (с избытком кислорода)
- 4P+3O2→2P2O3{\displaystyle {\mathsf {4P+3O_{2}\rightarrow 2P_{2}O_{3}}}} (при медленном окислении или при недостатке кислорода)
Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и восстановительные свойства:
с металлами — окислитель, образует фосфиды:
- 2P+3Ca→Ca3P2{\displaystyle {\mathsf {2P+3Ca\rightarrow Ca_{3}P_{2}}}}
фосфиды разлагаются водой и кислотами с образованием фосфина
с неметаллами — восстановитель:
- 2P+3S→P2S3{\displaystyle {\mathsf {2P+3S\rightarrow P_{2}S_{3}}}}
- 2P+5Cl2→2PCl5{\displaystyle {\mathsf {2P+5Cl_{2}\rightarrow 2PCl_{5}}}}
С водородом фосфор практически не соединяется. Однако разложением некоторых фосфидов водой по реакции, например:
- Ca3P2+6h3O→2Ph4+3Ca(OH)2{\displaystyle {\mathsf {Ca_{3}P_{2}+6H_{2}O\rightarrow 2PH_{3}+3Ca(OH)_{2}}}}
может быть получен аналогичный аммиаку фосфористый водород (фосфин) — РH3
Взаимодействие с водой
Взаимодействует с водяным паром при температуре выше 500 °С, протекает реакция диспропорционирования с образованием фосфина и фосфорной кислоты:
- 8P+12h3O→>500oC 5Ph4+3h4PO4{\displaystyle {\mathsf {8P+12H_{2}O{\xrightarrow {>500^{o}C}}\ 5PH_{3}+3H_{3}PO_{4}}}}
Реакция взаимодействия красного фосфора и воды с образованием ортофосфорной кислоты и водорода. Реакция протекает при температуре 700—900 °C. Катализатором могут выступать: платина, медь, титан, цирконий.[1]
- 2P+8h3O→700−900oC,kat 2h4PO4+5h3{\displaystyle {\mathsf {2P+8H_{2}O{\xrightarrow {700-900^{o}C,kat}}\ 2H_{3}PO_{4}+5H_{2}}}}
Взаимодействие со щелочами
В холодных концентрированных растворах щелочей также медленно протекает реакция диспропорционирования[13]:
- 4P+3KOH+3h3O→ τ Ph4+3Kh3PO2{\displaystyle {\mathsf {4P+3KOH+3H_{2}O{\xrightarrow {\ \tau \ }}PH_{3}+3KH_{2}PO_{2}}}}
Восстановительные свойства
Сильные окислители превращают фосфор в фосфорную кислоту:
- 3P+5HNO3+2h3O→3h4PO4+5NO{\displaystyle {\mathsf {3P+5HNO_{3}+2H_{2}O\rightarrow 3H_{3}PO_{4}+5NO}}}
- 2P+5h3SO4→2h4PO4+5SO2+2h3O{\displaystyle {\mathsf {2P+5H_{2}SO_{4}\rightarrow 2H_{3}PO_{4}+5SO_{2}+2H_{2}O}}}
Реакция окисления фосфора происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль:
- 6P+5KClO3→5KCl+3P2O5{\displaystyle {\mathsf {6P+5KClO_{3}\rightarrow 5KCl+3P_{2}O_{5}}}}
Изотопы
Известно более 20 изотопов фосфора (с массовым числом от 24 до 47). Природный изотоп 31P стабилен. Из радиоактивных изотопов наиболее долгоживущие: 30P (T1/2 = 2,5 мин), 32P (T1/2 = 14,26 сут) и 33P (T1/2 = 25,34 сут).[14].
Применение
Фосфор является важнейшим биогенным элементом и в то же время находит очень широкое применение в промышленности. Красный фосфор применяют в производстве спичек. Его вместе с тонко измельчённым стеклом и клеем наносят на боковую поверхность коробки. При трении спичечной головки, в состав которой входят хлорат калия и сера, происходит воспламенение.
Элементарный фосфор
Пожалуй, первое свойство фосфора, которое человек поставил себе на службу, — это горючесть. Горючесть фосфора очень велика и зависит от аллотропической модификации.
Наиболее активен химически, токсичен и горюч белый («жёлтый») фосфор, потому он очень часто применяется (в зажигательных бомбах и пр.).
Красный фосфор — основная модификация, производимая и потребляемая промышленностью. Он применяется в производстве спичек, взрывчатых веществ, зажигательных составов, различных типов топлива, а также противозадирных смазочных материалов, в качестве газопоглотителя в производстве ламп накаливания.
Соединения фосфора в сельском хозяйстве
Фосфор (в виде фосфатов) — один из трёх важнейших биогенных элементов, участвует в синтезе АТФ. Большая часть производимой фосфорной кислоты идёт на получение фосфорных удобрений — суперфосфата, преципитата, аммофоски и др.
Соединения фосфора в промышленности
Фосфаты широко используются:
Фосфатные связующие
Способность фосфатов формировать прочную трёхмерную полимерную сетку используется для изготовления фосфатных и алюмофосфатных связок.
Биологическая роль соединений фосфора
Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)2·Ca(OH)2. В состав зубной эмали входит фторапатит. Основную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D. При недостатке фосфора в организме развиваются различные заболевания костей.
Суточная потребность в фосфоре составляет:
- для взрослых 1,0—2,0 г
- для беременных и кормящих женщин 3—3,8 г
- для детей и подростков 1,5—2,5 г
При больших физических нагрузках потребность в фосфоре возрастает в 1,5—2 раза.
Усвоение происходит эффективнее при приёме фосфора вместе с кальцием в соотношении 3:2 (P:Ca).
Некоторые источники[15]:
Токсикология элементарного фосфора
- Красный фосфор практически нетоксичен (токсичность ему придают примеси белого фосфора). Пыль красного фосфора, попадая в легкие, вызывает пневмонию при хроническом действии.
- Белый фосфор очень ядовит, растворим в липидах. Смертельная доза белого фосфора — 50—150 мг. Попадая на кожу, тлеющий белый фосфор даёт тяжелые ожоги.
Острые отравления фосфором проявляются жжением во рту и желудке, головной болью, слабостью, рвотой. Через 2—3 суток развивается желтуха. Для хронических форм характерны нарушение кальциевого обмена, поражение сердечно-сосудистой и нервной систем. Первая помощь при остром отравлении — промывание желудка, слабительное, очистительные клизмы, внутривенно растворы глюкозы. При ожогах кожи обработать поражённые участки растворами медного купороса или соды. ПДК паров фосфора в воздухе производственных помещений — 0,03 мг/м³, временно допустимая концентрация в атмосферном воздухе — 0,0005 мг/м³, ПДК в питьевой воде — 0,0001 мг/дм³[17] .
Токсикология соединений фосфора
Некоторые соединения фосфора (фосфин) очень токсичны. Ввиду высокой (ЛД50 15-100 мг/кг) и чрезвычайно высокой (<15 мг/кг) токсичности большинство фосфорорганических соединений (ФОС) используются в качестве пестицидов (инсектициды, акарициды, зооциды и т. д.) или боевых отравляющих веществ. Примером боевых отравляющих веществ являются — зарин, зоман, табун, новичок, V-газы.
ФОС проявляют свойства веществ нервно-паралитического действия. Токсичность фосфорорганических соединений обусловлена ингибированием фермента ацетилхолинэстеразы, вследствие чего развивается головная боль, тошнота, головокружение, сужение зрачков (миоз), затруднение дыхания (отдышка), возникает слюнотечение, понижается артериальное давление, возникают конвульсии, проявляется паралитическое воздействие, кома, и как следствие может быстро возникнуть летальный исход. Эффективным антидотом при отравлении ФОС является атропин.
Опасность для здоровья
Рейтинг NFPA 704:
Фосфор относится к 1-му классу опасности.
Примечания
- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047—1078. — DOI:10.1351/PAC-REP-13-03-02.
- ↑ Phosphorus: electronegativities (англ.). WebElements. Дата обращения 15 июля 2010.
- ↑ Sulfur and Phosphorus Compounds (англ.). Дата обращения 27 января 2010. Архивировано 22 августа 2011 года.
- ↑ 1 2 3 Редкол.:Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. — Москва: Большая Российская энциклопедия, 1999. — Т. 5. — С. 145.
- ↑ J.P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- ↑ 1 2 3 Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 30. Фосфор // Неорганическая химия. Учебник для 9 класса. — 7-е изд. — М.: Просвещение, 1976. — С. 62—65. — 2 350 000 экз.
- ↑ Горение белого фосфора под водой — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ Kemal T. Saracoglu, Ahmet H. Acar, Tamer Kuzucuoglu, Sezer Yakupoglu. White phosphorus burn (англ.) // The Lancet. — 2010. — Vol. 376, no. 9734. — P. 68. — DOI:10.1016/S0140-6736(10)60812-4.
- ↑ Chou TD, Lee TW, Chen SL, Tung YM, Dai NT, Chen SG, Lee CH, Chen TM, Wang HJ. The management of white phosphorus burns (англ.) // Burns. — 2001. — Vol. 27, iss. 5. — P. 492—497. — DOI:10.1016/S0305-4179(01)00003-1. — PMID 11451604.
- ↑ Радиационная химия // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — С. 200. — ISBN 5-7155-0292-6.
- ↑ В. Шретер, К.-Х. Лаутеншлегер, Х. Бибрак и др. Химия = Chemie. — М.: Химия, 1989. — С. 351. — ISBN 5-7245-0360-3.
- ↑ Химическая энциклопедия / Редкол.: Зефиров Н. С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9.
- ↑ Лидин Р.А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- ↑ Данные приведены по Audi G., Bersillon O., Blachot J., Wapstra A. H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. — 2003. — Т. 729. — С. 3—128. — DOI:10.1016/j.nuclphysa.2003.11.001. — Bibcode: 2003NuPhA.729….3A.
- ↑ USDA
- ↑ Буланов Ю. Б. Химический состав продуктов. Пищевая ценность.
- ↑ УНИАН — здоровье — Что происходит с фосфором?
Ссылки
wikiredia.ru
Ответы Mail.ru: химическая формула красного фосфора
Красный фосфор, также называемый фиолетовым фосфором, — это более термодинамически стабильная модификация элементарного фосфора. Впервые он был получен в 1847 году в Швеции австрийским химиком А. Шрёттером при нагревании белого фосфора при 500 °С в атмосфере угарного газа (СО) в запаянной стеклянной ампуле.Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления красного фосфора, имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Растворить красный фосфор возможно лишь в некоторых расплавленных металлах (свинец и висмут) , чем иногда пользуются для получения крупных его кристаллов. Так, например, немецкий физико-химик И. В. Гитторф в 1865 году впервые получил прекрасно построенные, но небольшие по размеру кристаллы (фосфор Гитторфа) . Красный Фосфор на воздухе не самовоспламеняется, вплоть до температуры 240—250 °С (при переходе в белую форму во время возгонки) , но самовоспламеняется при трении или ударе, у него полностью отсутствует явление хемолюминесценции. Нерастворим в воде, а также в бензоле, сероуглероде и других, растворим в трибромиде фосфора. При температуре возгонки красный фосфор превращается в пар, при охлаждении которого образуется в основном белый фосфор.
Ядовитость его в тысячи раз меньше, чем у белого, поэтому он применяется гораздо шире, например, в производстве спичек (составом на основе красного фосфора покрыта тёрочная поверхность коробков) . Плотность красного фосфора также выше, и достигает 2400 кг/м³ в литом виде. При хранении на воздухе красный фосфор в присутствии влаги постепенно окисляется, образуя гигроскопичный оксид, поглощает воду и отсыревает («отмокает») , образуя вязкую фосфорную кислоту; поэтому его хранят в герметичной таре. При «отмокании» — промывают водой от остатков фосфорных кислот, высушивают и используют по назначению.
otvet.mail.ru
Формула красного фосфора в химии
Определение и формула красного фосфора
Цвет определяется способом получения и степенью дробления вещества. Имеет металлический блеск. При нагревании возгоняется. Окисляется на воздухе. Не растворяется в воде и сероуглерода. Химическая активность красного фосфора значительно меньше, чем белого и черного. Растворяется в расплаве свинца, из которого кристаллизуется фиолетовый фосфор (фосфор Гитторфа).

Рис. 1. Красный фосфор. Внешний вид.
Химическая формула красного фосфора
Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой.
Графическая (структурная) формула красного фосфора
Структурная (графическая) формула полимера красного фосфора является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
Электронная формула
Электронная формула, показывающая распределение электронов в атоме по энергетическим подуровням показана ниже:
15P 1s22s22p63s23p3
Она также показывает, что фосфор относится к элементам р-семейства, а также число валентных электронов — на внешнем энергетическом уровне находится 5 электронов (3s23p3).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Белый фосфор Вики
| Фосфор | |
|---|---|
| ← Кремний | Сера → | |
|
Белый, красный и фиолетовый фосфор |
|
| Название, символ, номер | Фосфор/ Phosphorus (P), 15 |
| Атомная масса (молярная масса) |
30,973762(2)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p3 |
| Радиус атома | 128 пм |
| Ковалентный радиус | 106 пм |
| Радиус иона | 35 (+5e) 212 (-3e) пм |
| Электроотрицательность | 2,19 [2] (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | 5, 3, 1, 0, −1, −3[3] |
| Энергия ионизации (первый электрон) |
1011,2(10,48) кДж/моль (эВ) |
| Плотность (при н. у.) | (белый фосфор)1,82 г/см³ |
| Температура плавления | 44,15 °C (317,3 K) |
| Температура кипения | 279,85 °C (553 K) |
| Уд. теплота плавления | 2,51 кДж/моль |
| Уд. теплота испарения | 49,8 кДж/моль |
| Молярная теплоёмкость | 21,6[4] (ромбич.) Дж/(K·моль) |
| Молярный объём | 17,0 см³/моль |
| Структура решётки | кубическая, объёмноцентрированная |
| Параметры решётки | 18,800 Å |
| Теплопроводность | (300 K) (0,236) Вт/(м·К) |
| Номер CAS | 7723-14-0 |
Фо́сфор (от др.-греч. φῶς — свет и φέρω — несу; φωσφόρος — светоносный; лат. Phosphorus) — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) третьего периода периодической системы Д. И. Менделеева; имеет атомный номер 15. Элемент входит в группу пниктогенов. Фосфор — один из распространённых элементов земной коры: его содержание составляет 0,08—0,09 % её массы. Концентрация в морской воде 0,07 мг/л[5]. В свободном состоянии не встречается из-за высокой химической активности. Образует около 190 минералов, важнейшими из которых являются апатит Ca5(PO4)3 (F,Cl,OH), фосфорит (Сa3(PO4)2) и другие. Фосфор входит в состав важнейших биологических соединений — фосфолипидов. Содержится в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ, ДНК), является элементом жизни.
История[ | код]
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень, а получил светящееся вещество. Бранд сфокусировался на опытах с человеческой мочой, так как полагал, что она, обладая золотистым цветом, может содержать золото или нечто нужное для его добычи. Первоначально его способ заключался в том, что сначала моча отстаивалась в течение нескольких дней, пока не исчезнет неприятный запах, а затем кипятилась до клейкого состояния. Нагревая эту пасту до высоких температур и доводя до появления пузырьков, он надеялся, что, сконденсировавшись, они будут содержать золото. После нескольких часов интенсивных кипячений получались крупицы белого воскоподобного вещества, которое очень ярко горело и к тому же мерцало в темноте. Бранд назвал это вещество phosphorus mirabilis (лат. «чудотворный носитель света»). Открытие фосфора Брандом стало первым открытием нового элемента со времён античности.

Несколько позже фосфор был получен другим немецким химиком — Иоганном Кункелем.
Независимо от Бранда и Кункеля фосфор был получен Р. Бойлем, описавшим его в статье «Способ приготовления фосфора из человеческой мочи», датированной 14 октября 1680 года и опубликованной в 1693 году.
Более усовершенствованный способ получения фосфора был опубликован в 1743 году Андреасом Маргграфом.
Существуют данные, что фосфор умели получать ещё арабские алхимики в XII в.
То, что фосфор — простое вещество, доказал Лавуазье.
Аморфную аллотропную модификацию фосфора — красный фосфор Pn — выделил, нагревая белый фосфор без доступа воздуха, А. Шрёттер в середине XIX в.
Происхождение названия[ | код]
В 1669 году Хеннинг Бранд при нагревании смеси белого песка и выпаренной мочи получил светящееся в темноте вещество, названное сначала «холодным огнём». Вторичное название «фосфор» происходит от греческих слов «φώς» — свет и «φέρω» — несу. В древнегреческой мифологии имя Фосфор (или Эосфор, др.-греч. Φωσφόρος) носил страж Утренней звезды.
Получение[ | код]
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре около 1600 °С:
- 2Ca3(PO4)2+10C+6SiO2→P4+10CO+6CaSiO3{\displaystyle {\mathsf {2Ca_{3}(PO_{4})_{2}+10C+6SiO_{2}\rightarrow P_{4}+10CO+6CaSiO_{3}}}} или Ca3(PO4)2 + 3SiO2+5C = 3CaSiO3+5CO+2P.
Образующиеся пары фосфора конденсируются в приёмнике под слоем воды в аллотропическую модификацию в виде белого фосфора. Вместо фосфоритов для получения элементарного фосфора можно восстанавливать углём и другие неорганические соединения фосфора, например, в том числе, метафосфорную кислоту:
- 4HPO3+10C→P4+2h3O+10CO{\displaystyle {\mathsf {4HPO_{3}+10C\rightarrow P_{4}+2H_{2}O+10CO}}}
Физические свойства[ | код]
Элементарный фосфор при нормальных условиях существует в виде нескольких устойчивых аллотропических модификаций. Все существующие аллотропные модификации фосфора пока (2016 г.) до конца не изучены. Традиционно различают четыре его модификации: зеленовато-белый, красный, чёрный и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные описываемые модификации являются смесью этих четырёх. При стандартных условиях устойчивы только три аллотропических модификации фосфора (например, белый фосфор термодинамически неустойчив (квазистационарное состояние) и переходит со временем при нормальных условиях в красный фосфор). В условиях сверхвысоких давлений термодинамически устойчива металлическая форма элемента. Все модификации различаются по цвету, плотности и другим физическим и химическим характеристикам, особенно по химической активности. При переходе состояния вещества в более термодинамически устойчивую модификацию снижается химическая активность, например, при последовательном превращении белого фосфора в красный, потом красного в чёрный (металлический).
 Аллотропные модификации фосфора (белый, красный, чёрный, металлический)
Аллотропные модификации фосфора (белый, красный, чёрный, металлический)
Белый фосфор[ | код]
Белый фосфор представляет собой белое вещество (из-за примесей может иметь желтоватый оттенок). По внешнему виду он очень похож на очищенный воск или парафин, легко режется ножом и деформируется от небольших усилий.
 Молекула белого фосфора
Молекула белого фосфора
Белый фосфор имеет молекулярную кристаллическую решётку, формула молекулы белого фосфора — P4, причём атомы расположены в вершинах тетраэдра[6]. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствии воздуха под слоем очищенной воды или в специальных инертных средах.
Плохо растворяется в воде[6], но легкорастворим в органических растворителях. Растворимостью белого фосфора в сероуглероде пользуются для промышленной очистки его от примесей. Плотность белого фосфора из всех его модификаций наименьшая и составляет около 1823 кг/м³. Плавится белый фосфор при 44,1 °C. В парообразном состоянии происходит диссоциация молекул фосфора.
Химически белый фосфор чрезвычайно активен. Например, он медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение). Явление такого рода свечения вследствие химических реакций окисления называется хемилюминесценцией (иногда ошибочно фосфоресценцией). При взаимодействии с кислородом белый фосфор горит даже под водой[7].
Белый фосфор не только активен химически, но и весьма ядовит: летальная доза белого фосфора для взрослого человека составляет 0,05—0,15 г[4], а при хроническом отравлении поражает кости, например, вызывает омертвение челюстей[4]. При контакте с кожей легко самовоспламеняется, вызывая серьёзные ожоги[8][9].
Под действием света, при нагревании до не очень высоких температур в безвоздушной среде[6], а также под действием ионизирующего излучения[10] белый фосфор превращается в красный фосфор.
Жёлтый фосфор[ | код]
Неочищенный белый фосфор обычно называют «жёлтый фосфор». Сильно ядовитое (ПДК в атмосферном воздухе 0,0005 мг/м³), огнеопасное кристаллическое вещество от светло-жёлтого до тёмно-бурого цвета. Плотность 1,83 г/см³, плавится при +43,1 °C, кипит при +280 °C. В воде не растворяется, на воздухе легко окисляется и самовоспламеняется. Горит ослепительным ярко-зёленым пламенем с выделением густого белого дыма — мелких частичек декаоксида тетрафосфора P4O10[11].
Так как фосфор реагирует с водой лишь при температуре свыше 500 °C, то для тушения фосфора используют воду в больших количествах (для снижения температуры очага возгорания и перевода фосфора в твёрдое состояние) или раствор сульфата меди (медного купороса), после гашения фосфор засыпают влажным песком. Для предохранения от самовозгорания жёлтый фосфор хранится и перевозится под слоем воды (раствора хлорида кальция)[12].
Красный фосфор[ | код]
Красный фосфорКрасный фосфор — это более термодинамически стабильная модификация элементарного фосфора. Впервые он был получен в 1847 году в Швеции австрийским химиком А. Шрёттером при нагревании белого фосфора при 500 °С в атмосфере угарного газа (СО) в запаянной стеклянной ампуле.
Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления, красный фосфор имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком, имеет металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Растворить красный фосфор возможно лишь в некоторых расплавленных металлах (свинец и висмут), чем иногда пользуются для получения крупных его кристаллов. Так, например, немецкий физико-химик И. В. Гитторф в 1865 году впервые получил прекрасно построенные, но небольшие по размеру кристаллы (фосфор Гитторфа). Красный фосфор на воздухе не самовоспламеняется, вплоть до температуры 240—250 °С (при переходе в белую форму во время возгонки), но самовоспламеняется при трении или ударе, у него полностью отсутствует явление хемилюминесценции. Нерастворим в воде, а также в бензоле, сероуглероде и других веществах, растворим в трибромиде фосфора. При температуре возгонки красный фосфор превращается в пар, при охлаждении которого образуется в основном белый фосфор.
Ядовитость его в тысячи раз меньше, чем у белого, поэтому он применяется гораздо шире, например, в производстве спичек (составом на основе красного фосфора покрыта тёрочная поверхность коробков). Плотность красного фосфора также выше, и достигает 2400 кг/м³ в литом виде. При хранении на воздухе красный фосфор в присутствии влаги постепенно окисляется, образуя гигроскопичный оксид, поглощает воду и отсыревает («отмокает»), образуя вязкую фосфорную кислоту; поэтому его хранят в герметичной таре. При «отмокании» — промывают водой от остатков фосфорных кислот, высушивают и используют по назначению.
Чёрный фосфор[ | код]
Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. Для проведения синтеза чёрного фосфора Бриджмен применил давление в 2⋅109 Па (20 тысяч атмосфер) и температуру около 200 °С. Начало быстрого перехода лежит в области 13 000 атмосфер и температуре около 230 °С.
Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Чёрный фосфор проводит электрический ток и имеет свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 1,8⋅106 Па.
Металлический фосфор[ | код]
При 8,3⋅1010 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу с плотностью 3,56 г/см³, а при дальнейшем повышении давления до 1,25⋅1011 Па — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает до 3,83 г/см³. Металлический фосфор очень хорошо проводит электрический ток.
Химические свойства[ | код]
Химическая активность фосфора значительно выше, чем у азота. Химические свойства фосфора во многом определяются его аллотропной модификацией. Белый фосфор очень активен, в процессе перехода к красному и чёрному фосфору химическая активность снижается. Белый фосфор в воздухе при окислении кислородом воздуха при комнатной температуре излучает видимый свет, свечение обусловлено фотоэмиссионной реакцией окисления фосфора.
В жидком и растворенном состоянии, а также в парах до 800 °С фосфор состоит из молекул Р4. При нагревании выше 800 °С молекулы диссоциируют: Р4 = 2Р2. При температуре выше 2000 °С молекулы распадаются на атомы.
Взаимодействие с простыми веществами[ | код]
Фосфор легко окисляется кислородом:
- 4P+5O2→2P2O5{\displaystyle {\mathsf {4P+5O_{2}\rightarrow 2P_{2}O_{5}}}} (с избытком кислорода)
- 4P+3O2→2P2O3{\displaystyle {\mathsf {4P+3O_{2}\rightarrow 2P_{2}O_{3}}}} (при медленном окислении или при недостатке кислорода)
Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и восстановительные свойства:
с металлами — окислитель, образует фосфиды:
- 2P+3Ca→Ca3P2{\displaystyle {\mathsf {2P+3Ca\rightarrow Ca_{3}P_{2}}}}
фосфиды разлагаются водой и кислотами с образованием фосфина
с неметаллами — восстановитель:
- 2P+3S→P2S3{\displaystyle {\mathsf {2P+3S\rightarrow P_{2}S_{3}}}}
- 2P+5Cl2→2PCl5{\displaystyle {\mathsf {2P+5Cl_{2}\rightarrow 2PCl_{5}}}}
С водородом фосфор практически не соединяется. Однако разложением некоторых фосфидов водой по реакции, например:
- Ca3P2+6h3O→2Ph4+3Ca(OH)2{\displaystyle {\mathsf {Ca_{3}P_{2}+6H_{2}O\rightarrow 2PH_{3}+3Ca(OH)_{2}}}}
может быть получен аналогичный аммиаку фосфористый водород (фосфин) — РH3
Взаимодействие с водой[ | код]
Взаимодействует с водяным паром при температуре выше 500 °С, протекает реакция диспропорционирования с образованием фосфина и фосфорной кислоты:
- 8P+12h3O→>500oC 5Ph4+3h4PO4{\displaystyle {\mathsf {8P+12H_{2}O{\xrightarrow {>500^{o}C}}\ 5PH_{3}+3H_{3}PO_{4}}}}
Реакция взаимодействия красного фосфора и воды с образованием ортофосфорной кислоты и водорода. Реакция протекает при температуре 700—900 °C. Катализатором могут выступать: платина, медь, титан, цирконий.[1]
- 2P+8h3O→700−900oC,kat 2h4PO4+5h3{\displaystyle {\mathsf {2P+8H_{2}O{\xrightarrow {700-900^{o}C,kat}}\ 2H_{3}PO_{4}+5H_{2}}}}
Взаимодействие со щелочами[ | код]
В холодных концентрированных растворах щелочей также медленно протекает реакция диспропорционирования[13]:
- 4P+3KOH+3h3O→ τ Ph4+3Kh3PO2{\displaystyle {\mathsf {4P+3KOH+3H_{2}O{\xrightarrow {\ \tau \ }}PH_{3}+3KH_{2}PO_{2}}}}
Восстановительные свойства[ | код]
Сильные окислители превращают фосфор в фосфорную кислоту:
- 3P+5HNO3+2h3O→3h4PO4+5NO{\displaystyle {\mathsf {3P+5HNO_{3}+2H_{2}O\rightarrow 3H_{3}PO_{4}+5NO}}}
- 2P+5h3SO4→2h4PO4+5SO2+2h3O{\displaystyle {\mathsf {2P+5H_{2}SO_{4}\rightarrow 2H_{3}PO_{4}+5SO_{2}+2H_{2}O}}}
Реакция окисления фосфора происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль:
- 6P+5KClO3→5KCl+3P2O5{\displaystyle {\mathsf {6P+5KClO_{3}\rightarrow 5KCl+3P_{2}O_{5}}}}
Изотопы[ | код]
Известно более 20 изотопов фосфора (с массовым числом от 24 до 47). Природный изотоп 31P стабилен. Из радиоактивных изотопов наиболее долгоживущие: 30P (T1/2 = 2,5 мин), 32P (T1/2 = 14,26 сут) и 33P (T1/2 = 25,34 сут).[14].
Применение[ | код]
Фосфор является важнейшим биогенным элементом и в то же время находит очень широкое применение в промышленности. Красный фосфор применяют в производстве спичек. Его вместе с тонко измельчённым стеклом и клеем наносят на боковую поверхность коробки. При трении спичечной головки, в состав которой входят хлорат калия и сера, происходит воспламенение.
Элементарный фосфор[ | код]
Пожалуй, первое свойство фосфора, которое человек поставил себе на службу, — это горючесть. Горючесть фосфора очень велика и зависит от аллотропической модификации.
Наиболее активен химически, токсичен и горюч белый («жёлтый») фосфор, потому он очень часто применяется (в зажигательных бомбах и пр.).
Красный фосфор — основная модификация, производимая и потребляемая промышленностью. Он применяется в производстве спичек, взрывчатых веществ, зажигательных составов, различных типов топлива, а также противозадирных смазочных материалов, в качестве газопоглотителя в производстве ламп накаливания.
Соединения фосфора в сельском хозяйстве[ | код]
Фосфор (в виде фосфатов) — один из трёх важнейших биогенных элементов, участвует в синтезе АТФ. Большая часть производимой фосфорной кислоты идёт на получение фосфорных удобрений — суперфосфата, преципитата, аммофоски и др.
Соединения фосфора в промышленности[ | код]
Фосфаты широко используются:
Фосфатные связующие[ | код]
Способность фосфатов формировать прочную трёхмерную полимерную сетку используется для изготовления фосфатных и алюмофосфатных связок.
Биологическая роль соединений фосфора[ | код]
Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)2·Ca(OH)2. В состав зубной эмали входит фторапатит. Основную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D. При недостатке фосфора в организме развиваются различные заболевания костей.
Суточная потребность в фосфоре составляет:
- для взрослых 1,0—2,0 г
- для беременных и кормящих женщин 3—3,8 г
- для детей и подростков 1,5—2,5 г
При больших физических нагрузках потребность в фосфоре возрастает в 1,5—2 раза.
Усвоение происходит эффективнее при приёме фосфора вместе с кальцием в соотношении 3:2 (P:Ca).
Некоторые источники[15]:
Токсикология элементарного фосфора[ | код]
- Красный фосфор практически нетоксичен (токсичность ему придают примеси белого фосфора). Пыль красного фосфора, попадая в легкие, вызывает пневмонию при хроническом действии.
- Белый фосфор очень ядовит, растворим в липидах. Смертельная доза белого фосфора — 50—150 мг. Попадая на кожу, тлеющий белый фосфор даёт тяжелые ожоги.
Острые отравления фосфором проявляются жжением во рту и желудке, головной болью, слабостью, рвотой. Через 2—3 суток развивается желтуха. Для хронических форм характерны нарушение кальциевого обмена, поражение сердечно-сосудистой и нервной систем. Первая помощь при остром отравлении — промывание желудка, слабительное, очистительные клизмы, внутривенно растворы глюкозы. При ожогах кожи обработать поражённые участки растворами медного купороса или соды. ПДК паров фосфора в воздухе производственных помещений — 0,03 мг/м³, временно допустимая концентрация в атмосферном воздухе — 0,0005 мг/м³, ПДК в питьевой воде — 0,0001 мг/дм³[17] .
Токсикология соединений фосфора[ | код]
Некоторые соединения фосфора (фосфин) очень токсичны. Ввиду высокой (ЛД50 15-100 мг/кг) и чрезвычайно высокой (<15 мг/кг) токсичности большинство фосфорорганических соединений (ФОС) используются в качестве пестицидов (инсектициды, акарициды, зооциды и т. д.) или боевых отравляющих веществ. Примером боевых отравляющих веществ являются — зарин, зоман, табун, новичок, V-газы.
ФОС проявляют свойства веществ нервно-паралитического действия. Токсичность фосфорорганических соединений обусловлена ингибированием фермента ацетилхолинэстеразы, вследствие чего развивается головная боль, тошнота, головокружение, сужение зрачков (миоз), затруднение дыхания (отдышка), возникает слюнотечение, понижается артериальное давление, возникают конвульсии, проявляется паралитическое воздействие, кома, и как следствие может быстро возникнуть летальный исход. Эффективным антидотом при отравлении ФОС является атропин.
Опасность для здоровья[ | код]
Рейтинг NFPA 704:
Фосфор относится к 1-му классу опасности.
Примечания[ | код]
- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047—1078. — DOI:10.1351/PAC-REP-13-03-02.
- ↑ Phosphorus: electronegativities (англ.). WebElements. Дата обращения 15 июля 2010.
- ↑ Sulfur and Phosphorus Compounds (англ.). Дата обращения 27 января 2010. Архивировано 22 августа 2011 года.
- ↑ 1 2 3 Редкол.:Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. — Москва: Большая Российская энциклопедия, 1999. — Т. 5. — С. 145.
- ↑ J.P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- ↑ 1 2 3 Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 30. Фосфор // Неорганическая химия. Учебник для 9 класса. — 7-е изд. — М.: Просвещение, 1976. — С. 62—65. — 2 350 000 экз.
- ↑ Горение белого фосфора под водой — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ Kemal T. Saracoglu, Ahmet H. Acar, Tamer Kuzucuoglu, Sezer Yakupoglu. White phosphorus burn (англ.) // The Lancet. — 2010. — Vol. 376, no. 9734. — P. 68. — DOI:10.1016/S0140-6736(10)60812-4.
- ↑ Chou TD, Lee TW, Chen SL, Tung YM, Dai NT, Chen SG, Lee CH, Chen TM, Wang HJ. The management of white phosphorus burns (англ.) // Burns. — 2001. — Vol. 27, iss. 5. — P. 492—497. — DOI:10.1016/S0305-4179(01)00003-1. — PMID 11451604.
- ↑ Радиационная химия // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — С. 200. — ISBN 5-7155-0292-6.
- ↑ В. Шретер, К.-Х. Лаутеншлегер, Х. Бибрак и др. Химия = Chemie. — М.: Химия, 1989. — С. 351. — ISBN 5-7245-0360-3.
- ↑ Химическая энциклопедия / Редкол.: Зефиров Н. С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9.
- ↑ Лидин Р.А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- ↑ Данные приведены по Audi G., Bersillon O., Blachot J., Wapstra A. H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. — 2003. — Т. 729. — С. 3—128. — DOI:10.1016/j.nuclphysa.2003.11.001. — Bibcode: 2003NuPhA.729….3A.
- ↑ USDA
- ↑ Буланов Ю. Б. Химический состав продуктов. Пищевая ценность.
- ↑ УНИАН — здоровье — Что происходит с фосфором?
Ссылки[ | код]
ru.wikibedia.ru
кто знает химическую формулу «чёрного фосфора» и как его получить из «белого фосфора»
купить чёрной краски и покрасить )))) самый верный и дешёвый способ ))))
Какая формула может быть у элемента? Формулы бывают у соединений. Что касается фосфора, то у него известно, вроде две аллотропии: белый и красный фосфор
Ты её найдёшь в любом вузовском учебнике по химии (а может и школьном) получают его из кра сного нагреванием под давлением
Фосфор образует несколько аллотропных модификаций, которые заметно различаются по свойствам. Белый фосфор — мягкое кристаллическое вещество. Состоит из молекул P4. Плавится при температуре 44,1°С. Очень хорошо растворим в сероуглероде CS2. Черезвычайно ядовит и легко загорается. При нагревании белого фосфора образуется Красный фосфор. Он представляет собой смесь нескольких модификаций, которые имеют различную длину молекул. Цвет красного фосфора в зависимости от способа и условий получения может меняться от светло-красного до фиолетового и темно-коричневого. Температура его плавления 585-600°. Черный фосфор — наиболее устойчивая модификация. По внешнему виду он похож на графит. В отличие от белого фосфора красный и черный фосфор не растворяются в сероуглероде, они не ядовиты и не огнеопасны. Фосфор химически более активен, чем азот. Химическая активность фосфора зависит от аллотропной модификации, в которой он находится. Так, наиболее активен белый фосфор, а наимнее активен черный фосфор. В уравнениях химических реакций белый фосфор обычно записывают формулой P4, которая соответствует составу его молекул. Красная и черная модификации фосфора обычно записываются формулой P. Этот же символ используют, если модификация неизвестна или может быть любой. Чёрный фосфор можно получить из белого или красного путём нагревания под давлением.
touch.otvet.mail.ru
Ответы@Mail.Ru: формула черного фосфора?
берешь формулу фосфора и пишешь чёрной краской вот и будет формула чёрного фосфора.. . Наиболее стабильной модификацией фосфора является черный фосфор. Его получают аллотропным превращением белого фосфора при t=2200C и повышенным давлением. По внешнему виду он напоминает графит. Кристаллическая структура черного фосфора слоистая, состоящая из гофрированных слоев (рис. 3). Черный фосфор – это наименее активная модификация фосфора. При нагревании без доступа воздуха он, как и красный, переходит в пар, из которого конденсируется в белый фосфор. Чёрный фосфор Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. Для проведения синтеза чёрного фосфора Бриджмен применил давление в 2·109 Па (20 тысяч атмосфер) и температуру около 200 °С. Начало быстрого перехода лежит в области 13 000 атмосфер и температуре около 230 °С. Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Удивительным свойством чёрного фосфора является его способность проводить электрический ток и свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 18·105 Па. Внешний вид: черн. ромбические кристаллы Брутто-формула (система Хилла) : P Молекулярная масса (в а. е. м.) : 31 Температура возгонки (в °C): 453 Растворимость (в г/100 г или характеристика) : серная кислота концентрированная: не растворим сероуглерод: не растворим Плотность: 2,69 (20°C, г/см3) Давление паров (в мм. рт. ст.) : 1 (290°C) 10 (337,5°C) 100 (394°C) Стандартная энтальпия образования ΔH (298 К, кДж/моль) : -38,9 (т) Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль) : -33,4 (т) Стандартная энтропия образования S (298 К, Дж/моль·K): 22,7 (т) Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K): 21,6 (т) Дополнительная информация: Переходит в красный фосфор при 593 С и давлении 4,36 МПа.
Нету там формулы. черный, белый и красный фосфор различны только строением кристаллической решетки. Это алотропы. А так фосфор это Р
на сколько мне известно белый P4, а чёрный, красный и в случае если модификация не известна, формула просто P.
Pn. Черный и красный фосфор нельзя разделить на фрагменты. См. рис <img src=»//otvet.imgsmail.ru/download/206650790_0e47ed420ddc09a3ab3e96ae398a545e_800.gif» data-lsrc=»//otvet.imgsmail.ru/download/206650790_0e47ed420ddc09a3ab3e96ae398a545e_120x120.gif» data-big=»1″>
touch.otvet.mail.ru
