ЕГЭ по химии — отработка задания №2
Задания для самопроверки
- Задания для самопроверки являются обязательным условием для усвоения материала, к каждому разделу прилагаются тестовые задания по пройденной тематике, которые необходимо решить.
- Решив все задания из раздела, вы увидите свой результат и сможете посмотреть ответы ко всем примерам, что поможет понять какие ошибки вы совершили, и где ваши знания необходимо укрепить!
- Тест представляет собой 10 тестов задания 2, части 1 ЕГЭ, ответы перемешиваются случайным образом, и берутся из созданной нами базы вопросов!
- Постарайтесь получить выше 90% верных ответов, чтобы быть уверенными в своих знаниях!
-
Если вы занимаетесь с репетитором, то пишите в начале тестирования свое реальное имя! Полагаясь на ваше имя, репетитор найдет пройденное вами тестирование, просмотрит ваши ошибки и учтет ваши пробелы чтобы в дальнейшем их заполнить!
- Пользуйтесь только справочным материалом представленным ниже, если вы хотите проверить закрепление материала!
- После прохождения теста посмотрите ответы к вопросам где вы ошиблись и закрепите материал перед повторным прохождением!
10 тестов по второму заданию в ЕГЭ по химии.
Рекомендуем также посмотреть разбор заданий №2 в ЕГЭ по химии!
Справочный материал для прохождения тестирования:
Таблица Менделеева Таблица растворимостиТипы вопросов которые встречаются в данном тесте (ответы на вопросы и полные условия заданий вы можете посмотреть пройдя тест выше до конца. Как решать данные вопросы мы советуем смотреть в нашем курсе химии):
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
- Расположите эти элементы в порядке уменьшения атомного радиуса.
- Расположите эти элементы в порядке уменьшения восстановительной способности.
- Расположите выбранные элементы в порядке уменьшения электроотрицательности.
- Расположите выбранные элементы в порядке уменьшения кислотных свойств образуемых ими высших гидроксидов.
- Расположите выбранные элементы в порядке уменьшения числа валентных электронов.
- Расположите выбранные элементы в порядке усиления восстановительных свойств.
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одной группе.
- Расположите выбранные элементы в порядке усиления основных свойств образуемых ими оксидов.
- Расположите выбранные элементы в порядке уменьшения электроотрицательности.
Из указанных в ряду химических элементов выберите три элемента-металла.
- Расположите выбранные элементы в порядке уменьшения числа валентных электронов.
Задание С2 на ЕГЭ по химии
Автор статьи — профессиональный репетитор О. В. Овчинникова.
Условие задачи С2 на ЕГЭ по химии — это текст, описывающий последовательность экспериментальных действий. Данный текст нужно превратить в уравнения реакций.
Трудность такого задания в том, что школьники слабо представляют себе экспериментальную, не «бумажную» химию. Не все понимают используемые термины и протекающие процессы. Попробуем разобраться.
Очень часто понятия, которые химику кажутся совершенно ясными, абитуриентами воспринимаются неправильно. Вот кратких словарь таких понятий.
Словарь непонятных терминов.
- Навеска — это просто некоторая порция вещества определенной массы (её взвесили на весах). Она не имеет отношения к навесу над крыльцом 🙂
- Прокалить — нагреть вещество до высокой температуры и греть до окончания химических реакций. Это не «смешивание с калием» и не «прокалывание гвоздём».
- «Взорвали смесь газов» — это значит, что вещества прореагировали со взрывом. Обычно для этого используют электрическую искру. Колба или сосуд при этом не взрываются!
- Отфильтровать — отделить осадок от раствора.
- Профильтровать — пропустить раствор через фильтр, чтобы отделить осадок.
- Фильтрат — это профильтрованный раствор.
- Растворение вещества — это переход вещества в раствор. Оно может происходить без химических реакций (например, при растворении в воде поваренной соли NaCl получается раствор поваренной же соли NaCl, а не щелочь и кислота отдельно), либо в процессе растворения вещество реагирует с водой и образует раствор другого вещества (при растворении оксида бария получится раствор гидроксида бария). Растворять можно вещества не только в воде, но и в кислотах, в щелочах и т.д.
- Выпаривание — это удаление из раствора воды и летучих веществ без разложения содержащихся в растворе твёрдых веществ.
- Упаривание — это просто уменьшение массы воды в растворе с помощью кипячения.
- Сплавление — это совместное нагревание двух или более твёрдых веществ до температуры, когда начинается их плавление и взаимодействие. С плаванием по реке ничего общего не имеет 🙂
- Осадок и остаток.
Очень часто путают эти термины. Хотя это совершенно разные понятия.
«Реакция протекает с выделением осадка» — это означает, что одно из веществ, получающихся в реакции, малорастворимо. Такие вещества выпадают на дно реакционного сосуда (пробирки или колбы).
«Остаток» — это вещество, которое осталось, не истратилось полностью или вообще не прореагировало. Например, если смесь нескольких металлов обработали кислотой, а один из металлов не прореагировал — его могут назвать остатком. - Насыщенный раствор — это раствор, в котором при данной температуре концентрация вещества максимально возможная и больше уже не растворяется.
Ненасыщенный раствор — это раствор, концентрация вещества в котором не является максимально возможной, в таком растворе можно дополнительно растворить ещё какое-то количество данного вещества, до тех пор, пока он не станет насыщенным.
Разбавленный и «очень» разбавленный раствор — это весьма условные понятия, скорее качественные, чем количественные. Подразумевается, что концентрация вещества невелика.
Для кислот и щелочей также используют термин «концентрированный» раствор. Это тоже характеристика условная. Например, концентрированная соляная кислота имеет концентрацию всего около 40%. А концентрированная серная — это безводная, 100%-ная кислота.
Для того, чтобы решать такие задачи, надо чётко знать свойства большинства металлов, неметаллов и их соединений: оксидов, гидроксидов, солей. Необходимо повторить свойства азотной и серной кислот, перманганата и дихромата калия, окислительно-восстановительные свойства различных соединений, электролиз растворов и расплавов различных веществ, реакции разложения соединений разных классов, амфотерность, гидролиз солей и других соединений, взаимный гидролиз двух солей.
Кроме того, необходимо иметь представление о цвете и агрегатном состоянии большинства изучаемых веществ — металлов, неметаллов, оксидов, солей.
Именно поэтому мы разбираем этот вид заданий в самом конце изучения общей и неорганической химии.
Рассмотрим несколько примеров подобных заданий.
-
Пример 1: Продукт взаимодействия лития с азотом обработали водой. Полученный газ пропустили через раствор серной кислоты до прекращения химических реакций. Полученный раствор обработали хлоридом бария. Раствор профильтровали, а фильтрат смешали с раствором нитрита натрия и нагрели.
Решение:
- Литий реагирует с азотом при комнатной температуре, образуя твёрдый нитрид лития:
- При взаимодействии нитридов с водой образуется аммиак:
- Аммиак реагирует с кислотами, образуя средние и кислые соли. Слова в тексте «до прекращения химических реакций» означают, что образуется средняя соль, ведь первоначально получившаяся кислая соль далее будет взаимодействовать с аммиаком и в итоге в растворе будет сульфат аммония:
- Обменная реакция между сульфатом аммония и хлоридом бария протекает с образованием осадка сульфата бария:
- После удаления осадка фильтрат содержит хлорид аммония, при взаимодействии которого с раствором нитрита натрия выделяется азот, причём эта реакция идёт уже при 85 градусах:
-
Пример 2: Навеску алюминия растворили в разбавленной азотной кислоте, при этом выделялось газообразное простое вещество. К полученному раствору добавили карбонат натрия до полного прекращения выделения газа. Выпавший осадок отфильтровали и прокалили, фильтрат упарили, полученный твёрдый остаток сплавили с хлоридом аммония. Выделившийся газ смешали с аммиаком и нагрели полученную смесь.
Решение:
- Алюминий окисляется азотной кислотой, образуя нитрат алюминия. А вот продукт восстановления азота может быть разным, в зависимости от концентрации кислоты. Но надо помнить, что при взаимодействии азотной кислоты с металлами не выделяется водород! Поэтому простым веществом может быть только азот:
- Если к раствору нитрата алюминия добавить карбонат натрия, то идёт процесс взаимного гидролиза (карбонат алюминия не существует в водном растворе, поэтому катион алюминия и карбонат-анион взаимодействуют с водой). Образуется осадок гидроксида алюминия и выделяется углекислый газ:
- Осадок — гидроксид алюминия, при нагревании разлагается на оксид и воду:
- В растворе остался нитрат натрия. При его сплавлении с солями аммония идёт окислительно-восстановительная реакция и выделяется оксид азота (I) (такой же процесс происходит при прокаливании нитрата аммония):
- Оксид азота (I) — является активным окислителем, реагирует с восстановителями, образуя азот:
-
Пример 3: Оксид алюминия сплавили с карбонатом натрия, полученное твёрдое вещество растворили в воде. Через полученный раствор пропускали сернистый газ до полного прекращения взаимодействия. Выпавший осадок отфильтровали, а к профильтрованному раствору прибавили бромную воду. Полученный раствор нейтрализовали гидроксидом натрия.
Решение:
- Оксид алюминия — амфотерный оксид, при сплавлении со щелочами или карбонатами щелочных металлов образует алюминаты:
- Алюминат натрия при растворении в воде образует гидроксокомплекс:
- Растворы гидроксокомплексов реагируют с кислотами и кислотными оксидами в растворе, образуя соли. Однако, сульфит алюминия в водном растворе не существует, поэтому будет выпадать осадок гидроксида алюминия. Обратите внимание, что в реакции получится кислая соль — гидросульфит калия:
- Гидросульфит калия является восстановителем и окисляется бромной водой до гидросульфата:
- Полученный раствор содержит гидросульфат калия и бромоводородную кислоту. При добавлении щелочи нужно учесть взаимодействие с ней обоих веществ:
-
Пример 4: Сульфид цинка обработали раствором соляной кислоты, полученный газ пропустили через избыток раствора гидроксида натрия, затем добавили раствор хлорида железа (II). Полученный осадок подвергли обжигу. Полученный газ смешали с кислородом и пропустили над катализатором.
Решение:
- Сульфид цинка реагирует с соляной кислотой, при этом выделяется газ — сероводород:
- Сероводород — в водном растворе реагирует со щелочами, образуя кислые и средние соли. Поскольку в задании говорится про избыток гидроксида натрия, следовательно, образуется средняя соль — сульфид натрия:
- Сульфид натрия реагирует с хлоридом двухвалентного железа, образуется осадок сульфида железа (II):
- Обжиг — это взаимодействие твёрдых веществ с кислородом при высокой температуре. При обжиге сульфидов выделяется сернистый газ и образуется оксид железа (III):
- Сернистый газ реагирует с кислородом в присутствии катализатора, образуя серный ангидрид:
-
Пример 5: Оксид кремния прокалили с большим избытком магния. Полученную смесь веществ обработали водой. При этом выделился газ, который сожгли в кислороде. Твёрдый продукт сжигания растворили в концентрированном растворе гидроксида цезия. К полученному раствору добавили соляную кислоту.
Решение:
- При восстановлении оксида кремния магнием образуется кремний, который реагирует с избытком магния. При этом получается силицид магния:
Можно записать при большом избытке магния суммарное уравнение реакции:
- При растворении в воде полученной смеси растворяется силицид магния, образуется гидроксид магния и силан (окисд магния реагирует с водой только при кипячении):
- Силан при сгорании образует оксид кремния:
- Оксид кремния — кислотный оксид, он реагирует со щелочами, образуя силикаты:
- При действии на растворы силикатов кислот, более сильных, чем кремниевая, она выделяется в виде осадка:
Ты нашел то, что искал? Поделись с друзьями!
Задания С2 из вариантов ЕГЭ по химии для самостоятельной работы.
- Нитрат меди прокалили, полученный твёрдый осадок растворили в серной кислоте. Через раствор пропустили сероводород, полученный чёрный осадок подвергли обжигу, а твёрдый остаток растворили при нагревании в концентрированной азотной кислоте.
- Фосфат кальция сплавили с углём и песком, затем полученное простое вещество сожгли в избытке кислорода, продукт сжигания растворили в избытке едкого натра. К полученному раствору прилили раствор хлорида бария. Полученный осадок обработали избытком фосфорной кислоты.
- Медь растворили в концентрированной азотной кислоте, полученный газ смешали с кислородом и растворили в воде. В полученном растворе растворили оксид цинка, затем к раствору прибавили большой избыток раствора гидроксида натрия.
- На сухой хлорид натрия подействовали концентрированной серной кислотой при слабом нагревании, образующийся газ пропустили в раствор гидроксида бария. К полученному раствору прилили раствор сульфата калия. Полученный осадок сплавили с углем. Полученное вещество обработали соляной кислотой.
- Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода.
- Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твёрдому веществу добавили избыток раствора соляной кислоты.
- Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. К полученному раствору прибавили сначала раствор хлорида бария, а после отделения осадка — добавили раствор нитрата серебра.
- Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился тёмно-зелёный раствор. К полученному щелочному раствору прибавили пероксид водорода. Получился раствор желтого цвета, который при добавлении серной кислоты приобретает оранжевый цвет. При пропускании сероводорода через полученный подкисленный оранжевый раствор он мутнеет и вновь становится зелёным.
- (МИОО 2011, тренинговая работа) Алюминий растворили в концентрированном растворе гидроксида калия. Через полученный раствор пропускали углекислый газ до прекращения выделения осадка. Осадок отфильтровали и прокалили. Полученный твердый остаток сплавили с карбонатом натрия.
- (МИОО 2011, тренинговая работа) Кремний растворили в концентрированном растворе гидроксида калия. К полученному раствору добавили избыток соляной кислоты. Помутневший раствор нагрели. Выделившийся осадок отфильтровали и прокалили с карбонатом кальция. Напишите уравнения описанных реакций.
Ответы к заданиям для самостоятельного решения:
- или
-
или -
или
Читаем дальше: Задачи на сплавы и смеси на ЕГЭ по химии.
Задача С5 на ЕГЭ по химии. Определение формул органических веществ.
Звоните нам: 8 (800) 775-06-82 (бесплатный звонок по России) +7 (495) 984-09-27 (бесплатный звонок по Москве)
Или нажмите на кнопку «Узнать больше», чтобы заполнить контактную форму. Мы обязательно Вам перезвоним.
ege-study.ru
Видеоразбор 2-го задания ЕГЭ 2017 по химии на периодическую систему
Видео по заданию 2 ЕГЭ 2017 по химии поможет вам подготовиться и не допустить ошибок на экзамене. Если у вас есть с ним проблемы — ниже выкладываем видео, готовьтесь. Задание 1 посвящено периодической системе.
Также у нас есть информация о других заданиях ЕГЭ по химии. Выбрать задание вы можете справа сверху.
Видеоурок задание 2 ЕГЭ 2017 по химии
Посмотров 384
Может вас заинтересовать
Дата ЕГЭ 2017 по химии. Когда будет?
ЕГЭ по химии
Видеоразбор 13 задания ЕГЭ 2017 по химии по изомерам
ЕГЭ по химии Видео
Видеоразбор 2-го задания ЕГЭ 2017 по химии на периодическую систему
ЕГЭ по химии Видео
vuzopedia.ru
МЕТОДИКА ПОДГОТОВКИ ОБУЧАЮЩИХСЯ К РЕШЕНИЮ ЗАДАНИЙ С2 ЕГЭ ПО ХИМИИ
МЕТОДИКА ПОДГОТОВКИ УЧАЩИХСЯ К РЕШЕНИЮ
ЗАДАНИЙ С2 ЕГЭ ПО ХИМИИ
При нагревании вещества оранжевого цвета оно разлагается; среди продуктов разложения – бесцветный газ и твердое вещество зеленого цвета. выделившийся газ реагирует с литием даже при небольшом нагревании. Продукт последней реакции взаимодействует с водой, при этом выделяется газ с резким запахом, который может восстанавливать металлы, например, медь из их оксидов.
Анализ содержания задания показывает, что первое вещество неизвестно, но зато известны характерные свойства самого вещества (цвет) и продуктов реакции (цвет и агрегатное состояние). Для всех остальных реакций указан реагент и условия проведения. Подсказками можно считать указания на класс полученного вещества, его агрегатное состояние, характерные признаки (цвет, запах). Заметим, что два уравнения реакций характеризуют особые свойства веществ (1 – разложение дихромата аммония; 4 – восстановительные свойства аммиака), два уравнения характеризуют типичные свойства важнейших классов неорганических веществ (2 – реакция между металлом и неметаллом, 3 – гидролиз нитридов).
При решении этих заданий можно порекомендовать учащимся составлять схемы:
toC Li h3O CuO
(Nh5 )2Cr2O7 → газ → X → газ с резким запахом → Сu
Выделять подсказки, ключевые моменты, например: вещество оранжевого цвета, которое разлагается с выделением азота (бесцветный газ) и Cr2O3 (вещество зеленого цвета) – дихромат аммония (Nh5)2Cr2O7.
toC
(Nh5 )2Cr2O7 → N2↑ + Cr2O3 + 4h3O
N2+ 6Li → 2Li3N
toC
Li3N + 3h3O → Nh4+ 3LiOH
toC
Nh4 + 3CuO → 3Cu + N2↑ + 3h3O
Какие затруднения могут вызвать у учащихся подобные задания?
1. Описание действий с веществами (фильтрование, выпаривание, обжиг, прокаливание, спекание, сплавление). Учащиеся должны понимать, где с веществом происходит физическое явление, а где – химическая реакция. Наиболее часто используемые действия с веществами описаны ниже.
Фильтрование – способ разделения неоднородных смесей с помощью фильтров – пористых материалов, пропускающих жидкость или газ, но задерживающих твёрдые вещества. При разделении смесей, содержащих жидкую фазу, на фильтре остается твердое вещество, через фильтр проходит фильтрат.
Выпаривание — процесс концентрирования растворов путём испарения растворителя. Иногда выпаривание проводят до получения насыщенных растворов, с целью дальнейшей кристаллизации из них твердого вещества в виде кристаллогидрата, или до полного испарения растворителя с целью получения растворенного вещества в чистом виде.
Прокаливание – нагревание вещества с целью изменения его химического состава.
Прокаливание может проводиться на воздухе и в атмосфере инертного газа.
При прокаливании на воздухе кристаллогидраты теряют кристаллизационную воду:
CuSO4∙5h3O →CuSO4 + 5h3O
Термически нестойкие вещества разлагаются (нерастворимые основания, некоторые соли, кислоты, оксиды): Cu(OH)2 →CuO + h3O; CaCO3→ CaO + CO2
Вещества, неустойчивые к действию компонентов воздуха, при прокаливании окисляются, реагируют с компонентами воздуха: 2Сu + O2 → 2CuO;
4Fe(OH)2 + O2 →2Fe2O3 + 4h3O
Для того, чтобы окисление при прокаливании не происходило, процесс проводят в инертной атмосфере: Fe(OH)2 → FeO + h3O
Спекание, сплавление – это нагревание двух и более твердых реагентов, приводящее к их взаимодействию. Если реагенты устойчивы к действию окислителей, то спекание можно проводить на воздухе:
Al2O3 + Na2CO3 → 2NaAlO2 + CO2
Если же один из реагентов или продукт реакции могут окисляться компонентами воздуха, процесс проводят с инертной атмосфере, например: Сu + CuO→ Cu2O
Обжиг – процесс термической обработки, приводящий к сгоранию вещества (в узком смысле. В более широком понимании, обжиг – разнообразные термические воздействия на вещества в химическом производстве и металлургии). В основном, используется по отношению к сульфидным рудам. Например, обжиг пирита:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2. Описание характерных признаков веществ (цвет, запах, агрегатное состояние).
Указание характерных признаков веществ должно служить для учащихся подсказкой или проверкой правильности выполненных действий. Однако, если учащиеся не знакомы с физическими свойствами веществ, подобные сведения не могут оказать вспомогательной функции при выполнении мысленного эксперимента. Ниже представлены наиболее характерные признаки газов, растворов, твердых веществ.
ГАЗЫ:
Окрашенные: Cl2 – желто-зеленый; NO2 – бурый; O3 – голубой (все имеют запахи). Все ядовиты, растворяются в воде, Cl2 и NO2 реагируют с ней.
Бесцветные без запаха: Н2, N2, O2, CO2, CO (яд), NO (яд), инертные газы. Все плохо растворимы в воде.
Бесцветные с запахом: HF, HCl, HBr, HI, SO2 (резкие запахи), Nh4(нашатырного спирта) –хорошо растворимы в воде и ядовиты,
Ph4(чесночный), h3S(тухлых яиц) — мало растворимы в воде, ядовиты.
ОКРАШЕННЫЕ РАСТВОРЫ:
желтые
Хроматы, например K2CrO4
Растворы солей железа (III), например, FeCl3,
бромная вода,
cпиртовые и спиртово-водные растворы йода – в зависимости от концентрации от жёлтогодобурого
оранжевые
Дихроматы, например, K2Cr2O7
зеленые
Гидроксокомплексы хрома (III), например, K3[Cr(OH)6], соли никеля (II), например NiSO4,
манганаты, например, K2MnO4
голубые
Соли меди (II), например СuSO4
От розового до фиолетового
Перманганаты, например, KMnO4
От зеленого до синего
Соли хрома (III), например, CrCl3
ОКРАШЕННЫЕ ОСАДКИ,
ПОЛУЧАЮЩИЕСЯ ПРИ ВЗАИМОДЕЙСТВИИ РАСТВОРОВ
желтые
AgBr, AgI, Ag3PO4, BaCrO4, PbI2,CdS
бурые
Fe(OH)3, MnO2
черные, черно-бурые
Сульфиды меди, серебра, железа, свинца
синие
Cu(OH)2, KFе[Fe(CN)6]
зеленые
Cr(OH)3 – серо-зеленый
Fe(OH)2 – грязно-зеленый, буреет на воздухе
ДРУГИЕ ОКРАШЕННЫЕ ВЕЩЕСТВА
желтые
сера, золото, хроматы
оранжевые
oксид меди (I) – Cu2O
дихроматы
красные
бром (жидкость), медь (аморфная), фосфор красный,
Fe2O3, CrO3
черные
СuO, FeO, CrO
Серые с металлическим блеском
Графит, кристаллический кремний, кристаллический йод (при возгонке – фиолетовые пары), большинство металлов.
зеленые
Cr2O3, малахит (CuOH)2CO3, Mn2O7 (жидкость)
Это, конечно, минимальные сведения, которые могут пригодиться для решения заданий С2.
В процессе подготовки учащихся к решению заданий С2 можно предложить им составить тексты заданий в соответствии со схемами превращений. Это задание позволит учащимся освоить терминологию и запомнить характерные признаки веществ.
Пример 1:
toC toC/h3 HNO3( конц) NaOH, 0oC
(CuOH)2CO3 → CuO → Cu → NO2 → X
Текст: Малахит прокалили, полученное твердое черное вещество нагрели в токе водорода. Образовавшееся красное вещество полностью растворили в концентрированной азотной кислоте. Выделившийся бурый газ пропустили через холодный раствор гидроксида натрия.
Пример 2:
O2 h3S р-р toC/Al h3O
ZnS → SO2 → S → Al2S3 → X
Текст: Сульфидцинкаподверглиобжигу. Образовавшийся газ с резким запахом пропустили через раствор сероводорода до выпадения жёлтого осадка. Осадок отфильтровали, просушили и сплавили с алюминием. Полученное соединение поместили в воду до прекращения реакции.
На следующем этапе можно предложить учащимся самим составлять как схемы превращения веществ, так и тексты заданий. Конечно же, «авторы» заданий должны представить и собственное решение. При этом ученики повторяют все свойства неорганических веществ. А учитель может сформировать банк заданий С2.
После этого можно переходить к решению заданий С2. При этом учащиеся по тексту составляют схему превращений, а затем и соответствующие уравнения реакций. Для этого в тексте задания выделяются опорные моменты: названия веществ, указание на их классы, физические свойства, условия проведения реакций, названия процессов.
Приведем примеры выполнения некоторых заданий.
Пример 1. Нитрат марганца (II) прокалили, к полученному твёрдому бурому веществу прилили концентрированную хлороводородную кислоту. Выделившийся газ пропустили через сероводородную кислоту. Образовавшийся раствор образует осадок с хлоридом бария.
Решение:
· Выделение опорных моментов:
Нитрат марганца (II) – Mn(NO3)2,
Прокалили – нагрели до разложения,
Твёрдое бурое вещество – MnО2,
Концентрированная хлороводородная кислота – HCl,
Сероводородная кислота – р-р Н2S,
Хлорид бария – BaCl2, образует осадок с сульфат-ионом.
· Составление схемы превращений:
toC HCl Н2Sр-р BaCl2
Mn(NO3)2 → MnО2 → ↑Х → У → ↓ (BaSO4 ?)
· Составление уравнений реакций:
1) Mn(NO3)2 → MnО2 + 2NO2
2) MnО2 + 4 HCl → MnCl2 + 2h3O + Cl2 (газХ)
3) Cl2 +Н2S→ 2HCl + S (не подходит, т.к. нет продукта, который дает осадок с хлоридом бария ) или 4Cl2 +Н2S + 4Н2О → 8HCl + Н2SO4
4) Н2SO4 + BaCl2 → BaSO4 + 2HCl
Пример 2.Оранжевый оксид меди поместили в концентрированную серную кислоту и нагрели. К полученному голубому раствору прилили избыток раствора гидроксида калия. Выпавший синий осадок отфильтровали, просушили и прокалили. Полученное при этом твёрдое черное вещество поместили в стеклянную трубку, нагрели и пропустили над ним аммиак.
Решение:
· Выделение опорных моментов:
Оранжевый оксид меди – Cu2O,
Концентрированная серная кислота – Н2SO4,
Голубой раствор – соль меди (II), СuSO4
Гидроксид калия – КОН,
Синий осадок – Cu(OH)2,
Прокалили – нагрели до разложения,
Твёрдое черное вещество – CuO,
Аммиак – Nh4.
· Составление схемы превращений:
Н2SO4 КОН toC Nh4
Cu2O → СuSO4 → Cu(OH)2 ↓ → CuO → X
· Составление уравнений реакций:
1) Cu2O + 3Н2SO4 → 2СuSO4 + SO2 +3h3O
2) СuSO4 + 2КОН → Cu(OH)2 + K2SO4
3) Cu(OH)2 → CuO + Н2О
4) 3CuO + 2Nh4 → 3Cu + 3Н2О + N2
ПРИМЕРЫ ЗАДАНИЙ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
1. Натрий сожгли в избытке кислорода, полученное кристаллическое вещество поместили в стеклянную трубку и пропустили через нее углекислый газ. Газ, выходящий из трубки, собрали и сожгли в его атмосфере фосфор. Полученное вещество нейтрализовали избытком раствора гидроксида натрия.
2. Карбид алюминия обработали соляной кислотой. Выделившийся газ сожгли, продукты сгорания пропустили через известковую воду до образования белого осадка, дальнейшее пропускание продуктов сгорания в полученную взвесь привело к растворению осадка.
3. Пирит подвергли обжигу, полученный газ с резким запахом пропустили через сероводородную кислоту. Образовавшийся желтоватый осадок отфильтровали, просушили, смешали с концентрированной азотной кислотой и нагрели. Полученный раствор дает осадок с нитратом бария.
4. Медь поместили в концентрированную азотную кислоту, полученную соль выделили из раствора, высушили и прокалили. Твёрдый продукт реакции смешали с медной стружкой и прокалили в атмосфере инертного газа. Полученное вещество растворили в аммиачной воде.
5. Железные опилки растворили в разбавленной серной кислоте, полученный раствор обработали избытком раствора гидроксида натрия. Образовавшийся осадок профильтровали и оставили на воздухе до тех пор, пока он не приобрёл бурую окраску. Бурое вещество прокалили до постоянной массы.
6. Сульфид цинка подвергли обжигу. Полученное твердое вещество полностью прореагировало с раствором гидроксида калия. Через полученный раствор пропустили углекислый газ до выпадения осадка. Осадок растворили в соляной кислоте.
7. Газ, выделившийся при взаимодействии цинка с соляной кислотой, смешали с хлором и взорвали. Полученный при этом газообразный продукт растворили в воде и подействовали им на диоксид марганца. Образовавшийся газ пропустили через горячий раствор гидроксида калия.
8. Фосфид кальция обработали соляной кислотой. Выделившийся газ сожгли в закрытом сосуде, продукт горения полностью нейтрализовали раствором гидроксида калия. К полученному раствору прилили раствор нитрата серебра.
9. Дихромат аммония разложили при нагревании. Твёрдый продукт разложения растворили в серной кислоте. К полученному раствору прилили раствор гидроксида натрия до выпадения осадка. При дальнейшем приливании раствора гидроксида натрия к осадку, он растворился.
10. Ортофорсфат кальция прокалили с углем и речным песком. Образовавшееся при этом белое светящееся в темноте вещество сожгли в атмосфере хлора. Продукт этой реакции растворили в избытке гидроксида калия. К полученной смеси прилили раствор гидроксида бария.
11. Алюминиевый порошок смешали с серой и нагрели. Полученное вещество поместили в воду. Образовавшийся осадок разделили на две части. К одной части прилили соляную кислоту, к другой – раствор гидроксида натрия до полного растворения осадка.
12. Кремний поместили в раствор гидроксида калия, после окончания реакции к полученному раствору прилили избыток соляной кислоты. Выпавший осадок отфильтровали, просушили и прокалили. Твёрдый продукт прокаливания реагирует с фтороводородом.
РЕШЕНИЯ
1. Натрий сожгли в избытке кислорода, полученное кристаллическое вещество поместили в стеклянную трубку и пропустили через нее углекислый газ. Газ, выходящий из трубки, собрали и сожгли в его атмосфере фосфор. Полученное вещество нейтрализовали избытком раствора гидроксида натрия.
1) 2Na+ O2 = Na2O2
2) 2Na2O2 + 2CO2 = 2Na2CO3 + O2
3) 4P + 5O2 = 2P2O5
4) P2O5 + 6 NaOH = 2Na3PO4 + 3h3O
2. Карбид алюминия обработали соляной кислотой. Выделившийся газ сожгли, продукты сгорания пропустили через известковую воду до образования белого осадка, дальнейшее пропускание продуктов сгорания в полученную взвесь привело к растворению осадка.
1) Al4C3 + 12HCl = 3Ch5 + 4AlCl3
2) Ch5 + 2O2 = CO2 + 2h3O
3) CO2 + Ca(OH)2 = CaCO3+ h3O
4) CaCO3+ h3O + CO2 = Ca(HCO3)2
3. Пирит подвергли обжигу, полученный газ с резким запахом пропустили через сероводородную кислоту. Образовавшийся желтоватый осадок отфильтровали, просушили, смешали с концентрированной азотной кислотой и нагрели. Полученный раствор дает осадок с нитратом бария.
1) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
2) SO2 + 2h3 S= 3S + 2h3O
3) S+ 6HNO3 = h3SO4+ 6NO2 +2h3O
4) h3SO4+ Ba(NO3)2 = BaSO4↓ + 2 HNO3
4. Медь поместили в концентрированную азотную кислоту, полученную соль выделили из раствора, высушили и прокалили. Твёрдый продукт реакции смешали с медной стружкой и прокалили в атмосфере инертного газа. Полученное вещество растворили в аммиачной воде.
1) Cu + 4HNO3 = Cu(NO3)2+ 2NO2 +2h3O
2) 2Cu(NO3)2 = 2CuO + 4NO2 + O2
3) Cu + CuO= Cu2O
4) Cu2O + 4Nh4 + h3O = 2[Cu(Nh4)2]OH
5. Железные опилки растворили в разбавленной серной кислоте, полученный раствор обработали избытком раствора гидроксида натрия. Образовавшийся осадок профильтровали и оставили на воздухе до тех пор, пока он не приобрёл бурую окраску. Бурое вещество прокалили до постоянной массы.
1) Fe + h3SO4 = FeSO4+ h3
2) FeSO4 + 2NaOH= Fe(OH)2 + Na2SO4
3) 4Fe(OH)2 + 2h3O + O2 = 4Fe(OH)3
4) 2Fe(OH)3 = Fe2O3 + 3h3O
6. Сульфид цинка подвергли обжигу. Полученное твердое вещество полностью прореагировало с раствором гидроксида калия. Через полученный раствор пропустили углекислый газ до выпадения осадка. Осадок растворили в соляной кислоте.
1) 2ZnS + 3O2 = 2ZnO + 2SO2
2) ZnO+ 2NaOH + h3O = Na2[Zn(OH)4]
3 Na2[Zn(OH)4] + CO2 = Na2CO3 + h3O + Zn(OH)2
4) Zn(OH)2 + 2 HCl = ZnCl2 + 2h3O
7. Газ, выделившийся при взаимодействии цинка с соляной кислотой, смешали с хлором и взорвали. Полученный при этом газообразный продукт растворили в воде и подействовали им на диоксид марганца. Образовавшийся газ пропустили через горячий раствор гидроксида калия.
1) Zn+ 2HCl = ZnCl2 + h3
2) Cl2 + h3 = 2HCl
3) 4HCl + MnO2 = MnCl2 + 2h3O + Cl2
4) 3Cl2 + 6KOH = 5KCl + KClO3 + 3h3O
8. Фосфид кальция обработали соляной кислотой. Выделившийся газ сожгли в закрытом сосуде, продукт горения полностью нейтрализовали раствором гидроксида калия. К полученному раствору прилили раствор нитрата серебра.
1) Ca3P2 + 6HCl = 3CaCl2 + 2Ph4
2) Ph4 + 2O2 = h4PO4
3) h4PO4 + 3KOH= K3PO4 + 3h3O
4) K3PO4 + 3AgNO3 = 3KNO3 + Ag3PO4
9. Дихромат аммония разложили при нагревании. Твёрдый продукт разложения растворили в серной кислоте. К полученному раствору прилили раствор гидроксида натрия до выпадения осадка. При дальнейшем приливании гидроксида натрия к осадку, он растворился.
1) (Nh5)2Cr2O7 = Cr2O3 + N2 + 4h3O
2) Cr2O3 + 3h3SO4 = Cr2(SO4)3 + 3h3O
3) Cr2(SO4)3 + 6NaOH= 3Na2SO4 + 2Cr(OH)3
4) 2Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]
10. Ортофорсфат кальция прокалили с углем и речным песком. Образовавшееся при этом белое светящееся в темноте вещество сожгли в атмосфере хлора. Продукт этой реакции растворили в избытке гидроксида калия. К полученной смеси прилили раствор гидроксида бария.
1) Ca3(PO4)2 + 5C + 3SiO2 = 3CaSiO3 + 5CO + 2P
2) 2P + 5Cl2 = 2PCl5
3) PCl5 + 8KOH= K3PO4 + 5KCl + 4h3O
4) 2K3PO4 + 3Ba(OH)2 = Ba3(PO4)2 + 6KOH
11. Алюминиевый порошок смешали с серой и нагрели. Полученное вещество поместили в воду. Образовавшийся осадок разделили на две части. К одной части прилили соляную кислоту, к другой – раствор гидроксида натрия до полного растворения осадка.
1) 2Al + 3S = Al2S3
2) Al2S3 + 6h3O = 2Al(OH)3 + 3h3S
3) Al(OH)3 + 3HCl= AlCl3 + 3h3O
4) Al(OH)3 + NaOH = Na[Al(OH)4]
12. Кремний поместили в раствор гидроксида калия, после окончания реакции к полученному раствору прилили избыток соляной кислоты. Выпавший осадок отфильтровали, просушили и прокалили. Твёрдый продукт прокаливания реагирует с фтороводородом.
1) Si + 2KOH + h3O = K2SiO3+ 2h3
2) K2SiO3 + 2HCl = 2KCl + h3SiO3
3) h3SiO3 = SiO2 + h3O
4) SiO2 + 4HF = SiF4 + 2h3O
www.metod-kopilka.ru
Как решать С2 по химии — подсказки и советы » HimEge.ru
Задание С2 ЕГЭ по химии представляет собой описание химического эксперимента, в соответствии с которым нужно будет составить 4 уравнения реакции. По статистике, это одно из самых сложных заданий, очень низкий процент сдающих с ним справляется. Ниже приводятся рекомендации по поводу решения задания С2.
Во — первых, чтобы верно решить задание С2 ЕГЭ по химии нужно правильно представлять себе те действия, которым подвергаются вещества (фильтрование, выпаривание, обжиг, прокаливание, спекание, сплавление). Необходимо понимать, где с веществом происходит физическое явление, а где – химическая реакция. Наиболее часто используемые действия с веществами описаны ниже.
Фильтрование – способ разделения неоднородных смесей с помощью фильтров – пористых материалов, пропускающих жидкость или газ, но задерживающих твёрдые вещества. При разделении смесей, содержащих жидкую фазу, на фильтре остается твердое вещество, через фильтр проходит фильтрат.
Выпаривание — процесс концентрирования растворов путём испарения растворителя. Иногда выпаривание проводят до получения насыщенных растворов, с целью дальнейшей кристаллизации из них твердого вещества в виде кристаллогидрата, или до полного испарения растворителя с целью получения растворенного вещества в чистом виде.
Прокаливание – нагревание вещества с целью изменения его химического состава. Прокаливание может проводиться на воздухе и в атмосфере инертного газа. При прокаливании на воздухе кристаллогидраты теряют кристаллизационную воду, например, CuSO4∙5H2O→CuSO4+ 5H2O
Термически нестойкие вещества разлагаются:
Cu(OH)2 →CuO + H2O; CaCO3→ CaO + CO2
Спекание, сплавление – это нагревание двух и более твердых реагентов, приводящее к их взаимодействию. Если реагенты устойчивы к действию окислителей, то спекание можно проводить на воздухе:
Al2O3 + Na2CO3 → 2NaAlO2 + CO2
Если же один из реагентов или продукт реакции могут окисляться компонентами воздуха, процесс проводят с инертной атмосфере, например: Сu + CuO → Cu2O
Вещества, неустойчивые к действию компонентов воздуха, при прокаливании окисляются, реагируют с компонентами воздуха:
2Сu + O2 → 2CuO;
4Fe(OH)2 + O2 →2Fe2O3 + 4H2O
Обжиг – процесс термической обработки, приводящий к сгоранию вещества.
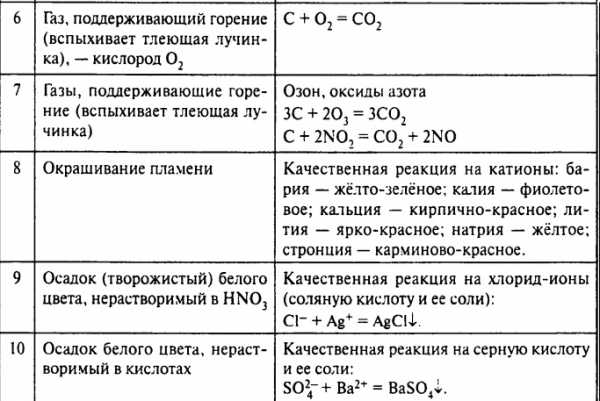
Во-вторых, знание характерных признаков веществ (цвет, запах, агрегатное состояние) Вам послужит подсказкой или проверкой правильности выполненных действий. Ниже представлены наиболее характерные признаки газов, растворов, твердых веществ.
Признаки газов:
Окрашенные: Cl2 – желто-зеленый; NO2 – бурый; O3 – голубой (все имеют запахи). Все ядовиты, растворяются в воде, Cl2 и NO2 реагируют с ней.
Бесцветные без запаха: Н2, N2, O2, CO2, CO (яд), NO (яд), инертные газы. Все плохо растворимы в воде.
Бесцветные с запахом: HF, HCl, HBr, HI, SO2 (резкие запахи), NH3(нашатырного спирта) –хорошо растворимы в воде и ядовиты, PH3(чесночный), H2S(тухлых яиц) — мало растворимы в воде, ядовиты.
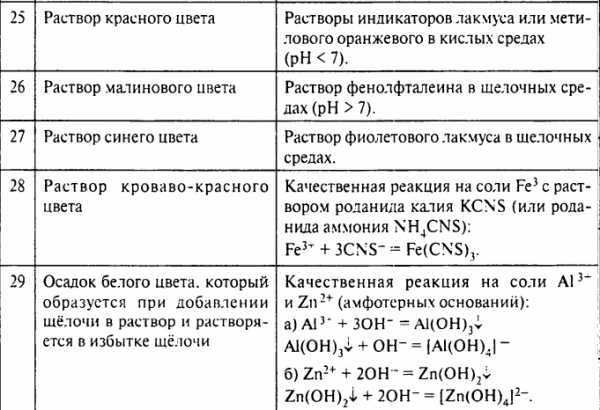
Окрашенные растворы:
Желтые: Хроматы, например K2CrO4, растворы солей железа (III), например, FeCl3.
Оранжевые: Бромная вода, cпиртовые и спиртово-водные растворы йода (в зависимости от концентрации от жёлтого до бурого), дихроматы, например, K2Cr2O7
Зеленые: Гидроксокомплексы хрома (III), например, K3[Cr(OH)6], соли никеля (II), например NiSO4, манганаты, например, K2MnO4
Голубые: Соли меди (II), например СuSO4
От розового до фиолетового: Перманганаты, например, KMnO4
От зеленого до синего: Соли хрома (III), например, CrCl3
Окрашенные осадки:
Желтые: AgBr, AgI, Ag3PO4, BaCrO4, PbI2,CdS
Бурые: Fe(OH)3, MnO2
Черные, черно-бурые: Сульфиды меди, серебра, железа, свинца
Синие: Cu(OH)2, KFе[Fe(CN)6]
Зеленые: Cr(OH)3 – серо-зеленый, Fe(OH)2 – грязно-зеленый, буреет на воздухе
Другие окрашенные вещества:
Желтые: сера, золото, хроматы
Оранжевые: oксид меди (I) – Cu2O, дихроматы
Красные: бром (жидкость), медь (аморфная), фосфор красный, Fe2O3, CrO3
Черные: СuO, FeO, CrO
Серые с металлическим блеском: Графит, кристаллический кремний, кристаллический йод (при возгонке – фиолетовые пары), большинство металлов.
Зеленые: Cr2O3, малахит (CuOH)2CO3, Mn2O7 (жидкость)
В-третьих, при решении заданий С2 по химии для большей наглядности, можно порекомендовать составлять схемы превращений или последовательность получаемых веществ.
И наконец, для того, чтобы решать такие задачи, надо чётко знать свойства металлов, неметаллов и их соединений: оксидов, гидроксидов, солей. Необходимо повторить свойства азотной и серной кислот, перманганата и дихромата калия, окислительно-восстановительные свойства различных соединений, электролиз растворов и расплавов различных веществ, реакции разложения соединений разных классов, амфотерность, гидролиз солей.






Типовые задания С2 ЕГЭ по химии с решениями
himege.ru
Разбор задания №11 ЕГЭ по химии
Задания данного типа направлены на химические свойства металлов, неметаллов и их соединений, солей, кислот, оксидов и щелочей. Подобные тесты решаются методом исключения посредством логики.Итак, попробуем провести ход рассуждений следующим образом, исключим варианты ответов, которые точно не подходят!
Алюминий:
1) Fe2O3, HNO3 (р-р), NaOH
Алюминий вытеснит железо из оксида, будучи более активным металлом, этот процесс называется алюмотермия:
Fe2O3 + 2Al → 2Fe + Al2O3
Согласно таблице алюминий реагирует с разбавленной HNO3!
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Алюминий растворяется в щелочах, образуя алюминаты:
2Al + 2NaOH → 2NaAlO2 + 3H2
Рассмотрим другие варианты и исключим их:
2) Fe, HNO3, H2
Очевидно что алюминий и железо, будучи металлами не будут реагировать между собой, исключаем этот вариант!
3) HI, Fe, SO2
Аналогичным образом исключаем и этот вариант!
4) C2H5OH, H2O, Cl2
Вода реагирует с алюминием только при нагревании и при удалении оксидной пленки!
5) CaCl2, KOH, HCl
Кальций более активный металл чем алюминий, поэтому алюминий не сможет его вытеснить!
Кислород:
Кислород не сможет окислить соединения, чьи элементы уже в своих высших степенях окисления:
1) Fe2O3, HNO3 (р-р), NaOH
Кислород не окислит высший оксид железа, железо и так окислено до +3!
2) Fe, HNO3, H2
Азотная кислота сама по себе сильный окислитель, а азот в своей максимальной степени окисления +5.
3) HI, Fe, SO2
Кислоты не окислители могут окисляться кислородом:
4HI + O2 → 2I2 + 2H2O
Железо окисляется на воздухе как и большинство металлов и горит в атмосфере кислорода:
3Fe + 2O2 → Fe3O4
Оксид серы (IV) не является высшим оксидом, поэтому он тоже может окислиться сильнее:
2SO2 + O2 → 2SO3
4) C2H5OH, H2O, Cl2
Вода с кислородом не реагирует, это и так оксид водорода!
5) CaCl2, KOH, HCl
Щелочи не способны окисляться водородом, металл в них и так окислен!
Сера:
1) Fe2O3, HNO3 (р-р), NaOH
Сера не прореагирует с оксидом железа, так имеет сходство с кислородом (в той-же группе), к тому же вытеснить кислород она не способна (ниже по группе).
2) Fe, HNO3, H2
При обычных условиях сера реагирует со всеми щелочными и щелочноземельными металлами, медью, ртутью, серебром (при нагревании сера реагирует и с другими металлами (Zn, Al, Fe), и только золото не взаимодействует с ней ни при каких условиях):
Fe + S = FeS
Сера играет роль восстановителя, причем из неметаллов с серой не реагирует только азот, йод и благородные газы. С азотной кислотой она реагирует при кипячении с получением H2SO4:
S + 6HNO3 → H2SO4 + 6NO2 + 2H2O
Окислительные свойства сера проявляет и с водородом, с которым реагирует при нагревании:
H2 + S → H2S
3) HI, Fe, SO2
Очевидно что сера не будет реагировать со своим оксидом.
4) C2H5OH, H2O, Cl2
Сера инертна к вода, как и кислород.
5) CaCl2, KOH, HCl
Cера не будет взаимодействовать с хлоридом кальция, равно как и с HCl.
Калий:
1) Fe2O3, HNO3 (р-р), NaOH
Натрий более активный метал чем калий, поэтому последний не вытеснить его из соединений.
2) Fe, HNO3, H2
Калий и железо не взаимодействуют, оба металлы.
3) HI, Fe, SO2
Аналогично предыдущему пункту исключим этот.
4) C2H5OH, H2O, Cl2
При взаимодействии калия с спиртом образуются алкоголяты. Катионами алкоголятов могут быть щелочные, щелочноземельные металлы и, при определенных условиях алюминий):
C2H5OH + K → C2H5OK + H2↑
Щелочные металлы (активные металлы) взаимодействуют с водой:
2K + 2H2O → 2KOH + H2↑
Большинство металлов реагируют с галогенами. Каждый галоген является самым сильным окислителем в своем периоде. Окислительные свойства галогенов отчетливо проявляются при их взаимодействии с металлами. При этом образуются соли:
2K + Cl2 → 2KCl
5) CaCl2, KOH, HCl
Калий не будет взаимодействовать с своей щелочью.
www.chem-mind.com
как сдать часть 2 ЕГЭ по химии — Учёба.ру

Александр Есманский,
преподаватель Олимпиадных школ МФТИ по химии, репетитор ЕГЭ и ОГЭ,
автор и составитель методических разработок
Задание № 30
Что требуется
Из предложенного перечня веществ необходимо выбрать те, между которыми возможно протекание окислительно-восстановительной реакции (ОВР), записать уравнение этой реакции и подобрать в ней коэффициенты методом электронного баланса, а также указать окислитель и восстановитель.
Особенности
Это одно из самых сложных заданий ЕГЭ по предмету, поскольку оно проверяет знание всей химии элементов, а также умение определять степени окисления элементов. По этим данным нужно определить вещества, которые могут быть только окислителями (элементы в составе этих веществ могут только понижать степень окисления), только восстановителями (элементы в составе этих веществ могут только повышать степень окисления) или же проявлять окислительно-восстановительную двойственность (элементы в составе этих веществ могут и понижать, и повышать степень окисления).
Также в задании необходимо уметь самостоятельно (без каких-либо указаний или подсказок) записывать продукты широкого круга окислительно-восстановительных реакций. Кроме того, нужно уметь грамотно оформить электронный баланс, после чего перенести полученные в балансе коэффициенты в уравнение реакции и дополнить его коэффициентами перед веществами, в которых элементы не изменяли степеней окисления.
Советы
Окислительно-восстановительные реакции основаны на принципе взаимодействия веществ противоположной окислительно-восстановительной природы. Согласно этому принципу любой восстановитель может взаимодействовать практически с любым окислителем. В задаче № 30 окислители и восстановители часто подобраны таким образом, что между ними точно будет протекать реакция.
Для нахождения пары окислитель/восстановитель нужно, прежде всего, обращать внимание на вещества, содержащие элементы в минимальной и максимальной степени окисления. Тогда вещество с минимальной степенью окисления будет являться типичным восстановителем, а вещество с максимальной степенью окисления с большой долей вероятности окажется сильным окислителем.
Если в списке только одно вещество (вещество 1) содержит элемент в максимальной или минимальной степени окисления, нужно найти ему в пару вещество, в котором элемент находится в промежуточной степени окисления и может проявлять свойства и окислителя, и восстановителя (вещество 2). Тогда вещество 1 определит окислительно-восстановительную активность вещества 2.
Когда пара окислитель/восстановитель определена, нужно обязательно проверить, в какой среде (кислой, нейтральной или щелочной) может протекать эта реакция. Если нет особенных правил, связанных со средой протекания выбранной реакции, то в качестве среды следует выбрать водный раствор того вещества (кислоты или щелочи), которое есть в предложенном списке реагентов.
Чтобы верно записать продукты окислительно-восстановительной реакции, нужно знать теоретические сведения о химии того или иного вещества и специфику его свойств. Однако запоминать все реакции наизусть — дело утомительное, да и не очень полезное. Для того чтобы упростить задачу, можно выявить некоторые общие закономерности в протекании ОВР и научиться предсказывать продукты реакций. Для этого нужно следовать трем простым правилам:
- Процессы окисления и восстановления — это две стороны единого процесса: процесса передачи электрона. Если какой-либо элемент (восстановитель) отдает электроны, то в этой же реакции обязательно должен быть какой-то элемент (окислитель), который принимает эти электроны.
- Если в реакции участвует простое вещество, эта реакция — всегда окислительно-восстановительная.
- При взаимодействии сильных окислителей с различными восстановителями обычно образуется один и тот же основной продукт окисления. Многие окислители при взаимодействии с различными восстановителями также часто восстанавливаются до какого-то одного продукта, соответствующего их наиболее устойчивой степени окисления.
Задание № 31
Что требуется
Из предложенного перечня веществ (того же, что и в задании № 30) необходимо выбрать такие вещества, между которыми возможна реакция ионного обмена. Необходимо записать уравнение реакции в молекулярной форме и привести сокращенную ионную форму.
Особенности
Это задание значительно легче предыдущего, поскольку круг возможных реакций ограничен и определен условиями протекания реакций ионного обмена, которые школьники изучают еще в 8-9 классах.
Советы
Нужно помнить, что любая реакция ионного обмена — это обязательно реакция, протекающая в растворе. Все реакции ионного обмена являются неокислительно-восстановительными!
В реакциях ионного обмена могут участвовать:
- солеобразующие оксиды;
- основания и амфотерные гидроксиды;
- кислоты;
- соли (средние, кислые, основные). Теоретически можно составить реакцию ионного обмена с участием смешанных, двойных или комплексных солей, но это для задания № 31 — экзотика.
Чаще всего в этой задаче встречаются реакции ионного обмена с участием оснований, амфотерных гидроксидов, кислот и средних солей. Однако обмен ионами может осуществляться далеко не с любыми парами веществ. Для того чтобы протекала реакция ионного обмена, необходимо выполнение некоторых ограничительных условий, которые связаны с реагентами и продуктами реакции.
Для написания ионных форм уравнений нужно следовать правилам, согласно которым одни вещества представляются в диссоциированной форме (в виде ионов), а другие — в недиссоциированной (в виде молекул).
Расписываем на ионы в реакциях ионного обмена:
- растворимые сильные электролиты;
- малорастворимые сильные электролиты, если они являются реагентами.
Не расписываем на ионы в реакциях ионного обмена:
- неэлектролиты;
- нерастворимые в воде вещества;
- слабые электролиты;
- малорастворимые сильные электролиты, если они являются продуктами реакции.
Когда уже сокращенная форма реакции ионного обмена записана, будет нелишним проверить для нее выполнение материального и электрического баланса. Другими словами, верно ли расставлены в сокращенной форме коэффициенты и сохраняется ли общий электрический заряд в левой и правой частях уравнения. Это позволит избежать потерянных коэффициентов или зарядов ионов на пути от молекулярной формы через полную ионную — к сокращенной.
Задание № 32
Что требуется
По приведенному текстовому описанию необходимо записать уравнения четырех реакций.
Особенности
Это задание так же, как и задание № 30, проверяет знание всей химии элементов, которая содержится в спецификации ЕГЭ. Однако часто составление четырех уравнений, описанных в задании № 32, является более простой задачей, чем составление одного уравнения в вопросе № 30. Во-первых, здесь не нужно самостоятельно выбирать реагенты, поскольку они уже даны в условии, а продукты часто можно угадать, используя данные условия, которые, по сути, являются подсказками. Во-вторых, из четырех описанных в задании уравнений, как правило, два можно записать, используя знания 8-9 классов. Например, это могут быть реакции ионного обмена. Два других уравнения — посложнее, подобные тем, которые предлагаются в задании № 30.
Советы
Конечно, можно просто выучить всю химию элементов наизусть и с ходу записать все уравнения. Это самый верный способ. Если же возникают трудности с определением продуктов, то нужно по максимуму использовать подсказки, приведенные в условии. Чаще всего в задании указываются наблюдаемые химические явления: выпадение или растворение осадков, выделение газов, изменение цвета твердых веществ или растворов. А если еще и указан конкретный цвет осадка, газа или раствора, можно с высокой точностью определить, о каком веществе идет речь. Для этого необходимо всего лишь знать цвета наиболее часто использующихся в задачах школьной программы осадков и газов, а также цвета растворов солей. Это сильно облегчит написание проблемного уравнения реакции, и задание № 32 покажется очень даже простым.
Задание № 33
Что требуется
Необходимо записать уравнение пяти реакций с участием органических веществ по приведенной схеме (цепочке превращений).
Особенности
В этом задании предлагается классическая цепочка превращений, какие школьники учатся решать с первого года изучения химии, только здесь в каждом уравнении участвует хотя бы одно органическое вещество. Задача на каждой стадии цепочки может быть сформулирована в двух вариантах. В первом варианте даются один из реагентов и продукт реакции. В этом случае необходимо подобрать второй реагент, а также указать все условия осуществления реакций (наличие катализаторов, нагревание, соотношение реагентов). Во втором варианте известны все реагенты, а часто и условия реакции. Необходимо только записать продукты.
Советы
Лучший способ успешно выполнить цепочку по органике — это знать наизусть все типы реакций каждого класса соединений и специфические свойства органических веществ, содержащиеся в школьном курсе органической химии.
Главное правило задания № 33 — использование графических (структурных) формул органических веществ в уравнениях реакций. Это указание обязательно прописано в каждом варианте тренировочных работ и пробных вариантов ЕГЭ по химии, поэтому известно всем выпускникам. Однако некоторые школьники все равно иногда пренебрегают этим правилом и часть органических веществ записывают в молекулярном виде. Будьте внимательны! Уравнения реакций с молекулярными формулами органических веществ в этом задании не засчитываются.
В задачах № 32 и № 33 уравнение считается написанным верно, если в нем расставлены все коэффициенты и при необходимости указаны условия протекания реакции. Уравнения реакций, в которых хотя бы один коэффициент неверен или не указаны важные условия, не засчитываются.
Задание № 34
Что требуется
Решить расчетную задачу, тематика которой меняется от года к году и от варианта к варианту.
Особенности
В спецификации ЕГЭ под номером 34 заявлены задачи с использованием понятия доли (массовой, объемной, мольной) вещества в смеси. Частным случаем таких задач являются задачи «на массовую долю вещества в растворе», задачи «на примеси», то есть с использованием понятия доли чистого вещества в составе технического. Сюда же относятся расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного, а также расчеты по уравнению реакции, если один из реагентов дан в избытке.
Предсказать, какие задачи будут отобраны для ЕГЭ именно в этом году, практически невозможно. Единственное, что можно ожидать по опыту прошлых лет, — это то, что задача не окажется сложной и будет полностью соответствовать профильной школьной программе (не олимпиадной). Это значит, что такая задача по зубам любому школьнику, освоившему курс химии на профильном школьном уровне и обладающему обыкновенной математической и химической логикой.
Советы
Для того чтобы решить эту задачу, прежде всего, нужно знать базовые формулы и определения основных физических величин. Необходимо осознать понятие «математической доли» как отношения части к целому. И тогда все типы долей в химии принимают одинаковый внешний вид.
| Массовая доля вещества в смеси | \({\omega_{1}} = {{m_{в-ва}} \over m_{смеси}}\) |
| Массовая доля вещества растворе | \({\omega_{1}} = {{m_{в-ва}} \over m_{р-ра}}\) |
| Мольная доля вещества в смеси (растворе) | \({\chi} = {{\nu_{в-ва}} \over \nu_{смеси}}\) |
| Объемная доля вещества в смеси (растворе) | \({\varphi} = {{V_{в-ва}} \over V_{смеси}}\) |
| Доля чистого вещества в составе технического (степень чистоты) | \({\omega_{чист}} = {{m_{чист}} \over m_{техн}}\) |
| Доля выхода продукта от теоретически возможного (выход продукта) |
\({\eta} = {{\upsilon_{практ}} \over \upsilon_{теор}} = {{m_{практ}} \over m_{теор}} \) \(m_{практ}\) — масса продукта, которая получилась в результате химической реакции \(m_{теор}\) — масса продукта, которая могла образоваться в соответствии с теоретическим расчетом по уравнению реакции |
| Количество вещества |
\({v} = {m \over M} \) \([{v}] = моль \) \({\nu} = {{V} \over V_{m}}\) Молярный объем, т.е. объем одного моля газа, одинаков для всех газов при одинаковых условиях |
| Молярная концентрация (молярность) вещества в растворе |
\({C} = {{v_{в-ва}} \over V_{р-ра}} \) \([{C}] = {моль \over л} = М\) |
| Плотность раствора |
\({\rho} = {{m_{р-ра}} \over V_{р-ра}} \) \([{\rho}] = {г \over мл} = {г \over см^3} \) |
Задание № 35
Что требуется
Решить расчетную задачу на установление молекулярной и структурной формулы вещества, записать предложенное уравнение реакции с данным веществом.
Особенности
Идеологическая часть задач на вывод формулы изучается школьниками еще в 8-9 классах, поэтому это наиболее простая задача части 2 ЕГЭ. Хотя в спецификации не указано, формулу какого вещества необходимо установить. Опыт показывает, что из года в год здесь традиционно участвуют органические вещества.
Советы
Все задачи на вывод формулы, встречающиеся в ЕГЭ, можно условно разделить на три типа. Первый тип — это установление формулы по массовым долям элементов в веществе. Здесь работает формула для массовой доли элемента в сложном веществе:
\({\omega} = {n \times {A_{r}(элемента)} \over {M_{r}(вещества)}} \times 100 \%\)где n — число атомов элемента в молекуле, то есть индекс элемента.
Иногда в этом типе задач нужно знать еще и общую формулу класса, к которому относится неизвестное органическое вещество. Затем следует выразить относительную молекулярную массу вещества через n и подставить в уравнение для массовой доли. Решением уравнения будет искомое значение n, а следовательно, и молекулярная формула вещества. Дополнительные сведений о веществе, указанные в условии задачи, позволяют установить структурную формулу вещества, с которой далее требуется записать уравнение реакции.
Второй тип задач — это установление формулы через расчеты по уравнению химической реакции. Здесь нужно обязательно знать еще общую формулу класса, к которому относится неизвестное органическое вещество, и записать с ним уравнение реакции. Иногда приходится расставлять коэффициенты в общем виде через n. Тем не менее это наиболее понятный тип задач на вывод формулы, поскольку он чаще всего сводится к одному уравнению с одним неизвестным n, решение которого дает нам искомую молекулярную формулу. Дополнительные сведения о веществе, указанные в условии задачи, позволяют установить структурную формулу вещества, с которой далее требуется записать уравнение реакции.
И, наконец, третий тип задач — это установление формулы по продуктам сгорания вещества. Этот вариант наиболее часто встречается на ЕГЭ в этом задании. Выглядит он чуть более громоздко, чем два предыдущих, однако решается также очень просто. План решения заключается в нахождении простейшей формулы вещества и переходе к истинной (то есть молекулярной) формуле через известную молярную массу вещества. Простейшая формула находится из закона, согласно которому индексы элементов относятся так же, как их количества вещества в молях. Если молярная масса вещества не дана в условии, то можно попробовать доказать единственность решения через соответствие формулы правилам валентности. Но такой подход часто бывает трудоемок, и его можно легко обойти, если использовать дополнительные сведения об искомом веществе, указанные в условии задачи. Это может быть класс соединения, наличие или отсутствие каких-либо типов изомерии и, наконец, химическая реакция, в которую это вещество способно вступать или с помощью которой оно может быть получено. Помимо молекулярной формулы, эти же дополнительные сведения позволяют однозначно определить и структурную формулу вещества, с которой далее требуется записать уравнение реакции.
www.ucheba.ru
