Задания ЕГЭ по химии по темам (по номерам заданий)
Задания ЕГЭ по темам (номерам задания).
- Первая часть (указывается только ответ, без решения)
1. Электронная конфигурация атома
2. Закономерности изменения химических свойств элементов. Характеристика элементов
3. Электроотрицательность, степень окисления и валентность химических элементов
4. Характеристики химических связей. Зависимость свойств веществ от их состава и строения
5. Классификация и номенклатура неорганических веществ
6. Химические свойства веществ
7. Свойства оснований, амфотерных гидроксидов, кислот и солей. Ионный обмен и диссоциация
8. Свойства неорганических веществ
9. Свойства неорганических веществ
10. Взаимосвязь неорганических веществ
11. Классификация и номенклатура органических веществ
12. Теория строения органических соединений. Типы связей в молекулах органических веществ. Изомеры. Гомологи
13. Свойства углеводородов. Получение углеводородов
14. Свойства кислородосодержащих соединений. Получение кислородосодержащих соединений
15. Свойства азотсодержащих органических соединений. Белки, жиры, углеводы
16. Характерные химические свойства углеводородов. Механизмы реакций
17. Свойства спиртов, альдегидов, кислот, сложных эфиров, фенола
18. Взаимосвязь углеводородов и кислородосодержащих органических соединений
19. Классификация химических реакций в неорганической и органической химии
20. Скорость реакции, ее зависимость от различных факторов
21. Реакции окислительно-восстановительные
22. Электролиз расплавов и растворов
23. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
24. Обратимые и необратимые химические реакции. Химическое равновесие
25. Качественные реакции органических и неорганических соединений
26. Химическая лаборатория. Химическая промышленность. Полимеры
27. Расчёты с использованием понятия «массовая доля вещества в растворе»
28. Расчеты объемных отношений газов при химической реакции. Тепловой эффект
29. Расчет массы или объёма вещества по параметрам одного из участвующих в реакции веществ
- Вторая часть (оформляется подробным решением на бланках ответов)
30. Окислительно-восстановительные реакции
31. Реакции ионного обмена
32. Взаимосвязь различных классов неорганических веществ: описание реакций
33. Взаимосвязь органических соединений
34. Расчеты массовой доли химического соединения в смеси
35. Нахождение молекулярной формулы вещества
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
www.yoursystemeducation.com
КУРС ХИМИИ | CHEM-MIND.com
- НОВОСТИ
- КУРС ХИМИИ
- Дополнительные уроки
- Курс химии
- Разбор заданий ЕГЭ
- ТЕСТЫ
- Вариаты ЕГЭ
- Тесты по заданиям
- Тесты по темам
- СТАТЬИ
- ОПЫТЫ
- ТАБЛИЦА МЕНДЕЛЕЕВА
Поиск
- НОВОСТИ
-
Новости
Алгоритм обучения для подготовки к ЕГЭ по химии
НовостиОтветы в тестах вновь правильно отображаются!
НовостиТехнические проблемы
НовостиНовый раздел на сайте
НовостиС 8 марта
-
Новости
- КУРС ХИМИИ
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
Разбор заданий ЕГЭ
Разбор задания №11 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №10 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №9 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №8 ЕГЭ по химии
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
Разбор заданий ЕГЭ
- ТЕСТЫ
www.chem-mind.com
Задания ЕГЭ по химии ЕГЭ с разбором. / Химия / ЕГЭ :: Бингоскул
За 2-3 месяца невозможно выучить (повторить, подтянуть) такую сложную дисциплину, как химия.
Изменений в КИМ ЕГЭ 2019 г. по химии нет.
Не откладывайте подготовку на потом.
- Приступив к разбору заданий сначала изучите теорию. Теория на сайте представлена для каждого задания в виде рекомендаций, что необходимо знать при выполнении задания. Кодификатор по химии направит в изучении основных тем и определяет какие знания и умения потребуются при выполнении заданий ЕГЭ по химии. Для успешной сдачи ЕГЭ по химии – теория важнее всего.
- Теорию нужно подкреплять практикой, постоянно решая задания. Так как большинство ошибок из-за того, что неправильно прочитал упражнение, не понял, что требуют в задаче. Чем чаще ты будешь решать тематические тесты, тем быстрее поймёшь структуру экзамена. Тренировочные задания разработанные на основе демоверсии от ФИПИ дают такую возможность решать и узнавать ответы. Но не спешите подглядывать. Сначала решите самостоятельно и посмотрите, сколько баллов набрали.
Баллы за каждое задание по химии
- 1 балл — за 1-6, 11-15, 19-21, 26-28 задания.
- 2 балла — 7-10, 16-18, 22-25, 30, 31.
- З балла — 35.
- 4 балла — 32, 34.
- 5 баллов — 33.
Всего: 60 баллов.
Структура экзаменационной работы состоит из двух блоков:
- Вопросы, предполагающие краткий ответ (в виде цифры или слова) – задания 1-29.
- Задачи с развернутыми ответами – задания 30-35.
На выполнение экзаменационной работы по химии отводится 3,5 часа (210 минут).
На экзамене будет три шпаргалки. И в них нужно разбираться
- Таблица Менделеева,
- Таблица растворимости,
- Ряд напряжения металлов.
Это 70% информации, которая поможет успешно сдать экзамен по химии. Остальные 30% — умение пользоваться представленными шпаргалками.
- Если хочешь получить больше 90 баллов, нужно тратить на химию очень много времени.
- Чтобы сдать успешно ЕГЭ по химии, нужно много решать: вариантов, тренировочных заданий, даже если они покажутся легкими и однотипными.
- Правильно распределять свои силы и не забывать об отдыхе.
Дерзайте, старайтесь и всё у вас получится!
bingoschool.ru
ЕГЭ: тематические тесты
В данном разделе представлена подборка заданий по отдельным темам курса химии. Задания составлены в формате ЕГЭ и направлены на помощь в подготовке к итоговой аттестации.
При возникновении вопросов по содержанию или решению заданий обращайтесь через поле «Оставьте отзыв».
Тематические тесты по химии элементов
Неметаллы
Тестовые задания по теме «Водород» (скачать).
Тестовые задания по теме «Галогены и их соединения» (скачать).
Металлы
Тестовые задания по теме «Элементы IA и IIA групп» (скачать).
Тестовые задания по теме «Алюминий» (скачать).
Тестовые задания по теме «Железо» (скачать).
Тестовые задания по теме «Марганец» (скачать).
Тестовые задания по теме «Медь» (скачать).
Тестовые задания по теме «Серебро» (скачать).
Тестовые задания по теме «Хром» (скачать).
Тестовые задания по теме «Цинк» (скачать).
Тематические тесты по органической химии
Тестовые задания по теме «Алканы» (скачать).
Тестовые задания по теме «Алкены» (скачать).
Тестовые задания по теме «Алкадиены» (скачать).
Тестовые задания по теме «Алкины» (скачать).
Тестовые задания по теме «Арены» (скачать).
Тестовые задания по теме «Спирты. Фенол» (скачать).
Тематические тесты по структуре КИМов ЕГЭ
А1. Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов (скачать).
А2. Закономерности изменения химических свойств элементов и их соединений по периодам и группам (скачать).
С1. Реакции окислительно-восстановительные. Коррозия металлов и способы их защиты от нее (скачать).
chemistry-edu.ru
Какие 20% знаний определяют 80% успеха на ЕГЭ по химии?
Статистика беспощадно утверждает, что даже далеко не каждому школьному «отличнику» удается сдать ЕГЭ по химии на высокий балл. Известны случаи, когда они не преодолевали нижнюю границу и даже «заваливали» экзамен. Почему? Какие существуют хитрости и секреты правильной подготовки к итоговой аттестации? Какие 20% знаний на ЕГЭ важнее остальных? Давайте разбираться. Сначала — с неорганической химией, через несколько дней — с органической.1. Знание формул веществ и их названий
Не выучив все необходимые формулы, на ЕГЭ делать нечего! В современном школьном химическом образовании — это существенный пробел. Но вы же не учите русский или английский язык, не зная азбуку? В химии есть своя азбука. Так что не ленимся — запоминаем формулы и названия неорганических веществ:
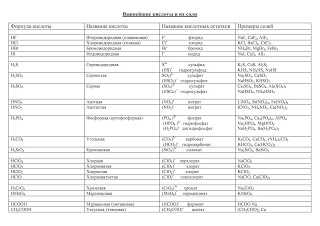
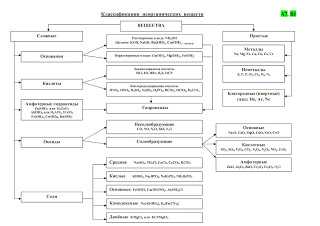
2. Применение правила противоположности свойств
Даже не зная детали тех или иных химических взаимодействий, многие задания части А и части В можно выполнить безошибочно, зная только это правило: взаимодействуют вещества, противоположные по своим свойствам
Неметаллы образуют только кислотные оксиды и гидроксиды.
Металлы более разнообразны в этом смысле, и все зависит от их активности и степени окисления. Например, у хрома, как известно, в степени окисления +2 — свойства оксида и гидроксида основные, в +3 — амфотерные, в +6 — кислотные. Всегда амфотерны бериллий, алюминий, цинк, а, значит, и их оксиды и гидроксиды. Только основные оксиды и гидроксиды — у щелочных, щелочно-земельных металлов, а также у магния и меди.
Также правило противоположности свойств можно применить к кислым и основным солям: вы точно не ошибетесь, если отметите, что кислая соль вступит в реакцию со щелочью, а основная — с кислотой.
3. Знание «вытеснительных» рядов
- Вытеснительный ряд металлов: металл, стоящий в ряду активностей левее вытесняет из раствора соли только тот металл, который находится правее его: Fe + CuSO4 = Cu + FeSO4
- Вытеснительный ряд кислот: только более сильная кислота вытеснит из раствора соли другую, менее сильную (летучую, выпадающую в осадок) кислоту. Большинство кислот справляется и с нерастворимыми солями: Na2CO3 + 2HCl = 2NaCl + CO2 + h3O
- Вытеснительный ряд неметаллов: более сильный неметалл (в основном, речь идет о галогенах) вытеснит более слабый из раствора соли: Cl2 + 2 NaBr = Br2 + 2 NaCl
4. Всегда спасет ситуацию четкая система знаний — но все может погубить «каша» в голове.
Не нужно читать дополнительные толстые учебники и пытаться вбить в голову массу новых сведений, если не помните основных. Выстройте сначала «скелет» из самого главного, а потом уже «наращивайте мышцы». Лишь то, что нужно — и ничего лишнего — вы найдете в пособии «Миниатюрный курс химии для 100% успеха на ЕГЭ». Выучите его как следует и блистайте на ЕГЭ!P.S. Если вам трудно самостоятельно весь материал разложить по полочкам и привести его в систему, то используйте готовых «помощников», которые находятся здесь:
him-ege.blogspot.com
Интерактивный курс подготовки к ЕГЭ по химии 2019 » HimEge.ru
В скобках указаны номера заданий ЕГЭ по химии согласно спецификации 2018 года.
Часть 1
Блок №1 Теоретические основы химии
Занятие №1. Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов (1). Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Общая характеристика металлов и неметаллов (2).
Занятие №2. Электроотрицательность. Степень окисления и валентность химических элементов (3). Химическая связь. Тип кристаллической решетки (4).
Занятие №3. Скорость реакции (20). Химическое равновесие (24)
Занятие №4. Электролитическая диссоциация. Реакции ионного обмена (31). Гидролиз солей (23).
Занятие №5. ОВР и степени окисления (21 и 30), электролиз (22)
Блок №2. Неорганическая химия
Занятие №6. Классификация и номенклатура неорганических веществ (5). Классификация химических реакций в неорганической химии (19).
Занятие №7. Характерные химические свойства оксидов и гидроксидов (оснóвных, амфотерных, кислотных) (6-10)
Занятие №8. Характерные химические свойства солей. Взаимосвязь неорганических веществ (7-10, 32)
Занятие №9. Элементы Ia группы и II a группы. Элементы III а группы (алюминий) (6-10, 32).
Занятие №10. Элементы IV a группы (углерод, кремний и их соединения) (6-10, 32).
Занятие №11.Элементы V a группы (азот, фосфор и их соединения) (6-10, 32).
Занятие №12. Элементы VI а группы (кислород, сера и их соединения) (6-10, 32).
Занятие №13. Элементы VII а группы (6-10, 32).
Занятие №14. d-Элементы (6-10, 32).
Занятие №15. Практическое занятие по прошедшим темам
Часть 2.
Блок №3. Органическая химия
Занятие №1. Введение в органическую химию. Классификация и номенклатура органических веществ (11, 12). Классификация химических реакций в органической химии (19).
Занятие №2. Насыщенные углеводороды. Алканы и циклоалканы (11-13, 16). Решение задач на тему “Расчет по уравнению химической реакции (29)
Занятие №3. Непредельные углеводороды. Алкены, алкадиены (11-13, 16). Решение задач на тепловой эффект (28).
Занятие №4. Алкины. Арены (11-13, 16, 18, 33)
Занятие №5. Спирты и фенолы (14, 17, 18, 33). Решение задач на массовую долю (27).
Занятие №6. Альдегиды и кетоны (14, 17, 18, 33). Решение задач на выход продукта от теоретически возможного (34).
Занятие №7. Карбоновые кислоты и сложные эфиры, жиры, мыла (14, 17, 18, 33). Взаимосвязь органических веществ. Решение задач на «избыток-недостаток» (34).
Занятие №8 Амины. Аминокислоты и белки (15, 16, 18, 33). Решение задач на примеси (34).
Занятие №9. Биологически важные вещества: углеводы (моносахариды, дисахариды, полисахариды), жиры, белки. (15, 16, 18, 33). Решение задач на “смеси” (34).
Блок №4. Методы познания в химии. Химия и жизнь
Занятие №10. Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Методы разделения смесей и очистки веществ (26).Качественные реакции на неорганические вещества и ионы. Идентификация органических соединений (25).
Занятие №11. Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. ВМС. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки. (26). Задачи «Вычисление массы/ массовой доли вещества в растворе» (24)
Занятие №12. Решение задач 25-26 (повтор). Решение задач «Установление молекулярной и структурной формулы вещества» (35).
Занятие №13. Решение задач 34 и 35.
Занятие №14. Повторение. Практика. Блок №1 Теоретические основы химии
Занятие №15. Повторение. Практика. Блок №2. Неорганическая химия
Занятие №16. Повторение. Практика. Блок №3. Органическая химия
Занятие №17. Повторение. Практика. Блок №4. Методы познания в химии. Химия и жизнь
himege.ru
MIND.com | Данный сайт сделан чтобы облегчить прохождение ЕГЭ/ОГЭ по химии и помочь школьникам в усвоении курса химии в школе.
- НОВОСТИ
- КУРС ХИМИИ
- Дополнительные уроки
- Курс химии
- Разбор заданий ЕГЭ
- ТЕСТЫ
- Вариаты ЕГЭ
- Тесты по заданиям
- Тесты по темам
- СТАТЬИ
- ОПЫТЫ
- ТАБЛИЦА МЕНДЕЛЕЕВА
Поиск
- НОВОСТИ
-
Новости
Алгоритм обучения для подготовки к ЕГЭ по химии
НовостиОтветы в тестах вновь правильно отображаются!
НовостиТехнические проблемы
НовостиНовый раздел на сайте
НовостиС 8 марта
-
Новости
- КУРС ХИМИИ
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
Разбор заданий ЕГЭ
Разбор задания №11 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №10 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №9 ЕГЭ по химии
Разбор заданий ЕГЭРазбор задания №8 ЕГЭ по химии
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
Разбор заданий ЕГЭ
- ТЕСТЫ
- ВсеВариаты ЕГЭТесты по заданиямТесты по темам
Тесты по темам
Тест №40 «Высокомолекулярные соединения»
Тесты по темамТест №39 «Химия и проблемы охраны окружающей среды»
Тесты по темамТест №38 «Общие научные принципы химического производства»
Тесты по темамТест №37 «Химическая лаборатория»
- ВсеВариаты ЕГЭТесты по заданиямТесты по темам
Тесты по темам
- СТАТЬИ
-
Статьи
Решение типовых задач по химии
СтатьиСовременная таблица Менделеева
СтатьиИонные уравнения реакций
СтатьиВнутренний экзамен МГМСУ по химии
СтатьиКниги для подготовки к химии
-
Статьи
- ОПЫТЫ
-
Опыты
Химическая ракета
ОпытыНеньютоновская жидкость
ОпытыЛодка на диоксиде углерода
ОпытыКак вырастить жеоду в домашних условиях
ОпытыГорящая рука/пузыри
-
Опыты
- ТАБЛИЦА МЕНДЕЛЕЕВА
www.chem-mind.com
